射频消融术对特发性右心室流出道室性期前收缩患者的心功能改善效果评价
刘玉芝,许宗磊,任玉华
(聊城市人民医院心内科,山东 聊城 252000)
右心室流出道是频发性室性期前收缩(premature ventricular contraction,PVC)和特发性室性心动过速的最常见起源部位。2015欧洲心脏病协会指南[1]指出,频繁的PVC是可逆性心肌病的主要原因,可导致死亡率的增加。Del Carpio Munoz等[2]研究发现,PVC负荷≥10%的右心室流出道起源的频发PVC可引起左心室收缩功能下降;而PVC负荷≥20%的左心室起源的频发PVC才能引起左心室收缩功能下降;起源于束支的PVC较前两者的预后好,提示右心室流出道起源的频发PVC更易诱发心功能不全。有数据显示,β受体阻滞剂是治疗有症状PVC的一线药物,非二氢吡啶类钙通道阻滞剂、经典的抗心律失常药物和胺碘酮可作为二线药物,对于无法耐受药物治疗或药物治疗失败的患者,应进行导管射频消融术(radiofrequency catheter ablation,RFCA),以预防频发PVC诱发的心肌病,RFCA可明确减轻PVC负荷,并可改善PVC诱发的左心室射血分数(left ventricular ejection fraction,LVEF)降低[3]。2017年,美国心脏协会/美国心脏病学会/美国心律学会指南建议将RFCA作为有明显临床症状且药物治疗效果欠佳或药物治疗不耐受频发PVC患者的一线治疗方法[4]。本研究通过比较RFCA及药物对频发右心室流出道起源PVC患者心功能的改善情况,以评价RFCA的效果,现报道如下。
1 资料与方法
1.1一般资料 选取2018年1月至2019年4月在聊城市人民医院心内科行RFCA治疗的37例特发性右心室流出道起源的频发PVC患者作为观察组,选取同期抗心律失常药物治疗的40例特发性右心室流出道起源的频发PVC患者作为对照组。两组患者性别、年龄、心率等一般资料比较差异无统计学意义(P>0.05),见表1。
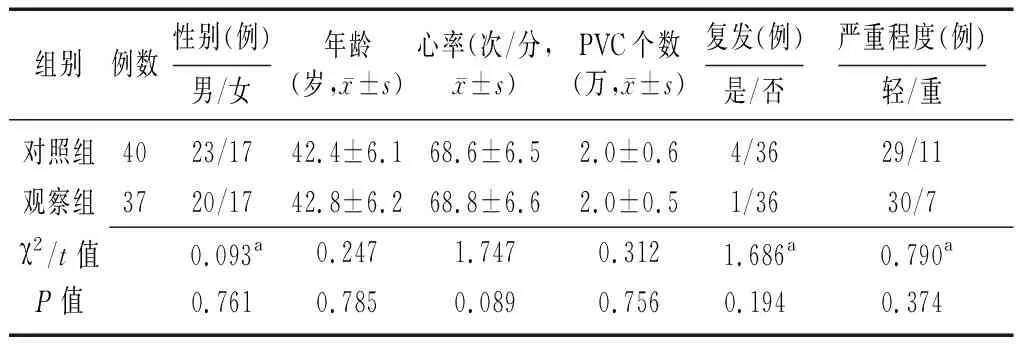
表1 两组特发性右心室流出道PVC患者一般资料比较
1.2纳入及排除标准
1.2.1纳入标准 ①24 h动态心电图显示24 h PVC总数均>10 000,伴有头晕、心悸甚至晕厥症状;②参考中华医学会心血管病分会制订的心律失常诊断及治疗标准[5],诊断右心室流出道PVC;③心电图示左束支传导阻滞,电轴右偏,Ⅱ、Ⅲ、AVF导联R波高大直立,AVL导联主波方向向下,R/S在胸前导联移行于V3导联以后。药物治疗后自觉心悸等症状明显减轻,拒绝行手术治疗者纳入对照组;药物治疗不耐受或治疗效果差,愿意接受手术治疗者纳入观察组,所有患者均签署知情同意书。
1.2.2排除标准 ①合并呼吸道及全身感染性疾病;②合并高血压;③合并甲状腺功能异常;④行心脏彩色多普勒超声排除瓣膜性或结构性心脏病;⑤行冠状动脉CT血管造影检查排除冠心病。
1.3治疗方法 对照组服用β受体阻滞剂治疗,其中23例服用酒石酸美托洛尔(英国阿斯利康制药有限公司生产,批号:1704A25),每次25 mg,每日2次;10例服用比索洛尔(德国默克公司生产,批号:NT001327),每次5 mg,每日1次;7例服用琥珀酸美托洛尔缓释片(英国阿斯利康制药有限公司生产,批号:1711010),每次47.5 mg,每日1次。疗程均为6个月。观察组行RFCA治疗,采用Seldinger法穿刺右股静脉,常规留置6 F、7 F鞘管,置入冠状窦、右心室标测电极,连接三维标测系统,将消融导管置入右心室流出道,建模,对患者进行激动标测、起搏标测,寻找起搏心电图与临床心电图QRS相同或最相似的位点作为消融靶点。放电消融温度控制在55~60 ℃,放电功率控制在25~35 W,试放电10~15 s,PVC消失为消融有效。
1.4观察指标 全部病例术前进行心脏超声、24 h动态心电图、冠状动脉CT血管造影等相关检查。观察组行RFCA前需停用所有抗心律失常药物至少5个半衰期。测定两组患者治疗前及治疗6个月后的左心室舒张末期内径(left ventricular end diastolic diameter,LVEDD)、LVEF、6 min步行距离、纽约心脏病协会(New York Heart Association,NYHA)分级、PVC负荷、联律间期、QRS时限,并进行对比分析。

2 结 果
2.1两组治疗前后LVEDD、LVEF、6 min步行距离、NYHA分级比较 治疗前后LVEDD、LVEF、6 min 步行距离、NYHA分级的主效应差异有统计学意义(P<0.05);不考虑测量时间,两组间LVEDD、LVEF、6 min步行距离、NYHA分级的主效应差异有统计学意义(P<0.05);各指标组间和时点间存在交互作用,治疗前后两组各指标变化趋势不同,两组LVEDD均缩小、LVEF均升高、6 min步行距离均增加、NYHA分级均改善,但观察组各指标变化更明显(P<0.05)。见表2。
2.2两组治疗前后心功能指标比较 治疗前后PVC负荷、联律间期、QRS时限的主效应差异有统计学意义(P<0.05);不考虑测量时间,两组间PVC负荷、联律间期、QRS时限的主效应差异有统计学意义(P<0.05);各指标组间和时点间存在交互作用,治疗前后两组各指标变化趋势不同,两组PVC负荷均降低,联律间期均延长,QRS时限均缩短,但观察组各指标变化更明显(P<0.05)。见表3。
2.3两组不良反应发生率比较 观察组发生心脏反应1例,血管反应1例,穿刺反应1例,疼痛反应1例,总不良反应发生率为10.81%(4/37);对照组发生心脏反应3例,血管反应2例,总不良反应发生率为12.50%(5/40),两组总不良反应发生率比较差异无统计学意义(χ2=0.053,P=0.818)。
表2 两组特发性右心室流出道PVC患者治疗前后LVD、LVEF、6 min步行距离、NYHA分级比较
表3 两组特发性右心室流出道PVC患者治疗前后心功能相关指标比较
3 讨 论
心力衰竭是发病率和死亡率较高的心血管疾病之一。确定与心室功能不全发展相关的潜在危险因素对预防和治疗心力衰竭非常重要。心力衰竭的病因包括心肌梗死、心肌病、血流动力学负荷过重等,均可造成心肌结构和功能的变化,最后导致心室泵血和(或)充盈功能低下,而心律失常也是心力衰竭的病因之一,包括频发的PVC、心房颤动等。近年来,频发PVC所致心功能不全逐渐受到关注。
右心室流出道PVC大多数为良性心律失常,但目前右心室流出道PVC的病因、治疗、发生机制等尚不完全明确。特发性右心室流出道PVC的病因较复杂,器质性心脏病是PVC的发病因素,但健康人群亦可发生PVC[6]。与左心室起源PVC相比,右心室起源PVC更易引起心功能下降[7],其机制可能是窦性心律时,左心室收缩,心尖部因心室挤压射血而发生扭转变形,继而向基底部产生收缩运动,对于右心室起源PVC,心室收缩方向与其相反,引起左心室室壁运动不协调。Altemose和Buxton[8]首先提出了特发性右心室流出道PVC、室性心动过速的概念,其占所有PVC的80%左右。Yao等[9-10]利用超声观察右心室流出道PVC患者节段型心肌运动的随访研究发现,期前收缩和窦性心律时的心肌收缩形式不同。Kass[11]建立左束支传导阻滞模型的实验结果提示,延迟激动部位心肌的传导速度、复极时间、动作电位时程等电生理参数均与提前激动心肌存在显著差异,提示右心室起源PVC致心肌病的可能性更大。因此,本研究主要对右心室流出道起源PVC患者进行研究。
随着三维系统的广泛应用,RFCA的临床应用日趋广泛,RFCA治疗频发PVC的随访成功率可达90%[12]。Sharma等[13]通过回顾性分析PVC和室性期前收缩性心肌病(premature ventricular contraction induced cardiomyopathy,PVC-ITCM)的自然历史,证实了RFCA可能逆转PVC诱发的心肌病。Zang等[14]的荟萃分析显示,RFCA治疗PVC的长期成功率为66%~90%,LVEF在RFCA后的总体均值较基线上升7.7% (95%CI6.1%~9.4%),LVD的总体均值下降-4.6 mm (95%CI-6.0~-3.1 mm);亚组分析显示,LVEF消融后总体均值较基线升高12.4%(95%CI8.1%~16.6%),左心室功能障碍患者总体均值降低-4.8 mm (95%CI-6.2~-3.4 mm)。证实频发PVC的消融可改善心功能,特别是对左心室功能障碍患者。Zhong等[15]纳入510例频发PVC患者,其中215例接受RFCA治疗,295例接受抗心律失常药物治疗,结果显示RFA降低PVC频率的作用大于抗心律失常药物(-21 799/24 h比-8 376/24 h,P<0.001);RFA治疗后LVEF显著升高,而抗心律失常药物治疗后LVEF无明显升高。Wojdya-Hordynska等[16]测定经RFCA治疗的93例频发PVC患者的LVEF,结果显示RFCA治疗可明显改善频发PVC患者的左心室功能;多因素分析显示,RFCA治疗成功后6个月,PVC负荷超过20 000/24 h患者的LVEF明显改善。心脏机械收缩、电激动不同步是PVC引起心功能不全的重要机制。RFCA改善PVC心功能不全的机制可能是导管RFCA利用低频电流使局部心肌细胞发生凝固性坏死,进而消融兴奋病灶,阻断异常的心电传导束,根治PVC,当窦性节律逐渐恢复后,房室舒缩趋于正常,冠状动脉血供恢复正常,细胞凋亡减少,心室重构进一步改善,心脏功能改善[17]。本研究结果显示,观察组治疗后的心脏彩色多普勒超声LVEDD明显低于对照组,而LVEF明显高于对照组,与既往研究结果一致;为明确心功能恢复情况,本研究进一步测定了治疗前后心功能分级及6 min步行距离,结果显示,RFCA组较对照组治疗后NYHA分级明显改善,6 min步行距离明显增加,证实RFCA能更好地改善心功能。
另有多项研究提出,PVC起源部位、期前收缩负荷、QRS时限、联律间期是PVC引起心功能障碍的重要影响因素[18-20]。Baman等[18]研究发现,PVC负荷≥24%可预测PVC-ITCM,其灵敏度、特异度分别为79%和78%。Del Carpio Munoz等[2]研究发现,PVC的QRS波时限≥150 ms可作为PVC-ITCM的独立预测指标,灵敏度可达100%。谢亮真[21]报道,短的联律间期亦可作为PVC-ITCM的预测因子,短联律间期致室性期前收缩性心肌病的机制可能为短的联律间期影响左心室充盈时间、左心室舒张末容积及脉压等,亦可加重心室的不同步收缩,心室收缩不同步会导致心脏有效泵血量减少,从而引起LVEF降低。本研究通过测定右心室流出道起源频发PVC患者治疗前及治疗6个月后的QRS时限、PVC负荷、联律间期发现,与对照组对比,RFCA组PVC负荷降低、联律间期延长、QRS时限缩短更明显,进一步证实了RFCA改善心功能的疗效优于抗心律失常药物。
本研究存在一定的局限性,如本研究为回顾性分析,样本量较少,动态心电图记录期间PVC的数量有所波动,心电图QRS时限、联律间期的测量存在一定主观性,有一定的误差,仍需要长时间、大样本研究的进一步证实。
综上所述,频发特发性右心室流出道PVC可引起心功能不全,与抗心律失常药物治疗相比,RFCA能更好地逆转心功能,可作为伴有心功能不全PVC患者的一线治疗,对预防频发PVC引起的结构改变和降低心脏性猝死长期风险有重要意义。

