磁性复合凝胶球的制备及其对亚甲基蓝的吸附性能
(齐齐哈尔大学化学与化学工程学院,黑龙江齐齐哈尔 161006)
纺织印染工业是水资源污染的主要来源之一[1]。全球纺织工业每年消耗一万多吨商用染料,大约15%的染料在使用过程中被排放[2]。染料废水成分复杂,难以降解,并且可能有毒和致癌[3-4]。目前,很多学者关注天然高分子凝胶在染料废水处理领域的应用[5]。Li[6]、Shao[7]和Wang[8]等分别制备了海藻酸钙凝胶、2-丙烯酰胺-2-甲基丙酮-1-丙磺酸(AMPS)/海藻酸钠(SA)凝胶球和聚乙烯醇/海藻酸钠/壳聚糖/蒙脱土复合凝胶球(MMTNS),对亚甲基蓝(MB)有良好的吸附效果。但由于凝胶球具有质轻和机械性能差等特点[9-10],不易从水中收集,所以循环使用性能低。而纳米Fe3O4具有易分离、灵敏度高的特点[11],加入凝胶球可以明显提高循环使用性能,便于回收利用[12-13]。因此,本实验采用落球法制备出一种新型Fe3O4/羧甲基壳聚糖(CMCS)/SA 复合凝胶球(MCSB)吸附剂,通过考察不同条件对MB 吸附性能的影响,探讨吸附剂结构与吸附性能间的关系,并研究MCSB吸附过程的动力学和热力学参数。
1 实验
1.1 试剂和仪器
试剂:羧甲基壳聚糖(脱乙酰度大于90%,聚合度为8~16,实验室自制),海藻酸钠(天津市福晨化学试剂厂),纳米Fe3O4[阿拉丁试剂(中国)有限公司],氯化钙(分析纯,天津市凯通化学试剂有限公司),亚甲基蓝(分析纯,天津市科密欧化学试剂开发中心)。
仪器:Nicolet 6700 型傅里叶变换红外光谱仪[赛默飞世尔科技(中国)公司],S-3400N 型扫描电子显微镜[日立高新技术(上海)国际贸易有限公司],TU-1901 型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司)。
1.2 磁性复合凝胶球的制备
在25 mL 单口烧瓶中加入1.5 g 羧甲基壳聚糖和5 mL 去离子水,搅拌溶解,再加入分散在聚乙二醇中的纳米Fe3O4形成磁性羧甲基壳聚糖溶液;在125 mL四口烧瓶中加入2.5 g 海藻酸钠和一定量去离子水,搅拌至均相。将磁性羧甲基壳聚糖溶液加入海藻酸钠溶液中混合,搅拌2 h 后冷藏1 h,采用滴管滴到2%的CaCl2溶液中形成磁性复合水凝胶球,交联1 h,经无水乙醇和去离子水各洗涤3次,冷冻干燥48 h。
1.3 吸附实验
将亚甲基蓝溶于蒸馏水模拟亚甲基蓝废水,以50 mg/L 亚甲基蓝溶液作为处理对象,pH 用0.1 mol/L的NaOH 和HCl 溶液进行调节,采用分光光度法测定664 nm 下的亚甲基蓝质量浓度。
1.4 表征
红外光谱:以KBr 压片法,采用傅里叶变换红外光谱仪在4 000~500 cm-1测定。
表面形貌:采用扫描电子显微镜进行扫描。
去除率和吸附容量的计算公式为:去除率=(1-ρ0/ρ1)×100%,吸附容量=(ρ0-ρ1)×V/m。式中,ρ0为亚甲基蓝染液初始质量浓度,mg/L;ρ1为亚甲基蓝染液吸附后的质量浓度,mg/L;V为亚甲基蓝溶液体积,mL;m为吸附剂质量,g。
2 结果与讨论
2.1 表征
2.1.1 FTIR
由图1 可知,CMCS 在1 311 cm-1处为—NH2羧甲基化后的伸缩振动峰,1 135、1 062 cm-1处为C 的特征吸收峰,说明羧甲基化在—OH 上也有发生,由此可知为N,O-羧甲基壳聚糖[14]。MCSB 中由于CMCS 和SA 的加入,纳米Fe3O4特征峰从590 cm-1处移动到564 cm-1处,同时具有CMCS 和SA 的特征峰(3 500~3 300 cm-1处有—OH 的伸缩振动峰和—NH2的伸缩振动峰;2 925 cm-1处是—CH2的不对称伸缩振动峰;1 603、1 422 cm-1处分别是羧基中双键和C—O 单键的伸缩振动峰),在1 695 cm-1处出现了明显的酰胺键特征峰,证明CMCS已交联到SA 上[15]。
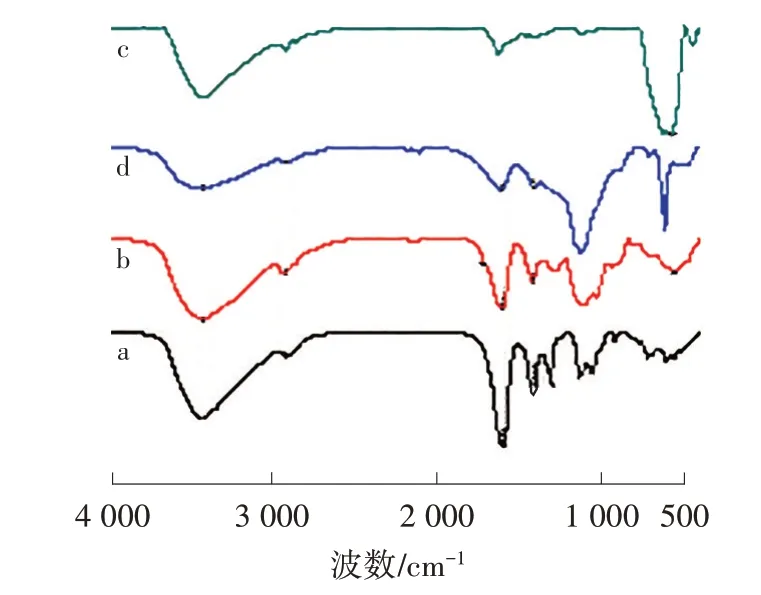
图1 CMCS(a)、SA(b)、Fe3O4(c)、MCSB(d)的红外光谱
2.1.2 SEM
由图2a 可知,磁性复合凝胶球呈黑色球状,表面光滑,直径在3 mm 左右。由图2b 可知,磁性复合凝胶球呈致密的三维片状结构,该结构增大了表面积,有利于吸附废水中的染料。
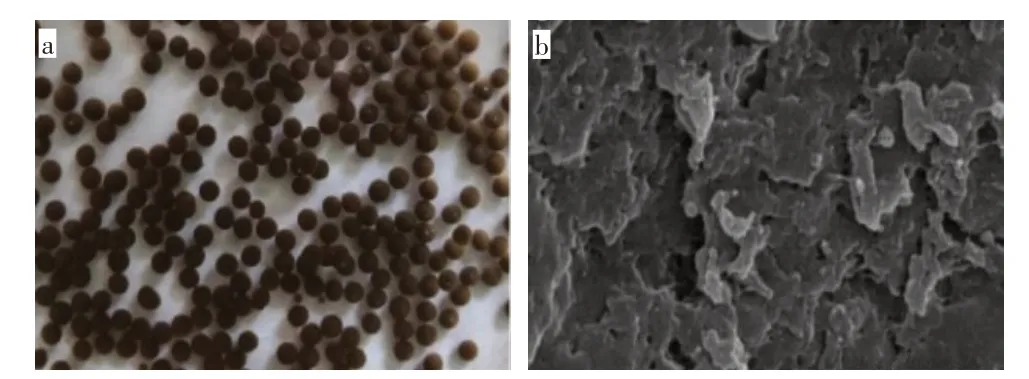
图2 MCSB 的外观图(a)和扫描电镜图(b)
2.2 亚甲基蓝吸附性能的影响因素
2.2.1 MCSB 用量
由图3 可知,随着MCSB 用量的增加,MB 去除率呈上升趋势。当用量较低时,提供的吸附位点较少,由此所吸附的MB 较少,表现为MB 去除率较低;随着用量的增加,吸附位点增加,MB 去除率提高;用量继续增加,MB 去除率增大缓慢,这是由于废水中游离的MB 分子较少,吸附进入缓慢增长阶段。从经济角度考虑,后续实验MCSB 用量选择0.4 g/L。
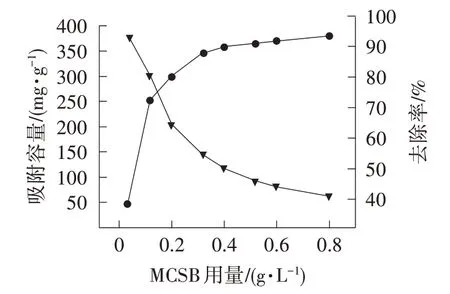
图3 MCSB 用量对亚甲基蓝去除效果的影响
2.2.2 废水pH
由图4 可知,pH 为2~12 时,随着pH 增大,MCSB对废水中MB 的去除率呈先上升后下降的趋势。pH由2 增大至7 时,MB 去除率由40.77%上升至最大值93.29%,因为在pH 为7 时,MCSB 表面和染料电荷之间达到静电平衡,可能会发生强烈的相互作用[16]。pH继续增大,亚甲基蓝去除率逐渐下降。此外,在pH为2时观察到的轻微染料吸附是H+和MB 阳离子对MCSB活性位点的竞争性吸附。在pH 为12 时,MCSB 的亲和力与反离子(Na+)的筛选作用有关[17]。所以亚甲基蓝废水pH 选择7。

图4 废水pH 对亚甲基蓝去除效果的影响
2.2.3 吸附时间
吸附时间对亚甲基蓝去除效果的影响见图5。
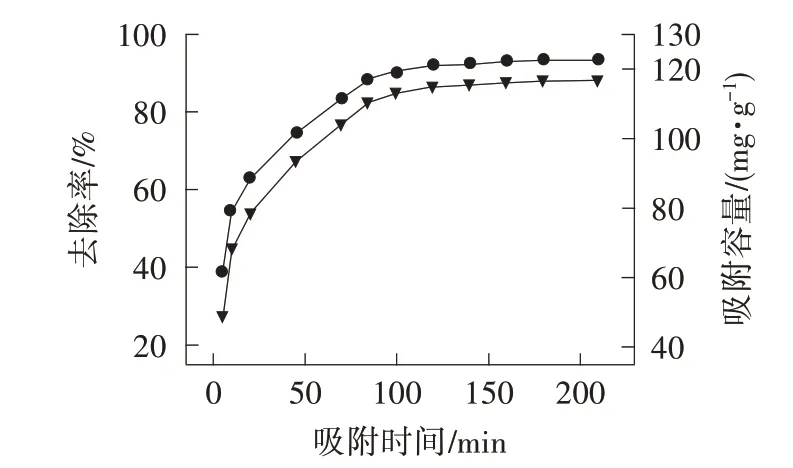
图5 吸附时间对亚甲基蓝去除效果的影响
由图5 可知,在0~100 min 内,由于MCSB 表面有丰富的自由吸附位点,对MB 的吸附能力随着吸附时间的延长而迅速增加;随着时间的继续延长,吸附逐渐减慢并趋于平衡。吸附的最佳时间为100 min,吸附容量最大为116.71 mg/g,MB 去除率最大为93.36%。
2.2.4 MB 初始质量浓度
由图6 可知,当MB 初始质量浓度较低时,MCSB的活性吸附位点充足,可以吸附溶液中的大部分MB;随着MB 初始质量浓度的增加,吸附剂用量固定限制了有效的吸附位点,MCSB 吸附位点逐渐饱和,去除率下降。这是由于MB 质量浓度增加所产生的压力梯度对吸附剂产生高驱动力,提高了对MB 的吸附亲和力;同时MB 在高质量浓度时发生的分子聚集延迟了它们在MCSB 结构中的扩散[17]。240 mg/L 时,MB去除率仍然可以保持在67.21%左右。

图6 MB 初始质量浓度对去除效果的影响
2.2.5 温度
由图7 可知,MCSB 对MB 的吸附容量随着温度的升高而降低,表明吸附是一个放热过程。这可能是由于温度升高,MCSB 表面的活性位点和MB 分子之间的吸附力降低,导致去除率降低。

图7 温度对亚甲基蓝去除效果的影响
2.3 重复使用性能
吸附实验完成后,利用外加磁场回收MCSB 置于0.1 mol/L 的HCl 溶液中,室温下在40 kHz 超声环境中脱附1 h,用蒸馏水冲洗,收集MCSB 进行下一次实验,以MCSB 对MB 的去除率为评价指标,结果如图8所示。通过5 个连续的吸附-脱附循环,MCSB 对亚甲基蓝的去除率仍然能保持在80.81%,吸附性能没有大幅度损失,表现出良好的再生效果。
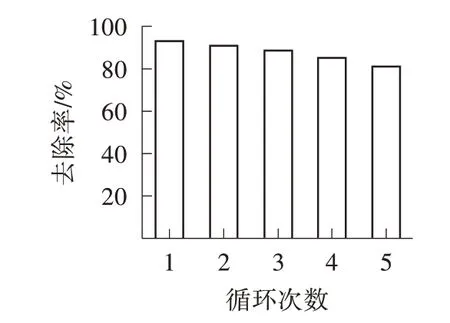
图8 吸附-解吸循环次数对亚甲基蓝去除效果的影响
2.4 动力学
采用准一级和准二级动力学方程[18]对2.2.3 实验数据进行拟合,相关参数见表1。准二级动力学方程的相关系数高于准一级动力学方程,预测的最大理论吸附量为127.71 mg/g,与实测值116.71 mg/g 更接近,因此磁性复合凝胶球对MB 的吸附符合准二级动力学方程,这说明吸附过程以化学吸附为主。

表1 准一级和准二级动力学参数
2.5 热力学
采用Langmuir 和Freundlich 等温吸附方程[18]对2.2.4 实验数据进行拟合,相关参数见表2。Langmuir吸附等温线模型的相关系数高于Freundlich 吸附等温线模型,预测的最大理论吸附量为444.44 mg/g,与实测值403.26 mg/g 更接近。这说明Langmuir 吸附等温线模型能更好地描述MCSB 对MB 的吸附过程,表明吸附质在吸附剂表面呈单分子层吸附。

表2 吸附等温线参数
3 结论
(1)制备纯黑色磁性复合凝胶球(大小均匀,直径3 mm左右,易回收)的条件:CMCS与SA质量比3∶5,纳米Fe3O4用量2.5 g/L,交联剂CaCl2用量2%。
(2)在温度为293 K、pH 为7、MB 初始质量浓度为50 mg/L、磁性复合凝胶球用量为0.4 g/L、吸附时间为100 min 时,CMCS 对MB 的去除率为90.62%,对MB 的吸附容量为113.28 mg/g。吸附过程更符合准二级动力学方程和Langmuir 吸附等温线模型,这说明MCSB 对MB 的吸附是化学吸附,且呈单分子层吸附。

