基础FSH值对DOR患者高孕激素状态下促排卵疗效观察
赵雪含 杨 菁 吴庚香
武汉大学人民医院生殖医学中心, 湖北省辅助生殖与胚胎发育医学临床研究中心(430060)
卵巢储备功能下降(DOR)患者卵巢内卵母细胞数量、质量均有下降,出现排卵障碍、内分泌功能紊乱等表现,超促排卵(COH)治疗中对促性腺激素(Gn)反应差、获卵少、优质胚胎少,早发黄体生成素(LH)峰增多,周期取消率高,难以获得理想的妊娠结局。月经周期第2~3天卵泡刺激素(FSH)常作为评价卵巢储备功能的重要内分泌指标[1],FSH升高患者卵巢储备功能降低,FSH>10 U/L患者妊娠结局较差,但同时也有研究认为高FSH对年轻IVF女性IVF结局预测能力有限[2]。 随着胚胎冷冻与冻融胚胎移植(FET)技术的快速发展,卵泡期高孕激素状态下促排卵(PPOS)配合全胚冷冻作为一种新方案,在国内多个中心得到应用。研究报道PPOS方案能够改善体外受精(IVF)治疗效果,为DOR人群获得理想妊娠创造可能[3-5]。本研究对本中心接受PPOS方案治疗的DOR患者临床资料进行回顾性分析,验证基础FSH(bFSH)对这一促排卵方案临床效果的影响,以探索PPOS方案在DOR人群中的进一步临床应用。
1 对象与方法
1.1 研究对象
回顾性分析2016年6月-2017年10月于武汉大学人民医院生殖医学中心行PPOS方案超促排卵助孕治疗DOR患者共328例。根据患者bFSH水平分为FSH正常组(FSH<10 U/L)117例,FSH升高组(FSH≥10 U/L)211例。
1.2 诊断标准
以下3条中任意2条符合即满足DOR诊断[6]:①基础FSH≥10 U/L或基础FSH(bFSH)/基础LH(bLH)>3.6;②年龄>35岁;③自然周期下双侧卵巢中窦卵泡计数≤5个。排除标准:①夫妻双方任意一方染色体异常;②甲状腺功能异常等内分泌系统异常疾病;③全身性疾病。
1.3 治疗方案
1.3.1PPOS 月经周期第2天,通过阴道B超、基础性激素测定评估患者卵巢储备情况,次日起直至人绒促性腺激素(hCG)日,每日口服醋酸甲羟孕酮10mg/d(浙江仙琚制药),根据患者卵巢储备情况与既往促排卵方案卵巢反应性每日肌内注射尿促性素(珠海丽珠医药)150~300U/d,每2~3d进行阴道超声及性激素检查监测卵泡生长情况,根据卵泡发育情况调整用药剂量。当有1个卵泡直径≥20mm或3个卵泡直径≥18mm时,使用hCG(珠海丽珠医药)10 000U扳机。
1.3.2取卵、IVF、胚胎质量评估hCG扳机后34~36h,在阴道超声引导下依次抽取直径>10mm卵泡取卵,根据男方精液、既往周期情况选择IVF或ICSI受精。取卵后18h评估卵子受精情况,48、72h后评估胚胎情况。胚胎分级[7]:I级为胚胎卵裂球大小均匀,形态规则且胞质清晰,无碎片或碎片<10%;II级胚胎为卵裂球大小不等,形态欠规则,碎片10~26%;III级胚胎为卵裂球大小不均等,碎片26~50%;IV级胚胎为卵裂球大小严重不均匀,碎片>50%。取卵后48h出现4~5细胞或72h出现6细胞或及以上,且碎片率<20%,形态评级为I级或II级胚胎,被定义为优质胚胎;而4细胞或以上,评级在III级以上,被定义为可移植胚胎[7]。因PPOS方案高孕激素水平导致子宫内膜容受窗口与移植时间不相符,故在取卵后72h后将全部可移植胚胎冻存,待日后行FET。
1.3.3冻胚移植内膜准备与临床妊娠监测FET患者采用人工周期准备内膜,自月经第3天起口服戊酸雌二醇(补佳乐,拜耳医药保健有限公司)4~8mg/d,内膜原≥8mm后给与黄体酮40mg/d进行黄体支持。胚胎解冻按照科室常规步骤进行,解冻后胚胎分级[7]:完整为100%细胞存活;部分受损为≥50%细胞存活;变性为<50%细胞存活。完整与部分受损胚胎用于胚胎移植。FET后12h测定血清β-hCG>10U判定为生化妊娠,FET后30d阴道超声下见孕囊者判定为临床妊娠。
1.3.4观察指标收集两组患者临床资料,包括患者年龄、不孕年限、不孕原因、体质指数(BMI)、bFSH、bLH、基础雌二醇(bE2)、窦卵泡计数 (AFC)、Gn初始剂量、Gn使用天数及Gn使用总量、hCG日E2水平、hCG日>10mm卵泡数目、hCG日>14mm卵泡数目、hCG日>18mm卵泡数目、获卵数、获卵率、无获卵周期率、2PN受精数、2PN受精率、2PN卵裂数、2PN卵裂率、优胚数、优胚率、有效胚胎数、有效胚胎率、周期取消率、移植胚胎数、子宫内膜厚度、胚胎复苏率、胚胎种植率、临床妊娠率。
1.4统计方法
2 结果
2.1 一般情况
两组对象不孕年限、年龄、BMI、AFC、不孕原因均无差异(P>0.05)。但FSH升高组bLH上升(P<0.001),bE2下降(P<0.01)。见表1。
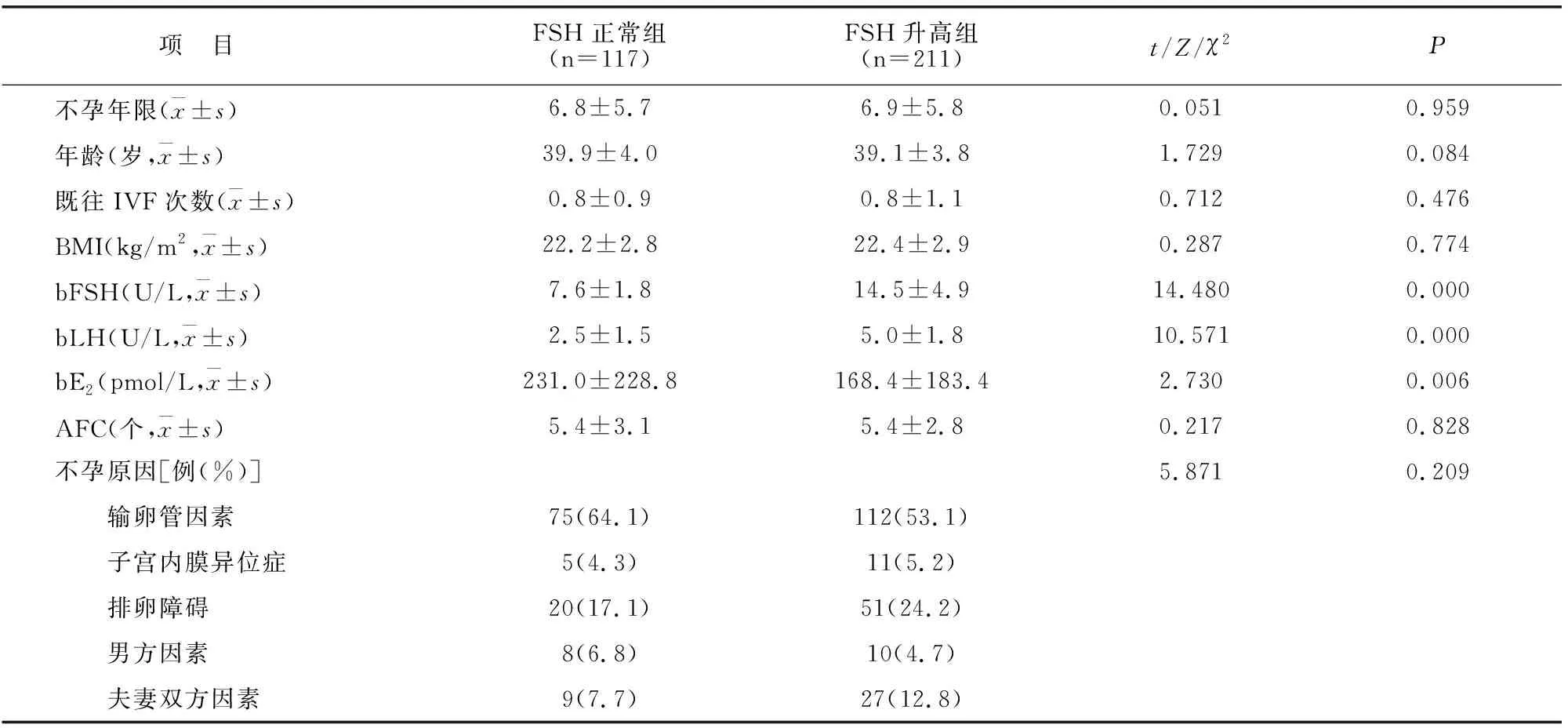
表1 两组对象一般情况比较
2.2 促排卵情况
较FSH正常组相比,FSH升高组hCG日>14mm卵泡数目降低(P<0.05),获卵数降低(P<0.01)。见表2。
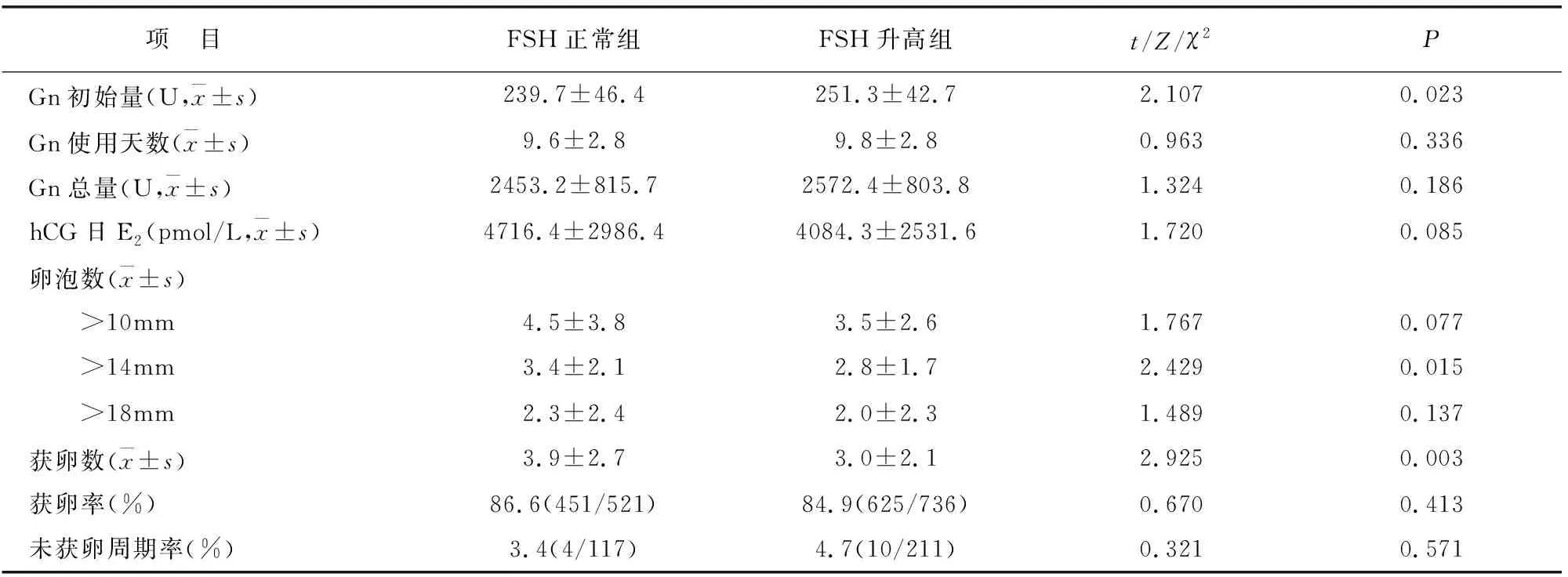
表2 两组促排卵情况比较
2.3 胚胎实验室结局
统计结果显示,FSH升高组优胚数、可移植胚胎数较FSH正常组稍有下降但无差异(P>0.05)。两组成熟卵率、2PN受精率、2PN卵裂率、优胚率、有效胚胎率、周期取消率均无差异(P>0.05)。见表3。
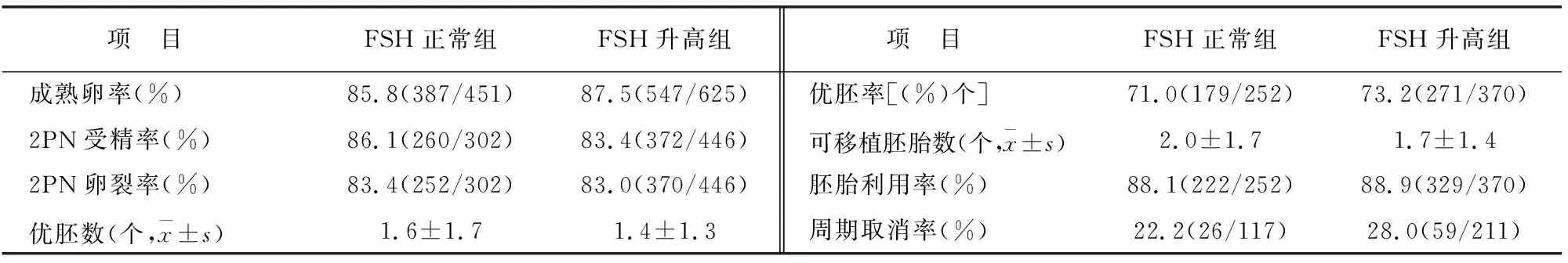
表3 两组胚胎实验室结局比较
2.4 冻胚移植结局
FET周期FSH正常组完成60个,FSH升高组完成101个周期FET。两组移植胚胎数、内膜厚度、胚胎复苏率、胚胎种植率、临床妊娠率均无差异(P>0.05)。见表4。
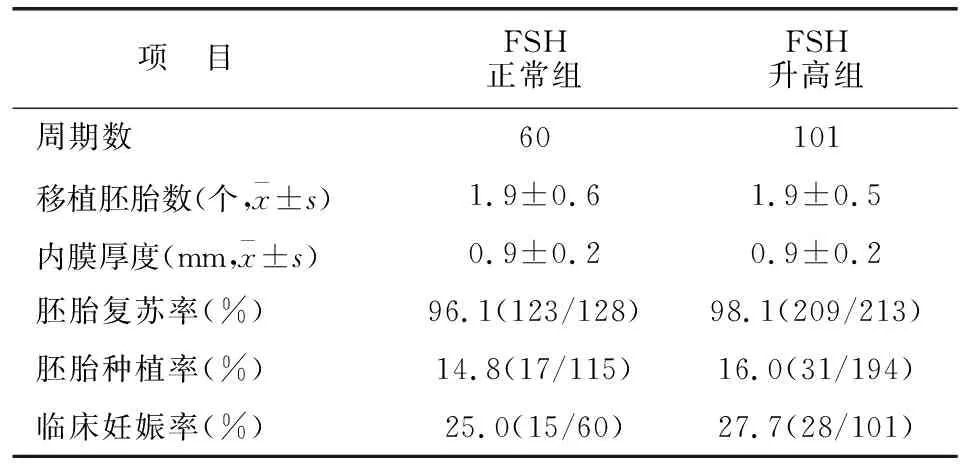
表4 两组FET结局比较
3 讨论
控制性超促排卵是体外受精-胚胎移植治疗的重要一环,卵巢储备功能是影响其效果的关键因素。以往给予DOR患者微刺激、短方案等促排卵,卵巢反应差、获卵少、卵子质量不佳、早发LH峰多见、周期取消与不良妊娠发生率高等大大增加这一人群的助孕难度。在胚胎冷冻条件日益成熟的背景下,Kuang等[8]首次报道黄体期应用hMG与来曲唑促排卵能有效降低LH峰出现,帮助卵巢功能正常患者获得临床妊娠。在此基础上卵泡早期持续给予口服孕激素并联合hMG注射的PPOS方案[9],同样能够保证卵母细胞、胚胎质量不受影响,并快速得到广泛应用。国内对多个中心DOR患者的临床资料总结发现,PPOS方案较克罗米芬微刺激显著增加优胚数、可移植胚胎数,获得更高的临床妊娠率,并能较拮抗剂方案显著增加可移植胚胎数[4],可作为DOR患者较为理想促排卵方案[10]。
临床中FSH常与年龄、AFC、AMH等指标一同用于患者卵巢功能评价[1]。以往研究认为卵泡数量随FSH升高、年龄的增长而下降[11],卵泡质量随女性年龄增长而下降[12],但目前尚缺乏FSH对卵泡质量预测价值的有力研究。本研究根据FSH水平对DOR患者进行分组,FSH升高组bLH显著上升,bE2显著下降,提示卵巢储备功能下降更为明显,内分泌功能紊乱更为严重。
分析两组患者促排卵情况发现,FSH升高组hCG日>14mm卵泡数明显减少,获卵数明显下降。尽管以往研究认为FSH对卵巢反应性的预测能力有限,但有学者发现FSH升高人群中卵巢低反应的发生率升高[12]。本研究中两组患者AFC无显著差异,但促排卵过程中FSH升高组卵泡数、获卵数下降,Gn初始剂量显著升高,提示高FSH患者PPOS方案的卵巢反应性较差。但比较两组胚胎实验室结局发现,成熟卵率、2PN受精率、2PN卵裂率、优胚率、胚胎利用率均无差异,与以往观点一致,FSH升高患者卵子质量、胚胎形成潜能未受影响。同时,FSH升高患者优胚数、可移植胚胎数虽有下降但无统计学差异,提示PPOS方案能够有效帮助FSH升高患者获得优质胚胎。
PPOS方案进入临床应用较晚,冻胚移植增加患者整体治疗时长,DOR患者常需经多个促排卵周期积攒胚胎,因而本研究患者尚未全部完成冻胚移植,缺少部分妊娠随访数据。以往研究证实,9489个IVF周期中,FSH升高仅与高龄患者妊娠丢失相关[13]。本研究结果与前期研究一致,患者FET胚胎复苏率、胚胎种植率、临床妊娠率均无差异,FSH升高对患者卵子与胚胎质量未产生影响。但考虑到患者妊娠结局与年龄的相关性,我们将在接下来研究中完成妊娠随访,并细化年龄分组。
综上,PPOS方案中FSH升高DOR患者内分泌紊乱加重,卵泡数、获卵数下降,但其获得的卵子质量与胚胎数量未见明显影响。PPOS方案能够帮助DOR患者在有限周期中获得优质胚胎,及时挽救生育力,尤其对已有FSH升高的DOR患者可能有更大的应用价值。本研究为回顾性分析,样本量不大,结果可能存在偏差,需要大样本、多中心、前瞻性随机对照研究,进一步完成FSH水平对PPOS方案疗效的影响分析。

