近红外荧光BODIPY/aza-BODIPY染料的研究进展
岳 帅,邵竹梅,姜新东,2*
(1.沈阳化工大学 应用化学学院,辽宁 沈阳 110142;2.大连理工大学 精细化工国家重点实验室,辽宁 大连 116024)
1 引言
近红外荧光染料能够减少背景吸收、荧光、光散射,并能够提高荧光探针和化学传感器的灵敏度[1],更重要的是,近红外区域(650~900 nm)的光在组织中具有深度穿透能力,能够进行体内成像和光动力学治疗[2]。因此,新型近红外荧光染料的合成与设计,引起了越来越多人的兴趣[3-5]。氟硼二吡咯甲川(BODIPY)荧光强、稳定,并且容易修饰。所以,人们将BODIPY染料作为生物标记的候选物[6-8]。
aza-BODIPY的结构是以氮原子取代BODIPY的meso位碳原子,使吸收光谱显著红移[9-13]。使用亚胺基取代BODIPY系统中的一个亚甲基,可以缩小分子轨道间能隙差值(图1)。事实上,aza-BODIPY的荧光量子产率要比BODIPY减少很多,然而随着仪器和设备的发展,只要荧光量子产率超过0.01就能被检测并使用。因此,新型近红外aza-BODIPY吸引了越来越多科研工作者的兴趣。
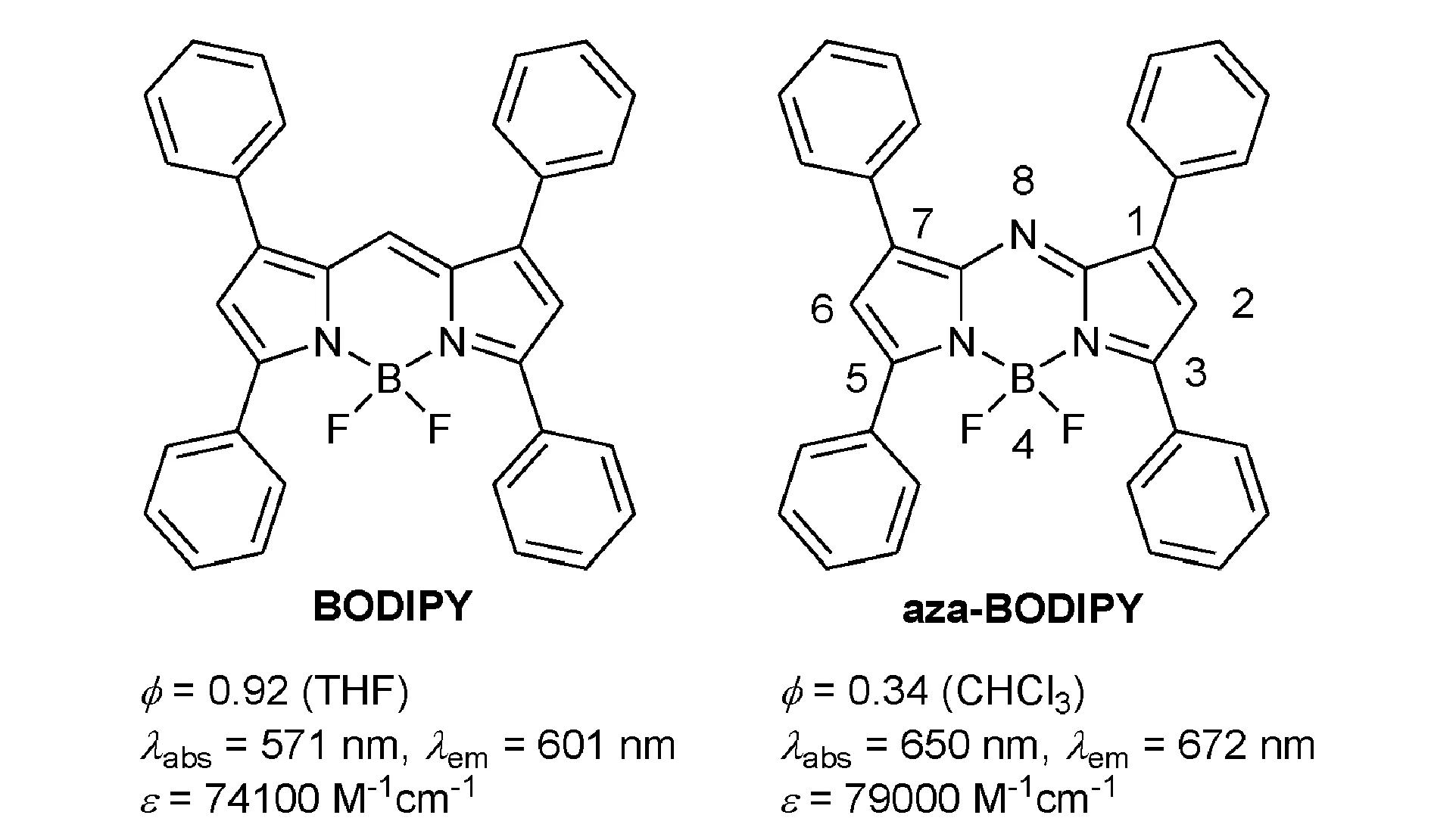
图1 BODIPY和aza-BODIPY的光学性能比较
2 aza-BODIPY染料的合成方法
相对于BODIPY,aza-BODIPY的合成方法较少[14,15]。最近,O’shea等开发了合成路线,得到了由1,3-二芳基-4-硝基-1-丁酮或3-甲基-4-硝基-1-芳基丁烷产生的对称aza-BODIPY的合成方法(图2a)[16-18],该方法可广泛用于合成各种结构aza-BODIPY,并且,O’Shea等也报道了不对称 aza-BODIPY的合成方法(图2b)。Lukyanets报道了含有苯基的aza-BODIPY的合成方法,将邻苯二甲腈与格式试剂反应,产率10%~30%(图2c)[19]。Carreira等利用单独的2,4-二芳基吡咯或芳基稠合的2,4-二芳基吡咯,提供了更普遍、更有效的合成对称与不对称aza-BODIPY的方法(图2d)[20]。
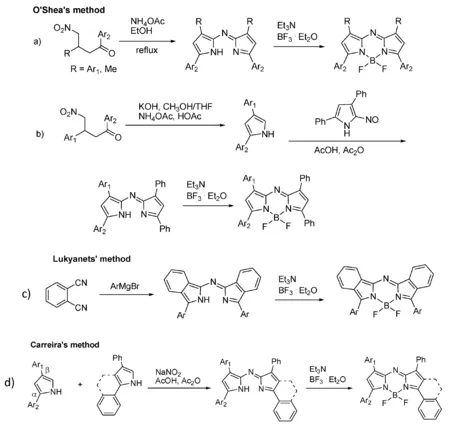
图2 aza-BODIPY染料合成方法
3 aza-BODIPY染料的结构及应用
3.1 O’shea方法合成的aza-BODIPY
O’Shea等在2002年首次报道了aza-BODIPY1~4的合成及性质,并且溴取代的aza-BODIPY (3和4)被证实具有光动力治疗的功能。随后,O’shea等还制备了在1/7位具有—OMe/Br的氮杂-BODIPY5~7[16-18]。利用光诱导电子转移(PET)机制,aza-BODIPY8和9的二乙胺和吗啉作为质子的受体,可以对酸值感应[21]。通过内部电荷转移(ICT)调节,aza-BODIPY10和11能用作pH探针[22]。合成的具有冠醚的aza-BODIPY12,对中性小分子能够响应[23](图3)。对于aza-BODIPY13,在1,7位的2-吡啶基取代基对于金属离子的结合有着非常明确的效果。化学传感器对Hg2+有选择性[24]。引入供电子或吸电子基团,可以通过增加HOMO或降低LUMO能量进一步降低HOMO-LUMO间隙,并使相应染料的吸收发生红移[25]。如3、5位的—OMe基团和1、7位的—CN基团取代的aza-BODIPY14与母体aza-BODIPY1(图1)相比,其吸收、发射明显发生红移[26]。基于1,7-苯基取代的aza-BODIPY受限旋转,通过制限旋转芳基的引入,aza-BODIPY15具有更高荧光量子产率(高达0.81),并减少溶液中的非辐射弛豫过程[27]。为冻结1,7位苯基的旋转,进行具有乙二醇片段连接的两个芳基取代,同时,增加aza-BODIPY16的亲水性,并将其应用于细胞内HepG2细胞成像[28]。Burgess等报道了含有NH2基的氮杂-BODIPY17[29]。含有叠氮基的aza-BODIPY18表现出对H2S的选择性[30]。羟基取代的aza-BODIPY19,是二氧化碳的传感器[31]。硼酸取代的近红外荧光染料20可以用于血液系统中葡萄糖含量的监控[32],其原理是aza-BODIPY上作为缺电子基团的硼酸基团与过氧化氢反应生成富电子酚基团,导致其发射波长从682 nm到724 nm显著红移。相对1,3,5,7-四苯基aza-BODIPY1,用噻吩代替其苯环发生了显著红移。aza-BODIPY21具有较强的近红外荧光,在乙腈中的荧光量子产率是0.46,是非常有竞争力的近红外荧光团[33]。
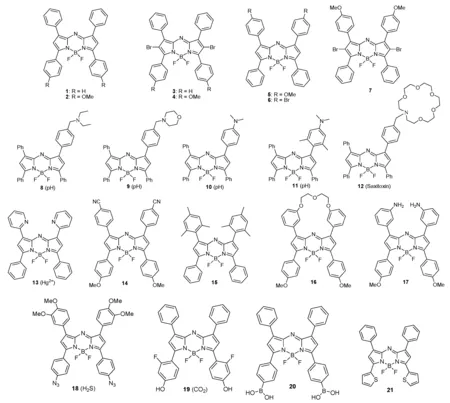
图3 O’shea法合成的染料及其应用
3.2 Lukyanets方法合成的aza-BODIPY
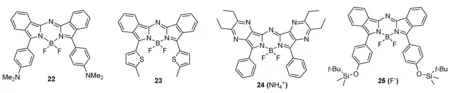
图4 Lukyanets法合成的染料及其应用
3.3 Carreira方法合成的aza-BODIPY
为了制备2,4-二苯基吡咯,使用相应的酮(如苯乙酮)与2-苯基氮丙烯反应,在LDA或NaH存在下得到2,4-二苯基-1H-吡咯(图5)[20],利用这种方法,已合成了许多典型的吡咯。吡咯的独特结构已经通过X射线单晶衍射证实[37]。采用Carreira的方法,这些新型吡咯适合于合成aza-BODIPY及其衍生物(图6)。Carreira等在2006年开发了具有适当取代和限制的新型荧光染料aza-BODIPY26~29(图7)[20],新的aza-BODIPY染料拥有700~900 nm的峰值荧光,有高量子产率、窄半峰宽、高稳定性的特点。
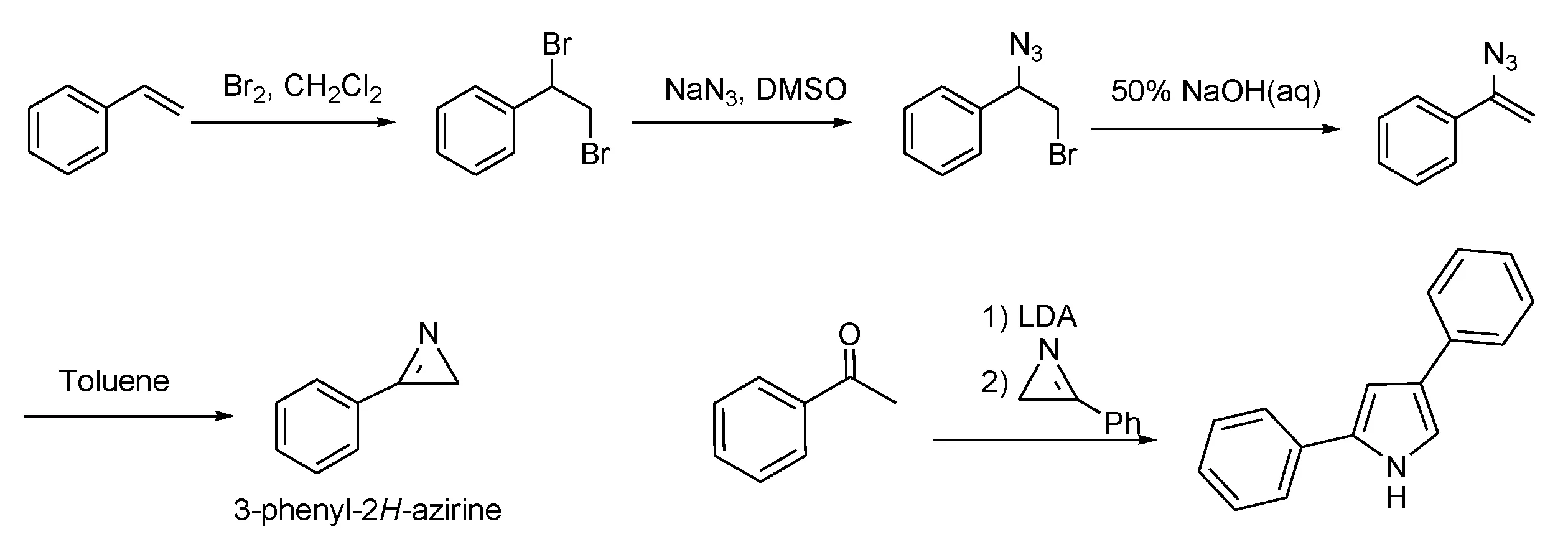
图5 2,4-二苯基吡咯的合成
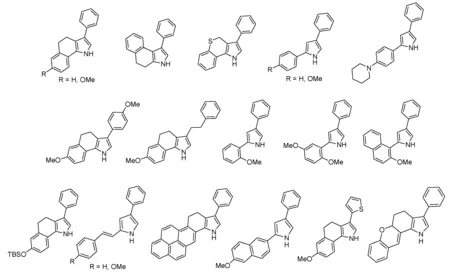
图6 用于合成BODIPY、aza-BODIPY染料的吡咯和ORTEP图[37]
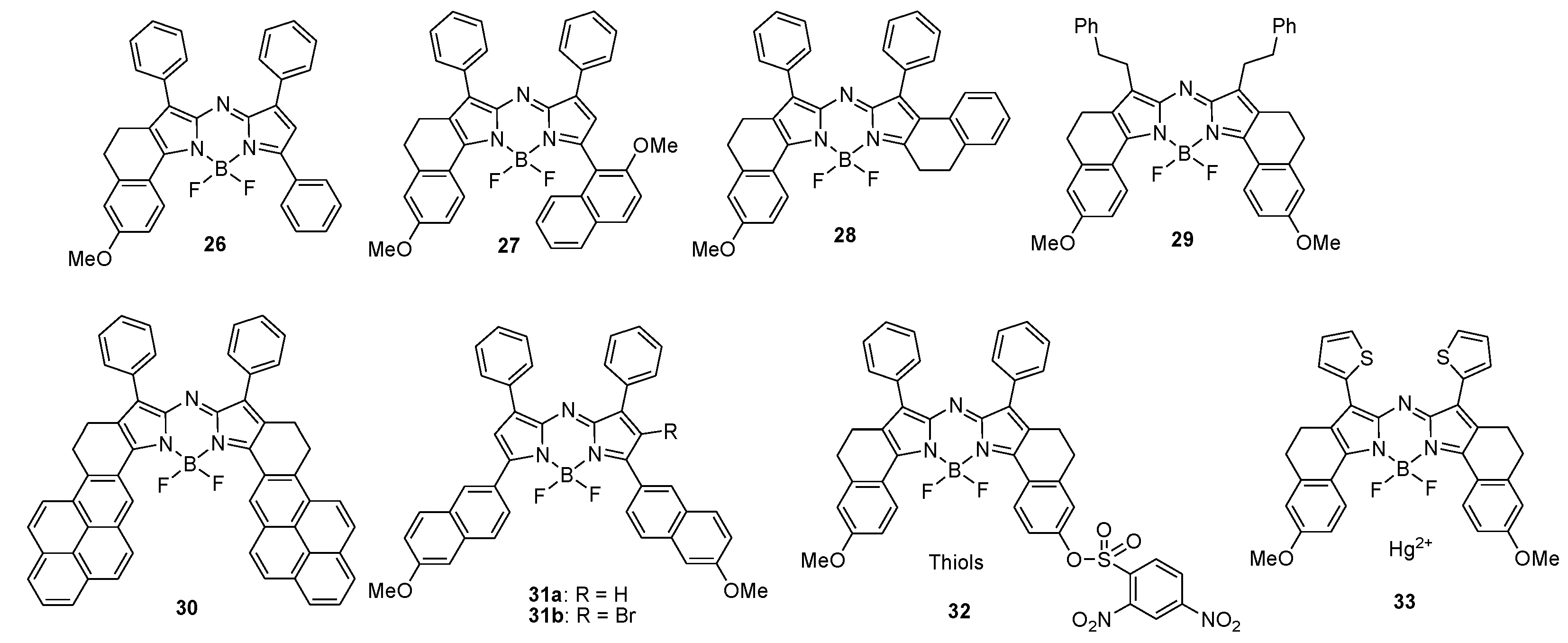
图7 Carreira方法合成的染料及其应用
此外,在Carreira法的基础上,Jiang团队最近在aza-BODIPY领域中,在可旋转部分的π共轭延伸和刚性的方面取得了突破,由于刚性化和π共轭的延伸的组合效应,在近红外区域(λabs=746 nm,λem=762 nm)制备了对称的含芘aza-BODIPY30。在芘稠合的aza-BODIPY中,观察到HOMO-LUMO(轨道)带隙的最低能量吸收带降低[38]。
Jiang等成功制备了含有萘基的aza-BODIPY31a[39],通过萘基延长π共轭系统对其光物理性质有显著影响,具有萘基的aza-BODIPY31a的最大吸收和发射波长分别为λabs=706 nm,λem=733 nm,与带有苯基的2(λabs=688 nm,λem=715 nm)的BDP相比,有显著红移。作为光敏剂aza-BODIPY31b(在甲苯中λabs=704 nm)可以产生一定的单重态氧,并且被认为是潜在地用于产生单重态氧的光敏剂。Jiang等在aza-BODIPY染料的基础上制造出近红外的荧光探针32[40],探针32具有弱荧光,用硫醇裂解DNBS释放aza-BODIPY荧光,同时在NIR区域发出荧光(λem=755 nm,Φf=0.14),对半胱氨酸具有高度选择性,并且检测快速。
Jiang等还报道了含噻吩基的aza-BODIPY33[41],aza-BODIPY33在氯仿中其NIR区域吸收在760 nm处,发射在782 nm处。作为NIR型化学传感器的33对Hg2+具有高度选择性,其荧光猝灭是由于与Hg2+结合后电子从噻吩基到aza-BODIPY母核的转移,化学传感器33可用于检测MCF-7细胞中的Hg2+,表明其可用于研究Hg2+在生物系统中的作用。
修饰aza-BODIPY 的关键在于母体分子的修饰,非常有效的修饰方法之一是通过Knoevenagel反应延伸共轭系统[42-45]。在aza-BODIPY系统中的3,5位缺少甲基,Knoevenagel反应对其是无效的。使用3-乙基-2,4-二甲基-吡咯预期的产物是在3,5位上包含甲基的aza-BODIPY,但得到的是3-氨基或3-乙酰氨基BODIPY[46-48]。如上所述,表明使用Carreira方法(图2)合成aza-BODIPY的基本要求是在吡咯的α、β位具有芳基。Jiang组挑战了这一假设,在NIR区成功制备了不对称的含苯乙烯基的aza-BODIPY34和35(图8)[49],这是一个带有苯乙烯基的新型aza-BODIPY结构,可以避免使用Knoevenagel反应。
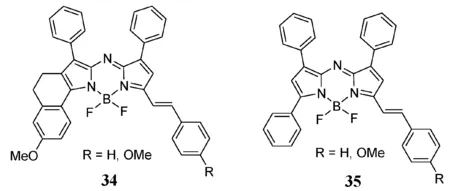
图8 不对称苯乙烯基取代的aza-BODIPY染料
Jiao小组最近报道了一类近红外β-噻吩稠合aza-BODIPY,使用的吡咯是在Suzuki-Miyaura偶联反应中获得的[50]。aza-BODIPY36(图9)在800 nm处可以看到尖锐的吸收和荧光发射带,在700~380 nm的可见光范围内具有非常低的吸收。
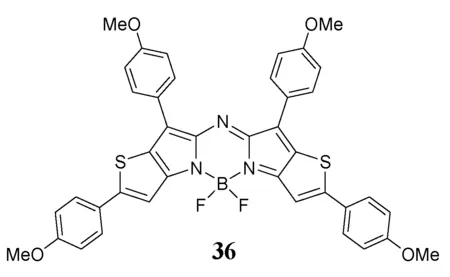
图9 噻吩融合的aza-BODIPY染料
4 近红外荧光染料衍生物的合成及应用
4.1 aza-BODIPY硼中心的取代
尽管Ziessel等已经详细报道了氟原子在BODIPY体系中的取代[51],但硼中心取代的aza-BODIPY报道较少。37结构具有B—O键,将中心硼原子与3/5位苯基的邻位相连(图10)[51]。与38[52]的无制限结构相比,37的吸收和发射最大值分别红移了88 nm和58 nm,荧光量子产率也大幅提升,这主要归因于BODIPY核的与3,5位的芳基之间的共面性增强[52]。而aza-BODIPY39中硼中心用芳基修饰,致使荧光量子产率极低,而40炔基化修饰导致荧光量子产率较高[53],并且,Jiang等还通过X射线晶体学证实了39和40的结构(ORTEP图见图10)[54]。
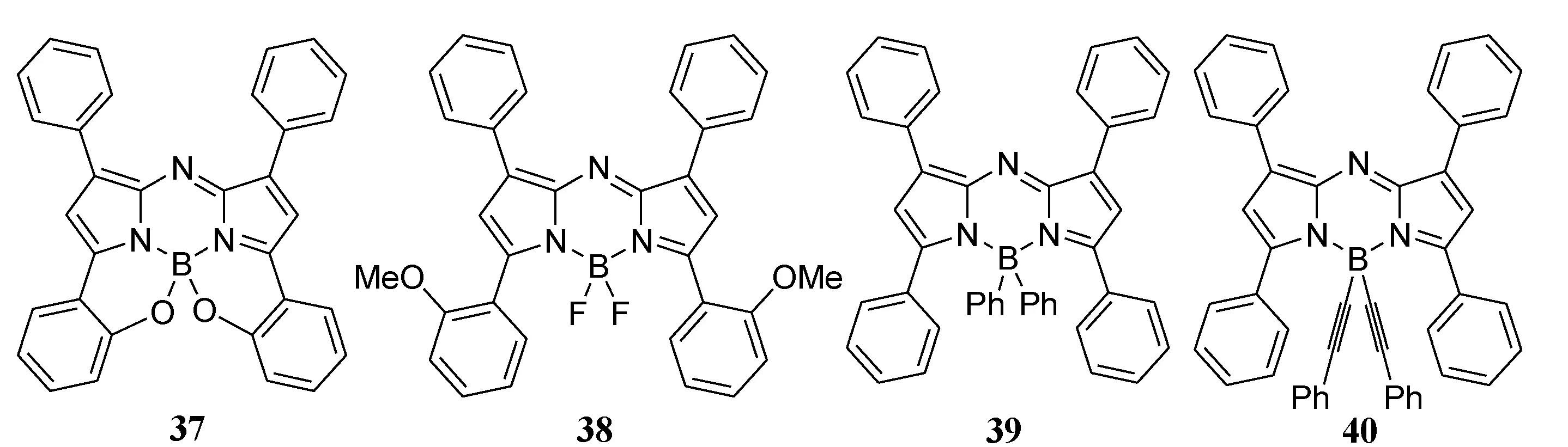
图10 F取代的aza-BODIPY染料及aza-BODIPY ORTEP图[54]
4.2 1-甲基-1H-吡咯基取代3,5位的近红外荧光aza-BODIPY染料
尽管研究人员已经获得了多种aza-BODIPY体系,但目前还没有报道在3,5位上合成带有吡咯基的aza-BODIPY体系。作者曾报道了在3,5位上含有吡咯基的近红外荧光aza-BODIPY染料41和42的设计和合成(图11)[55],染料41和42的吸收和发射最大值明显不同,41的光谱在721 nm处吸收,751 nm处发射,而42比41具有更长的吸收和发射波长(λabs=754 nm,λem=803 nm),由于吡咯环的电子供体作用导致红移。然而,染料41和42的不同构象导致了其光物理性质的显著差异,与41相比,42中吡咯取代基的自由旋转,由于硼中心的氟原子而变得复杂,并且似乎在减慢或被禁止,这与Burgess小组报道的受约束的aza-BODIPY(由B—O键引起)和它的不受约束的前驱体之间的光谱对比一致[52,56]。此外,41和42具有较高的消光系数和较大的荧光量子产量,而42具有较大的斯托克斯位移。染料41在近红外区域稳定性好、灵敏度高、荧光量子产率高,适合标记活细胞用于近红外区域的成像检测。
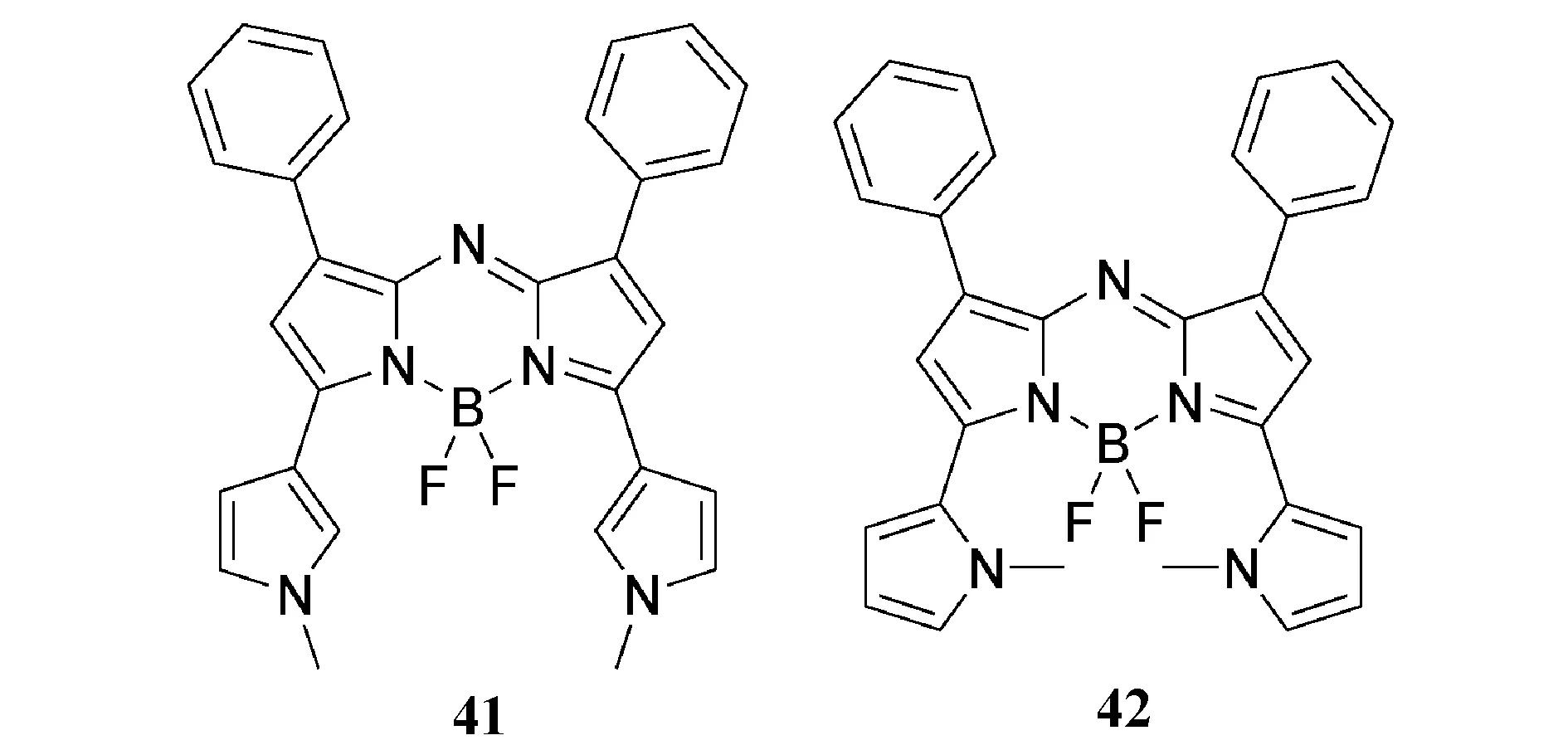
图11 近红外荧光染料aza-BODIPY 41和42
在细胞染色实验中,将含量1.0×10-5mol/L染料41(在0.5%DMSO体积比的PBS中)与Hep-2细胞在37 ℃下孵育15 min,除去多余的染料后,用ArrayScan VTI HCS Reader倒置荧光显微镜进行荧光成像,激光激发波长为620 nm,结果表明,染料41可以有效进行细胞染色(图12)[55]。染料41具有可透膜性,位于细胞质中,而细胞核保持完好,未被染色。
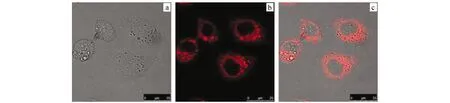
图12 1.0×10-5 mol/L染料41在37 ℃下、0.5%DMSO的PBS中,孵育Hep-2细胞15 min的荧光显微镜成像,黑色区域为细胞核,比例尺:25 μma.白光成像;b.激发光λex=620 nm的成像;c.图像a和b的叠加
4.3 二溴化含噻吩基aza-BODIPY的单重态氧产生性能
由于3,5位具有噻吩环的aza-BODIPY染料的单重态氧产生尚未见报道,作者曾设计合成了2,6-二溴化的aza-BODIPY43和3,5-二溴化的aza-BODIPY44(图13)[57]。43和44的半峰宽(FWHM)有着显著不同,44的吸收带更窄,43的荧光寿命明显短于44的。尽管二者的荧光量子产率略有不同,但消光系数几乎相同。检测单重态氧,结果发现在2,6-位具有溴取代的43的单重态氧的产生比在3,5-位具有溴取代的44更有效。但43是比亚甲蓝弱得多的PS[58]。
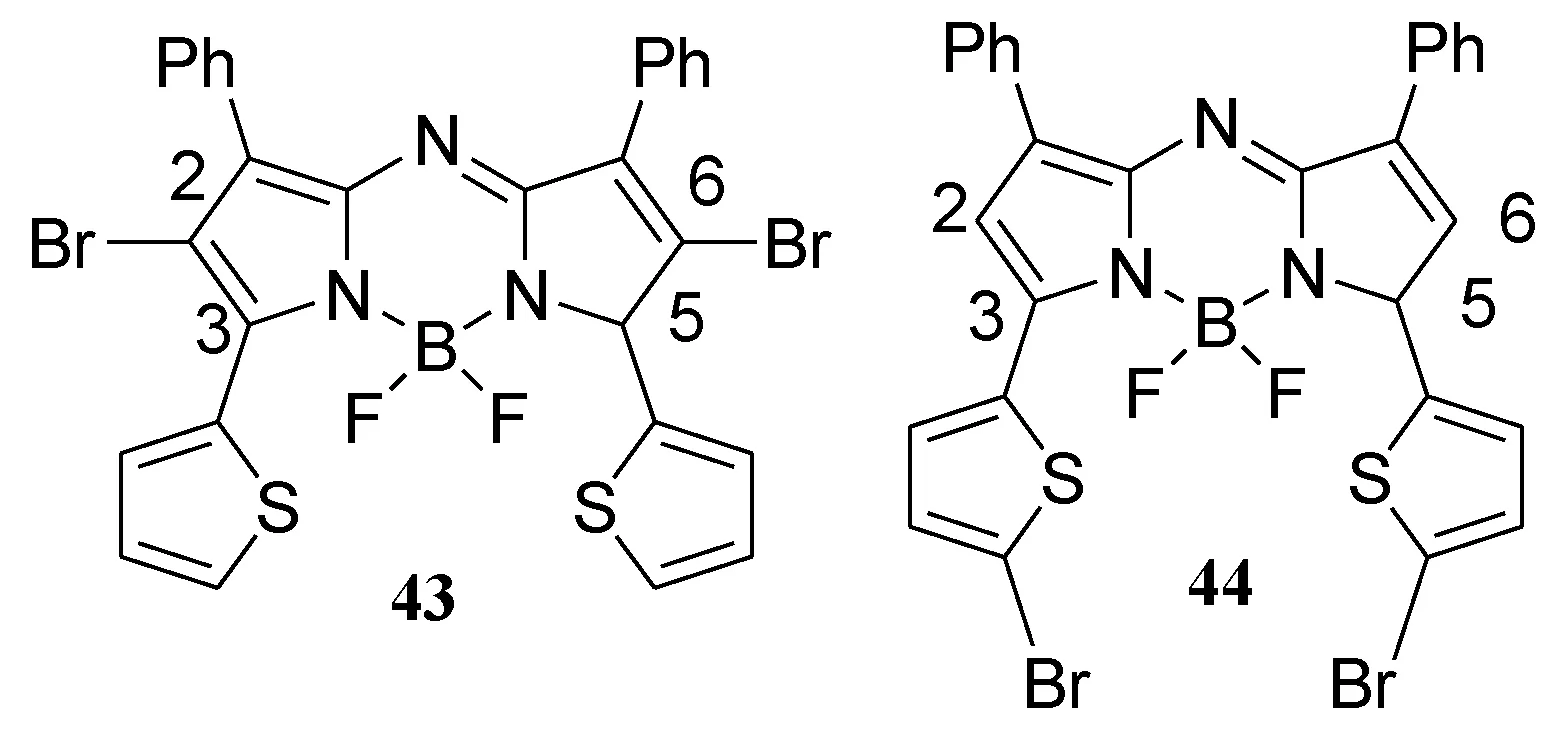
图13 含噻吩基的aza-BODIPY光敏剂
4.4 具有—F/—N3/—NH2基团的近红外aza-BODIPY的合成、结构及光物理性质
aza-BODIPY通过引入一个供电子/吸电子基团,可以增加HOMO和/或降低LUMO能量,进一步减小HOMO-LUMO能级差,达到更大的红移吸收和发射带[59,60]。相比之下,在1/7位置上带有吸电子基团(如—CN)的aza-BODIPY也会使吸收/发射带红移[61]。由于氟是一种强诱导受体,引入氟原子,成功设计合成了45~48(图14)。aza-BODIPY46的固态结构通过单晶X射线分析得到了证实(图15),发现其F—CPh键距比报道的氟化物短。NaN3通过亲核取代,形成了含—N3/—NH2的aza-BODIPY49和50[62](图16),这些aza-BODIPY在近红外区域有吸收和发射。虽然在45~48的1/7位置引入了F原子,但氟原子对光物理性质的影响微乎其微,而带有—N3/—NH2的49和50有着显著的红移,50可作为pH值的荧光探针。
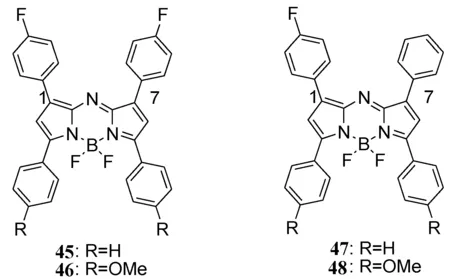
图14 含氟的染料aza-BODIPY 45-48
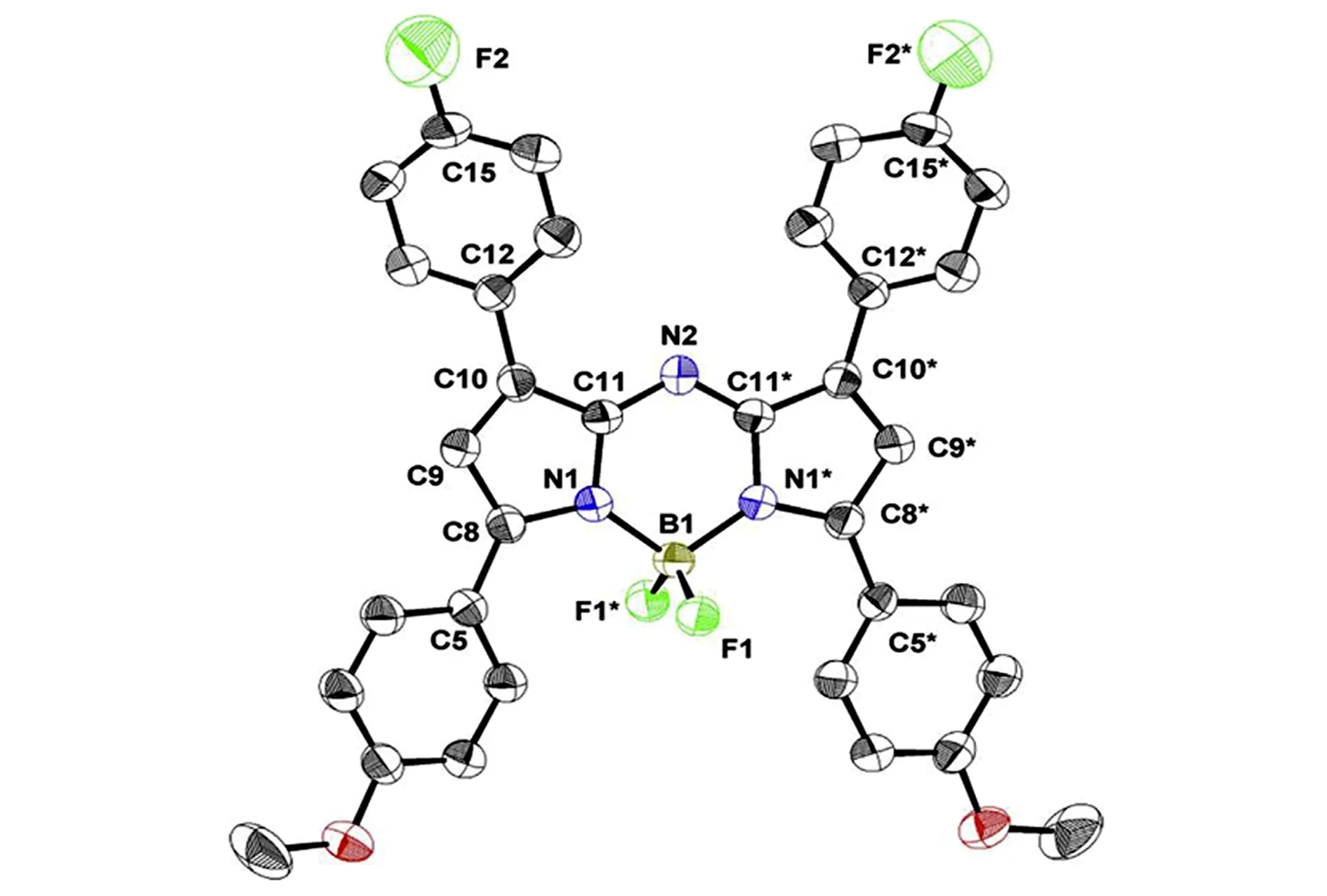
图15 aza-BODIPY 46的ORTEP图[61]
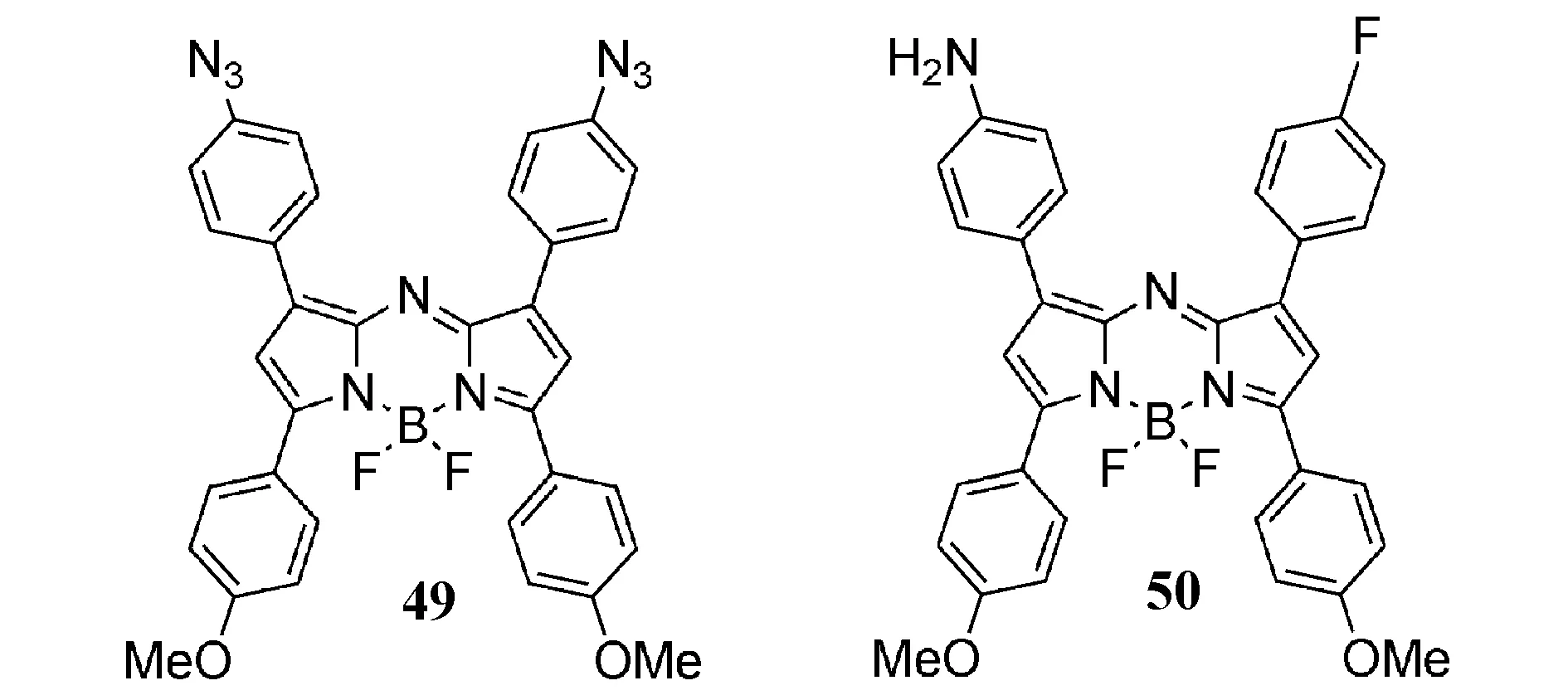
图16 aza-BODIPY 染料49和50
4.5 甲硫基取代BODIPY/aza-BODIPY的合成及应用
甲硫基取代BODIPY/aza-BODIPY极为罕见[63-65],Jiang课题组制备了含有—SMe基团的新吡咯,并应用于合成一系列新的BODIPY/aza-BODIPY51~55[66](图17),为了与—SMe基团的51的光物理性质进行严格比较,我们还制备了—OMe基团取代的已知aza-BODIPY56[67]。由于ICT效应,在荧光染料中引入供电子的甲硫基可以显著降低量子产率,使光谱红移,提高消光系数和大斯托克斯位移。此外,MO计算很好地支持并解释了51和56之间吸收最大值的差异。通过HClO将BODIPY53的硫醚转化为相应的吸电子亚砜,可以恢复量子产率并使其发射光谱蓝移,染料53对HClO具有高敏感性和选择性。
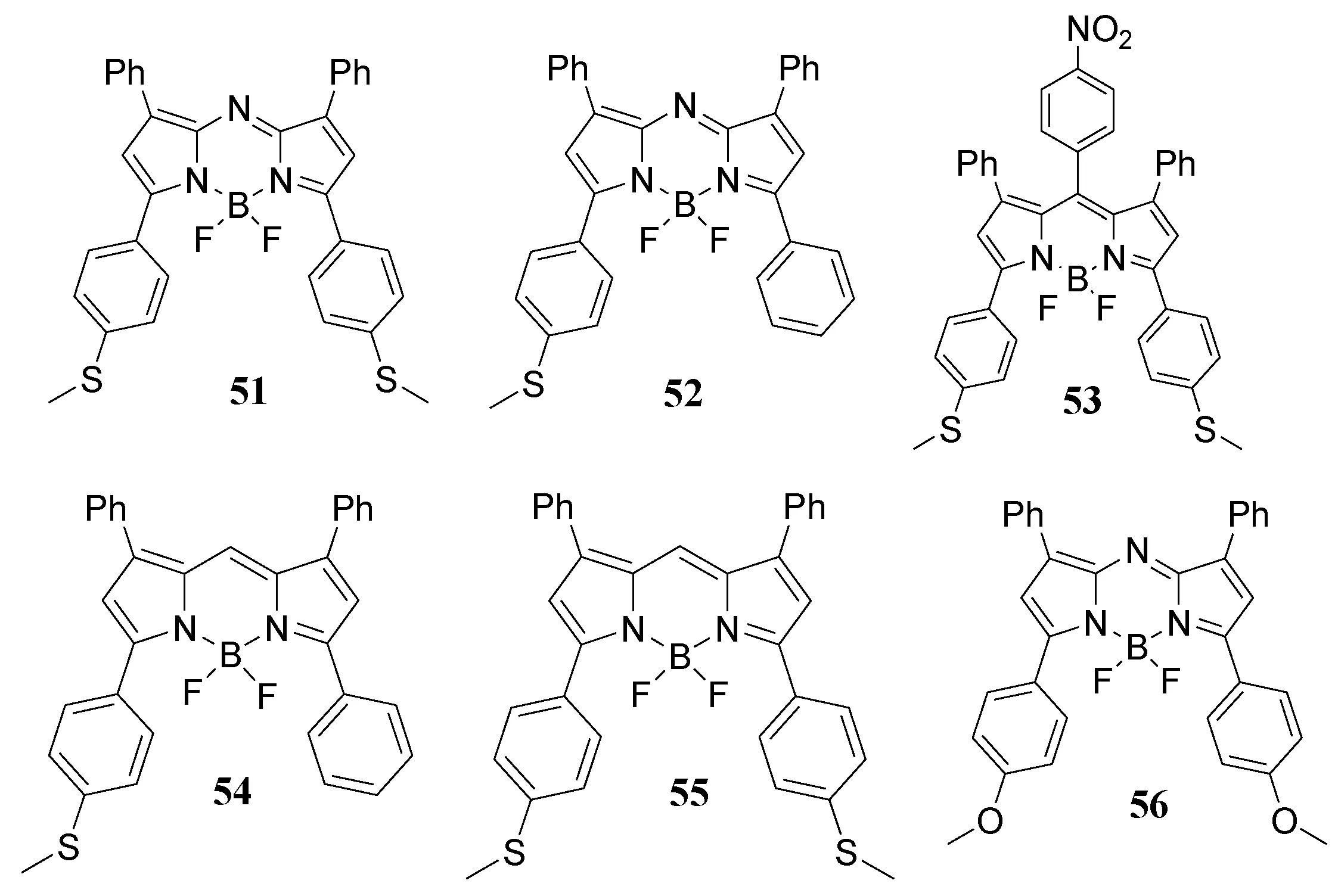
图17 甲硫基取代的染料BODIPY / aza-BODIPY
4.6 Meso-CF3-BODIPY化合物的合成
一锅法合成meso-CF3-BODIPY染料[57,68-72],PhSiCl3在这一合成中起着至关重要的作用,提供了Cl源,生成酰氯。BODIPY57~62[73](图18)吸收光谱覆盖红光区域 (λabs=553~703 nm)。与相应的R-BODIPY (R=H、烷基、芳基等)对比[52],强吸电子基—CF3基团导致吸收光谱红移。Meso-CF3-BODIPY58~61没有荧光。然而,染料62有窄的半峰宽、高摩尔消光系数和较好的荧光量子产率[41]。X-ray单晶衍射证实了meso-CF3-BODIPY59的固态结构 (图 19)。sp3杂化的硼中心出现轻微歪曲的四面体结构,这是—CF3基团的立体位阻引起的结果。
由于强吸电子—CF3基团稳定了反应生成的碳负离子,在80 ℃的低温下,通过Knoevenagel缩合反应合成了BODIPY63(图20)[74,75]。63中的二甲氨基不仅用作pH识别单元,而且又与—CF3组建了推拉系统,染料63是一种近红外pH响应的荧光探针。
Meso-CF3-BODIPY58与NBS反应,生成二溴取代meso-CF3-BODIPY64(图21),64单重态氧生成效率是母体58的2.4 倍。
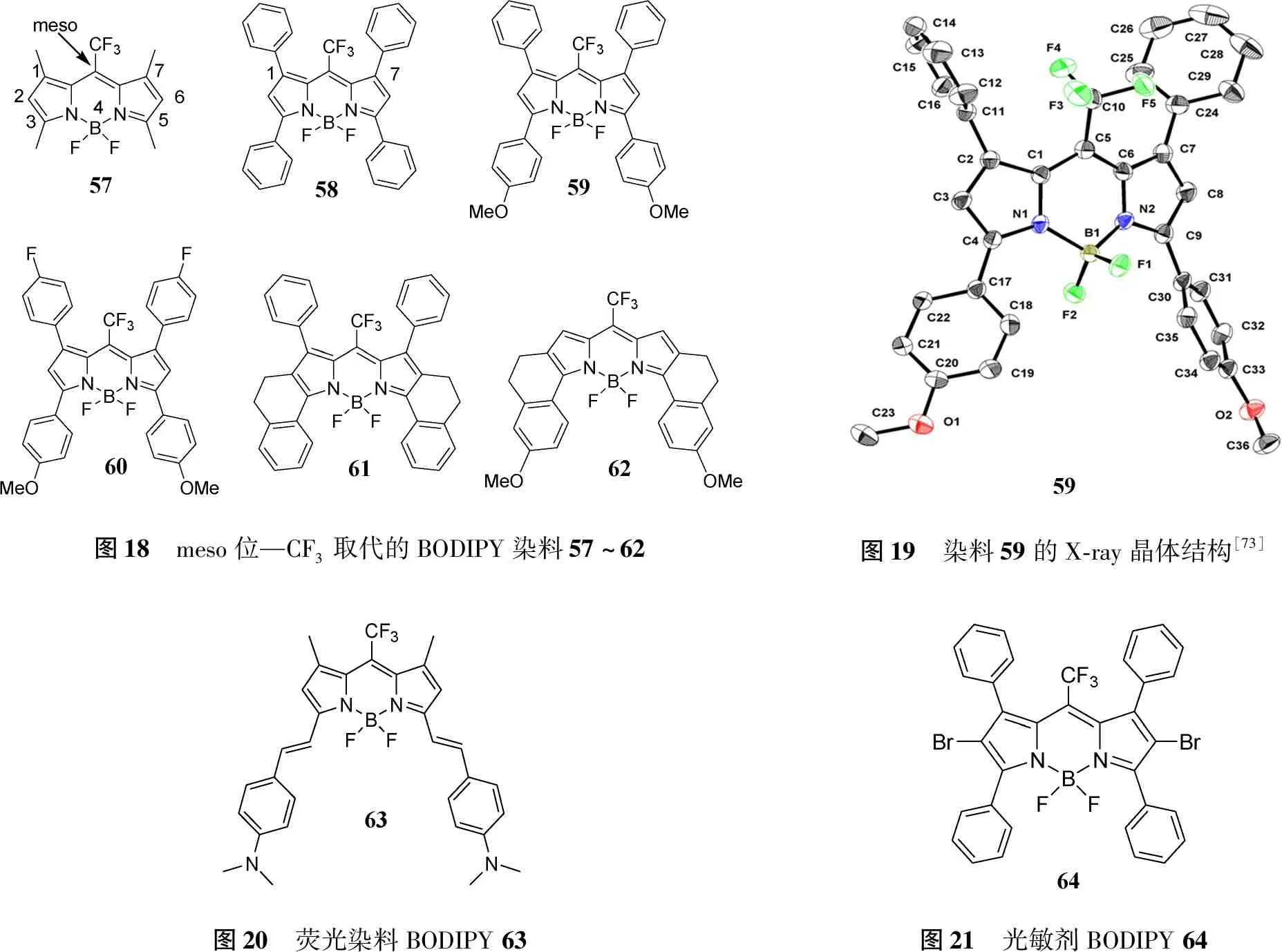
图18 meso位—CF3取代的BODIPY染料57~62图19 染料59的X-ray晶体结构[73]图20 荧光染料BODIPY63图21 光敏剂BODIPY64
4.7 长波长吸收五元环BODIPY/aza-BODIPY的合成及光物理性质
五元环稠合BODIPY/aza-BODIPY具有近似平面的结构[76,77],作者利用五元环设计合成了BODIPY/aza-BODIPY65~68[78](图22)。
为了严格比较光物理性质,还制备了新的BODIPY69(图22)。五元并环和六元并环结构的BODIPY/aza-BODIPY光谱性质几乎一致,通过X射线晶体学分析证实了BODIPY69的固态结构[78](图23),六元环稠合的BODIPY69的母核不是平面而是扭曲的。
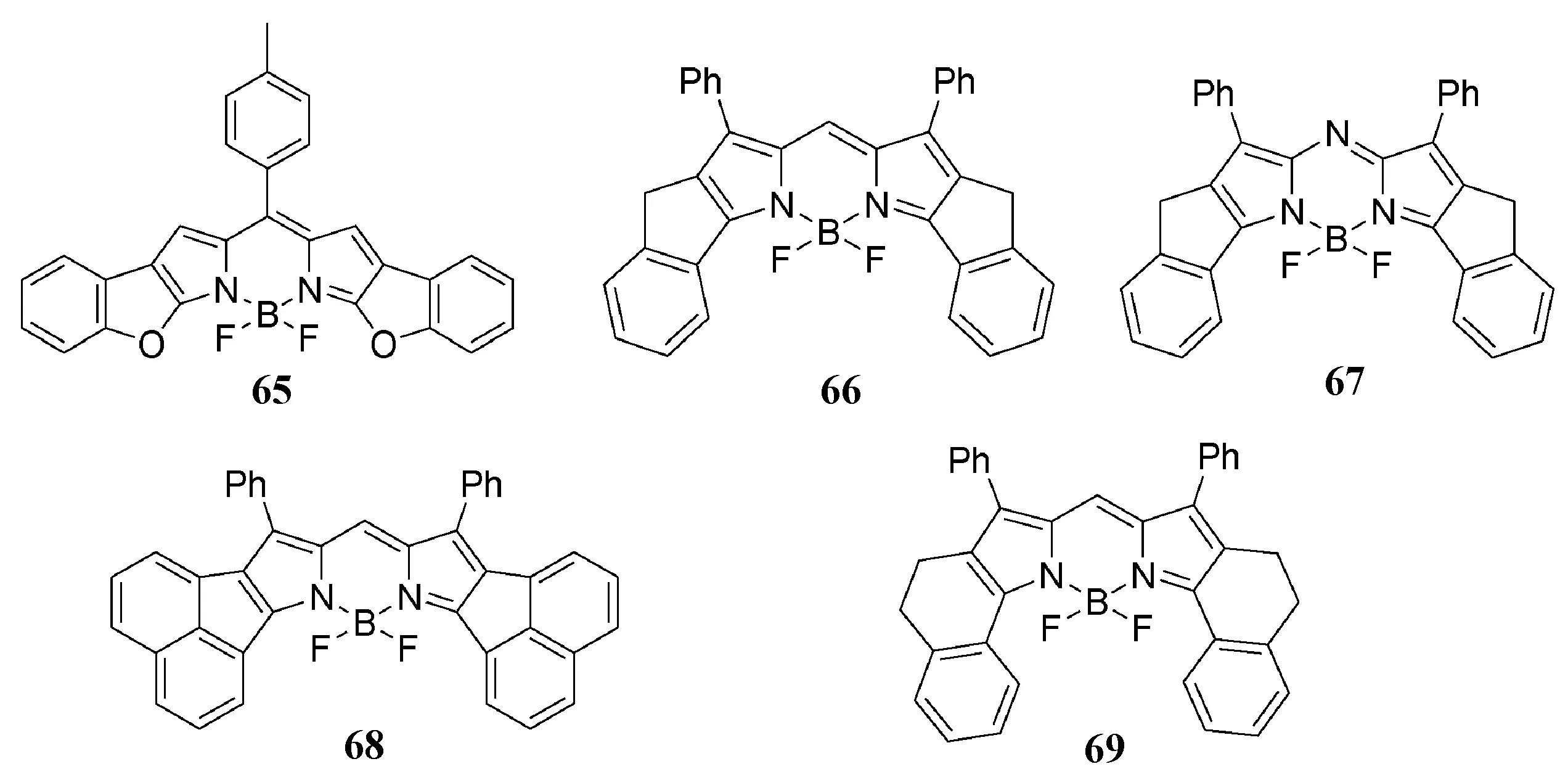
图22 五元环融合BODIPY/aza-BODIPY染料65~69
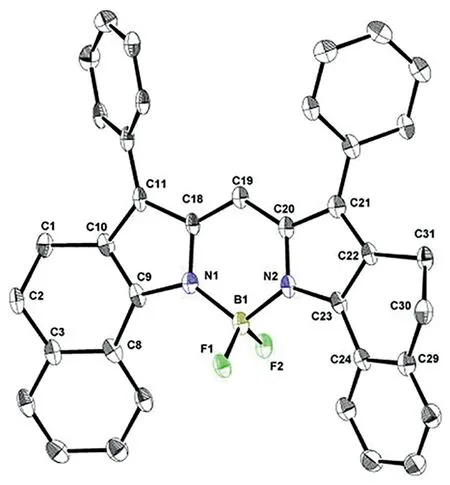
图23 染料69的分子结构[78]
4.8 近红外荧光aza-BODIPY探针用于L-赖氨酸的特异性检测
基于3-氯BODIPY的荧光化学传感器的反应原理[79,80],作者对其进行新的修饰,并通过在C—Cl键中插入噻吩基来构建荧光探针(图24)[81],在CH2Cl2中,aza-BODIPY70在近红外区域有吸收和发射(λabs/λex=732/753 nm),具有高摩尔消光系数和中等荧光量子产率。加入Lys后,N-亲核试剂直接攻击芳环的卤素,产生氨基取代的aza-BODIPY,导致PET效应。探针70对Lys具有选择性和敏感性,并可用于检测PC3细胞中的Lys。
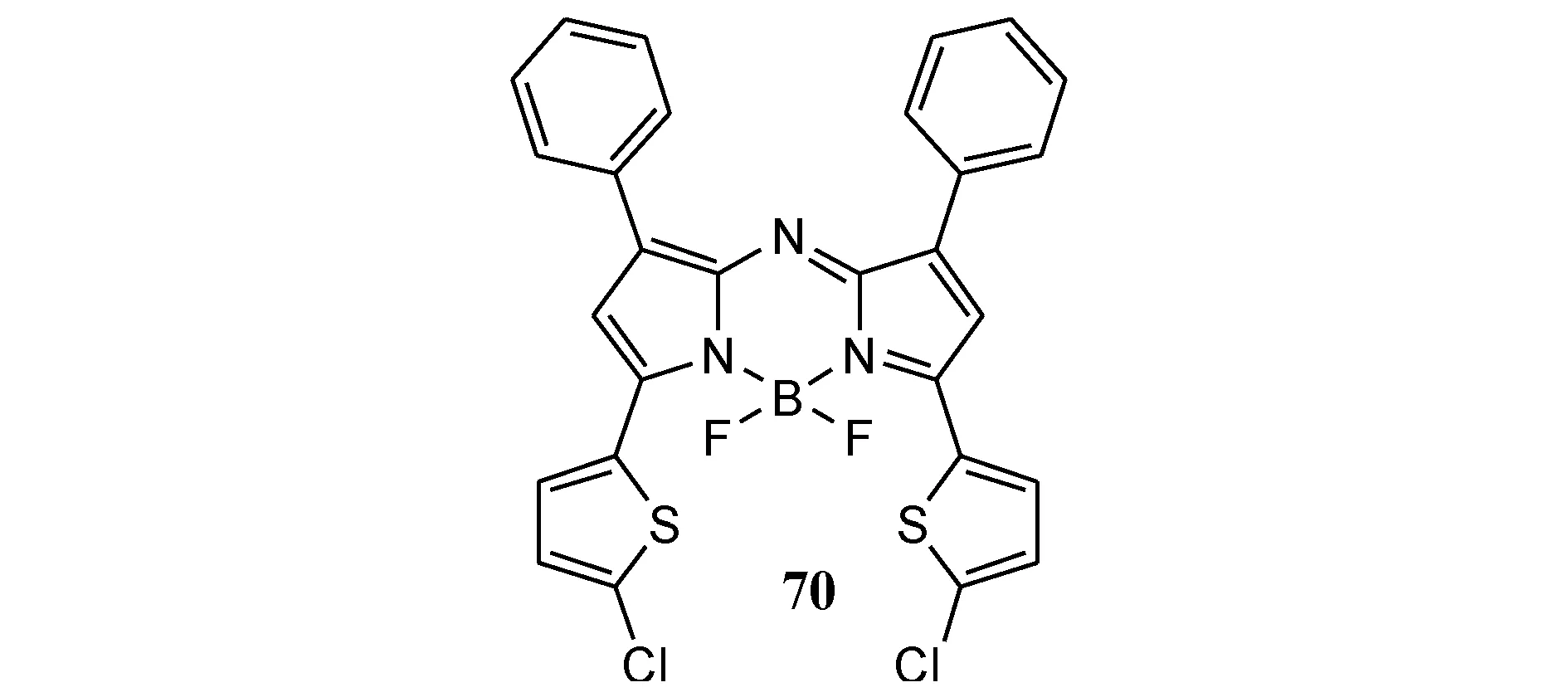
图24 荧光染料BODIPY 70
将2 μmol/L的70与PC3细胞在37 ℃下孵育20 min后,洗涤除去过量的染料。用ArrayScanS VTI HCS Reader倒置荧光显微镜进行荧光成像,在细胞质区域观察到强而明亮的红色荧光图像(λex=655 nm),表明探针70具有出色的细胞膜通透性(图25)。将处理过的细胞与Lys在培养基中于37 ℃孵育20 min后,PC3细胞显示出明显的荧光衰减,显然,添加Lys 20 min后,显微镜图像的荧光强度变得很弱,表明染料70能够有效地检测活细胞内的细胞内Lys摄取。
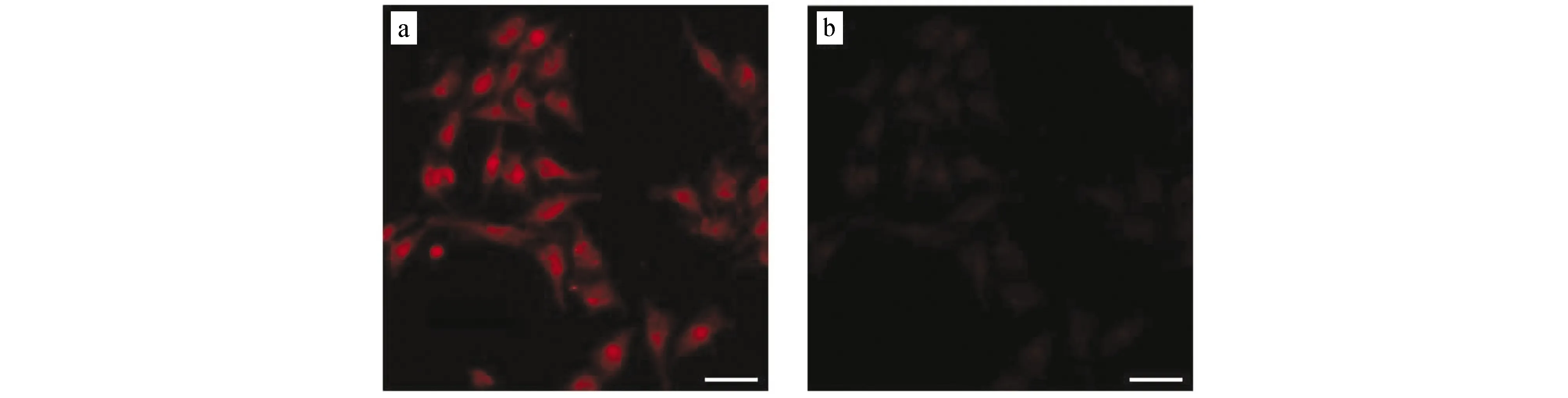
图25 2 μmol/L染料70在37 ℃下、5%DMSO(体积分数)的PBS中孵育PC3细胞20 min的荧光显微镜图像比例尺:20 μma.红色表示细胞质区域被70染色(λex=655 nm);b.进一步与20 μmol/L赖氨酸在37 ℃下反应20 min
4.9 对H2S的高选择性的二硝基氟苯硫解的荧光探针的合成
设计合成了一种检测H2S的“裸眼”荧光开关探针(图26)。在生理pH值7.4时,H2S的主要形态为HS-,HS-/H2S的比值约为3/1[82]。根据文献报道[83-85],作者采用NaHS作为H2S的当量化合物[86],加入NaHS时,通过保护DNP基团可以顺利进行裂解反应。探针71的吸收和发射最大值分别为580 nm和615 nm,探针71为强荧光,加入NaHS后,吸收最大值红移至617 nm,荧光强度显著降低90%。这些结果表明,这种DNP基团与BODIPY母核的直接连接可以有效地恢复荧光团的量子产率。然而,当通过H2S除去71中的二硝基苯以释放羟基时,72中的羟基向BODIPY母核进行电子转移,引起荧光猝灭。
将5 μmol/L的71与HCT-116和CT-26细胞在37 ℃下孵育30 min。在可视化之前,洗涤除去多余的染料。ArrayScanS VTI HCS Reader倒置荧光显微镜进行荧光成像(图27),在细胞质区域观察到强而明亮的红色荧光图像(λex=550 nm),表明探针71具有出色的细胞膜通透性,将处理过的细胞与NaHS(20.0 μmol/L)在培养基中于37 ℃孵育50 min后,HCT-116和CT-26细胞显示出明显的荧光猝灭,并且细胞质区域中未发现明显的荧光,表明染料71能够有效检测活细胞内的细胞内HS-摄取。
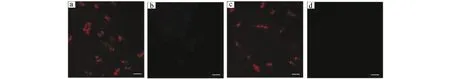
图27 5 μmol/L染料71在37 ℃下孵育HCT-116、CT-26细胞30 min,而后,进一步与20 μmol/L NaHS 在37 ℃孵育50 min的荧光显微镜图像,比例尺:20 μm[86]a.红色表示HCT-116细胞质区域被染料71染色(λex=550nm);b.HCT-116细胞质无色区域为染料71与NaHS (λex=550 nm);c.红色表示CT-26细胞质区域被染料71染色(λex=550 nm);d.CT-26细胞质无色区域为染料71与NaHS (λex=550 nm)
4.10 1,7位含萘基aza-BODIPY染料的合成及其在单重态产氧中的应用
利用重原子效应,通过增加S1→T1跃迁,可以提高单重态氧的生成效率[87]。近红外吸收染料73Br和74Br(λabs=705 nm)光照下可以产生单重态氧(图28)[88]。由于重原子效应,与73H和74H相比,73Br和74Br荧光均非常弱。与相应的母体aza-BODIPY74H(λabs=718 nm)相比,74Br的最大吸收蓝移至698 nm。近红外染料73和74具有高消光系数。与母体aza-BODIPY相比,二溴取代的aza-BODIPY作为PS产生单重态氧,更为有效。在此过程中,没有观察到含萘基的aza-BODIPY染料被光漂白。
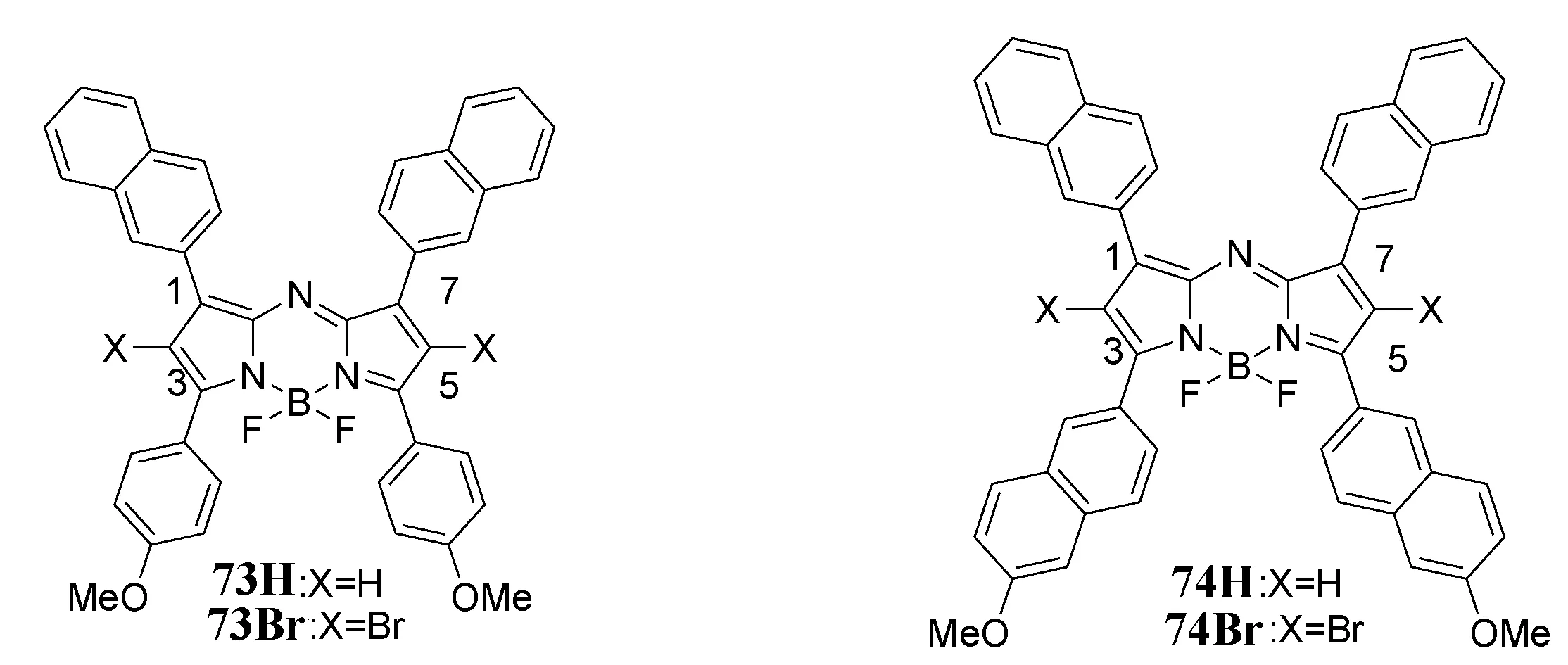
图28 萘取代的aza-BODIPY染料
4.11 新型5,6,5,6-四环吡嗪/吡咯稠合不对称双(BF2)荧光染料BOPYPY的合成、性能及应用
Jiao等[89]报道了含有吡咯和N-杂芳烃衍生物(BOPPY)的不对称双(BF2)荧光团的新结构。2019年,我们首次报道了5,6,5,6-四环吡嗪/吡咯稠合的不对称双(BF2)荧光染料(BOPYPY)(图29)[90],BOPYPY75在490 nm、522 nm处发射,与典型的BODIPY染料相比,具有大的斯托克斯位移(79 nm)。与75相比,BOPYPY76~80通过相应吡咯的π-共轭的延伸,具有长波长吸收(λabs=498~546 nm),并且它们的发射甚至达到红色区域(λem=560~610 nm)。此外,BOPYPY76~80具有高摩尔消光系数、高荧光量子产率和更大的斯托克斯位移(96~106 nm)。BOPYPY75与4-二甲基氨基苯甲醛的Knoevenagel反应,能够平稳地生成带二甲基氨基取代的染料81(图30),其可作为pH响应性荧光传感器检测酸值。
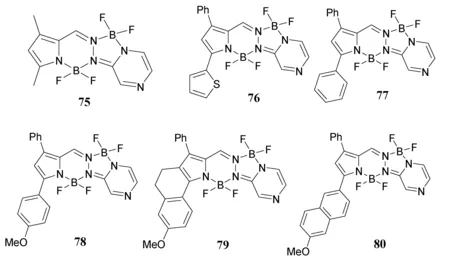
图29 荧光染料BOPYPY 75~80
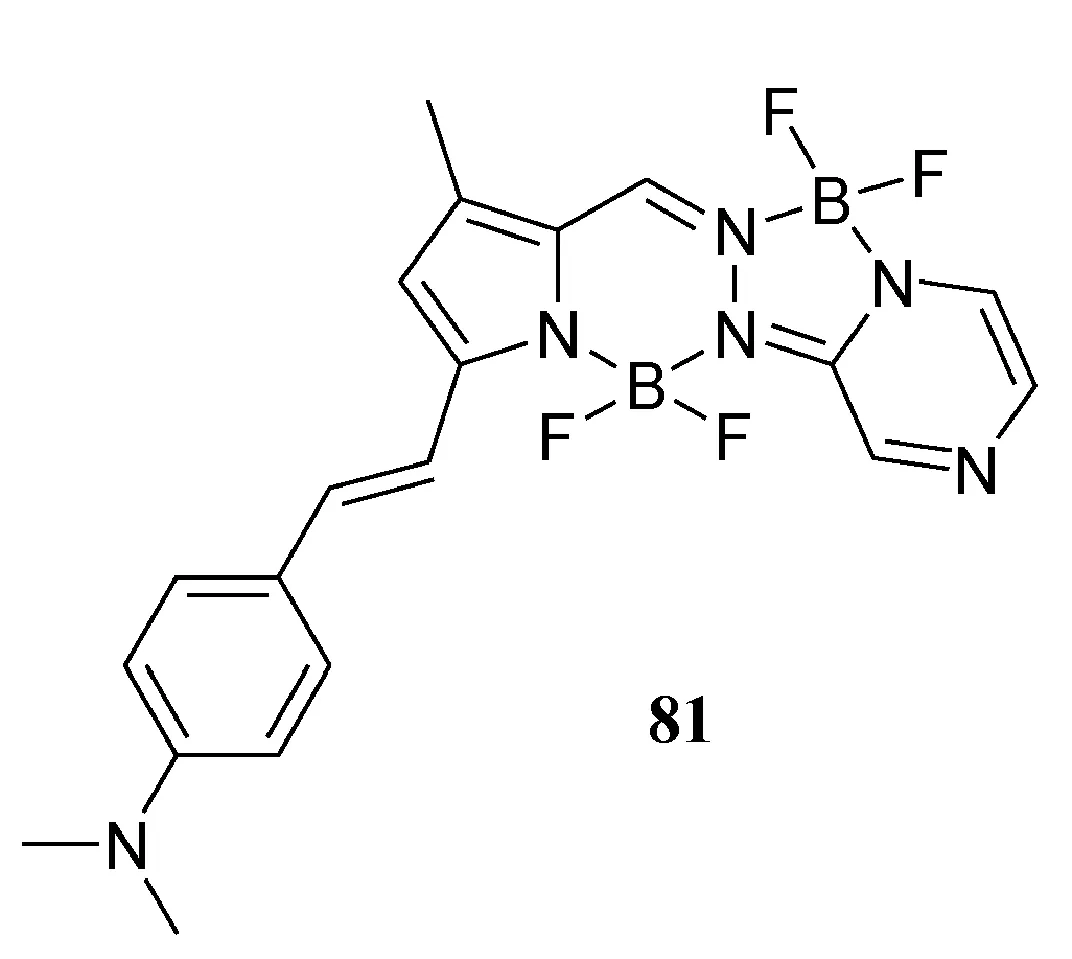
图30 pH荧光分子探针81
4.12 BODIPY/aza-BODIPY在光扳机方面的应用
为了对活细胞中的CO进行选择性成像,Chang及其同事使用了钯配合物82(图31)[91]。由于钯的重原子效应,82的荧光被猝灭。与CO反应后,钯原子从BODIPY中释放出来,导致荧光恢复,荧光开启,对CO具有选择性,并且几乎不受ROS或活性氮(RNS)的影响。
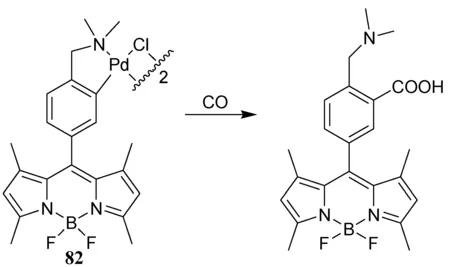
图31 基于钯的重原子效应淬灭的CO响应探针
通过环二氧甲烷中间体进行的苯酚分子内氧化可用于检测ONOO-(图32)[92,93]。通过PeT控制,化合物83与ONOO-反应产生荧光,开启响应[94]。
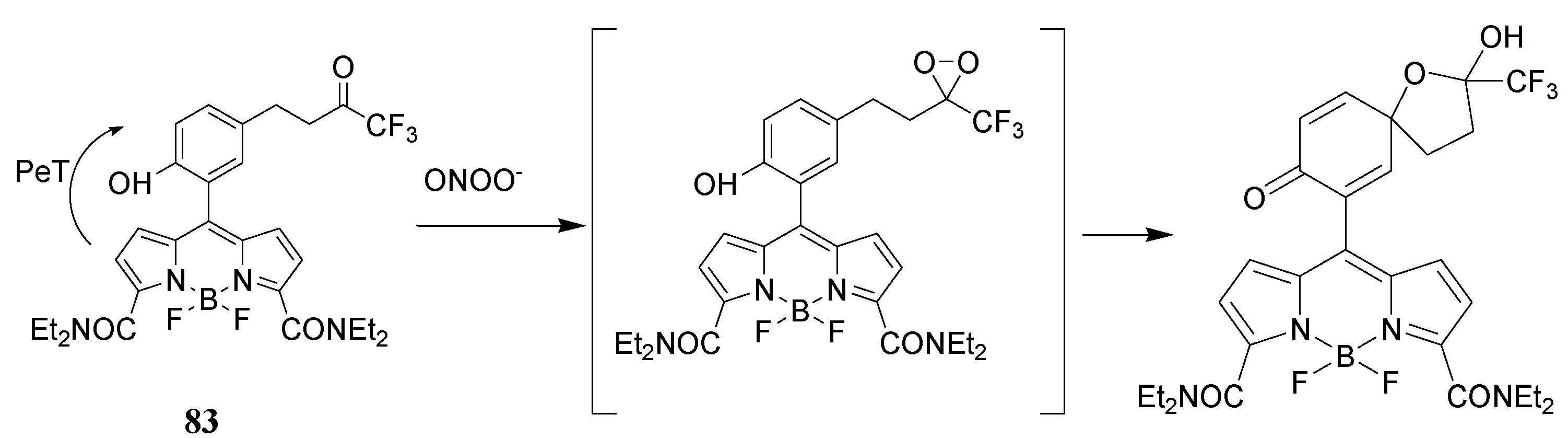
图32 基于ONOO-检测的BODIPY探针
5 结论
尽管Lukyanets的方法很容易实现且在商业上可行,但合成的aza-BODIPY结构单一,其功能很少被报道。O’Shea的方法占据了合成aza-BODIPY的主要位置[95]。而通过Carreira方法合成的具有更长波长的芳基稠合的aza-BODIPY及其应用,未来值得提倡和期待。

