急性缺血性卒中患者脑小血管病总负荷与静脉溶栓治疗转归的关系研究
卓子良,聂志余,刘渊华,郑国将,毛相濡,刘梦,刘务朝
急性缺血性卒中(acute ischemic stroke,AIS)治疗的关键在于早期血管再通、恢复血流灌注、挽救缺血半暗带,而静脉溶栓治疗是当前AIS主要的治疗手段。然而,在溶栓获益的同时还存在梗死后出血转化、高灌注综合征等不良事件的发生,且临床预后难以预判。
脑小血管指脑的小穿支动脉和小动脉(直径40~200 μm)、毛细血管及小静脉,由它们构成了脑组织血供的基本单位,对脑功能的维持和调节起着重要作用。脑小血管病(cerebral small vessel disease,CSVD)泛指上述脑小血管的各种病变所导致的临床、影像及病理表现的综合征,在卒中、痴呆、脑老化及神经变性疾病等发病和进展过程中均具有重要作用[1]。临床上多以神经影像学特征作为CSVD的观察指标,包括腔隙性脑梗死(lacunar infarction,LI)、脑白质病变(white matter hyperintensities,WMH)、脑微出血(cerebral microbleed,CMB)、血管周围间隙扩大(enlarged perivascular spaces,ePVS)和脑萎缩。
目前的研究大多仅关注某一种CSVD表现对于AIS静脉溶栓结局的影响,未重视CSVD的综合评估对AIS静脉溶栓治疗的影响。鉴于患者可能同时存在2种甚至更多亚型的CSVD,Staals等[2]提出的基于脑MRI的CSVD总负荷评分可以整体反映脑小血管病变情况。本研究主要探讨CSVD总负荷评分与AIS患者静脉溶栓转归的相关性。
1 研究对象与方法
1.1 研究对象 本研究为回顾性研究,收集2012年3月-2018年1月就诊于同济大学附属同济医院神经内科接受rt-PA静脉溶栓治疗的AIS患者。入选标准:①符合《中国急性缺血性卒中诊治指南2014》[3]中AIS的诊断标准;②符合静脉溶栓治疗适应证;③静脉溶栓治疗取得患者或者家属的知情同意;④入院24 h内完成多模MRI检查(包含T1WI、T2WI、DWI、FLAIR和SWI序列),DWI显示新发脑梗死病灶。排除标准:①同AIS静脉溶栓禁忌证;②入院前1周有肺部感染及泌尿道感染;③既往有胃溃疡病史的患者;④后循环梗死患者;⑤临床资料不完整者。
1.2 研究方法
1.2.1 资料收集 记录患者的人口学信息、基线NIHSS评分、发病至溶栓治疗时间(onset to needle time,ONT)、血管相关危险因素(年龄、高血压、糖尿病及吸烟史等)、住院期间并发症、头颅MRI影像学资料等。在发病后90±7 d通过卒中门诊面对面/电话对患者进行常规随访,由受过培训的研究者对患者进行mRS评分。所有数据均来源于同济大学附属同济医院溶栓卒中数据库及患者住院病历档案。参与病例收集和录入的人员均经过培训。
高血压诊断标准参照《中国高血压防治指南》[4]。糖尿病诊断标准参照《中国2型糖尿病防治指南(2013年版)》[5]。高脂血症参照标准符合《中国成人血脂异常防治指南(2016修订版)》[6]。
1.2.2 脑小血管病总体负荷判定标准 使用西门子公司3.0 T磁共振扫描仪对患者进行头颅MRI检查,由经过培训的神经内科医师和影像科医师共同进行CSVD总负荷评分。如有争议,通过协商达成一致。为了全面评估脑小血管病变情况,本研究纳入脑萎缩指标,CSVD总负荷评分为0~5分,总评分越高表示脑小血管病变程度越重。CSVD总负荷评分具体评分细则如下。
(1)LI:≥2个腔隙性脑梗死灶(3 mm<直径<20 mm),记1分。
(2)WMH:使用Fazekas分级法[7]对WMH进行评估。脑室旁WMH评分:0分,无病变;1分:帽状或者铅笔样薄层病变;2分:病变呈光滑的晕圈;3分:不规则的脑室旁高信号,延伸到深部白质。深部WMH评分:0分:无病变;1分:点状病变;2分:病变开始融合;3分:病变大面积融合。Fazekas分级法中脑室旁WMH达到3分或深部WMH达2或3分,记1分。
(3)基底节区ePVS:根据Doubal等[8]研究使用的半定量量表将ePVS(直径≤3 mm)评为5级。0级:0个ePVS;1级(轻度):1~10个ePVS;2级(中度):11~20个ePVS;3级(重度):21~40个ePVS;4级(极重度):≥40个ePVS。基底节区ePVS≥2级,即基底节区ePVS数量>10个,记1分。
(4)脑萎缩:参照Farrell等[9]的评分方式对脑萎缩进行评级,将脑萎缩程度>50%的参照对象定义为中重度脑萎缩,记1分。
(5)CMB:≥1个微出血病灶,记1分。
1.2.3 主要结局事件的定义
(1)采用mRS量表在发病后90(±7)d时对患者进行预后评估。mRS评分≤2分定义为预后良好;mRS评分≥3分定义为预后不良。
(2)AIS患者住院期间(1~15 d)新发的肺部感染、消化道出血、泌尿道感染(泌尿系统症状伴尿白细胞计数>10个/高倍视野或菌落计数>1×105/mL)等并发症定义为住院期间并发症。
1.2.4 统计学方法 采用SPSS 20.0软件进行统计学处理。符合正态分布的计量资料以表示,组间比较采用独立样本t检验;不符合正态分布的计量资料以中位数(四分位数)表示,组间比较采用非参数Mann-Whitney U检验;计数资料以频数(%)表示,组间比较采用χ2检验。将单因素分析中P<0.05的变量纳入多因素Logistic回归分析模型分析确定预后不良、住院期间并发症的独立危险因素。以P<0.05为有差异具有统计学意义。
2 结果
最终纳入符合入排标准的患者178例,其中男性125例(70.2%),女性53例(29.8%),平均年龄62.3±10.5岁。中重度脑萎缩者57例(32.0%);≥2个LI者104例(58.4%);基底核区ePVS者119例(66.9%),其中中度以上病变21例(11.8%);CMB者41例(23.0%)。基线NIHSS评分为8(4~13)分,其中轻型卒中(NIHSS评分≤3分)34例(19.1%)。发病至开始治疗时间为173.00(130.00~210.00)min。90 d预后良好128例(71.9%),预后不良50例(28.1%)。住院期间发生并发症(肺部感染、消化道出血和泌尿道感染等)38例(21.3%)。死亡5例(2.8%),其中3例死于重症肺炎、2例死于脑疝。CSVD总负荷评分0分44例(24.7%),1分49例(27.5%),2分50例(28.1%),3分24例(13.5%),4分10例(5.6%),5分1例(0.6%)。
2.1 急性缺血性卒中患者静脉溶栓90 d预后的影响因素 单因素分析显示:与预后良好组相比,预后不良组患者年龄>65岁、高血压、心房颤动、糖尿病、吸烟、中重度脑白质病变、多发性腔隙性脑梗死、CSVD总负荷评分≥3分的比例和基线NIHSS评分均高于预后良好组,差异具有统计学意义(表1)。
多因素Logistic分析显示:糖尿病(OR 2.919,95%CI 1.044~8.162,P=0.041),吸烟(OR 7.752,95%CI 2.300~26.192,P=0.001),心房颤动(OR 6.553,95%CI 1.733~24.785,P=0.006),基线NIHSS评分(OR 1.354,95%CI 1.224~1.497,P<0.001),CSVD总负荷评分≥3分(OR 3.787,95%CI 1.127~12.728,P=0.031)是AIS患者静脉溶栓预后不良的独立危险因素。高血压(P=0.354)、中重度脑白质病变(P=0.34)、多发性腔隙性脑梗死(P=0.358)、年龄>65岁(P=0.828)不是患者90 d预后的独立影响因素。
2.2 脑小血管病变与静脉溶栓患者住院期间并发症的关系 单因素分析表明:与无并发症组相比,并发症组患者年龄>65岁、心房颤动、糖尿病、多发性腔隙性脑梗死、中重度脑萎缩、CSVD总负荷评分≥3分的比例和基线NIHSS评分均高于无并发症组,差异具有统计学意义(表2)。
多因素Logistic分析发现:CSVD总负荷评分≥3分(OR 4.643,95%CI 1.562~13.801,P=0.006)、基线NIHSS评分(OR 1.266,95%CI 1.163~1.377,P<0.001)是静脉溶栓患者住院期间发生并发症的独立危险因素。年龄>65岁(P=0.938)、糖尿病(P=0.140)、心房颤动(P=0.366)、多发性腔隙性脑梗死(P=0.240)、中重度脑萎缩(P=0.107)不是患者住院期间并发症的独立影响因素。
3 讨论
本研究通过回顾性分析发现,CSVD总体负荷与AIS静脉溶栓患者90 d不良预后、住院期间并发症密切相关。既往研究大多数仅限于研究单一的CSVD影像学特征,如脑白质病变严重程度与卒中后神经功能缺损程度呈正相关[10];CMB可增加AIS患者溶栓后临床不良转归风险及症状性出血转化的风险[11];基底核区ePVS与高血压导致的血管损害相关,其中严重病变者(基底核区病变数量>20)与卒中的复发相关[12]。单一的CSVD影像学特征并不能有效预测静脉溶栓患者临床转归情况,而CSVD总负荷评分能更好地反映全脑小血管病变负荷情况,有望用于对卒中单元静脉溶栓患者不良预后及住院期间并发症的评估与预测研究。
近年来国内外对CSVD总负荷评分较为关注。Lau等[13]将CSVD总体负荷作为影像学标志物预测非致残性和致残性复发性卒中,CSVD总负荷评分越高则AIS复发率越高;Arba等[14]的研究显示,CSVD总负荷评分2~3分的AIS患者溶栓后约半数转归不良或在90 d内死亡;朱慧等[15]发现CSVD总体负担与大动脉粥样硬化型卒中患者90 d预后密切相关。但目前国内外关于CSVD总负荷评分在静脉溶栓人群中的研究尚少。本研究经多因素Logistic回归分析表明,CSVD总负荷评分≥3分是AIS患者静脉溶栓90 d不良预后的独立危险因素,说明全脑小血管病变的严重程度会影响静脉溶栓患者的短期预后。
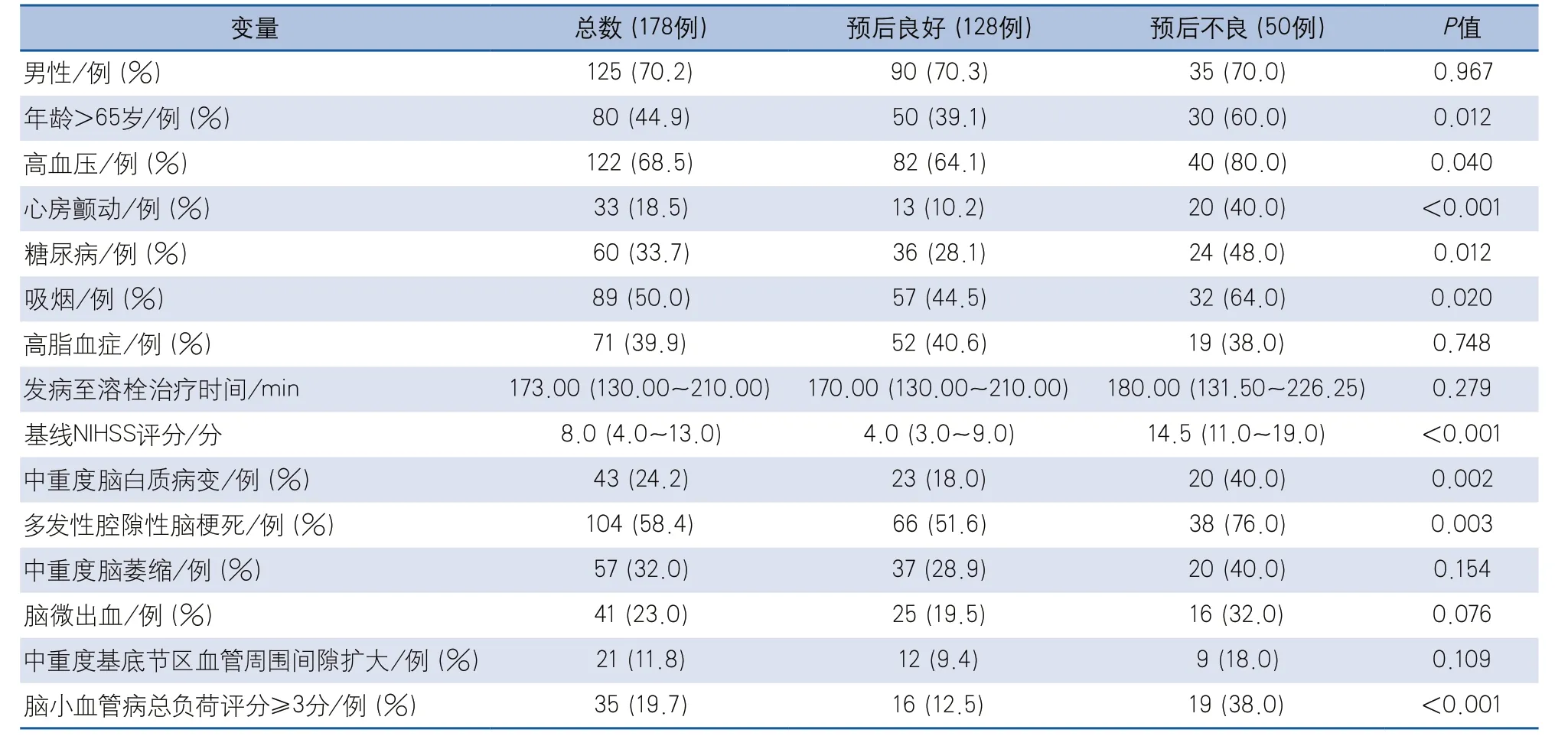
表1 入组患者按90 d不同预后分组的基线资料比较
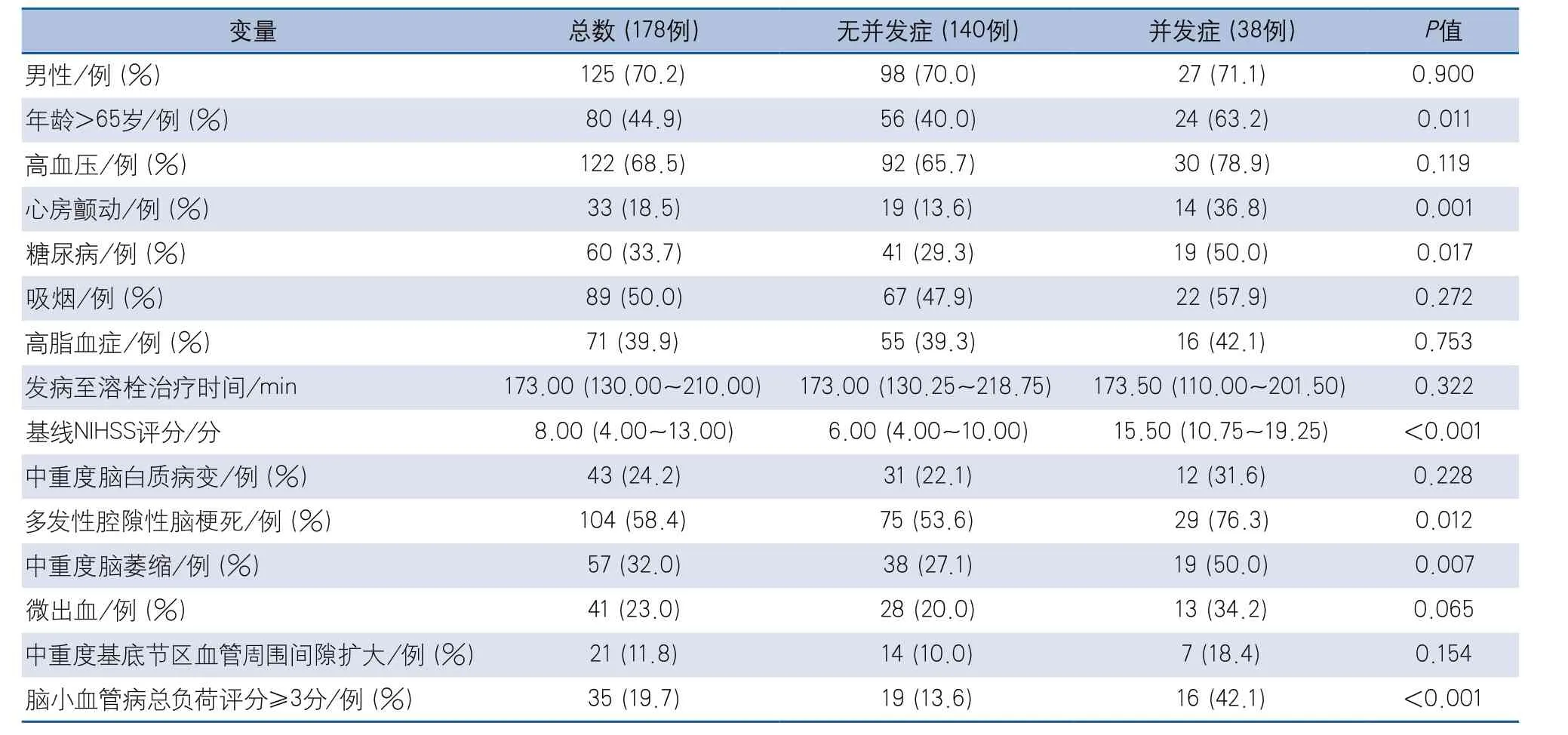
表2 入组患者按有无并发症分组的基线资料比较
临床上AIS患者特别是重症患者容易出现如肺部感染、泌尿感染和消化道溃疡等并发症,但目前国内外关于脑小血管病变与卒中后并发症相关研究尚少,它们之间的联系尚不明确。本研究从CSVD角度,探讨CSVD的严重程度与住院期间并发症的关系。结果显示CSVD总负荷评分≥3分是AIS静脉溶栓患者住院期间发生并发症的独立危险因素。
CSVD影响静脉溶栓患者临床预后的机制可能包括:①卒中的功能恢复涉及广泛的神经网络,通过替代受损的结构和建立新的神经网络以改变功能受损状态,严重CSVD对神经网络、脑血管自动调节能力及侧支循环代偿功能损害会影响卒中预后转归[13];②CSVD负荷高也与神经变性疾病有关,如阿尔茨海默病,导致日常生活自理能力的下降,这会进一步影响卒中二级预防药物的规律使用及康复训练的依从性,使并发症发生率的增加[16-17];③总CSVD常伴随高血压、糖尿病、高龄和心房颤动等血管危险因素,这些因素也与卒中相关性肺炎的发生密切相关[18];④CSVD负荷较大的患者多具有高龄的特点,高龄可能会造成心肺功能储备下降、卧床比例的上升,进而导致住院期间并发症的发生;⑤多发性腔隙性脑梗死累及皮质核束、锥体外通路、皮质脑室周围连接时可引起卒中后吞咽障碍导致肺部感染的发生率增高;脑白质疏松是大脑功能减退的重要病理改变,与卒中后肺炎的发生情况密切相关[19]。
综上所述,CSVD总负荷评分有望作为预测AIS静脉溶栓治疗预后的工具,在未来的临床研究中对危险分层有帮助。本研究尚存在以下不足:①本研究是回顾性单中心研究,样本量较小;②没有排除既往卒中遗留有后遗症的患者;③没有校正一些潜在的混杂因素,如脑梗死体积、颅内外动脉狭窄/闭塞、卒中后二级预防及后续康复和护理等情况。

