吡格列酮治疗非酒精性脂肪肝有效性及安全性的Meta分析
于淙 欧阳天佐 周培
摘要:目的 对吡格列酮治疗非酒精性脂肪肝是否有效及安全进行系统评价。方法 电子检索截至2019年8月之前公开发表在万方数据库、中国期刊全文数据库(CNKI)、中国生物医学文献数据库(CBM)、中文科技期刊全文数据库(VIP)、PubMed、Cochrane Library的随机对照试验,包括使用任何方案的吡格列酮与安慰剂的非酒精性脂肪肝患者的比较。主要结局包括肝脏病理、肝脏生化、胰岛素抵抗、不良反应。结果 最终纳入10篇文献,共有723例患者。Meta分析结果显示,吡格列酮可以减轻非酒精性脂肪肝患者肝脂肪变性(OR=0.26,95%CI:0.14~0.46)、肝气球样变(OR=0.38,95%CI:0.24~0.60)、肝小叶炎症(OR=0.33,95%CI:0.21~0.50)、肝纤维化(OR=0.57,95%CI:0.37~0.88),改善ALT(MD=10.33,95%CI:3.27~17.38)、AST(MD=9.51,95%CI:3.03~15.99)、空腹血糖(MD=0.47,95%CI:0.20~0.75)、胰岛素抵抗指数(HOMA-IR)(MD=1.17,95%CI:0.82~1.51)等指标,与对照组比较,差异有统计学意义(P<0.05)。结论 吡格列酮可有效治疗非酒精性脂肪肝,尤其在改善肝组织学、肝功能、改善胰岛素抵抗等方面有較为明显优势。不良反应主要为肌肉酸痛,总体不良反应较少且均较轻。
关键词:吡格列酮;非酒精性脂肪肝;不良反应
中图分类号:R575 文献标识码:A DOI:10.3969/j.issn.1006-1959.2020.13.017
文章编号:1006-1959(2020)13-0060-05
Meta-analysis of the Efficacy and Safety of Pioglitazone
in the Treatment of Non-alcoholic Fatty Liver
YU Cong1,OUYANG Tian-zuo1,ZHOU Pei2
(1.Department of Infectious Diseases,Weihai Central Hospital,Weihai 264400,Shandong,China;
2.Department of Infectious Diseases,the Affiliated Hospital of Tibet Nationalities University,Xianyang 712000,Shaanxi,China)
Abstract:Objective To systematically evaluate whether pioglitazone is effective and safe in the treatment of non-alcoholic fatty liver.Methods Electronic retrieval as of August 2019. Randomized controlled trials published in Wanfang database, Chinese Journal Full-text Database (CNKI), Chinese Biomedical Literature Database (CBM), Chinese Science and Technology Journal Full-text Database (VIP), PubMed, Cochrane Library, Including comparison of pioglitazone with placebo in nonalcoholic fatty liver patients. The main outcomes include liver pathology, liver biochemistry, insulin resistance, and adverse reactions.Results Finally, 10 articles were included, with a total of 723 patients. Meta analysis results showed that pioglitazone can reduce hepatic steatosis (OR=0.26, 95%CI: 0.14~0.46), hepatic balloon-like degeneration (OR=0.38, 95%CI: 0.24~0.60), liver Lobular inflammation (OR=0.33, 95%CI: 0.21~0.50), liver fibrosis (OR=0.57, 95%CI: 0.37~0.88), improve ALT (MD=10.33, 95%CI: 3.27-17.38), AST (MD=9.51, 95%CI: 3.03~15.99), fasting blood glucose (MD=0.47, 95%CI: 0.20~0.75), insulin resistance index (HOMA-IR) (MD=1.17, 95%CI: 0.82~1.51 )and other indicators, compared with the control group, the difference was statistically significant (P<0.05).Conclusion Pioglitazone can effectively treat non-alcoholic fatty liver, especially in improving liver histology, liver function and insulin resistance. The adverse reactions were mainly muscle aches, and the overall adverse reactions were few and mild.
Key words:Pioglitazone;Non-alcoholic fatty liver;Adverse reactions
非酒精性脂肪肝(non-alcoholic fatty liver)已成为最常见的慢性肝病[1],其特点是在早期没有大量饮酒的情况下,甘油三酯积累(>5%的肝细胞),出现脂肪变性、小叶炎症、肝细胞损伤,并在晚期进展为肝硬化和肝细胞癌[2,3]。非酒精性脂肪肝相关的肝硬化可能成为肝移植的主要原因[4]。目前未见单独针对非酒精性脂肪肝治疗的药物报道,唯一有效治疗是生活方式干预,主要为运动和减轻体重[5]。因此,寻找新的治疗靶点和开发新的治疗方法十分重要。由于非酒精性脂肪肝和2型糖尿病之间有共同的流行病学和病理生理特征,多年来许多抗糖尿病药物在非酒精性脂肪肝患者中得到了广泛的评价[6]。本研究通过对吡格列酮治疗非酒精性脂肪肝相关随机对照实验进行Meta分析,旨在评价吡格列酮治疗非酒精性脂肪肝的安全性及有效性,现报道如下。
1资料与方法
1.1检索策略 应用计算机检索2019年8月之前被收录在PubMed、万方数据库、Cochrane、Library、中国期刊全文数据库(CNKI)、中文科技期刊全文数据库(VIP)、中国生物医学文献数据库(CBM)关于吡格列酮治疗非酒精性脂肪肝的随机对照实验。英文检索词为piogliatzone,non-alcoholic fatty liver。中文检索词为吡格列酮、非酒精性脂肪肝。
1.2纳入与排除标准 纳入标准:①研究设计:获取使用吡格列酮治疗非酒精性脂肪肝的随机对照试验,选择指标统一的文献;②研究对象:确诊为非酒精性脂肪肝并且使用吡格列酮治疗的患者,标准符合美国肝病研究学会的相关要求[7];③干预措施:试验组与对照组使用同样的辅助干预方案,在此基础上试验组加用吡格列酮(种类、方案、剂量、疗程不限)治疗;④结局指标:肝脏病理、肝脏生化、空腹血糖、胰岛素抵抗指数、不良反应。排除标准:①动物实验研究;②试验设计方案不妥;③统计学方法欠严谨;④经验、个案、综述;⑤文献质量差;⑥不能获取全文。
1.3文献质量评价 采用Cochrane系统评价员手册偏倚风险评价工具[8],评价的内容包括以下7个方面:①随机方法;②分配隐藏;③对研究者和研究对象是否采用盲法;④研究结局盲法评价;⑤结果数据完整性;⑥选择性报告研究结果;⑦其他偏倚。将评价数据填入偏倚风险表,最后将偏倚风险总结为偏倚风险总结图。
1.4资料提取 根据上述标准,由2名评价者独自检索、纳入并评价。如果意见不统一,则进行讨论或交由第3方评价者协商。提取的内容包括以下4个方面:①论文标题,第一作者姓名,论文发表刊物年代,研究起源;②研究设计方案;③干预细节、随访时间;④结局指标:肝脏病理、肝脏生化、空腹血糖、胰岛素抵抗指数、不良反应。
1.5统计学分析 采用由 Cochrane 协作网提供的 RevMan5.3 软件进行分析。将纳入的研究进行异质性检验。若P>0.1,I2<50%,表明纳入的各项研究具有同质性,采用固定效应模型计算合并统计量;若P<0.1,I2>50%,表明纳入的各项研究存在异质性,则采用随机效应模型计算合并统计量。计量资料采用均数差(MD)、计数资料采用相对危险度(OR)为疗效分析统计量,各效應量均以95%可信区间(CI)表示。当 P≤0.05 时,认为差异有统计学意义。
2结果
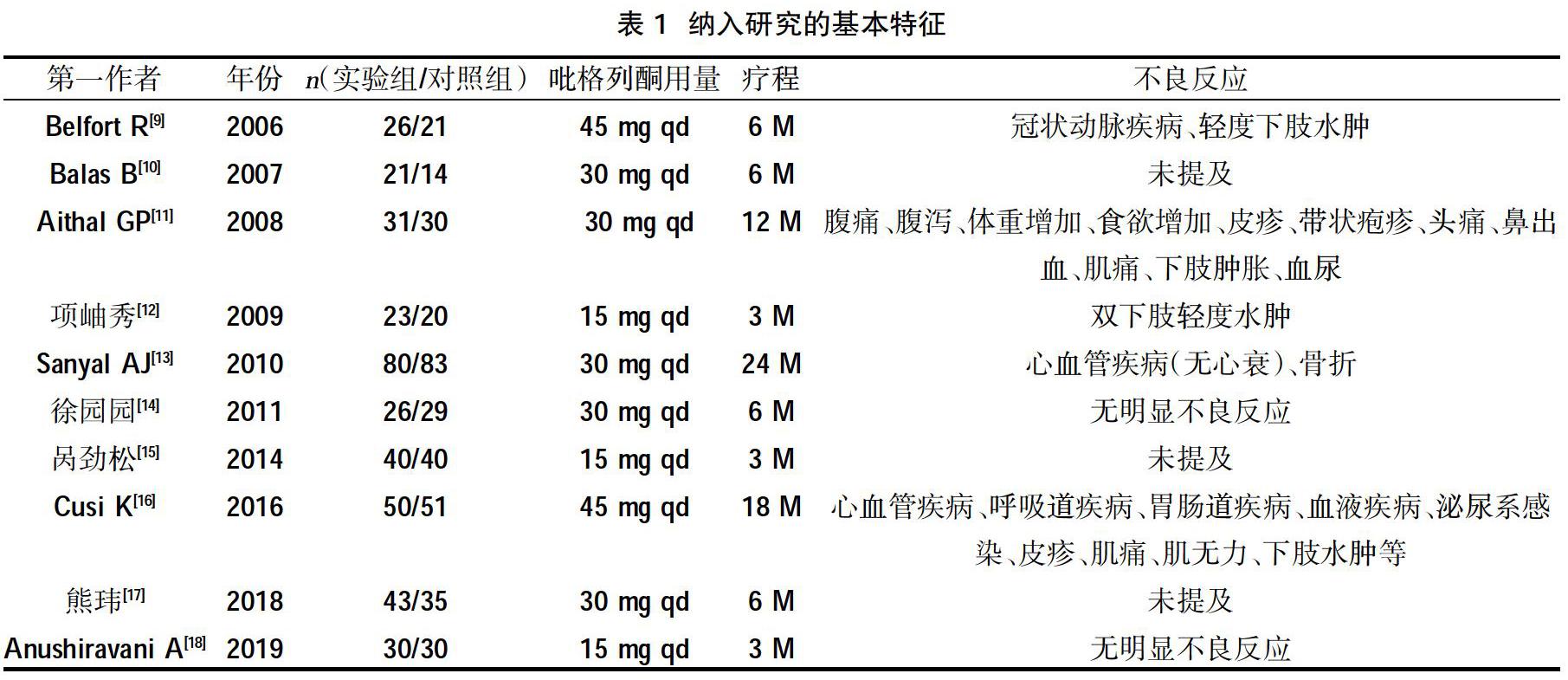
2.1纳入研究的检索及筛选结果 PubMed检索到文献8篇、万方检索到文献12篇、Cochrane Library检索到文献4篇、CNKI检索到文献2 篇。经过阅读文题及摘要后,根据文献纳入及排除标准,阅读全文后最终纳入符合要求的文献 10 篇。其中英文文献6篇,中文文献4篇,总样本量为723例,其中实验组370例,对照组353例。纳入文献的基本特征见表1,方法学质量评价见图1、图2。
2.2 Meta分析
2.2.1两组对肝脏脂肪变性的影响 共纳入4项研 究[9,11,13,16],采用随机效应模型进行Meta分析,结果显示实验组对肝脏脂肪变性的改善优于对照组(OR=0.26,95%CI=0.14~0.46,P<0.00001),见图3。
2.2.2两组对肝脏气球样变性的影响 共纳入4项研究[9,11,13,16],采用随机效应模型进行Meta分析,结果显示实验组对肝脏气球样变性的改善优于对照组(OR=0.38,95%CI=0.24~0.60,P<0.0001),见图4。
2.2.3两组对肝脏小叶炎症的影响 共纳入4项研 究[9,11,13,16],采用随机效应模型进行Meta分析,结果显示实验组对肝脏小叶炎症的改善优于对照组(OR=0.33,95%CI=0.21~0.50,P<0.00001),见图5。
2.2.4两组对肝脏纤维化的影响 共纳入4项研 究[9,11,13,16],采用随机效应模型进行Meta分析,结果显示实验组对肝脏纤维化的改善高于对照组(OR=0.57,95%CI=0.37~0.88,P=0.01),见图6。
2.2.5两组对肝脏ALT的影响 共纳入8项研 究[9,11,12,14-18],采用随机效应模型进行Meta分析,结果显示实验组对肝脏ALT的改善优于对照组(MD=10.33,95%CI=3.27~17.38,P=0.004),见图7。
2.2.6两组对肝脏AST的影响 共纳入6项研 究[9,14-18]。采用随机效应模型进行Meta分析,结果显示实验组对肝脏ALT的改善优于对照组(MD=9.51,95%CI=3.03~15.99,P=0.004),见图8。
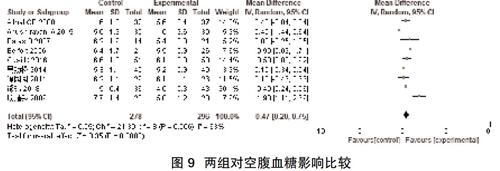
2.2.7两组对空腹血糖的影响 共纳入9项研 究[9-12,14-18],采用随机效应模型进行Meta分析,结果显示实验组对空腹血糖的改善优于对照组(MD=0.47,95%CI=0.20~0.75,P=0.0008),见图9。
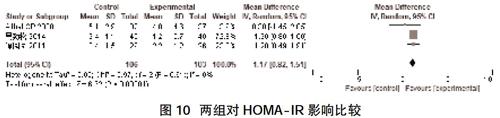
2.2.8两组对HOMA-IR的影响 共纳入3项研 究[11,14,15]。采用随机效应模型进行Meta分析,结果显示实验组对HOMA-IR的改善优于对照组(MD=1.17,95%CI=0.82~1.51,P<0.00001),见图10。
2.2.9不良反应 所有研究均未报告重大不良事件。虽然部分患者出现不良反应(心血管疾病14例,轻度下肢水肿4例,呼吸系统疾病14例,骨折3例,肌肉疼痛25例,皮疹8例,带状疱疹1例,胃肠道疾病14例,头痛1例,鼻出血1例,血尿1例,体重增加1例,食欲增加1例),但不良反应均较轻。
3讨论
近年来,非酒精性脂肪肝作为一个重要的公共卫生问题,受到了更多关注[19],其发生和发展是由脂类和葡萄糖代谢的几个基本生化和免疫过程变化驱动的,是环境、饮食和遗传因素相互作用的结果[20]。尽管相关研究较多,但非酒精性脂肪肝的发病机制仍不完全清楚,该病是代谢综合征的肝脏表现,也是代谢综合征的最早征兆之一,与2型糖尿病、胰岛素抵抗等特征密切相关[21]。胰岛素抵抗在非酒精性脂肪肝的发展中起着至关重要的作用,导致脂肪细胞水平的脂解增加,非酯化脂肪酸从脂肪组织到肝脏的流量增加[22]。肝胰岛素抵抗可促进肝细胞损伤和炎症,导致非酒精性脂肪肝发生。因此,为增加康复几率,应主要减少脂肪变性、炎症或肝纤维化[23]。吡格列酮属于噻唑烷类胰岛素增敏剂,通过激动过氧化物酶体增殖物激活受体r(PPARr)改善胰岛素抵抗。本研究对吡格列酮进行有效及安全性分析,以期能为临床用药提供循证医学依据。
Meta分析结果显示,吡格列酮治疗非酒精性脂肪肝患者疗效优于对照组,可减轻肝脂肪变性、肝气球样变、肝小叶炎症、肝纤维化,改善肝功能,降低ALT、AST,说明吡格列酮对因脂肪肝而致的肝酶增高有治疗作用,其机制为吡格列酮激活PPARr后,可促进白色脂肪细胞分化,增加小脂肪细胞的数量而减少大脂肪细胞的数量。小脂肪细胞对胰岛素的反應性更强,有利于促进葡萄糖的摄取,能量消化,减少多余能量在脂肪组织中的储存,从而减少肝内脂肪堆积,减轻肝脏的脂肪变性及炎症[24]。吡格列酮还可改善非酒精性脂肪肝患者空腹血糖、HOMA-IR等指标,这与吡格列酮本身并不增加胰岛素分泌量的前提下加强体内胰岛素的作用有关,血糖下降及胰岛素抵抗减轻在理论上可延缓非酒精性脂肪肝的发展。唯一不足的是吡格列酮可升高患者的BMI,但BMI升高的原因是将肌肉和肝脏的脂肪重新分布到外周组织,从而减少内脏脂肪[25],利于脂肪肝恢复。
本研究存在一些不足之处:①所包含的研究区域限制。纳入的研究只有中英文文献,其他语种未涉及,是在小部分地区进行的,因此结论可能不能推广到其他人口;②部分文献采用的试验方案设计欠严谨,导致研究质量不高;③因各试验中研究对象、诊断标准稍有不同、吡格列酮剂量和疗程的差异等,导致各结果间有一定的异质性,并且一些数据不能从每个研究中获得,导致所得结果的证据强度有限;④总样本量较小,在一定程度上可能影响分析结果的可靠性,对临床指导意义有限。因此,吡格列酮治疗非酒精性脂肪肝的有效性及安全性仍需进一步的随机双盲对照试验证实。
参考文献:
[1]Younossi ZM,Koenig AB,Abdelatif D,et al.Global epidemiology of nonalcoholic fatty liver disease-Meta-analytic assessment of prevalence,incidence,and outcomes[J].Hepatology,2016,64(1):73-84.
[2]Byrne CD,Targher G.NAFLD:a multisystem disease[J].Hepatol,2015,62 (1 Suppl):S47-S64.
[3]Shakir AK,Suneja U,Kevin R,et al.Overview of Pediatric Nonalcoholic Fatty Liver Disease:A Guide for General Practitioners Okla State Med Assoc[J].J Okla State Med Assoc,2018,111(8):806-811.
[4]Doycheva I,Issa D,Watt KD,et al.Nonalcoholic Steatohepatitis is the Most Rapidly Increasing Indication for Liver Transplantation in Young Adults in the United States[J].Clin Gastroenterol,2008(52):339-346.
[5]European Association for the Study of the Liver (EASL);European Association for the Study of Diabetes (EASD);European Association for the Study of Obesity (EASO).EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease[J].Diabetologia,2016,59(6):1121-1140.
[6]Koopman N,Molinaro A,Nieuwdorp M,et al.Review article:can bugs be drugs?The potential of probiotics and prebiotics as treatment for non-alcoholic fatty liver disease[J].Aliment Pharmacol Ther,2019,50(6):628-639.
[7]Gaggini M,Morelli M,Buzzigoli E,et al.Non-Alcoholic Fatty Liver Disease(NAFLD)and Its Connection with Insulin Resistance,Dyslipidemia,Atherosclerosis and Coronary Heart Disease[J].Nutrients,2013,5(5):1544-1560.
[8]Higgins J.Cochrane Handbook for Systematic Reviews of Interventions Version 5.0.1.The Cochrane Collaboration[J].Naunyn Schmiedebergs Archiv Für Experimentelle Pathologie Und Pharmakologie,2008,5(2):S38.
[9]Belfort R,Harrison SA,Brown K,et al.A Placebo-Controlled Trial of Pioglitazone in Subjects with Nonalcoholic Steatohepatitis[J].N Engl J Med,2006,355(22):2297-2307.
[10]Balas B,Belfort R,Harrison SA,et al.Pioglitazone treatment increases whole body fat but not total body water in patients with non-alcoholic steatohepatitis [J].Hepatol,2007,47(4):565-570.
[11]Aithal GP,Thomas JA,Kaye PV,et al.Randomized,Placebo-Controlled Trial of Pioglitazone in Nondiabetic Subjects With Nonalcoholic Steatohepatitis[J].Gastroenterology,2008,135(4):1176-1184.
[12]项岫秀,张慧芹,刘秀玲,等.吡格列酮对2型糖尿病合并非酒精性脂肪肝病患者血浆同型半胱氨酸水平的影响[J].临床荟萃,2009,24(15):1349-1350.
[13]Sanyal AJ,Chalasani N,Kowdley KV,et al.Pioglitazone,Vit.Amin E,or Placebo for Nonalcoholic Steatohepatitis[J].N Engl J Med,2010,362(18):1675-1685.
[14]徐园园,纪易斐.吡格列酮对糖尿病合并非酒精性脂肪肝炎的疗效观察[J].中华全科医学,2011,9(6):895,916.
[15]呙劲松,陈艳.吡格列酮对糖耐量异常合并非酒精性脂肪肝患者血浆瘦素水平及胰岛素抵抗的影响[J].中南医学科学杂志,2014(4):379-381.
[16]Cusi K,Orsak B,Bril F,et al.Long-Term Pioglitazone Treatment for Patients With Nonalcoholic Steatohepatitis and Prediabetes or Type 2 Diabetes Mellitus:A Randomized Trial[J].Ann Intern Med,2016,165(5):305-315.
[17]熊玮,唐淑亚,唐顺利.吡格列酮治疗非酒精性脂肪肝的疗效分析[J].中国社区医师,2018,34(22):65,67.
[18]Anushiravani A,Haddadi N,Pourfarmanbar M,et al.Treatment options for nonalcoholic fatty liver disease:a double-blinded randomized placebo-controlled trial[J].Eur J Gastroenterol Hepatol,2019,31(5):613-617.
[19]Younossi ZM.Non-alcoholic fatty liver disease--a global public health perspective[J].Hepatol,2019,70(3):531-544.
[20]Hardy T,Oakley F,Anstee QM,et al.Nonalcoholic fatty liver disease:pathogenesis and disease spectrum[J].Annu Rev Pathol Mech Dis,2016(11):451-496.
[21]Ekstedt M,Nasr P,Kechagias S.Natural History of NAFLD[J].Curr Hepatol Rep,2017,16(4):391-397.
[22]Marchesini G,Brizi M,Bianchi G,et al.Nonalcoholic fatty liver disease:a feature of the metabolic syndrome[J].Diabetes,2001,50(8):1844-1850.
[23]Saadati S,Sadeghi A,Mansour A,et al.Curcumin and inflammation in non-alcoholic fatty liver disease:a randomized,placebo controlled clinical trial[J].BMC Gastroenterol,2019,19(1):133.
[24]Takao T,Kumagai C,Hisakawa N,et al.Effect of 17beta-estradiol on tumor necrosis factor-alpha-induced cytotoxicity in the human peripheral T lymphocytes[J].J Endocfinol,2005,184(1):191-197.
[25]Miyazaki Y,Mahankali A,Matsuda M,et al.Effect of pioglitazone on abdominal fat distribution and insulin sensitivity in type 2 diabetic Patines[J].Clin Endocrinol Metab,200,87(6):2784-2791.
收稿日期:2020-05-06;修回日期:2020-05-25
編辑/肖婷婷
作者简介:于淙(1986.2-),女,山东威海人,硕士,主治医师,主要从事慢性肝病的防治工作
通讯作者:周培(1982.10-),男,湖北荆州人,硕士,主治医师,主要从事各种感染性疾病的诊治工作

