高效液相色谱法测定大鼠血浆中厄洛替尼的浓度及其口服药动学研究
李 欣 李晓琴 李新霞
(1.新疆医科大学中心实验室,乌鲁木齐 830011;2.新疆医科大学附属肿瘤医院内二科,乌鲁木齐 830011;3.新疆医科大学药学院,乌鲁木齐 830011)
肺癌已成为严重威胁我国城市人口生命和健康的疾病,非小细胞肺癌(non-small cell lung cancer, NSCLC)约占肺癌总数的75%~80%,其中约75%的肺癌患者在确诊时已经是中晚期,失去了最佳的治疗时间[1,2]。作为目前临床上治疗非小细胞肺癌的一线用药,厄洛替尼(Erlotinib)是一种小分子络氨酸激酶抑制剂,能穿过表皮生长因子(epidermal growth factor receptor, EGFR)过量表达的实体瘤细胞膜,并与EGFR分子的酪氨酸结构域特异性结合,阻断其信号传导,进而抑制酪氨酸激酶的活性,降低肿瘤细胞的黏附能力,促进肿瘤细胞的凋亡,增加患者对化疗的敏感度[3-5]。因此,厄洛替尼对存在EGFR敏感突变或既往化疗失败的晚期NSCLC患者是一类可供选择的有效药物。
与常规化疗相比,厄洛替尼的耐受性较好,其不良反应较少而轻,但其主要不良反应,如皮疹、腹泻、肝功能损害、间质性肺炎也不能被低估[6,7]。文献报道88例服用厄洛替尼治疗的患者其血药浓度相差可达8倍[8],可见其药物动力学存在明显的个体差异性,有必要对其进行血药浓度监测。因此,建立一个快速、灵敏、可靠的方法检测人血浆中厄洛替尼的浓度,对于指导临床用药、实施个体化治疗十分重要[9-13]。本实验拟建立相关高效液相法用于厄洛替尼的生物样品浓度测定,并在大鼠体内初步研究厄洛替尼的药物动力学。
1 材料
1.1 仪器
Waters e2695高效液相色谱仪(美国Waters);Waters 2489紫外/可见检测器(美国Waters);Sigma 2-16K离心机(德国Sigma);IKA MS3 basic旋涡混合仪(IKA);HSC-12A氮吹仪(天津恒奥)。
1.2 试剂
厄洛替尼(纯度:99%,广州珠海嘉成医药有限公司,批号:183319-69-9);索拉非尼(纯度:99%,南京安格医药化工有限公司,批号284461-73-0)。其他试剂均为色谱纯。
1.3 动物
SD大鼠,雌雄兼半,体重220±20g,由本校实验动物中心提供,试验前未服用其他药物,饲养2周后进行试验。所有实验均遵照新疆医科大学实验动物保护和使用指导执行。
2 方法与结果
2.1 对照品溶液的配制
2.1.1厄洛替尼储备液
精密称取厄洛替尼10mg置100mL量瓶中,加乙醇并定容至刻度,超声助溶,即得100mg/L的厄洛替尼储备液。置于4℃冰箱保存,备用。
2.1.2索拉菲尼储备液
精密称取索拉菲尼10mg置100mL量瓶中,加乙醇并定容至刻度,超声助溶,即得100mg/L的厄洛替尼储备液。置于4℃冰箱保存,备用。
2.2 血浆样品的处理
取血浆200μL置肝素抗凝离心管中,加入50μL(20mg/L)内标溶液和2mL的处理液(乙腈∶二氯甲烷=4∶1),超声助溶10min。3000rpm离心10min。取上清液于45℃氮气吹干,残渣用200μL流动相复溶,过0.22μm微孔滤膜,滤液进行HPLC分析。
2.3 测定方法
2.3.1色谱条件
色谱柱为150mm ×4.6mm C18柱(Waters,Milford,USA);流动相为乙腈(A)-水(B),梯度洗脱程序: 0~23min,V(A)∶V(B)= 48∶52~25∶75;23~25min,V(A)∶V(B)= 25∶75~48∶52。流速为1.0mL/min;柱温为35℃;检测波长249nm;进样体积10μL。
2.3.2方法的专属性
在2.3.1项色谱条件下,将一定浓度的厄洛替尼标准溶液加入空白血浆中,按2.2项下操作,进行HPLC分析。同时对处理后的空白血浆和大鼠给药后的血浆样品进行HPLC分析。色谱图见图1。结果表明,空白血浆中内源性物质及给药后的代谢产物不干扰厄洛替尼及内标的测定,厄洛替尼和内标的分离度分别为2.47和1.67。
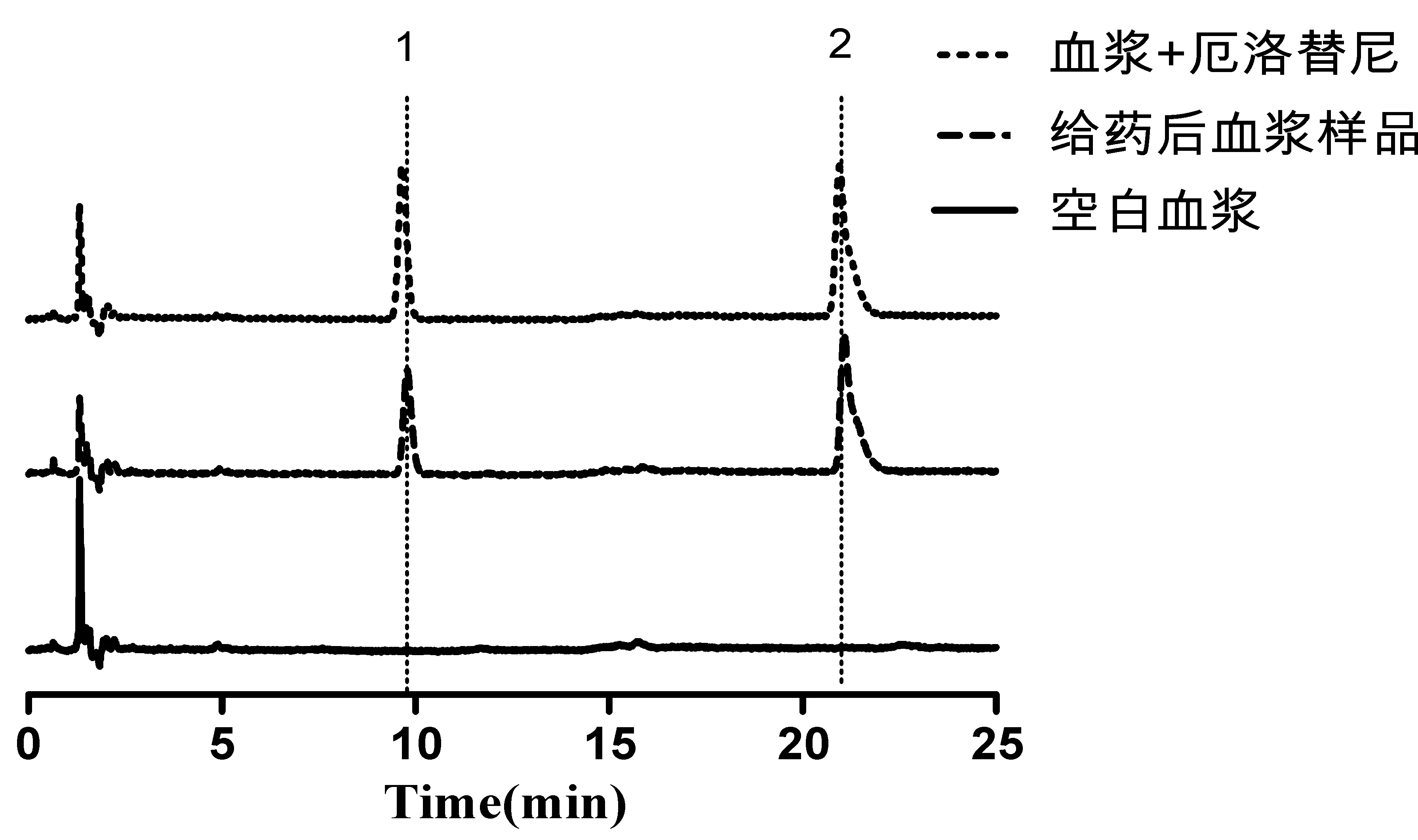
图1 血浆中厄洛替尼的色谱图
2.3.3标准曲线和最低检测浓度
取空白血浆200μL准确加入厄洛替尼储备液,使其浓度分别为100、1000、3000、4000、6000和7000μg/L,按2.2项下操作,将测得的厄洛替尼与内标峰面积比A对药物浓度C进行线性回归。回归方程为C=6515.7A-464.5,r=0.9998。在100~7000μg/L与峰面积比呈良好的线性关系,最低检测浓度为80μg/L (S/N=5)。
2.3.4精密度试验
配制1000、3000和6000μg/L的厄洛替尼标准血样各6组,于同一日按2.2项下方法处理后作HPLC分析,计算日内精密度;后连续测定6天,计算日间精密度,见表1。由结果可知,日内及日间精密度相对标准偏差均远小于15%,达到生物样品检测标准。

表1 精密度结果
2.3.5回收率试验
厄洛替尼采用1000、3000和6000μg/L为低、中、高3个浓度,用标准品对照法测得实测量,以实测量与加入量之比计算方法回收率;以血样中厄洛替尼的峰面积与相同浓度厄洛替尼标准溶液的峰面积之比计算厄洛替尼的提取回收率,见表2。由结果可知,方法回收率高、中、低浓度均大于90%,提取回收率方法回收率高、中、低浓度均大于50%。因此,该血浆样品处理方法及色谱方法可以用于大鼠血浆中厄洛替尼的含量测定。

表2 回收率结果
2.3.6样品稳定性
分别考察1000、3000和6000μg/L3个浓度的厄洛替尼标准血浆样品在-20℃的冰箱中放置30d,反复冻融3次以及血浆样品按2.2项下处理后用流动相复溶并于室温下保存24h后的稳定性,检测结果表明,血浆中厄洛替尼的含量没有发生明显变化,结果见表3。说明厄洛替尼具有较好的血浆稳定性。

表3 样品稳定性
2.4 血浆样品采集
取6只SD大鼠,雌雄兼半,实验前1日禁食12h,实验当日按单剂量方案对大鼠口服灌胃给予厄洛替尼溶液(15mg/kg)。给药后自由饮食。给药前取空白血浆,给药后分别于2、4、6、8、12、24、36、48、72和144h眼眶静脉取血浆各400μL,分别置于涂有肝素的离心管中, 10900r/min离心5min,取上层血浆200μL于-20℃保存。6只SD大鼠单剂量口服灌胃给予厄洛替尼后体内的平均药-时曲线见图2,吸收情况与已报道的替尼溶液代谢过程基本一致[14,15]。

图2 SD大鼠单剂量灌胃给予厄洛替尼药-时曲线图
2.5 药物动力学参数
以统计矩分析方法估算6只SD大鼠单剂量口服灌胃给予厄洛替尼后的药物动力学参数,结果见表4。SD大鼠口服给予厄洛替尼后的平均药物动力学参数与已报道的人类的相关数据差异较大,可能是由于物种差异性引起。

表4 大鼠给予厄洛替尼后的主要药动学参数
3 讨论
本实验建立了HPLC-UV法测定厄洛替尼血浆样品浓度的方法,该方法灵敏、可靠、特异性强,适用于药物代谢动力学研究和治疗药物监测[16-18]。样品处理时采用液-液萃取方法,操作简单、快速,整个提取系统的回收率较高,杂质干扰也较小,在临床上和实验中均有较强的适用性。虽然LC-MS/MS方法较本方法有更低的检测限,但极低浓度的血浆厄洛替尼含量检测通常只应用于毒理学研究或抑制剂的相关实验中,而临床意义不大,LC-MS/MS方法的检测上限仅仅4000μg/L,这就进一步限制了该方法的使用。而此前报导均采用等度洗脱方式,空白血浆对样品干扰较大,本实验采用梯度洗脱方式进行分离,能有效避免血浆本底的干扰。因此,相较于操作复杂、耗时,且价格昂贵的LC-MS/MS方法,本实验建立的HPLC-UV方法具有更广泛的实用价值。
此前已有文献报道了不同给药方式的厄洛替尼药动学参数,但较多局限在连续服用厄洛替尼数日后或单剂量静脉给予厄洛替尼的药动学参数,并无单剂量口服给予厄洛替尼的相关报道[19-21]。因此,本研究不仅可以提供灵敏、简便的检测方法,更为临床用药提供基础实验数据,以期更好地为临床患者用药服务。

