9540例帕瑞昔布相关药品不良反应的自动监测研究
(.解放军总医院医疗保障中心,北京 00853;2.重庆医科大学药学院,重庆 4033)
非甾体类抗炎药是治疗疼痛的重要选择,其用于术后镇痛优势主要在于降低其他麻醉药用量及其相关不良反应,减少应激反应,完善镇痛。然而,传统的非甾体类抗炎药不良反应较多,如诱发胃肠道并发症、影响血小板功能等,严重制约了其在临床的应用[1]。帕瑞昔布是一种选择性的环氧合酶-2(cyclooxygenase-2,COX-2)抑制剂,可肌肉和静脉注射,具有良好的抗炎活性[2]。有研究[3]表明,帕瑞昔布40 mg对缓解术后疼痛比吗啡4 mg效果好,减少患者术后对阿片类镇痛药的需求。目前,帕瑞昔布已被广泛用于术后镇痛,但对患者血小板、血红蛋白以及肝肾功能的影响研究较少报道。我院自主研发的医疗机构ADE主动监测与智能评估警示系统(adverse drug events active surveillance and assessment system,ADE-ASAS),可以实现多个ADE的自动识别和辅助评估[4-5]。本研究借助该系统,自动监测应用帕瑞昔布的住院患者相关ADR发生情况,并尝试探索分析帕瑞昔布相关不良反应的影响因素。
1 资料与方法
1.1 模块选定及其事件配置器参数设置
根据帕瑞昔布说明书中发生相关ADR的情况,参照国家药品不良反应监测中心的《药品不良反应术语使用指南》(征求意见稿)[6],设置“血小板”、“血红蛋白”、“肝功能”及“肾功能”四个模块回顾性分析研究的事件配置器。
1.1.1 病例入选标准 四个模块事件配置器入选标准相同,均为经静脉途径使用帕瑞昔布的住院患者。患者一次住院期间用药间隔大于72 h计为2个用药例次[7]。
1.1.2 病例排除标准 四个模块事件配置器均排除检验指标缺失,其他排除条件详见表1(启用:表示排除;禁用:表示不予排除)。
1.2 研究对象与方法
采用真实世界研究方法,利用ADE-ASAS回顾性自动监测2018年1月1日 - 12月31日期间我院使用帕瑞昔布注射液(40 mg/支,辉瑞制药有限公司,国药准字J20080045)的所有住院患者。参照国家药品不良反应监测中心的《药品不良反应术语使用指南》(征求意见稿),设置“血小板”、“血红蛋白”、“肝功能”及“肾功能”四个模块的报警规则,详见表2。由两名临床药师分别对ADE-ASAS筛查出的报警病例进行人工评价,最终确定阳性病例,分析系统各个模块的阳性报警率及ADR发生率。
1.3 统计学处理
采用SPSS21.0对数据进行统计学分析,计数变量采用χ2检验,以P < 0.05为差异具有统计学意义。
2 结果
2.1 用药人群概况
本研究纳入患者共计9540例,用药10 156例次。其中男性4822例,女性4718例,男女比例为1.02∶1。患者平均年龄(53±16.20)岁,年龄分布区间为10岁~100岁,其中≥65岁患者共计2592例,≥18岁且< 65岁患者6829例,< 18岁患者119例。患者主要分布于骨科(4991例,52.32%),肝胆外科(2507例,26.28%),妇科(715例,7.49%),泌尿外科(602例,6.31%),其他(725例,7.60%)。对119例未成年病例进一步统计分析,患儿在用药后病情均好转,且未出现任何不良反应。

表1 排除条件设置Tab 1 Settings of exclusion criteria

表2 ADR报警及判定规则Tab 2 ADR alarm and determination rules
2.2 监测数据及评价结果
一次住院多个用药例次的患者中,未评价出再激发目标ADR的病例,阳性患者中未评价出同时发生血小板减少、血红蛋白减少、或肝、肾损害的病例。按照ADE-ASAS中血小板、血红蛋白、肝功能及肾功能各模块设定条件进行自动监测,血小板减少模块纳入2296例,血红蛋白减少模块纳入2847例,肝损害模块纳入2677例,肾损害模块纳入4047例。系统报警病例由两名研究人员分别进行人工关联性评价,结果见表3。
2.3 帕瑞昔布相关不良反应的影响因素分析
对帕瑞昔布相关血小板减少、贫血和肝肾损害的患者年龄、性别、BMI等因素分别进行统计学分析。血小板减少模块共计纳入2296例患者,其中1例患者身高体重缺失,所以BMI项目共计2295例;血小板减少相关因素分析结果显示年龄、性别、BMI等因素均无统计学差异,详见表4。血红蛋白减少模块共计纳入2847例患者,其中1例患者身高体重缺失,故BMI项目共计2846例;贫血相关因素分析结果显示有统计学差异的因素为性别(P < 0.001)及年龄(P <0.05),详见表5。肝损害模块共计纳入2677例患者,其中1例患者身高体重缺失,故BMI项目共计2676例;肝损害相关因素分析结果显示年龄、性别、BMI等因素均无统计学差异,详见表6。肾损害模块共计纳入4047例患者,其中2例患者身高体重缺失,所以BMI项目共计4045例;肾损害相关因素分析结果显示有统计学差异的因素为年龄(P < 0.001),详见表7。
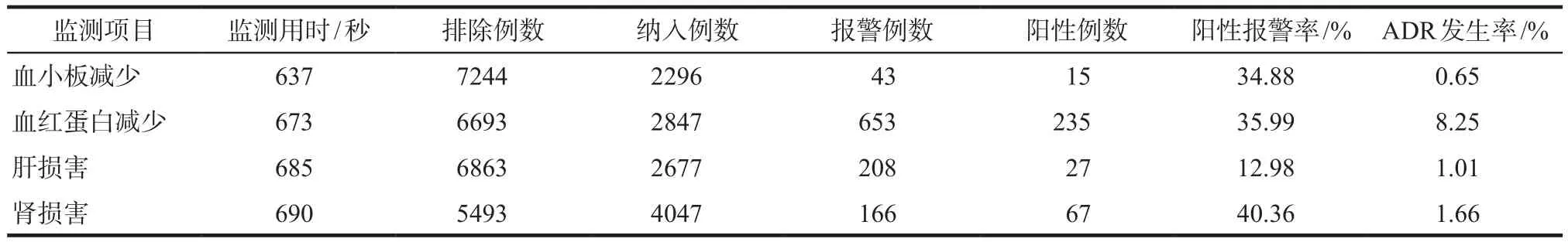
表3 系统监测及评价结果Tab 3 Outcomes of system monitoring and manual review
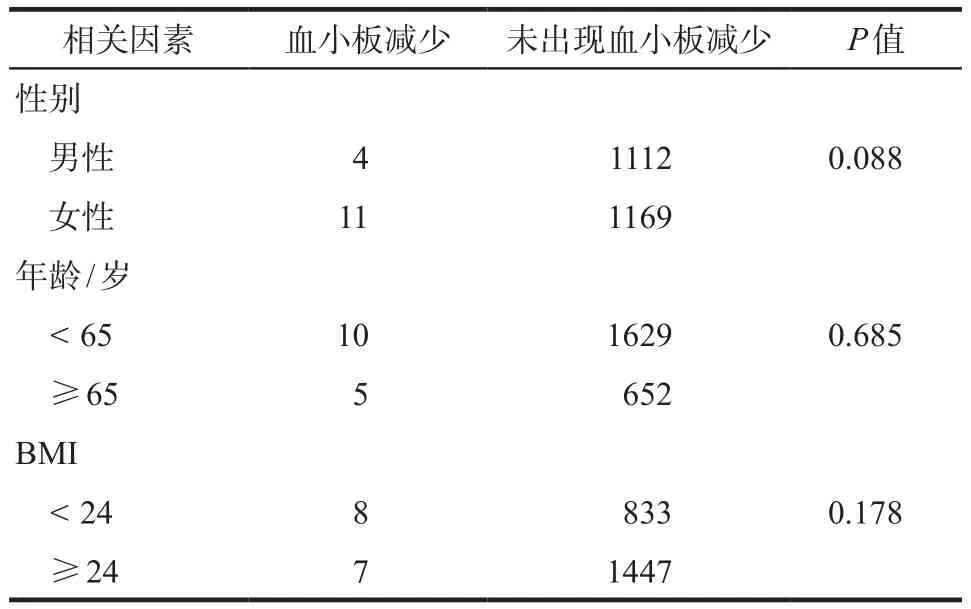
表4 帕瑞昔布致血小板减少的相关因素分析Tab 4 Analysis of related factors about thrombocytopenia caused by parecoxib
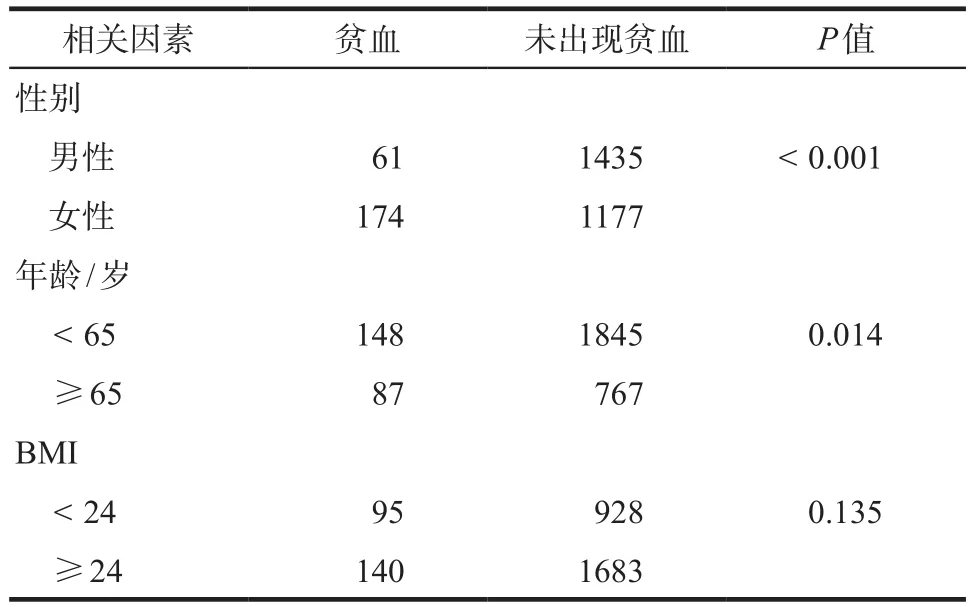
表5 帕瑞昔布致贫血的相关因素分析Tab 5 Analysis of the related factors about anemia caused by parecoxib
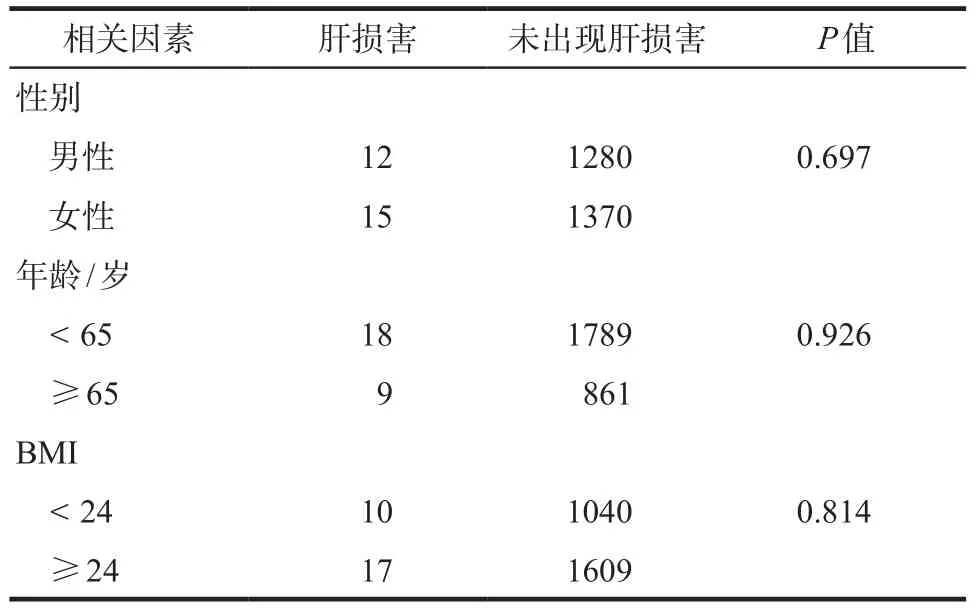
表6 帕瑞昔布致肝损害的相关因素分析Tab 6 Analysis of the related factors about hepatic injury caused by parecoxib

表7 帕瑞昔布致肾损害的相关因素分析Tab 7 Analysis of the related factors about kidney injury caused by parecoxib
3 讨论
3.1 帕瑞昔布相关ADR发生率分析
帕瑞昔布为选择性的COX-2抑制剂,对环氧合酶有选择性,在推荐剂量下基本不会作用于环氧合酶-1,也不会出现与之相关的不良反应,因而被应用于术后镇痛领域[8]。有研究[9-14]表明帕瑞昔布被用于术后镇痛对患者的肝肾功能无明显影响,不良反应少,且可以增强镇痛疗效,安全性较高。帕瑞昔布说明书中血小板减少和肝功能异常的发生率范围在0.1% ~ 1.0%,贫血和肾功能异常的发生率范围在1% ~ 10%。本研究结果显示,血小板减少发生率为0.65%,贫血发生率为8.25%,肝功能异常发生率为1.01%,肾功能异常发生率为1.66%,帕瑞昔布相关不良反应发生率基本与说明书一致。
3.2 帕瑞昔布相关不良反应的影响因素分析
本研究通过对帕瑞昔布相关血小板减少、贫血和肝肾损害的患者年龄、性别、BMI等因素分别进行统计学分析,发现帕瑞昔布致贫血与患者的性别或年龄有关,女性或老年患者更容易出现贫血,而导致肾损害与年龄因素有关,老年患者更容易出现肾损害。说明书显示帕瑞昔布在18岁以下儿童使用的安全性和疗效尚未确定,而对研究中119例用药患儿逐例统计分析结果显示,用药后病情均好转,且未发现有任何不良反应。
帕瑞昔布致贫血的发生率比较高,与术后贫血的发生相互影响,很难区分。有文献报道,术前Hb较低者、女性和体表面积较小者是术后贫血的高风险人群;贫血的患病率随年龄增长而升高[15]。帕瑞昔布也可以导致胃肠道出血、溃疡或穿孔等不良反应,从而引起贫血,尤其老年患者使用帕瑞昔布增加了这种不良反应的出现频率,所以女性或老年患者术后应用帕瑞昔布镇痛时要警惕贫血的发生,并根据贫血类型及严重程度及时对症治疗。
严进军等[16]研究发现,有些选择性COX-2抑制剂如塞来昔布会对老年患者的肾血流量有轻微的影响、或者影响患者血压。本研究显示≥65岁的患者较< 65岁的患者更容易出现肾损害,分析可能与老年患者本身肾功能状态降低有关,老年患者表观清除率降低,导致帕瑞昔布血浆暴露水平升高,更易出现药品相关不良反应。另外,帕瑞昔布在静注或肌注后经肝脏酶水解,迅速转化为有药理活性的物质伐地昔布。而伐地昔布主要在肝脏内消除,仅少于5%通过尿液排泄,因此对已患肝脏疾病的患者应慎重用药,严重肝功能不良的患者则不推荐使用帕瑞昔布。本研究设置肝损害模块时已排除肝功能不全、肝功能衰竭等疾病,分析中显示帕瑞昔布致肝损害与患者的年龄、性别及BMI等无关,但因纳入病例少,难免存在偏倚,有待更大数据的分析。
3.3 自动监测效能分析
ADE-ASAS能够大大减少主动监测研究的工作量,显著提高效率。本研究完成9540例用药患者四个模块的病例自动监测评估工作仅用时45 min左右,其报警阳性率除肝损害外均在35%左右,而肝损害模块的报警规则中相关指标异常涉及因素多,尤其是合并用药多,导致假阳性较多。相比人工筛查病例、填写问卷调查等常用研究方式,自动监测可以低成本、快速度、高准确性的筛选大样本目标药物的用药人群,获得准确的量化ADR发生率,为高效开展药品上市后的安全性再评估提供了可能。
综上,帕瑞昔布相关贫血发生率为常见,血小板减少、肝损害及肾损害发生率均为偶见;老年或女性患者应用帕瑞昔布时应更加谨慎,并注意监测肾功能及血常规变化。借助ADE-ASAS实施帕瑞昔布相关ADR的自动监测,能够高效快速的获取其真实世界重点ADR发生率及相关影响因素;该系统经过8年的应用实践,已成为开展大样本真实世界安全性再评价回顾性监测研究的可靠工具[17-18]。

