一种新型次氯酸消毒剂对纤维支气管镜的消毒效果
钱 麟,史庆丰,许 华,王春灵,3
(复旦大学附属中山医院 1. 消毒供应中心; 2. 感染管理科; 3. 手术室,上海 200032)
纤维支气管镜检查及治疗作为一种侵入性、微创性的诊疗技术,已经越来越广泛地应用于临床,成为肺部疾病的主要检查手段之一[1]。然而纤维支气管镜的管腔细长、结构精细,且不耐高温,使用过程中会接触患者的体液和血液,多种呼吸道病原体也可附着在内镜内、外表面,若清洗、消毒不当易导致交叉感染。研究[1]显示,0.8%的患者可在支气管镜检查后发生感染,严重时可引起医院感染暴发,给感染的预防和控制带来严峻考验。因此,加强纤维支气管镜的规范化消毒和管理,选择合适的消毒剂对内镜的安全使用有着重要意义。次氯酸消毒剂作为一种新型的内镜消毒剂,具有安全、高效、方便、环保等特点,能在短时间内达到良好的消毒效果[2]。一款新型次氯酸消毒剂用于纤维支气管镜的消毒,为了解该消毒剂对临床纤维支气管镜实际消毒效果是否可达到高水平消毒,以及其有效性如何,开展了本研究,以期为临床的内镜清洗消毒工作提供参考,现将结果汇总如下。
1 对象与方法
1.1 研究对象 2018年7—10月,选取临床使用过且即将进行清洗、消毒的60条纤维支气管镜,随机抽取30条内镜列为消毒5 min组,机洗消毒时间为5 min;剩余30条内镜列为消毒3 min组,机洗消毒时间为3 min。
1.2 试剂与器材 Olymups BF P180/Q180/MH-533型纤维支气管镜6条,新华牌Rider60B型全自动软式内镜清洗消毒机,佳姆巴医疗器械消毒剂(上海日洁环境科技有限公司,有效氯含量在50~210 mg/L)[3],3M 70508-M型全效快速多酶清洗液,3M ATP荧光检测仪,50 mL一次性注射器,无菌薄膜过滤器,HTY-WP0型取样泵,HTY-101微生物检验仪,哈纳 HI96771次氯酸浓度检测仪,中和剂(100 mL 磷酸盐缓冲液+0.2 g硫代硫酸钠+0.5 g 吐温+1 g卵磷脂)、R2A琼脂培养基及培养器材。
1.3 清洗、消毒流程 纤维支气管镜清洗和流程按照《软式内镜清洗消毒技术规范》WS 507-2016[4]要求,纤维支气管镜拆卸到最小单位在流动水下洗刷,多酶浸泡和冲洗,随后放置于全自动软式内镜清洗消毒机按照预先设定消毒时间进行清洗和消毒,消毒剂采用佳姆巴医疗器械消毒剂。
1.4 采样方法 每条消毒好后的纤维支气管镜进行干燥处理后,同时采用内腔采样法和外表面采样法进行消毒效果评价。内腔采样法:在清洁环境下,使用无菌注射器抽取50 mL含中和剂的采样液,从待检内镜的活检口注入,用水样薄膜过滤器进行收集,及时送检至实验室并采用滤膜法进行细菌菌落计数。外表面采样法:在清洁环境下,将ATP水样拭子在纤维支气管镜的表面进行顺时针旋转涂抹采样,并将采好的拭子放置于荧光检测仪中并按压到底,记录读数(RLU)。
1.5 评价标准 ATP生物荧光法按照设备参考值:≤200 RLU作为消毒合格;菌落计数法按照《软式内镜清洗消毒技术规范》标准,菌落总数≤20 CFU/件为合格。
1.6 统计分析 应用SPSS 21.0软件对数据进行统计分析,非正态分布资料采用中位数和极值进行描述。
2 结果
2.1 ATP生物荧光检测 30条纤维支气管镜使用后未清洗前,内镜外表面RLU中位值为911.5,合格率为16.7%;酶洗后机洗前,内镜外表面RLU中位值为234.0,合格率为43.3%。每组30条纤维支气管镜经消毒剂分别浸泡消毒5、3 min后,气管镜外表面RLU中位值分别为25.0、23.5,合格率均为100.0%。见表1。
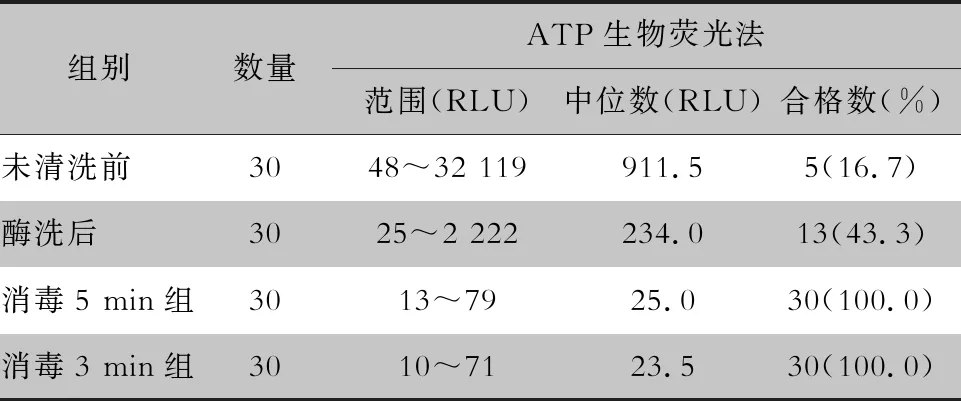
表1 各组纤维支气管镜外表面ATP生物荧光法检测结果
2.2 菌落计数 30条纤维支气管镜消毒后进行滤膜法采样,消毒5 min组有5条检出细菌,菌落数0~7 CFU/件;消毒3 min组有4条检出细菌,菌落数0~5 CFU/件,不同消毒作用时间合格率均为100%。
2.3 消毒衰减指标研究 使用次氯酸消毒剂进行机洗消毒,消毒作用时间分别为5、3 min,连续使用7 d作为一个循环,每个循环期间消毒纤维支气管镜20~31条,共进行4个循环研究。共检测23条纤维支气管镜,结果显示,滤膜法和倾注法均未检测出活菌,消毒合格率均为100%。次氯酸浓度检测结果显示,次氯酸消毒剂连续机洗使用7 d后,浓度仍在80 mg/L左右,在有效浓度范围内,见表2。

表2 次氯酸消毒剂临床连续消毒现场试验结果
3 讨论
本研究采用ATP生物荧光法对纤维支气管镜表面进行采样,采用滤膜法对纤维支气管镜内腔进行采样,评价次氯酸消毒剂消毒效果。ATP荧光法是一种简便、快捷的生物学监测方法,主要通过检测细胞内的能量物质ATP而反映活菌数量[5]。研究[6]显示,菌落计数法和ATP生物荧光法对活菌悬浮液检测结果基本一致,ATP生物荧光法检测的RLU值能反应实际细菌含量的高低。由于人体呼吸道可正常定植大量细菌,使用后的纤维支气管镜可被患者污染。本次ATP生物荧光检测结果也显示,使用后、未清洗前纤维支气管镜中位数为911.5 RLU,经过酶洗后中位数为234.0 RLU,但次氯酸消毒剂消毒5 min或3 min后,ATP数值降低至10~79,说明纤维支气管镜仅清洗和酶洗并不能有效清除污染,而次氯酸消毒可有效降低外表面污染情况。细菌菌落计数是一种直观而准确反映内镜清洗、消毒效果的监测方法,滤膜法通过50 mL的采样液对内镜管腔进行充分冲洗,经过滤膜富集浓缩后较倾注法得到更为精准的检测结果[7]。本组结果显示,消毒后的纤维支气管镜经滤膜法检测仅有9条培养出细菌,且最高的一条内镜菌落数仅为7 CFU,说明本次所用的次氯酸消毒剂具有良好的消毒效果。次氯酸消毒剂分别进行5、3 min的消毒,滤膜法、倾注法和ATP生物荧光法均显示消毒合格率为100%,提示该消毒剂作用3 min可有效杀灭纤维支气管镜污染的细菌,达到高效杀毒的效果。
目前,2%的戊二醛是国内最常使用的内镜消毒剂,具有消毒耗时过长的缺点,在消毒管理方面也需要专人守候操作,降低了清洗效率。此外,2%戊二醛具有挥发性和刺激性,对人的呼吸道和皮肤黏膜有一定的刺激,对清洗和操作人员的个人防护带来一定的挑战[8]。过氧乙酸和邻苯二甲醛是近年来开始应用于内镜消毒的化学消毒剂,过氧乙酸具有高效、作用时间短、无有害物质残留等优点[9],已在部分国内医院的内镜中心大规模应用[10]。但这种灭菌型的消毒剂也存在一定的安全隐患,如二元固体或液体的过氧乙酸,其化学性质不稳定,具有现用现配、易燃易爆、需特殊废液处理等缺点,不利于临床大规模使用[11],而邻苯二甲醛对光和空气敏感,并存在使蛋白变性的缺点,对人的皮肤、黏膜存在一定的损伤[12],需从业人员做好相应的防护。普通酸性氧化电位水主要通过电解水中次氯酸以及高电压作用下将细菌菌体蛋白氧化而达到杀菌的作用[13],可应用于内镜消毒。但该消毒剂性质不稳定,需现用现配,对不锈钢以外的金属具有一定的腐蚀性,限制了其大规模应用[14]。有研究报道,次氯酸钠消毒剂能够穿透生物膜,降低生物膜表面胞外多糖-蛋白质复合物或细菌连贯性,对管腔内壁附有的生物膜具有较强的破坏能力[15]。
本组研究还对佳姆巴医疗器械消毒剂的稳定性进行了监测。次氯酸消毒剂是一种无色、透明、对人体无明显刺激性和异味的消毒剂[16],主要通过次氯酸卤化或氧化细胞成分或蛋白质和脂质而破坏病原体[17],有效氯含量在50~210 mg/L可发挥消毒效果,对耐碳青霉烯的鲍曼不动杆菌也有很好的杀灭效果[18]。次氯酸易受到有机物和光照条件的影响而降低稳定性,前期研究已证实该消毒剂存在自然衰减的特性,平均每消毒一条胃肠镜消耗10 mg有效成分[3],但该研究集中在单一时间段内大量内镜清洗中,对自然天数的衰减率和使用天数未进行深入研究。本研究发现次氯酸连续消毒7 d,消毒循环数在20~31条,平均每条纤维支气管镜消耗5 mg/L有效氯,且第7天末有效氯监测浓度仍维持在有效浓度范围内,满足日常的清洗要求。研究过程中发现该消毒剂使用后无残留,肉眼观察纤维支气管镜外表面无发白、发黏、破损等老化现象,同时也未对内镜清洗人员产生不良影响,与黄育红等[19]研究结果一致,符合内镜高水平、安全消毒的要求。

