中国近12年静脉内平滑肌瘤病病例分析(附5例报道)
邱阳,刘芸
(首都医科大学附属北京友谊医院妇产科,北京100050)
静脉内平滑肌瘤病(intravenous leiomyomatosis,IVL)是一种介于子宫良性平滑肌瘤与肉瘤之间的特殊类型的子宫平滑肌瘤,虽然其组织学上为良性,但可以蔓延至子宫内及子宫外的静脉系统[1],进入下腔静脉、右心房、右心室,甚至肺动脉,引起猝死[2]。1896年Birch-Hirschfeld[3]首次报道了IVL,并认为肿瘤可超出子宫范围,沿静脉系统蔓延。1907年,Durck[4]和Hormann[5]首次报道了进入心脏的IVL,称为心脏内平滑肌瘤病。1959年,Marshall和Morris[6]发表了第一篇英文文献病例报道。IVL较为罕见,1959—2010年英文文献报道的IVL病例共298例,占2002—2008年全部生殖道平滑肌肿瘤的0.097%[7]。近年来IVL的相关报道逐渐增多,马国涛等[8]报道,北京协和医院2002年11月至2015年1月共收治IVL患者76例,占同期子宫肌瘤病例的0.25%。但国内相关信息多为个案报道,缺乏大宗病例汇总以及特点分析。本研究收集国内近12年中文文献报道的694例IVL病例,统计分析其发病特征、临床表现,总结诊治要点,并结合首都医科大学附属北京友谊医院收治病例,复习相关文献。
1 资料与方法
1.1资料检索 以“静脉内平滑肌瘤病”“静脉平滑肌瘤”“子宫静脉内平滑肌瘤病”为关键词,全面检索在线中文数据库中国知网、万方数据库,获取2007年1月至2018年12月有关IVL的所有中文文献。共获取文献135篇,去除重复报道的病例,共694例。
1.2方法 获取的数据录入Microsoft Excel,应用软件的计算功能及绘制图表功能,对病例的时间、地区分布、性别、发病年龄、病史、临床表现、血管受累情况、诊断、治疗及预后进行分析和描述,并对首都医科大学附属北京友谊医院2010年1月至2019年5月收治的5例IVL病例进行报道。
2 结 果
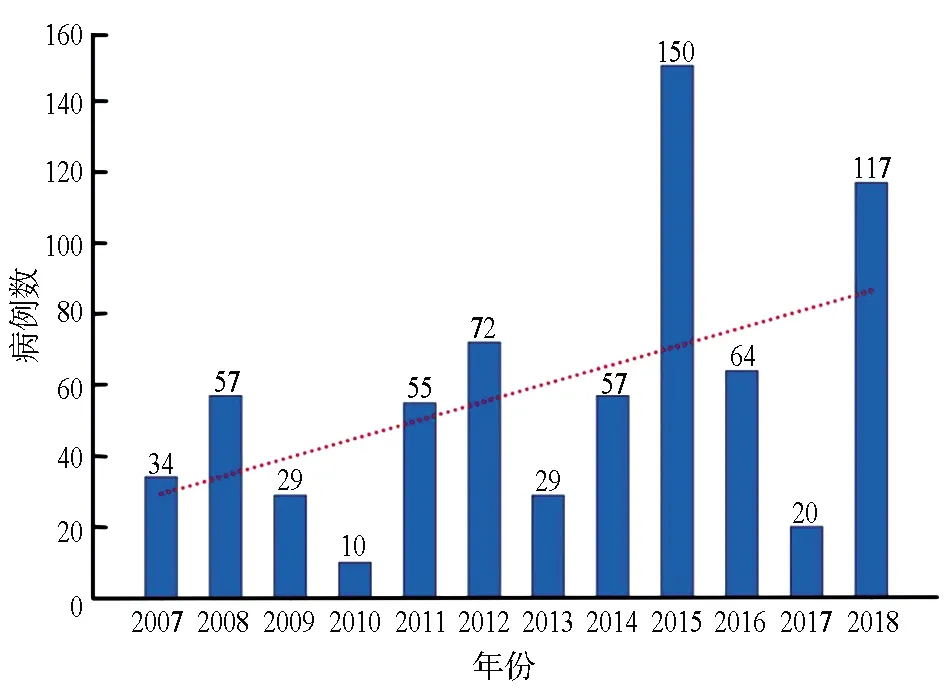
2.1文献报道时间及地区分布 近12年相关文献和报道的病例数整体呈上升趋势,见图1。相关文献报道主要集中在华北(266例,38.3%)、华东地区(200例,28.8%),东北地区(127例,18.3%)次之,华中(44例,6.3%)、西南(26例,3.7%)、华南地区(16例,2.3%)及西北(15例,2.2%)报道较少。
2.2性别及年龄分布 所有患者均为女性,年龄23~76岁。其中,文献提供患者准确年龄信息的147例,平均年龄43.6岁。多数患者57.1%(84/147)年龄为41~50岁,见图2。其余文献提供的患者平均年龄或中位年龄均为40~50岁。
2.3既往病史 文献中提及生育史的病例192例,其中181例(94.3%)为经产妇,11例为未产妇。在169例提及月经史的病例中,157例(92.9%)未绝经,12例(7.1%)已绝经。352例提供了子宫肌瘤病史信息的病例中,258例(73.3%)有子宫肌瘤病史,其中66例(25.6%)曾行子宫肌瘤剔除术,48例(18.6%)曾行全子宫或次全子宫切除术,5例(1.9%)曾行全子宫加单侧或双侧附件切除术;剩余139例(53.9%)未行手术治疗。
IVL:静脉内平滑肌瘤病

IVL:静脉内平滑肌瘤病
2.4临床症状 在603例描述临床症状的病例中,查体发现或无明显症状222例(36.8%),异常子宫出血201例(33.3%),腹痛腹胀123例(20.4%),胸闷或呼吸困难100例(16.6%),下肢水肿76例(12.6%),心悸45例(7.5%),晕厥38例(6.3%),头晕心慌35例(5.8%),心前区疼痛5例(0.8%),乏力4例(0.7%),布-加综合征、腹水各2例(0.3%),面部潮红、心力衰竭、产后1 d突发心脏停搏各1例(0.2%)。
2.5血管受累情况 在报道的所有病例中,560例提供了肿瘤血管蔓延的范围,其中319例(57.0%)仅局限于子宫及周围,27例(4.8%)最远蔓延至髂静脉,5例(0.9%)至卵巢静脉,62例(11.1%)至下腔静脉,111例(19.8%)至右心房,20例(3.6%)至右心室,16例(2.9%)至肺动脉(37.3%的病例累及下腔静脉,26.3%的病例累及心脏)。9例出现肺内转移。47例提供了肿瘤与血管壁的粘连情况,其中38例(80.9%)无任何粘连,2例与髂静脉粘连,1例与卵巢静脉粘连,1例与左肾静脉粘连,4例与下腔静脉粘连,1例与右心房粘连。研究的病例中,静脉内瘤栓长度为3.5~64 cm,直径为0.2~6 cm。
2.6诊断 在有术前诊断信息的132例病例中,116例(87.9%)术前未准确诊断,83例误诊为子宫肌瘤或子宫腺肌病,1例误诊为子宫肉瘤,2例误诊为卵巢肿瘤,5例误诊为右心房黏液瘤,1例误诊为风湿性心脏病,2例误诊为下腔静脉栓塞或血栓。
2.7治疗 在提供具体治疗方式的477例病例中,222例(46.5%)行全子宫+双侧附件切除术,160例(33.5%)行全子宫切除术,23例(4.8%)行全子宫+同侧附件切除术,14例(2.9%)行子宫肌瘤剔除术,3例(0.6%)行子宫次全切除术。进入子宫外静脉的病例中,12例行髂静脉切开取栓,5例行卵巢静脉切开取栓,1例行肾静脉切开取栓,72例行下腔静脉切开取栓,73例行心脏切开取栓。肿瘤完全切除172例(88.7%),不完全切除22例(11.3%)。术中死亡2例。涉及的术后并发症有切口并发症、肠梗阻各2例,静脉血栓1例,腹泻1例,心律失常、肾功能不全1例,术后出血1例,声音嘶哑1例,心内膜炎1例,肾积水1例,腹水1例,心房颤动1例,右侧胸腔积液1例。
2.8预后 在所有报道病例中,344例提供了术后随访信息,随访时间为1个月至29年,复发33例,死亡9例,其中5例术后复发死亡,4例未手术死亡。
2.9病例临床资料 2010年1月至2019年5月首都医科大学附属北京友谊医院共收治经手术病理证实的IVL病例5例,报道如下。
病例1:患者女,34岁,孕3产1。因双下肢水肿,伴有夜间阵发性呼吸困难于2010年9月入院。18个月前因“盆腔肿物”于外院行开腹全子宫+左附件切除+盆腔肿物切除术,术后病理考虑为IVL。查体见腹壁浅静脉曲张。血管造影提示左髂静脉显影欠佳,全下腔静脉扩张,其内可见多发不规则充盈缺损,肿物突入右心房。超声心动图提示下腔静脉至右心房内可见多腔、形态不规则的异常回声团,并随心动周期形态改变,舒张期经三尖瓣进入右心室流入道,收缩期位于右心房内至三尖瓣口。磁共振成像:盆腔、左侧髂内静脉及下腔静脉内富血供结节块影。手术切除盆腔肿瘤,术中见盆腔左侧肿物与周围粘连固定,不规则,有分支,并沿左侧卵巢静脉向上延伸生长,左卵巢静脉内有质韧肿物。12 d后Ⅱ期手术行体外循环下右心房、腔静脉切开血管内平滑肌瘤切除术。术后病理符合IVL。术后24 d出院,总住院时间52 d。术后失访。
病例2:患者女,39岁,孕1产1。因下腹部胀痛,双下肢水肿于2011年2月入院。既往高血压病史。查体下腹部可扪及一30 cm×25 cm巨大包块,局部轻压痛,活动度差。双下肢膝下可见凹性水肿,张力稍高。超声提示子宫左侧及后方见边界不清、不均质低回声肿物。CT:盆腔巨大占位病变,下腔静脉、双侧髂总静脉及左侧髂内外静脉内混杂密度。血管造影:双侧髂静脉近端及下腔静脉未见显影。磁共振成像:盆腔、左侧髂内静脉及下腔静脉内富血供结节块影。行手术治疗,术中见下腹部及盆腔腹膜后巨大分叶状圆球形占位,外有不完整包膜。静脉内可见不规则长条状瘤体,肿瘤体根部与盆腔静脉丛粘连。左侧髂静脉及下腔静脉内充满瘤体,静脉增粗。手术切除腹盆腔肿瘤+全子宫及左侧附件切除+下腔静脉内瘤栓。术后病理符合IVL,免疫组织化学:Vimentin阳性,Actin阳性,Desmin阳性。术后第2天二次手术清除腹腔内血肿。术后19 d出院,总住院时间32 d。术后失访。
病例3:患者女,52岁,孕3产1。因月经紊乱,经量增多,扪及下腹包块于2013年9月入院。既往左侧乳腺纤维瘤切除术史。查体子宫增大如孕5月大小。超声:子宫肌层回声极不均匀,内呈结节状回声,其内血流丰富,提示多发性子宫肌瘤。腹盆腔CT:盆腔见巨大软组织肿块,怀疑子宫肌瘤可能性大。行手术治疗,术中见子宫体增大如孕10周,表面多发结节样肿瘤,充满整个盆腔。探查左侧髂内静脉内见一长条形白色肌瘤样肿物长约10 cm。行盆腔肿瘤切除术+次全子宫切除术+左侧附件切除术+左侧髂内静脉瘤栓取出术。术后病理符合IVL。术后9 d出院,总住院时间10 d。随访6年无复发。
病例4:患者女,56岁,孕2产1。因下腹部不适于2017年10月入院。患者2002年于外院因子宫肌瘤行开腹全子宫切除术,2017年9月外院行盆腔肿物切除术+双附件切除术,术后病理为IVL。查体无明显阳性体征。血管超声:下腔静脉后壁自肾动脉水平以下可见附壁低回声,残余管腔内可见血流信号通过。CT:静脉内瘤栓形成。手术治疗,术中探查见下腔静脉内充满肿瘤,行下腔静脉肿瘤切除。术后19 d出院,总住院时间27 d。随访2年无复发。
病例5:患者女,42岁,孕3产2。因前次手术诊断IVL为求二次手术于2019年5月入院。患者2019年1月因盆腔包块于外院行子宫阔韧带肌瘤剔除术+左侧附件切除术,术后诊断为IVL。查体子宫左侧可触及实性结节,不平。超声提示左侧附件区不规则分叶状低回声肿物,其内血流丰富。CT:左侧附件区见不规则软组织密度影,增强后与子宫同步强化,静脉期左侧髂内静脉、髂总静脉内见充盈缺损,延伸至下腔静脉起始处。行全子宫+右侧附件切除术+左侧髂总静脉切开取瘤术,术中见子宫增大如孕10周大小,探查左侧髂总静脉内可及子宫肌瘤瘤栓,上延至下腔静脉水平。手术切除全子宫+右侧附件+左侧髂总静脉内瘤栓。术后7 d出院,总住院时间12 d。术后4个月复查CT提示左侧附件区见不规则软组织密度影,性质待定。
3 讨 论
虽然IVL较为罕见,但近年报道的文献和病例数有增多趋势,可能与对该病的临床认识增加以及诊断方法的进步有关。由于临床认识不足及早期诊断困难,且当病灶局限于子宫肌层内的小血管时,易被病理忽视[9],因此IVL的发病率可能远低于实际情况[7,10]。
有关IVL的发病机制尚不清楚,目前有两种理论:①Knauer理论认为,IVL来源于血管壁本身的平滑肌瘤组织[11];②Sitzenfry理论认为,IVL是肌瘤组织侵至肌层中血管内[12],两种理论均有证据支持[13-14]。但更多学者发现被平滑肌瘤侵入的血管壁是完整的,另外普通的肌层和IVL均为Desmin阳性,雌激素受体和孕激素受体在IVL通常为阳性,但静脉壁的平滑肌细胞Desmin、雌激素受体和孕激素受体均为阴性[9,15-16]。以上这些证据均支持第二种理论。
IVL全见于女性患者,世界范围内文献报道的年龄为21~80岁,但绝大多数为绝经前女性[17]。本研究中,所有患者均为女性,年龄23~76岁,文献报道的平均年龄或中位年龄为40~50岁。在有生育史信息的192例中,94.3%为经产妇,1例患者产后 1 d突发心搏骤停就诊发现该病[18],提示孕期高雌孕激素水平可能促进IVL的发生发展。本研究患者多数有子宫肌瘤病史[73.3%(258/352)]或子宫切除史,36.8%(222/603)的患者无任何症状,其余患者出现的临床症状也无特异性,主要表现为异常子宫出血,包括经量增多,经期延长,周期缩短等,也可能表现为腹部不适或盆腔痛等与盆腔肿物有关的症状。肿瘤沿静脉蔓延有两条途径:①子宫静脉、髂内静脉、髂总静脉、下腔静脉,进入心脏;②卵巢静脉、肾静脉、下腔静脉,进入心脏。当肿瘤蔓延超出盆腔沿静脉蔓延,可出现静脉回流障碍、体循环淤血的症状:呼吸困难、下肢水肿、胸痛,甚至晕厥或猝死。
IVL的病理表现大体为肿瘤由子宫肌层蔓延至肌壁间或子宫外静脉腔隙中,可游离在血管腔内或与血管壁相粘连,质地较韧,表面光滑,切面呈灰白或锈红色条索状或蠕虫状[19]。有文献报道,IVL的最长瘤栓为75 cm[20]。本研究中瘤栓最长为64 cm,经胸腹联合切口于静脉内剥除[21]。IVL的镜下特点为肿瘤由分化成熟、形态良性的平滑肌细胞组成,表面被覆一层扁平的内皮细胞,细胞形态多呈纺锤体或梭形,细胞核异型性和核分裂象罕见[22],核分裂象通常小于1个/15个高倍镜视野。其免疫组织化学:覆盖瘤体表面的单层扁平内皮细胞CD31、CD34阳性是病理诊断的重要依据。肿瘤平滑肌组织呈现和普通平滑肌瘤相似的特点,即Vimentin、Desmin和平滑肌肌动蛋白阳性,CD10阴性,可有雌激素和孕酮受体的表达[23]。
由于IVL罕见,临床症状无特异性,且早期肿瘤局限于子宫肌层内小静脉时不能被CT或磁共振成像检出,故IVL早期难以诊断。多数病例因肿瘤蔓延较远出现静脉回流障碍或心力衰竭等症状,通过进一步影像学检查得以诊断[24]。因猝死、心力衰竭死亡后才被确诊为IVL的病例也不少见[18,23]。因此,早期诊断对预后至关重要。如在术前即怀疑为IVL,可增加血管超声、心脏超声、CT、磁共振成像等影像检查了解其血管受累情况,以指导手术方式。对于诊断为子宫肌瘤、子宫腺肌病的病例,行全子宫切除术中可能发现IVL征象:子宫增大呈不规则形,均为暗红色结节状和特殊的静脉形态。血管内见表面光滑的条索样肿物,质韧,超出子宫肌瘤范围沿静脉向外延伸。有研究发现盆腔静脉内病灶的概率从高至低依次为阔韧带、子宫、卵巢、阴道[25]。若术中肉眼检查未发现,术后镜下病理检查应能诊断IVL,且取材不应局限于子宫肌瘤范围,周围的子宫平滑肌组织及腹膜反折下的子宫下段因血管极丰富,均应取材镜检[7,26]。
IVL的鉴别诊断包括子宫平滑肌肉瘤、子宫内膜间质肉瘤、弥漫性平滑肌瘤病、良性转移性平滑肌瘤等。肿瘤延伸至子宫外静脉引起阻塞症状易误诊为血管栓塞或血栓,心脏内平滑肌瘤病易误诊为心房黏液瘤[24]。因此,绝经前女性出现血管栓塞症状或发现右心肿瘤,应考虑IVL的可能[27-28]。本研究中,9例患者出现肺内转移,因此IVL患者发现双肺多发结节时,应考虑良性转移性平滑肌瘤的可能,且需避免因误诊为恶性转移性肿瘤而导致过度治疗[29]。
对IVL的治疗包括全子宫切除术+双侧附件切除术,且完全切除子宫外静脉内延伸的平滑肌瘤组织。对于要求保留子宫或卵巢的年轻患者,或由于侵犯周围脏器、与血管壁粘连未完全切除肿瘤的患者,术后应用促性腺激素释放激素类似物和抗雌激素治疗可能有效[16,30]。如累及心脏,可行胸腹分期手术或同期手术。分期手术为分两次手术,分别切除腹部和心脏内肿瘤,间隔时间为7 d至2年[31]。无法耐受同期手术的患者,有学者认为肿瘤延伸过长或严重粘连时可采取分期手术的方式[31]。但两次手术间期有肿瘤复发并进一步延伸至心脏的报道[32]。同期手术的优点包括避免二次麻醉风险、减少手术间期血流动力学并发症风险、减少第一次手术未完全切除的肿瘤脱落风险、减轻患者痛苦并降低医疗费用[31]。同期手术需妇科、心脏外科及血管外科等多学科配合完成。本研究中,80.9%(38/47)的病例肿瘤与血管壁无任何粘连,此为腹部或胸部单一切口牵拉切除肿瘤提供更多可能性,最大限度减小患者手术痛苦,但手术中应避免强行牵拉造成瘤栓断裂和出血。
本研究行手术治疗的患者中,33例术后随访期间复发,均未行全子宫及双侧附件切除术,或未完全切除脉管内肿瘤。由于雌激素和孕激素受体存在于肿瘤细胞和血管壁中,故双侧附件的切除有必要,且需避免外源性雌激素补充[33]。IVL极其罕见,临床对其认识不足,术前极易误诊,导致未行充分影像学检查,手术仅切除肿瘤或全子宫,致术后复发。因此,术中见肿瘤向静脉内蔓延,疑诊为IVL,可行冰冻病理检查,帮助诊断,确定手术范围[34-35]。如术后确诊为IVL而手术未行全子宫及双侧附件切除术,应进一步行影像学检查明确蔓延范围及残留肿瘤[36],对于无生育要求的患者,应尽早二次手术切除全子宫及双侧附件,并切除可见的静脉内蔓延的肿瘤。
文献报道,IVL的复发率为16.6%~30%[7]。患者较年轻及肿瘤较大可能是复发的易感因素[7]。Valdés Devesa等[17]报道的术中行全子宫、双侧附件切除并切除所有可见肿瘤的病例复发率为7.6%(1/13),行全子宫切除的病例为25%(4/20),行全子宫加单侧附件切除的病例为44%(5/9),仅行肌瘤切除而保留子宫及附件的病例复发率最高,为75%(3/4)。可见,手术未完全切除肿瘤和残留镜下肿瘤细胞是导致IVL复发的常见原因,且复发可能出现在手术后较长时间,文献报道复发可见于初次手术后7个月至15年,因此术后有必要长期随访[35]。腹部、盆腔和胸部CT有助于发现早期复发的肿瘤,必要时可增加磁共振成像检查。磁共振血管内成像可有效地发现IVL。一旦复发,应尽早再次手术切除。
本院近10年收治的经手术病理证实的5例IVL病例,年龄34~56岁,中位年龄42岁,均为已婚已育女性,与国内文献报道相符。其中3例既往行盆腔肿物切除术,此次为二次手术。临床症状均无特异性,3例患者自觉下腹包块或下腹不适,1例表现为月经紊乱、经量增多,2例因静脉回流障碍出现下肢水肿、夜间阵发性呼吸困难。1例血管内瘤栓最远蔓延至髂内静脉,3例至下腔静脉,1例至右心房。2例行全子宫、双侧附件及静脉内肿瘤切除术,2例因患者年轻行全子宫、单侧附件及静脉内肿瘤切除术,1例因粘连严重行次全子宫、单侧附件及静脉内肿瘤切除术。1例术前误诊为子宫肌瘤,3例因前次手术治疗得以诊断为IVL,仅1例(病例2)根据症状、辅助检查术前即考虑诊断为IVL。住院时间为10~52 d,平均27 d,1例因行胸腹分期手术住院52 d,1例因术后腹腔内出血二次手术住院32 d。1例(病例5)术后4个月复查CT提示左侧附件区软组织密度影,性质不明,2例随访2、6年无复发,2例失访。
综上可知,由于该病罕见、对其认识不足及临床症状缺乏特异性,IVL的早期诊断困难,误诊率高,导致术前未充分评估。绝经前女性出现血栓栓塞症状或心脏症状,应考虑IVL的可能。IVL的手术方式应为全子宫加双侧附件切除术,并完全切除血管内肿瘤,可降低复发率。术后应长期密切随访,对于复发的肿瘤应再次手术切除,可获得良好预后。

