3 种铕(Ⅲ)-(β-二酮)配合物合成及发光性能
倪貌貌,陈佳祎,汤淑利,庞钰君,宋亚萍,张凯龙
(浙江万里学院生物与环境学院,浙江宁波315100)
0 引 言
照明摆脱了黑夜的束缚,扩展了人类活动时空范围,从化学燃烧到电热辐射,从电离辐射到发光二极管,照明方式变化是人类文明进步和科技发展的历史见证。发光二极管(LED)能直接将电能转化为光能,驱动电压低、电光转换效率高,同时亮度高、寿命长、绿色环保,是目前和可预见未来电致发光材料器件发展的主要方向[1-4]。
适宜照明的白光LED 可以通过红绿蓝3 芯片组合或者单芯片激发复合获得。原位红绿蓝3 芯片发光效率高,颜色调节方便灵活,多个LED 组合成本较高,限制了该方案的应用。单芯片蓝光转换黄光复合获得白光是目前广泛使用的方案,但存在专利技术壁垒,获得的白光缺乏红光成分、色温偏高且显色指数较低,难以满足低色温照明与高显色性。近紫外单芯片转换红、绿、蓝三基色复合白光是一个开放方案,调控灵活,显色指数高、色温漂移低,色彩稳定,是未来发展方向[5-7]。光转换材料中红光材料发光效率较低,而且红光缺失会导致显色品质恶化、色温升高等问题,是制备白光LED的关键和亟待突破的瓶颈。
稀土铕配合物单色性能好、发光强度高、衰变寿命长而备受关注[8-9]。β-二酮类有机化合物具有较高的吸收系数,激发能量较低,易进行合成与修饰,为开发高效稳定的铕有机配合物红光材料提供了优良配体[10-12]。近紫外转换红光铕配合物配体吸收近紫外光,通过“天线效应”将能量转移给中心铕原子发射,研究、总结配体对荧光激发和发射光谱的影响及规律可以从理论高度上指导设计新型、高效的红光材料。
实验以Eu(Ⅲ)为中心原子,2-噻吩甲酰三氟丙酮(TTA)和二苯甲酰甲烷(DBM)为第一配体,三苯基氧膦(TPPO)和1,10-菲罗啉(Phen)为第二配体,采用超声辅助溶剂热法组合制备3 种Eu-(β-二酮)配合物,通过多种手段对配合物进行确认和表征,对比分析不同配体对发光性能的影响,以合成配合物为组分制作了近紫外光转换红光和白光LED器件。
1 材料与方法
1.1 主要试剂与仪器
试剂:六水氯化铕(EuCl3·6H2O,AR)、2-噻吩甲酰三氟丙酮(TTA,≥98%)、三苯基氧膦(TPPO,≥98%)、二苯甲酰甲烷(DBM,≥98%)、1,10-菲罗啉(Phen,≥99%)均为上海阿拉丁化学试剂,无水乙醇、氢氧化钠、氯化钾均为国药分析纯试剂,甲醇为国药HPLC试剂,磷酸钠、浓硝酸、高氯酸为国药优级纯,Mili-Q去离子水。
仪器电子天平(ME104E,梅特勒-托利多公司),水热反应釜(50 mL聚四氟乙烯内胆,科盾办公用品旗舰店),超声波清洗机(KS-1000T,宁波科生超声波设备有限公司),真空干燥箱(DZF-6090,上海慧泰仪器制造有限公司),荧光光谱仪(FL3-111,法国Horiba),荧光光谱仪(FLS920,英国爱丁堡),热重分析仪(Diamond TG,美国PerkinElmer),电感耦合等离子发射光谱仪(ICAP6300,美国Thermo Fisher),元素分析仪(VarioMicro cube,德国Elementar),傅里叶变换红外光谱仪(Vertex 70,德国Bruker),电导率仪(DDSJ-308F,上海雷磁);全自动旋光仪(P850,山东海能),紫外-可见分光光度计(UV2600,日本岛津),离心机(5404R,德国eppendorf)。
1.2 Eu-(β-二酮)配合物制备
Eu-(β-二酮)配合物采用超声辅助溶剂热法合成,如图1 所示,将1 mmol六水氯化铕溶解于10 mL无水乙醇中,分别搅拌滴加溶解有化学计量比的第一、二配体的10 mL乙醇溶液,调节pH为6 ~7,将反应釜放入80 ℃超声波清洗槽,超声反应2 h,自然冷却到室温,沉淀离心后用少量乙醇洗涤,50 ℃真空干燥。合成铕(Ⅲ)-(2-噻吩甲酰三氟丙酮)-三苯基氧膦、铕(Ⅲ)-二苯甲酰甲烷-三苯基氧膦、铕(Ⅲ)-二苯甲酰甲烷-邻菲罗啉分别记为Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBMPhen。
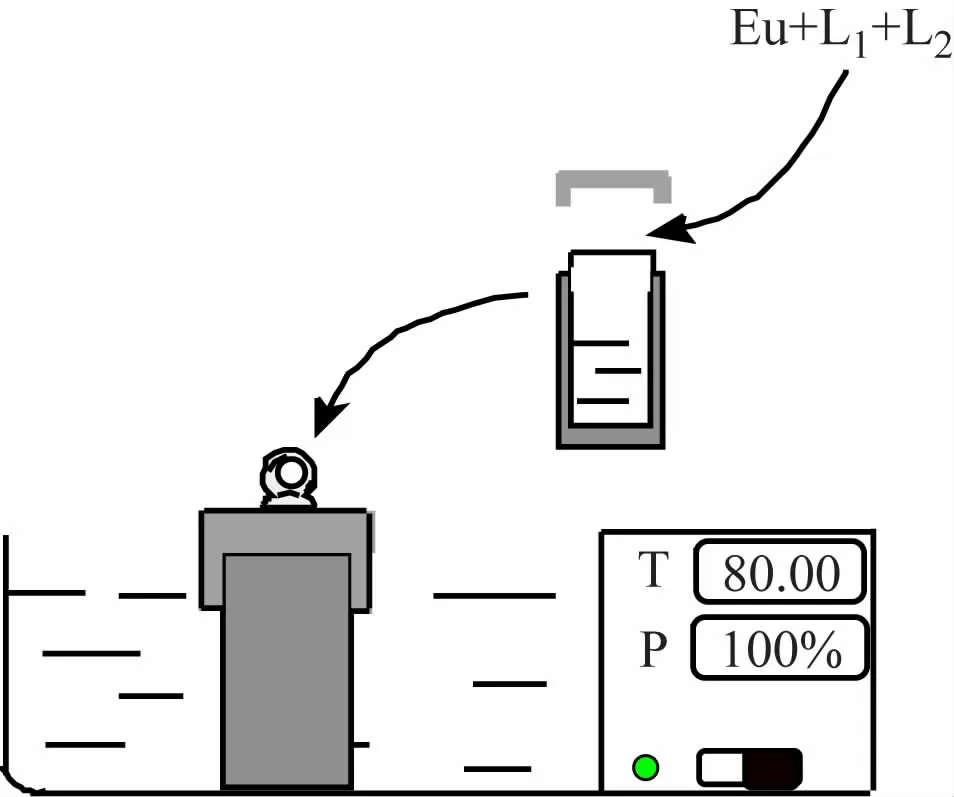
图1 超声辅助溶剂热合成反应装置
根据元素分析仪测定CHNS 含量,ICP-AES 测定Eu和P 含量,并根据Eu3+、TTA、DBM、TPPO、Phen 可能成键方式,确定3 种铕(Ⅲ)-(β-二酮)配合物组成为Eu (TTA )3(TPPO )2、 Eu (DBM )3TPPO、Eu(DBM)3Phen,合成反应方程式如图2 ~4 所示。

图2 Eu-TTA-TPPO合成反应方程式
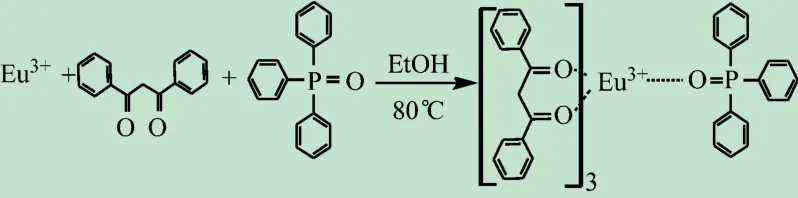
图3 Eu-DBM-TPPO合成反应方程式

图4 Eu-DBM-Phen合成反应方程式
1.3 铕配合物测试表征方法
(1)外观形态。取少量样品置于超滤膜上,观察自然日光、365 nm 近紫外LED照射下颜色形态。
(2)溶解性。取少量样品于离心管中,滴加0.5 mL溶剂振荡10 min,观察溶解情况。
(3)电导率。1 mmol/L氯化钾校准,取适量待测液于烧杯,自动调节量程并测定。
(4)旋光。10 cm 旋光管注入甲醇调零,样品溶液润洗2 或3 次,装样测定。
(5)元素分析。CHNS 使用元素分析仪测定,测定前使用对氨基苯磺酸校准;P、Eu 元素使用ICP-AES测定,配合物使用浓硝酸、高氯酸加热消解,1%稀硝酸稀释定容。
(6)热重分析。空气氛围,室温到800 ℃,升温速率10 ℃ /min。
(7)红外光谱。溴化钾压片,扫描范围4 000 ~400 cm-1,分辨率4 cm-1,扫描16 次。
(8)紫外吸收光谱。以甲醇为参比,在200 ~400 nm波长范围进行扫描。
(9)荧光光谱。采用固体粉末法直接测定,在615 nm发射波长和365 nm激发波长下测定材料激发光谱和发射光谱,测定量子产率和荧光寿命。
2 结果与讨论
2.1 基本性质
3 种铕(Ⅲ)-(β-二酮)配合物外观形态如表1 所示,自然光照下Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen分别为浅橙红色、浅橙黄色、浅黄色粉末,在365 nm近紫外LED 照射下均发射出耀眼红色,艳丽纯正。

表1 3 种配合物外观形态
Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen均在空气中性质稳定,易溶于乙醇、丙酮、乙酸乙酯、二氯甲烷、N,N-二甲基甲酰胺、二甲亚砜。
Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen摩尔电导率分别为6.88、8.00、8.07 mS·m2/mol,表明3种配合物在甲醇中均为非电解质。
Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen测定旋光值均为0,表明3 种配合物均无旋光活性。
2.2 紫外光谱
以甲醇为参比,在紫外区测定4 种配体和3 种配合物吸收光谱,如图5 所示。自由配体时,HTTA 在267 nm处的特征吸收对应噻吩环π→π*跃迁,TPPO在223 nm处、268 nm 处特征吸收对应苯环磷氧键π→π*、n→π*跃迁,HDBM在257 nm处、340 nm处特征吸收为苯环羰基π→π*跃迁,Phen 在230 nm 处、264 nm处的特征吸收峰为芳杂环结构π→π*、n→π*跃迁。合成配合物在紫外区吸收强烈,吸收峰包括各配体特征吸收,同时配体吸收峰在配合物中呈现出加强、衰减、偏移等行为,确认各配体与铕原子配位成键,形成紫外强吸收多元配体配位结构,这有利于配体紫外光能量吸收、转移,从而促进中心铕原子发光。

图5 3种配合物及配体紫外光谱
2.3 红外光谱
4 种配体和3 种配合物红外光谱如图6 所示,图6(a)自由配体HTTA中C =O伸缩振动峰1 610、1 539 cm-1在Eu-TTA-TPPO 中偏移到1 604、1 525 cm-1,TPPO中P =O 键伸缩振动峰由1 190 cm-1偏移到1 172 cm-1,538 cm-1中出现Eu-O 伸缩振动峰,相关配体吸收峰偏移及新键吸收出现表明TTA、TPPO 与Eu 配位成功[13]。图6(b)自由配体HDBM 中C = O伸缩振动峰由1 597、1 524 cm-1红移到1 554、1 518 cm-1,TPPO 中P = O 键吸收峰偏移及Eu-O 吸收峰的出现确认DBM、TPPO 与Eu 配位成功。图6(c)中Phen在1 504 cm-1的C =N伸缩振动峰红移到1 467,1 418 cm-1的C—N 伸缩振动峰红移到1 406 cm-1,DBM吸收峰偏移及Eu-O 键的出现同样确认了DBM、Phen与Eu有效配位。
2.4 热稳定性

图6 3种配合物及配体红外光谱
如图7所示Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen热稳定性良好,起始分解温度均在250 ℃左右,远高于LED材料使用温度150 ~180 ℃,3 种配合物都能满足近紫外光转换材料使用条件[14]。3 种配合物在250 ~ 400 ℃、450 ~ 550 ℃ 范围出现2 次最大热解速率温度,主要为第1、2 配体不完全分解贡献,600 ~700 ℃以上3 种配合物热解完全,残留主要为Eu氧化物和配体热解碳化物。
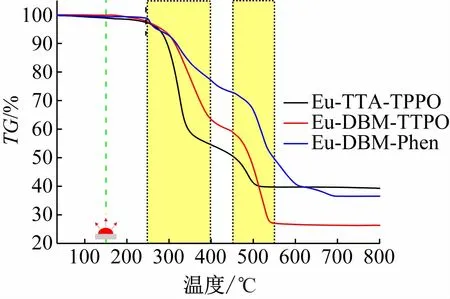
图7 3种配合物热重曲线
2.5 荧光光谱、量子产率及荧光寿命
以615 nm 为监测波长,测定3 种配合物激发光谱,峰值激发强度Eu-TTA-TPPO >Eu-DBM-Phen >Eu-DBM-TPPO。为研究波长对激发光谱的影响,对Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen的激发光谱进行归一化处理,如图8 所示,三者均在370 nm 处具有最大激发强度,可激发波长范围Eu-TTA-TPPO <Eu-DBM-Phen < Eu-DBM-TPPO,Eu-DBM-TPPO、Eu-DBM-Phen在300 ~500 nm较宽波长范围均具有强紫外激发能力,这有利于在更大的紫外光激发范围内的使用,而Eu-TTA-TPPO的峰宽相对较窄,主要集中在365 nm 两侧300 ~400 nm 范围,三者在365 nm 近紫外激发波长下均能发射出铕(Ⅲ)优良的特征红光。Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen在激发强度和激发波长范围方面各有优劣,为光转换红光材料调制提供了更多的选择。
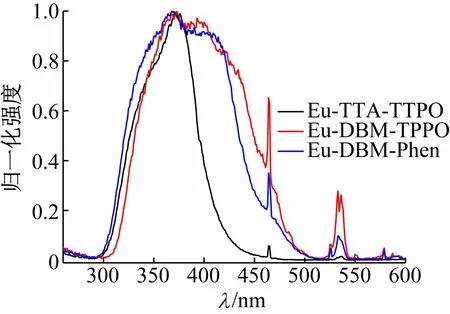
图8 3种配合物激发光谱
在365 nm 激发下,615 nm 附近荧光峰值强度依次为Eu-TTA-TPPO > Eu-DBM-Phen > Eu-DBM-TPPO。为研究波长与发射光谱关系,归一化发射光谱如图9所示,在365 nm 紫外灯照射下,Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen 3 种三元配合物均呈现出中心离子Eu(Ⅲ)的特征红色荧光,位于578、590、613、650、700 nm 附近的峰谱,分别与5D0→7FJ(J= 0,1,2,3,4)相对应,没有观察到各配体的发射带,表明3 种铕配合物中的各配体将激发能有效地传递给中心离子Eu3+。
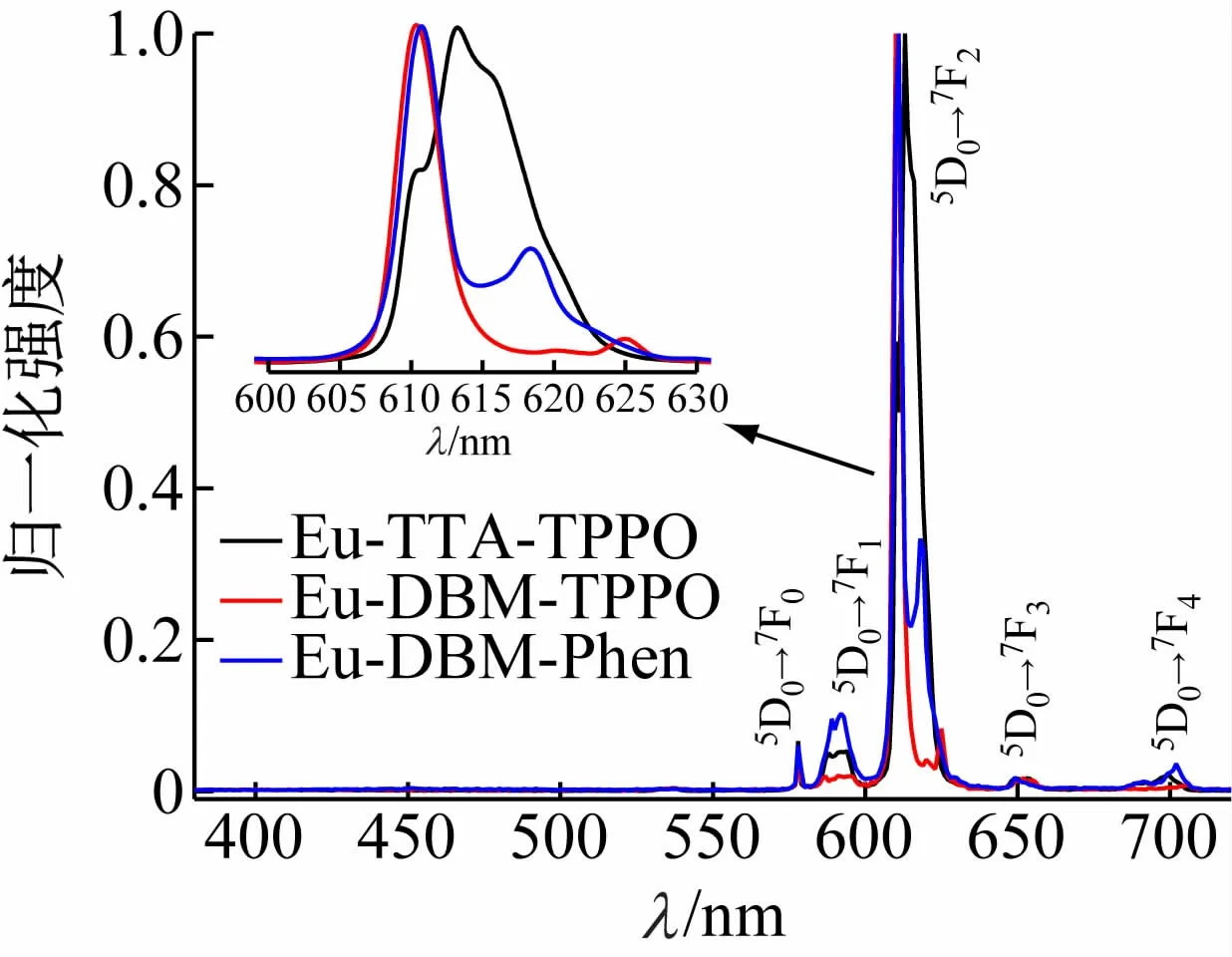
图9 3种配合物发射光谱
两种β-二酮类第1 配体TTA、DBM均能与铕离子生成螯合环,并包含电子可运动的共轭链,使得配合物具有稳定的化学性质。由于TTA是不对称配体,更容易实现f-f 跃迁,而DBM 是对称配体,且TTA 中的噻吩比DBM 中的苯环具有更强的电子给予特性,Eu-TTA-TPPO相较于Eu-DBM-TPPO 具有更高的荧光发射效率[15]。
TPPO、Phen均是配位能力比溶剂乙醇强的中性配体,且其共轭程度较高、刚性较好,能有效减小乙醇分子的高频O—H 振动所带来的能量损失,并能增加对紫外的吸收能力,从而提高配合物的荧光效率。TPPO、Phen 最低三重态能级分别为18 867 cm-1、22 131 cm-1,铕(Ⅲ)最低激发态能级在17 200 cm-1,根据Latva经验规则,>2 500 cm-1时,能量传递效果最佳,ΔETPPO= 1 667 cm-1,ΔEPhen= 4 931 cm-1,Phen 能量传递效果比TPPO 更佳[16]。
以Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen配合物的发射光谱数据计算其色坐标分别为(0.657,0.331)、(0.631,0.338)、(0.630,0.340),如图10 所示,Eu-TTA-TPPO 的红光单色光特性最好,Eu-DBMTPPO和Eu-DBM-Phen无显著区别。
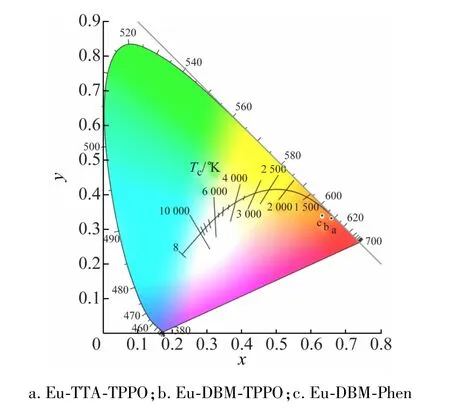
图10 2种配合物色坐标
测定Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen量子产率分别为27.7%、17.3%、19.4%,和同类Eu光转换材料接近。
瞬态荧光测定Eu-TTA-TPPO、Eu-DBM-TPPO、Eu-DBM-Phen荧光寿命,指数拟合如图11 所示,荧光寿命分别为0.491、0.184、0.247 ms。

图11 3种配合物荧光寿命
2.6 近紫外光转换红光及白光器件
取少量Eu-TTA-TPPO 样品与少量硅胶粉末在研钵中混匀,分散到封装胶中,用毛细管蘸取少量涂于365 nm 近紫外LED 灯表面,静置固化,接通电源,如图12 所示,近紫外LED发射出明亮艳丽的红光。

图12 Eu-TTA-TPPO涂覆近紫外LED转换红光
以Eu-TTA-TPPO 为红光材料,合成Tb-AA-Phen为绿色材料,商品铕激活铝酸镁钡BaMgAl10O17:Eu2+(BAM)为蓝光材料,按红粉∶绿粉∶蓝粉=0.5∶3∶1的比例与硅胶粉研磨混匀,分散到封装胶中,用毛细管蘸取少量涂覆于LED灯表面,静置固化,接通电源,如图13 所示,近紫外LED发射出明亮耀眼的白光。

图13 Eu-TTA-TPPO调制近紫外LED转换白光
3 结 语
(1)实验采用超声辅助溶剂热法成功制备了3 种近紫外转换红光铕配合物,三者均具有强烈紫外吸收,良好的热稳定性和近紫外转换红光性能。比较发现TTA不对称配体结构比DBM 更容易实现f-f 跃迁,TTA天线效应强于DBM,荧光发射效率更高。Phen协同配体的敏化作用强于TPPO,能量传递效果更好。
(2)实验涉及多门课程多个知识点,可以根据课程特点进行适当调整,如无机合成侧重配合物合成和铕元素滴定分析,有机合成设计修饰配体并比较其对发光性能影响,仪器分析进行多种手段分析表征,也可以作为综合实验进行较为完整系统研究,撰写研究论文,提升学生基本科研能力。
(3)课题扩展性强,在课程实验中不同分组可以自由选择配体、稀土或过渡金属中心原子,甚至扩展到近紫外无机光转换材料,组间对比分析结构对性能的影响,培养学生的研究创新、分析比较、归纳综合、团队协作能力。
(4)课题贴近生活日常,融合基础理论和实际应用,从原料到器件实物,操作性强,富有趣味性,可以充分激发并调动学生的学习热情。融入课程思政和专业认知,结合生活中经历过的不同照明方式,感受科技发展对生活和社会的巨大影响,讨论化学学科创造新物质的核心地位及其对人类生存发展的巨大贡献,建立正确的化学观、提高专业认可和热爱。

