不同载体蛋白制备的3 型肺炎球菌结合物在小鼠体内免疫原性比较
杨英英 张钰奇 任珍芸 张丽芝 马凯凯 高晶晶 杜娇 王欣茹 乔瑞洁 马钰 周海飞 王玺 罗树权
兰州生物制品研究所有限责任公司,甘肃 兰州730046
肺炎链球菌是肺炎的主要病原体,可引发脑膜炎、菌血症、败血症等侵袭性感染疾病及中耳炎、社区获得性肺炎等常见的疾病。据统计,全球已有120 万儿童死于肺炎球菌引起的肺炎和脑膜炎[1]。在发达国家,肺炎球菌引起的肺炎死亡率为11%~40%[2]。在引起肺炎球菌发病的诸多血清型中,3 型肺炎球菌是引起儿科复杂肺炎球菌性肺炎和中耳炎的主要病原体,同时也是引起儿童和成人侵袭性肺炎最常见的病原体[3,4]。
荚膜多糖是肺炎链球菌的主要毒力因子和保护性抗原,其属于T 细胞非依赖性抗原,不能保护两岁以下婴幼儿肺炎球菌引起的感染,只有与载体蛋白结合后成为T 细胞依赖性抗原才能对婴幼儿产生免疫保护。
GSK 公司最初研制的11 价肺炎结合疫苗中包含3 型肺炎球菌,使用流感嗜血杆菌蛋白D(PD)为载体,但最终因为3 型肺炎球菌的保护效果差而放弃加入3型肺炎球菌,以10 价肺炎结合疫苗上市[5]。2010 年辉瑞公司上市的PCV13 中包含血清型3 型肺炎球菌,使用的载体为CRM197。PCV13 上市后,儿童侵袭性肺炎和中耳炎的发病率显著降低[6],并产生了疫苗血清型群体免疫保护作用[7],但来自7 个国家的研究数据显示,PCV13 对3 型肺炎球菌的免疫保护效果差[8-16]。
多糖蛋白结合疫苗的免疫原性受多糖结构完整性、多糖糖链长度、游离多糖含量、载体蛋白性质、结合物分子大小、多糖与蛋白比值及佐剂的免疫增强效应等多种因素影响,而载体蛋白的性质是免疫原性影响因素中最重要的一个[17]。由于3 型肺炎球菌、PD 及CRM197 制备的结合物的免疫保护效果欠佳,本文选择了2 种载体蛋白(TT 和rEPA),并将这两种蛋白分别进行己二酸二酰肼(adipic acid dihydrazide,ADH)衍生,制备出两种衍生蛋白(TTAH和rEPAAH),用相同的结合方法将3 型荚膜多糖与这4 种载体蛋白制备了4种结合物,比较不同载体蛋白制备的3 型肺炎球菌结合物在小鼠体内的免疫原性,评价不同载体蛋白制备的3 型肺炎球菌结合物在小鼠体内免疫原性的差异。
1 材料与方法
1.1 样品 3 型肺炎球菌荚膜多糖(PS3)、破伤风类毒素(TT)、破伤风类毒素衍生物(TTAH)、重组铜绿假单胞菌外毒素A(rEPA)、重组铜绿假单胞菌外毒素A 衍生物(rEPAAH)均由兰州生物制品研究所有限责任公司制备。
1.2 实验动物 实验动物为美国国立卫生研究院(NIH)雌性小鼠[编号:SYXK(甘·2017-0001)]150 只,SPF 级,体重约12~14g,由兰州生物制品研究所有限责任公司动物室提供。
1.3 主要试剂 ADH、1-氰基-4-二甲胺基吡啶四氟硼酸盐(CDAP)、三乙胺(TEA)、乙腈、脱氧胆酸钠(DOC)和蒽酮均购自Sigma 公司;碱性磷酸酶标记的羊抗-鼠、羊抗-兔IgG 均购自美国Southernbiotech 公司;精制破伤风抗毒素血清、精制重组铜绿假单胞菌外毒素血清及3 型肺炎球菌超免血清均由兰州生物制品研究所有限责任公司制备;HCl、乙酸、NaOH 和NaCl均购自国药集团化学试剂有限公司。
1.4 仪器 Labscale 超滤系统和超滤膜均购自Millipore 公司;Spectra MAX190 酶标仪购自Costar 公司;96 孔酶标板(Costar 92592)购自美国Corning 公司;AKTA prime plus 型层析系统、Sepharose CL-4B 凝胶、Sepharose 4 fast flow 凝胶及XK16/100 层析柱均购自GE 公司;高压液相色谱仪、2707 型自动进样器和2489型紫外检测器均购自Waters 公司;高效液相排阻层析柱(TSK-4000 PWXL、TSK-6000 PWXL及TSK-3000 SWXL)购自TOSOH 公司;十八角激光光散射仪(Wyatt DAWN HELEOS-Ⅱ)和示差监测器(Wyatt Optilab T-rEX)均购自美国Wyatt 公司。
1.5 多糖水解物的制备 PS3 反应终浓度为5mg/mL,醋酸终浓度为0.5M,80℃反应15h、次日冷却至室温,用5M NaOH 调节水解物溶液pH 至7.0 左右终止反应。水解物溶液用注射用水超滤4 次后冻干。水解物经Sepharose CL-4B 上样,测定其分子大小分布。用高效液相-排阻层析-十八角激光光散射仪(HPSECMALLS)联用法测定水解物分子量[18]。并通过1H NMR确认水解物结构的正确性。
1.6 TT 及rEPA 衍生物的制备 采用EDAC 缩合法,将TT 及rEPA 分别用0.85%NaCl 溶液稀释至终浓度为10mg/mL,然后将其加入等体积的0.9mol/L ADH 中,调节至pH6.5,加入EDAC 使其终浓度为7.5mmol/L,控制pH 在(6.5±0.1),反应2h,调节至pH8.0,终止反应,用含0.85%NaCl 将衍生物超滤浓缩,除菌过滤得到的衍生物为TTAH及rEPAAH。以Lowry 法测定两种衍生物的蛋白含量,TNBS 法测定衍生率。
1.7 结合物的制备及纯化 PS3 水解物用0.85%NaCl 溶解成5mg/mL,室温静置过夜,测初始pH 值并将其调至5.8~6.0。将CDAP 以200mg/mL 浓度溶于乙腈中,加入多糖降解物一半质量的CDAP,维持pH5.8~6.0 反应30s。用TEA 溶液(28μL TEA+972μL WFI)将pH 维持在(7.3±0.5)反应2min。按投入糖:蛋白质量比为1∶1 分别加入TT、TTAH、rEPA 及rEPAAH,维持pH(8.0±0.2)反应2h。反应结束后将pH 值调至7.0,将反应物装入截留分子量为10kDa 的透析袋中,以0.85%NaCl 溶液为透析外液,透析2天,收集结合物。制备的四种结合物分别为PS3-TT、PS3-TTAH、PS3-rEPA 及PS3-rEPAAH。
四种结合物均经Sepharose 4fast flow 层析柱纯化,收集KD≤0.2 的洗脱液,流动相为0.85%NaCl 溶液。将收集的洗脱液以0.22μm 膜除菌过滤后于2℃~8℃保存。
1.8 鉴别试验 运用琼脂糖免疫双扩散法分别对四种结合物进行鉴别试验,方法参照《中华人民共和国药典》2015 版(四部)的通则3403 要求执行[18]。
1.9 结合物的理化检测 分别测定上述四种3 型肺炎球菌结合物的多糖含量、蛋白质含量、游离多糖、游离蛋白含量及重均分子量。多糖含量检测参照采用蒽酮硫酸法;蛋白质含量检测采用Lowry 法;游离多糖含量检测采用脱氧胆酸钠法[18];游离蛋白质含量检测采用高效液相色谱法[18]。采用高效液相-排阻层析-十八角激光光散射仪(HPSEC-MALLS)联用法测定结合物分子量[18]。
1.10 结合物免疫原性研究
1.10.1 动物免疫。将小鼠随机分为多糖对照组、免疫PS3-TT、PS3-TTAH、PS3-rEPA、PS3-rEPAAH四种结合物,每组30 只。多糖对照组是将3 型多糖水解物用生理盐水稀释为4.0μg/mL。四种结合物根据其对应的多糖含量分别用生理盐水其稀释至多糖终浓度为4.0μg/mL。免疫程序为0、14、28 天分别进行第1、2、3针腹股沟皮下注射,剂量为每针次每只小鼠免疫0.1mL,即每针次每只小鼠0.4μg。
1.10.2 ELISA。每针免疫后间隔14 天进行小鼠眼球采血,分离血清,用间接ELISA 测定血清抗PS3 IgG 含量[18]。
1.11 统计学分析 采用Softmax 软件分析中提供的四参数拟合法分析数据,阳性血清ELISA 单位为800EU/mL,应用分析模板计算各样品的ELISA 单位,根据血清数量计算几何平均值得到ELISA 单位的几何平均值(GMU)。采用SPSS 17.0 软件进行统计学分析,免疫原性的比较采用方差分析,P<0.05 为差异有统计学意义。
2 结果
2.1 水解物的分子大小 3 型多糖经乙酸水解后呈对称性分布,顶峰KD值为0.5。见图1。HPLC-SECMALLS 测定其重均分子量为6.45×104g/mol,分子量分布范围为1.74×104~44.75×104g/mol。
2.2 水解物的NMR 分析 多糖经水解后,水解物的结构与水解前相比结构完全相同,说明多糖水解过程中并未改变多糖的结构。见图2。
2.3 TT 及rEPA 衍生物的化学检定结果 从衍生率结果看,两种蛋白上均成功地与ADH 连接。见表1。
2.4 鉴别试验 四种3 型结合物均能同时与3 型多糖免疫血清和TT/rEPA 免疫血清产生沉淀线,且两条沉淀线发生融合,阴性对照生理盐水与3 型多糖免疫血清和TT/rEPA 免疫血清均不产生沉淀线,说明四种结合物均具有良好的抗原性。见图3。
2.5 3型肺炎球菌结合物理化及分子量检测 四种结合物中游离多糖含量较低,均在3%以内;游离蛋白质含量也较低,在5%以内。四种结合物的糖蛋白比在0.60~1.00。PS3-TTAH与PS3-rEPAAH重均分子量结果相近,均在3.60×106左右,PS3-TT 与PS3-rEPA 重均分子量结果相近,均在2.00×106~2.60×106。见表2。
2.6 IgG 抗体含量检测 随着免疫针次的增加,PS3对照组3 针免疫IgG 含量无明显差异,但结合物组IgG含量明显升高。4 种结合物在小鼠体内均能产生较高水平的抗体。蛋白衍生后的结合物组(PS3-TTAH及PS3-rEPAAH)第2、3 针IgG 含量均明显低于其对应的蛋白未衍生组(PS3-TT 及PS3-rEPA)。见表3。

图1 3 型肺炎球菌多糖水解物的Sepharose CL-4B 分布图
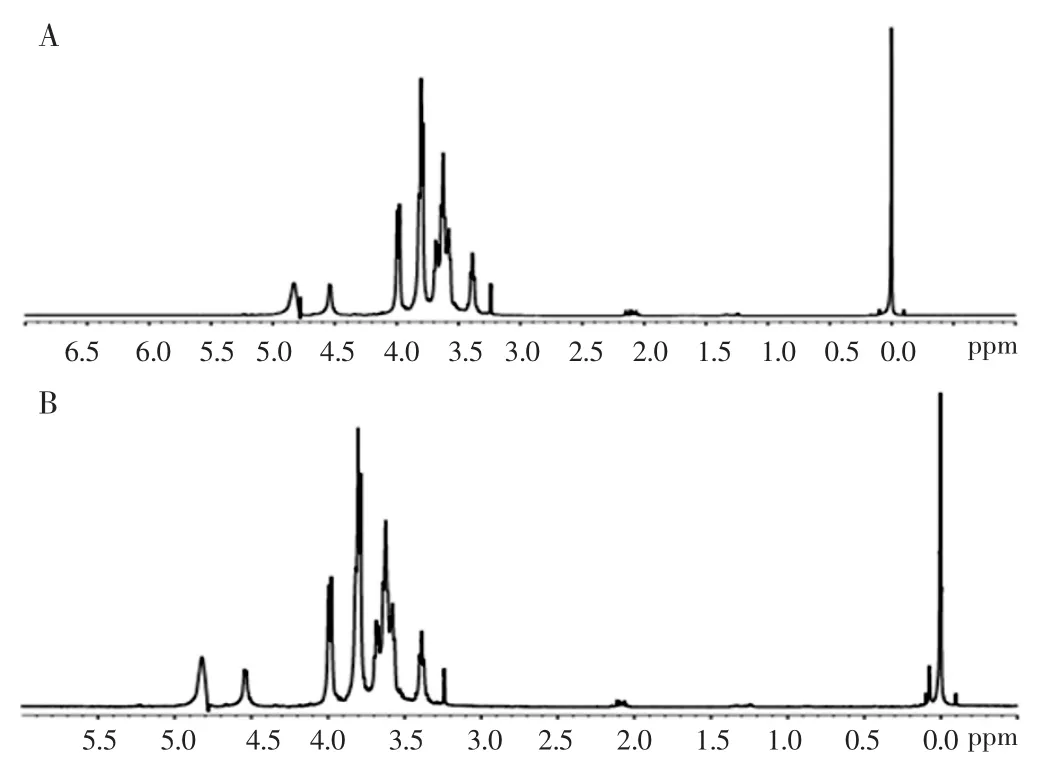
图2 3 型肺炎球菌多糖水解物1H NMR 图谱

表1 蛋白质衍生物检测结果
随着免疫针次的增加,PS3 组3 针免疫无剂次加强效应,4 组结合物第2、3 针之间均有明显的剂次加强效应。对于同类载体蛋白,PS3-TTAH比PS3-TT 第3针抗体的水平低,但差异无统计学意义(P=0.31);PS3-rEPAAH比PS3-rEPA 第3 针抗体的水平低,差异无统计学意义(P=0.21)。对于不同类均未衍生载体蛋白,PS3-TT 比PS3-rEPA 第3 针抗体的水平高,差异无统计学意义(P=0.17);对于不同类均经衍生的载体蛋白,PS3-TTAH比PS3-rEPAAH第3 针抗体的水平高,差异无统计学意义(P=0.28);PS3-TTAH与PS3-rEPA 第3 针抗体水平相当,差异无统计学意义(P=0.99)。见图4。
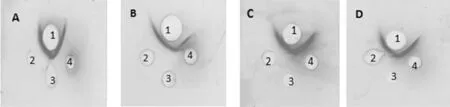
图3 四种3 型肺炎球菌结合物免疫双扩散检测结果
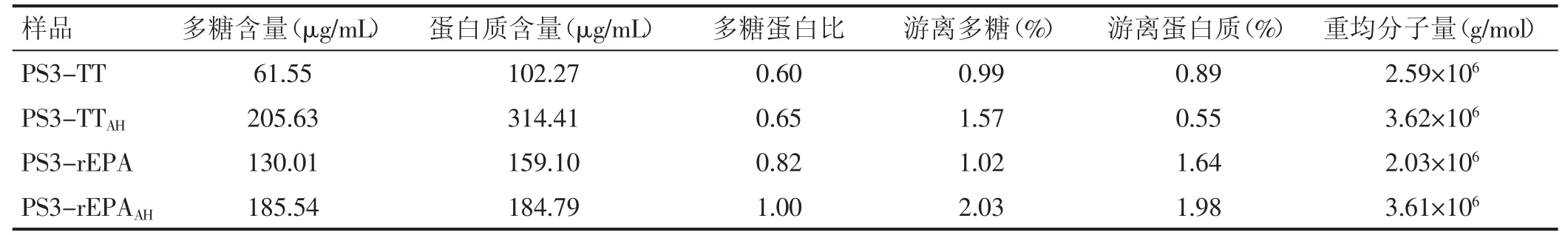
表2 结合物理化及分子量检测结果
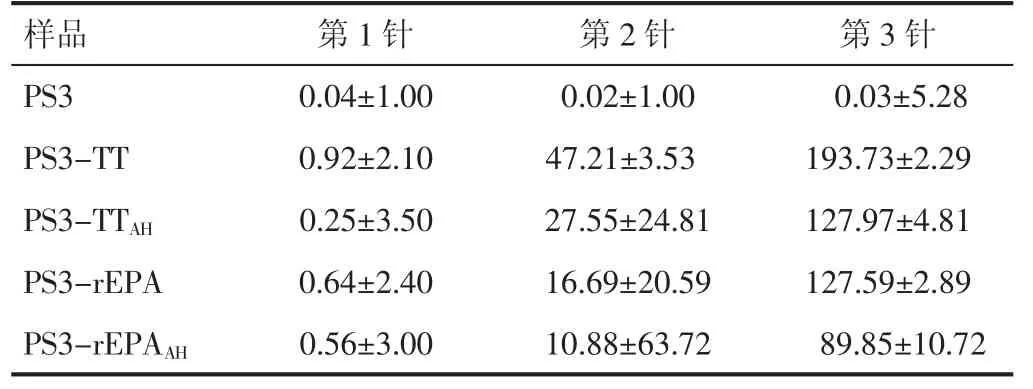
表3 3 型肺炎球菌结合物免疫小鼠后血清中特异IgG 抗体含量(EU/mL)

图4 3 型肺炎球菌结合物免疫小鼠后血清中特异IgG 抗体含量柱状图
3 讨论
目前,用于上市疫苗的载体蛋白有五种:DT、TT、CRM197、PD 及B 群脑膜炎球菌外膜蛋白(OMPC)。其中,用于肺炎结合疫苗的载体主要是DT、TT、CRM197和PD,其中辉瑞公司Prevenar13 使用的是CRM197作为载体,GSK 公司的10 价肺炎结合疫苗使用了三种载体TT、DT 及PD,其中18C 型结合物以DT 为载体,19F 型结合物以TT 为载体,其余8 个型结合物以PD为载体。
本试验尝试用肺炎结合疫苗中未使用过的一种新的载体-重组铜绿假单孢菌外毒素A(rEPA)制备2 种3 型肺炎球菌多糖蛋白质结合物。比较其与TT 为载体制备的2 种3 型肺炎球菌多糖蛋白质结合物在小鼠体内的免疫原性差异。从四种结合物小鼠免疫原性结果来看,4 种均能产生较高的抗体滴度,其中PS3-TT 产生的抗体滴度最高,PS3-TTAH及PS3-rEPA 产生的抗体滴度相当,PS3-rEPAAH产生的抗体滴度最低,但4 组结合物之间抗体浓度的差异均无统计学意义。同时,蛋白TT 和rEPA 经衍生后再结合,结合物的免疫原性有所降低。
蛋白质衍生是通过EDAC 将蛋白质的羧基端与ADH 连接从而增加蛋白质表面的氨基或肼基的数量,进而增加蛋白与多糖结合时的结合率。本试验显示,衍生后的蛋白质制备的结合物的免疫原性比未衍生的蛋白质制备的结合物的免疫原性低,可能是衍生后蛋白质的结构发生了改变,从而影响了结合物的免疫原性。从结合物的重均分子量来看,衍生后的蛋白(TTAH及rEPAAH)与3 型多糖制备的结合物的分子量均比衍生前的蛋白(TT 及rEPA)高。说明蛋白经过衍生后增加了与多糖结合的效率,使多糖与蛋白质的交联程度提高。但同时也说明并非结合物的分子量与结合物的免疫原性一定呈正相关。
肺炎球菌荚膜多糖有诸多血清型,每个血清型最适合的载体蛋白可能并不相同,本试验只针对3 型多糖,对于其他血清型最适宜的载体还需进一步研究。对于3 型肺炎球菌多糖,TT、TTAH、rEPA 及rEPAAH均是较好的载体。同时rEPA 可以作为一种新的候选载体运用于肺炎球菌多糖蛋白质结合疫苗。3 型肺炎球菌多糖与其他蛋白如CRM197、DT、PD 免疫原性的比较今后还需进一步探讨。

