冷循环射频消融治疗88例结直肠癌肝转移临床疗效
杨宏军,王晓斌,孙相华,李治纲
(1) 昆明医科大学第一附属医院干疗科,云南昆明 650032;2) 昆明医科大学基础医学院生物化学与分子生物学系,云南昆明 650500)
结直肠癌是常见的胃肠道恶性肿瘤,近年来其发病率呈逐年上升的趋势,在美国大约50%的结直肠癌患者会发生转移[1],其中肝转移是该病主要的死亡原因之一[2]。由于结直肠癌肝转移(colorectal liver metastases,CRLM) 的发生率较高,手术切除是根治肿瘤的重要手段,但不是所有的肝转移患者都适合或愿意接受手术。目前,射频消融治疗(radiofrequency ablation,RFA) 作为CRLM重要的治疗手段取得了不错的效果,本研究对88例冷循环射频消融治疗结直肠癌肝转移患者治疗效果报道如下。
1 资料与方法
1.1 临床资料
回顾性分析2012年7月至2015年10月昆明医科大学第一附属医院干疗科收治的行冷循环射频消融治疗的88例结直肠癌肝转移患者的临床资料,其中男性59例,女性29例,年龄30~90 岁。本组病例88例,共125 个病灶,其中单发病灶67例,多发病灶21例;病灶大小0.5~10.5 cm,其中<3 cm 病灶84 个,3~5 cm 病灶29 个,大于5 cm 病灶12 个;肝转移病灶多数位于肝右叶,以S5 为主。合并肝硬化25例、高血压17例、COPD12例、心功能不全8例、糖尿病7例。肝功能Child-pugh 分级为A 级76例,B 级12例,C 级0例。
1.2 方法
常规在手术前行B 超、超声造影、CT 或MRI等影像学检查,了解肝转移灶的大小、数目、位置及毗邻关系,确定布针方案及治疗策略。治疗过程中,先用彩色超声找到肿瘤,推注声诺维针行超声造影,观察病灶区域的血流分布情况及拟穿刺路径,进一步明确病灶。病人取平卧位或左侧卧位,粘贴好负极板,确定穿刺点及穿刺路径。臀部肌注盐酸哌替啶针100 mg,于拟穿刺点附近局部皮肤常规消毒铺巾,2%利多卡因针5 mL 局麻,在超声引导下将射频电极针快速穿刺进入肝脏肿瘤内部,确定位置无误,开始行冷循环射频消融治疗,治疗过程中,功率在80~200 W 之间,针尖温度控制在20℃以下,单次消融时间为12 min,烧灼针道3 min,术后患者均禁食、平卧6 h。治疗结束后常规行超声造影检查。
1.3 统计学处理
数据经SPSS 软件处理,计数资料采用χ2检验进行比较,P<0.05 为差异具有统计学意义。
2 结果
2.1 肝转移病灶消融情况
所有患者肝转移病灶总数为125 个,消融病灶119 个,单次冷循环射频消融最多病灶数为4个,消融比例为95.52%;6 个病灶由于位置特殊、定位困难、射频消融风险较大等原因未予冷循环射频消融。未消融病灶与消融病灶比较有统计学意义(P<0.05),见表1。

表1 冷循环射频消融术处理病灶统计(n)Tab.1 Statistics of lesions after Cold-circulatioRFA(n)
2.2 疗效评价
冷循环射频消融治疗后1 个月行超声造影检查,109 个病灶超声造影显示肿瘤血供完全消失,表示肿瘤完全消融毁损(见图1)。其余10 个消融病灶血供减少,但怀疑有肿瘤病灶残留,行再次冷循环射频消融治疗,部分消融病灶与完全消融病灶比较具有统计学意义(P<0.05),见表2。88例患者术后1月复查发现4例出现肝脏新发病灶,其中3例再次行射频消融毁损病灶。
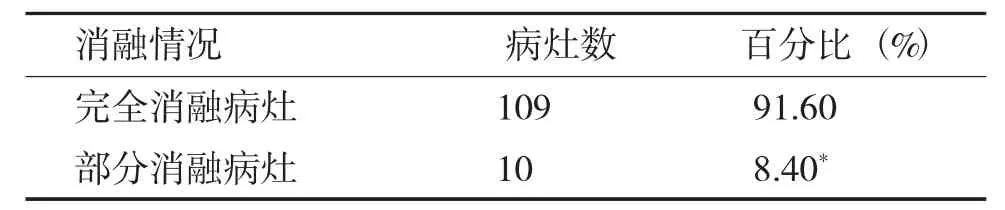
表2 冷循环射频消融术后1月疗效统计(个)Tab.2 Efficacy statistics of 1 month after Cold-circulatioRFA(piece)
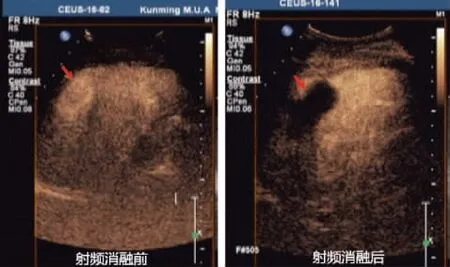
图1 结肠癌肝转移患者冷循环射频消融术前后超声表现Fig.1 The ultrasonographic manifestations in colon cancer patients with liver metastasis before and afterCold-circulatioRFA
2.3 术后并发症情况
72例患者术后出现腹部穿刺部位周围疼痛不适,疼痛的发生及程度与肿瘤位置相关,肿瘤越靠近肝包膜疼痛越明显,一般疼痛不剧烈,可耐受,必要时可行止痛处理。另外,部分病例出现不同程度的肝功能损伤、发热及胃肠道等症状。其中55例患者术后肝功能异常,经积极护肝、降酶处理后好转;13例患者术后发热患者体温一般<38℃,对症处理体温降低;2例患者术后出现恶心、呕吐等消化道症状,予止吐处理后均有改善;1例患者术后出现少量胸水,未行处理观察1 周后复查超声显示基本吸收(见表3)。患者术中未出现死亡现象,无腹腔内出血、血胸、气胸等症状,未出现邻近脏器损伤、胆漏等严重并发症。

表3 88例结直肠癌肝转移患者冷循环射频消融治疗并发症情况分析Tab.3 Ananalysis of complications ofCold-circulatioRFA in88 colorectal cancer patients with liver metastasis
2.4 患者术后随访
本治疗组88例患者,采用门诊或电话随访,部分病例因各种原因中断随访,坚持随访58例,1、2、3 a 生存率分别为100%,93.1%,76%。
3 讨论
肝脏是结直肠癌最常见的远处转移器官,结直肠癌肝转移的发生率高达50%,且20%~30%的结直肠癌患者仅有肝脏转移,故肝转移灶的治疗是决定结直肠癌患者预后的关键。据报道结直肠癌并发肝转移的患者如果未经治疗,其中位生存期仅有6.9 个月,未行手术切除的患者5 a 生存率几乎为0[3-4]。手术切除是目前治疗结直肠癌肝转移的最佳治疗方法,肝转移病灶能根治性切除患者的中位生存期能达到35 个月,5 a 存活率达30%~50%[5]。但80%的CRLM 病人初诊时肝转移灶不可切除,且术后1 a 内复发率为30%~47%[6-7]。近年来,随着多学科综合治疗协作组模式的开展,对结直肠癌肝转移病人进行全面评估,对于不能或不愿手术切除的肝转移灶,选择合适的治疗方法,如化疗、靶向治疗、放疗、介入治疗、局部消融等。目前,射频消融是应用最多、疗效最好的局部治疗方法,其不仅在原发性肝癌中的治疗地位非常重要,在转移性肝癌的治疗中效果也非常确切,局部复发率为0%~46%不等[8-9]。其中,超声引导下经皮穿刺冷循环射频消融术近年来广泛应用,在结直肠癌肝转移患者治疗中获得了很好的疗效。在本研究中,笔者采用开腹直视和超声引导下经皮穿刺冷循环射频消融术对88例结直肠癌肝转移患者的肝转移病灶进行治疗,125个肝转移病灶消融119 个,单次射频消融最多病灶数为4 个,消融比例达到95.52%;6 个病灶由于位置特殊、定位困难、射频消融风险较大等原因未予射频消融。消融病灶1月后超声造影复查,仅有10 个病灶显示有残留情况,治疗效果良好。
另外,射频消融治疗肿瘤的原理是使肝脏肿瘤组织细胞发生热凝固坏死和变性,并且封闭其中的微小血管及胆管,从而达到毁损病灶的目的。穿刺途径可分为开腹、经腔镜辅助及经皮穿刺三种。其中,超声引导下经皮穿刺冷循环射频消融治疗具有创伤小、治疗时间短、疗效确切、病人痛苦小、无严重并发症、可反复多次治疗等优点。在本研究中,所有患者术中及术后均未出现严重并发症,术后穿刺点疼痛、肝功能异常及发热等症状经过简单对症治疗后均好转。这与相关报道是一致的。同时,经射频消融治疗后,患者的生存率明显增加,Solbiati 等[10]报道了117例CRLM,经射频消融治疗后中位生存期为36 个月,1、2、3 a生存率分别为93%、69%、46%。KOS 等对比手术治疗与射频消融的结果,两者5 a 总生存率没有差异,射频组与手术组的5 a 无病生存率分别为17.6%和22%,两者差异没有统计学意义[11]。本研究中,去除无法随访的病人,剩余58例,1、2、3 a 生存率分别为100%,93.1%,76%,其生存率较上述报道的高。
总之,对结直肠癌肝转移患者,肝脏肿瘤大小和部位良好时,射频消融治疗可获得与外科切除相近的治疗效果。射频消融代表肿瘤治疗的微创化趋势,是外科切除最好的补充和替代,也可作为部分结直肠癌肝转移的治疗首选,将射频消融技术灵活应用于结直肠癌肝转移患者,大大拓宽了治疗手段的选择范畴,可以使更多的患者获益,具有较高的临床应用价值。

