KCl辅助溶液燃烧法制备高光催化活性的ZnONPs
付云芝, 李琼霞, 周美双
(海南大学理学院,海南海口 570228)
抗生素作为一种广泛使用的药物,广泛应用于水产养殖业中,其残留对环境和人体的健康影响越来越大。通常处理由抗生素残留引起污水的方法只是抑制了细菌的增殖而不能有效降解抗生素[1-3]。先进的氧化工艺(Advanced oxidation process, AOP)是去除有毒和持久性污染物最有效的技术之一[4-5],而半导体光催化技术作为AOPs中的一种新型高效的绿色技术,可以方便地将太阳能转换为化学能,为能源和环境问题提供了一种解决方案[6-7]。ZnO是典型的ⅡB-ⅢA族化合物的直接带隙宽带半导体材料,禁带宽度为3.37 eV,通常在室温下其自由激子束缚能为60 meV[8-9],它具有催化效率高、成本低和环境可持续性等优点[10-11]。ZnONPs作为半导体光催化剂具有降解普适性,降解彻底等性能,可以将很多难降解的有机物降解成CO2和H2O[12]。因此寻求高催化效率,绿色环保和操作简单的ZnONPs制备方法尤为重要。近年来关于制备ZnONPs的方法有水热合成法[13]、化学气相沉积法[14]、沉淀法[15]、溶胶凝胶法[16]和溶液燃烧法[17]等,其中溶液燃烧法以技术简单、能耗低、时间短、产率高且可商业化生产等优点成为备受关注的半导体氧化物制备方法[18]。在传统的溶液燃烧法中添加KCl可以破环颗粒的团聚性,得到高分散的CeO2纳米颗粒[19]。笔者引入KCl通过盐助溶液燃烧法制备ZnONPs,通过X射线衍射(XRD)、扫描电镜(SEM)、紫外-可见漫反射光谱(UV-Vis DRS)和傅里叶红外线变换(FTIR)等,分析硝酸锌和KCl不同物质的量比时ZnONPs的性质。
1 实 验
1.1 试剂与仪器
试剂:试剂均为分析纯。硝酸锌(Zn(NO3)2·6H2O),上海阿拉丁生化科技有限公司;葡萄糖(C6H12O6)和氯化钾(KCl),国药集团化学试剂有限公司;乙醇胺(HOCH2CH2NH2),上海麦克林生化科技有限公司;盐酸环丙沙星(CIP)和氧氟沙星(OFL),东京化学工业公司;实验用超纯水。
仪器:Nova Nano SEM 200型场发射扫描电子显微镜,美国FEI公司;D &ADVANCE型X射线衍射仪,德国布鲁克道尔顿公司;NICOLET380型傅里叶红外光谱,美国热电公司;UV-3600型紫外可见漫反射吸收光谱仪和UV-2500PC紫外可见分光光度计,日本岛津公司;PLS-SXE300氙灯,北京泊菲莱科技有限公司;HK5200超声波清洗仪,上海可导超声波仪器有限公司。
1.2 ZnONPs的制备
称取Zn(NO3)2·6H2O∶C6H12O6∶HOCH2CH2NH2=1∶2∶0.9(物质的量比,全文同)各物质溶解在50 mL水中,在磁力搅拌器下搅拌10 min,得到乳白色澄清的前驱体溶胶,将该溶胶放到加热套中加热,当温度升至120 ℃,该溶胶中的水分开始蒸发,经过浓缩、发泡、放气和爆燃等一系列过程,约30 min反应完成,得到黑色泡沫状物质,将其移至马弗炉中500 ℃煅烧2 h[20],得到白色样品记为0-ZnONPs。在上述前驱体溶胶中按照Zn(NO3)2·6H2O∶KCl=1∶0.1、1∶0.5、1∶1(物质的量比)加入KCl,通过盐助溶液燃烧法得到黑色泡沫状物质,在马弗炉中500 ℃煅烧2 h,得到白色样品,用纯水和乙醇交替洗涤样品中存在K+并离心洗涤3次,得到ZnONPs浓缩液,65 ℃下烘6 h后研磨,得到白色粉末样品,分别记为0.1-ZnONPs,样品0.5-ZnONPs,样品1-ZnONPs。
1.3 样品表征
将反应得到的ZnONPs样品研磨,以CuKα为辐射源,管电流 20 mA,管电压 36 kV,扫描范围采用广角(2θ=20° ~ 80°)的X射线衍射仪对ZnONPs晶型结构进行物相分析。将ZnONPs样品液滴滴到硅片上,放在红外灯下烤干,利用扫描电子显微镜对ZnONPs的表面形貌观察和分析。ZnONPs样品与溴化钾压片,利用傅里叶红外光谱仪进行化学分析,检测波长为440~4 000 cm-1。ZnONPs粉末利用紫外可见漫反射吸收光谱仪进行吸光度分析,波长范围为250~800 nm。
1.4 光催化反应
取质量浓度为 40 mg/L的CIP溶液15 mL作为测试的抗生素源,用来评价所合成的ZnONPs的光催化性能。采用功率为300 W的氙灯在模拟太阳光下作为唯一光源。称取5 mg的ZnONPs并加入到35 mL水中得到催化剂溶液,再将CIP溶液与其混合得到50 mL混合溶液。将混合液移置带回流的敞口石英光反应池中,暗室中搅拌0.5 h,以达到吸附-解吸平衡。然后,将其放在光源下方(反应液体距光源25 cm)进行光降解催化反应,反应过程每隔5 min取2 mL,连续取6次。经离心去除催化剂后通过紫外分光光度计测量271 nm处吸光度。
2 结果分析
2.1 XRD表征
图1为掺杂不同量KCl制备的ZnONPs的XRD图谱。从图1看出:所有样品均在{100}、{002}、{101}、{102}、{110}、{103}、{200}、{112}、{201}出现特征峰,而且峰形都尖锐表明样品的结晶性能好,与PDF标准卡号上一致,证实了是六角纤锌矿结构;加入助燃剂KCl的样品0.1-ZnONPs、 0.5-ZnONPs及1-ZnONPs的XRD特征吸收峰处的半峰宽比没加助燃剂KCl的样品0-ZnONPs大,0.1-ZnONPs、 0.5-ZnONPs及1-ZnONPs的峰强度也比0-ZnONPs的弱,说明加入助燃剂KCl后的样品颗粒变小了,这与其SEM电镜相一致(图2)。另外,XRD图谱中未观察到其他杂质的特征峰,这证实了产物是纯ZnONPs。根据主要特征峰{101}面和{100}面的半峰全宽(FWHM),使用Scherrer公式计算样品的平均晶粒粒径,结果表明,0-ZnONPs、0.1-ZnONPs、 0.5-ZnONPs和1-ZnONPs的平均粒径分别为31.58、30.07、25.53、28.23 nm,因此0.5-ZnO的平均粒径最小。
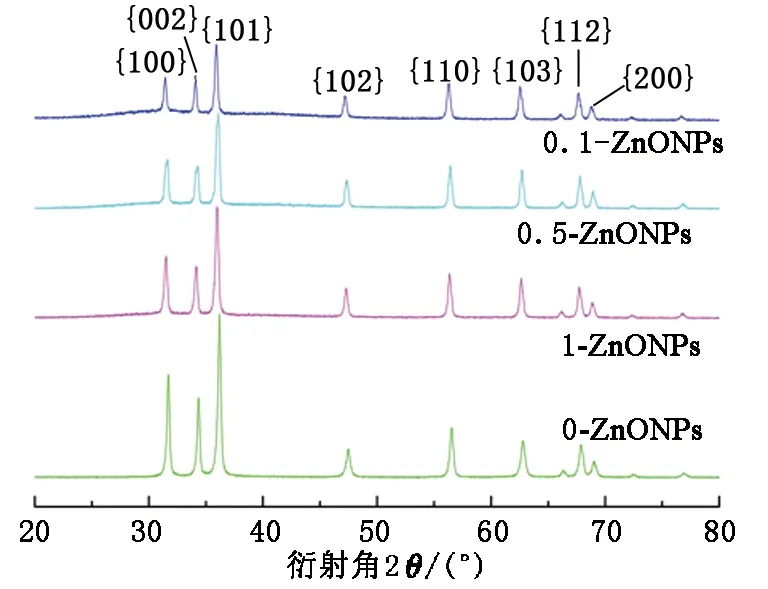
图1 掺杂不同量KCl制备的ZnONPs的XRD图谱Fig.1 XRD spectra of ZnONPs prepared by doping different amounts of KCl
2.2 SEM表征
从图2可以看出,助燃剂KCl的加入极大影响了ZnONPs的尺寸和形貌。在不加KCl的情况下,即0-ZnONPs样品是由粒径约为31.58 nm的颗粒从侧面致密粘连成大片结构的纳米片,就像颗粒的二维组装一样,这极大影响了颗粒活性位点的暴露。这是由于C6H12O6在碳化过程中形成的石墨片作为硬膜版约束了ZnONPs的运动,又由于C6H12O6单元比较小,仅仅为ZnONPs的薄层保护,在脱碳过程中,由于该薄层的脱除使得ZnONPs间粘连见图2(a)。当加入KCl时,随着其物质的量的不同,得到3种粒径的ZnONPs样品,都具有明确的六晶面结构,由图2(b)和(c)可知,当物质的量比n(Zn2+/KCl)<0.5时,提高了样品的分散性,但当n(Zn2+/KCl)>0.5时,样品开始向着团聚的方向靠拢(图2(d))。由Scherrer公式算出,加入KCl得到的样品颗粒的粒径较小,因为盐在加热时,可以加快样品的冷却速度,抑制晶体的生长,得到小颗粒样品。且n(Zn2+/KCl)=0.5时,样品颗粒粒径最小。从图2(e)给出的信息看,这个样品是有Zn和O这2个元素的组成,没有其他元素掺进来,虽然前期加了助燃剂KCl,但通过脱碳及脱碳后的洗涤,将元素K和Cl去掉,这与XRD分析一致。

图2 掺杂不同量KCl制备的ZnONPs的SEM和EDS图谱Fig.2 SEM and EDS spectra of ZnONPs prepared by doping different amounts of KCl SEM spectra
2.3 FTIR表征
图3描绘了掺杂不同量KCl制备的ZnONPs的FTIR图谱。在440~4 000 cm-1记录了所有样品的光谱。在所有的样品中,440~550 cm-1都有明显的Zn—O吸收峰,证实了ZnO的存在[21]。不加KCl时得到ZnO的吸收峰为445 cm-1,添加KCl后,氧化锌的吸收峰蓝移至501 cm-1,可能是由于原子间作用力的变化引起的[22]。3 420~3 445 cm-1和1 620~1 640 cm-1的吸收峰可以归因于—OH的拉伸和弯曲模式,可能是表面吸附水羟基[23-24]。1 370~1 380 cm-1的峰是由于—CH3的拉伸[25],2 350 cm-1观察到1个小峰,可能是燃烧过程中表面吸收了CO2[26]。说明加入KCl后,没有引起其他官能团的增加。

图3 掺杂不同量KCl制备的ZnONPs的FTIR图谱Fig.3 FTIR spectra of ZnONPs prepared by doping different amounts of KCl
2.4 UV-Vis DRS表征
利用紫外-可见漫反射光谱UV-Vis DRS研究掺杂不同量KCl下制备的ZnONPs结构的光学性质,结果见图4。
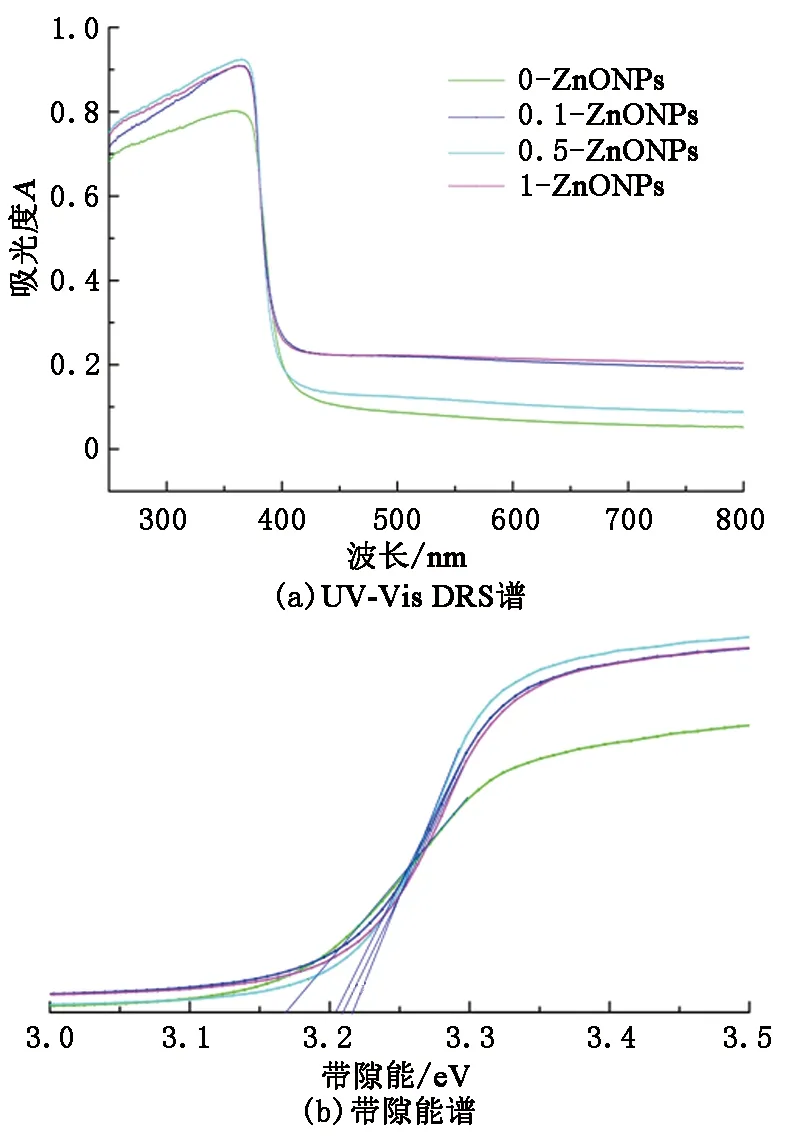
图4 掺杂不同量KCl制备的ZnONPs的UV-Vis DRSFig.4 UV-Vis DRS and band gap energy spectra of ZnONPs prepared by doping different amounts of KCl
由图4(a)看出,4个样品在365 nm处有明显的吸光度,通过加入KCl,制备的ZnONPs的在紫外区和红外区的光吸收强度明显增强,具有更加广泛的光响应区间,可以为后续的光催化过程提供更加丰富的光能,且0.5-ZnONPs粉末在紫外区光吸收强度最高。通过应用Kubelka-Munk规则进行带隙计算(图4(b)),0-ZnONPs、0.1-ZnONPs、 0.5-ZnONPs和 1-ZnONPs 粉末的带隙值分别为3.17、3.204、3.218和3.209 eV。 根据久保公式,有
(1)
式中,δ为能级间距;EF为费米能级;N为总电子数;V为颗粒体积;d为颗粒直径。该理论表明带隙δ与颗粒的体积V或者直径d的三次方成反比,粒径越小,带隙越宽。由于0.5-ZnONPs粉末的带隙为3.218,比其他3种成分带隙都大,所以其粒径最小。这与XRD及SEM测试相符。
2.5 ZnOPNs光催化性能测试
ZnONPs粉末作为高效的光催化剂降解污染物,主要是由于在能量大于或者等于禁带宽度的光照射时,光激发到纳米颗粒的表面层,纳米颗粒吸收E=hλ的能量后会产生光生e-—h+对, h+可以与催化剂ZnONPs表面结合的H2O或OH-发生反应生成羟基自由基(OH·),另一方面,e-可能被溶解氧O2捕获生成超氧自由基·O2-,该自由基对有机污染物具有强还原性,一定时间后最终氧化成二氧化碳和水。同时,产生的O2-会对e-—h+的复合过程产生阻碍,有助于量子产率的增加,进而助推光催化反应。
(2)

(3)

(4)
OH·与·O2-具有很强的反应活性,可以直接把有机污染物氧化成CO2和H2O而达到彻底矿化。
2.5.1 光催化降解实验
为评估上述不同反应条件下生成的ZnONPs材料的光催化活性,采用CIP作为模型有机污染物,在模拟太阳光的照射下进行光催化降解反应(辐照前CIP的初始浓度为c0)。得到CIP浓度c与c0比值随时间的变化,结果见图5。由图5看出:在无光催化剂的空白实验下,即使在30 min后,c/c0也没有产生明显的变化;与空白实验相比,加入ZnONPs光催化剂后,随着辐照时间的增加,c/c发生了明显的下降,说明制备得到的ZnONPs具有较好的光催化活性。而对于不同比例制备的ZnONPs对CIP的降解能力为:0.5-ZnONPs>1-ZnONPs>0.1-ZnONPs>0-ZnONPs,与紫外漫反射的表征结果一致。
当n(Zn2+/KCl)=1∶0.5时制备得到的0.5-ZnONPs降解CIP效果最好,降解率约为95.5%。
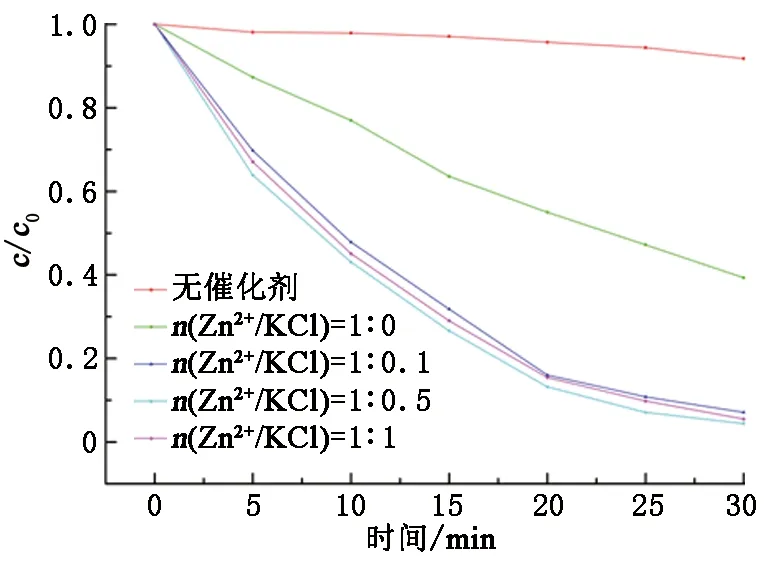
图5 不同催化剂条件下CIP的降解情况Fig.5 CIP degradation under different catalyst conditions
使用Langmuir-Hinshelwood公式(lnc/c0=kt,其中k是反应速率常数)计算了CIP光降解反应的速率常数。由图6看出,当n(Zn2+/ KCl)=1∶0.5时降解速率最高,计算得出该样品的降解速率为k=0.106 79 min-1,比n(Zn2+/KCl)=1∶0(k=0.031 2 min-1)高出3.42倍。说明加入KCl作为助溶剂时,ZnONPs的光催化活性得到了明显的提高。
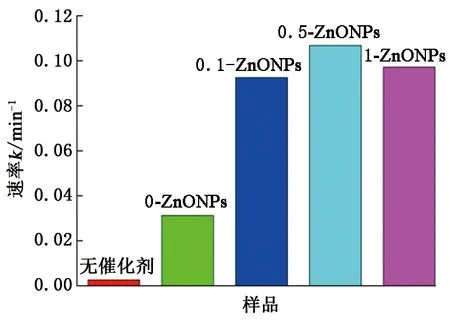
图6 不同催化剂条件下CIP的降解速率Fig.6 Degradation rate of CIP under different catalyst conditions
从其表征手段可以看出,通过加入KCl作为助溶剂进行溶液燃烧提高了合成的ZnONPs光催化活性。当添加KCl时,提高了ZnONPs的带隙值。带隙值的增加导致光激发的e-—h+的氧化还原电势升高,可能在一定程度上提高了光催化剂的催化活性。另一方面,由于催化降解发生在催化剂的表面,所以当催化剂的颗粒较小、分散性能好时e-与h+复合几率就越小,电荷分离效果就越好,可能也提高了催化剂的催化活性。所以,当n(Zn2+/KCl)=1∶0.5时为制备ZnONPs的最佳比例。
2.5.2 光催化重复性实验
实际应用中,光催化剂的稳定性是一个非常重要的因素。为评价制备的0.5-ZnONPs的稳定性,进行光降解CIP的循环实验。结果见图7。

图7 0.5-ZnO循环降解CIP实验Fig.7 Regeneration phtogradation of CIP with 0.5-ZnO as catalyst
由图7看出,经过5次循环实验后,光催化效率仅下降约6%。这说明合成纳米氧化锌催化剂的稳定性能高,且在实际应用中可以重复使用。
为了进一步说明0.5-ZnONPs光催化活性,进行氧氟沙星降解实验,结果见图8。在光催条件与光催化主体实验相同情况下,30 min内氧氟沙星降解了96.9%,这高降解率说明了0.5-ZnONPs在降解各种有机污染物方面具有很大的应用价值。

图8 0.5-ZnO降解氧氟沙星Fig.8 CIP degradation under 0.5-ZnO
3 结束语
通过KCl辅助溶液燃烧合成法制备的ZnONPs光催化活性高,对环丙沙星、氧氟沙星等有机污染物都具有较高的降解性。当Zn2+和KCl的物质的量比为1∶0.5时,光催化性能最好,且经循环实验证实了该样品的稳定性能好,可在实际应用中使用。

