山药不同炮制品丸剂物性参数及成分含量间相关性研究*
陈天朝,李 沁 , 姚 超 , 耿梦丽 , 常倩倩,于兰兰,马彦江
(1.河南中医药大学药学院, 河南 郑州 450046; 2.河南中医药大学第一附属医院药学部,河南 郑州 450000; 3.河南医药技师学院制剂工程系,河南 开封 457000;4.河南省直第三人民医院药学部,河南 郑州 450000)
山药来自薯蓣科植物薯蓣DioscoreaoppositeThunb.的干燥根茎,载于《神农本草经》,位列上品,具有补脾胃、益肺肾的作用[1]。山药的炮制有麸制和清炒制。有关麸炒的研究比较多,也有侧重于清炒炮制中的炒黄、炒焦研究[2-3]。经清炒制的山药在降血糖、调节免疫和抗衰老方面有疗效[4]。饮片的炮制好坏直接影响到制备丸剂的优劣。在前期的研究中,根据山药饮片的最优炮制工艺炮制饮片制备丸剂,研究了山药丸剂内主要成分(淀粉)及指标成分(薯蓣皂苷、尿囊素)的含量变化,结果表明,炮制前后饮片的“形”“色”“气”“味”及物理化学性质均发生变化,成分含量及物性变化可作为研究炮制的参数指标[5]。本实验着重研究炮制前后山药丸剂物性参数吸水膨胀、相对密度pH值、过氧化值及主要成分(淀粉)、指标成分(薯蓣皂苷、尿囊素)的含量,通过大、小分子研究山药炒黄、炒焦后物性变化,使传统的主观性判断可以数据化表示,为中药炮制智能化提供基础实验数据。
1 药品、试剂与仪器
山药饮片(批号1710201)购自河南中一医药经营有限公司,经河南中医药大学第一附属医院药学部王宏贤副主任药师鉴定为薯蓣科植物薯蓣DioscoreaoppositeThunb.的干燥根茎;山药炒黄、炒焦品均为山药饮片自制。薯蓣皂苷,纯度≥98%,上海叶源生物科技有限公司提供,批号P20A8F3449;尿囊素,纯度≥98%,中国食品药品检定研究所提供,批号111501-200202;甲醇(批号20170903)、无水乙醇(批号20170529)、乙醚(批号20170415),均为分析纯,烟台市双双化工有限公司产品;甲醇,色谱纯,Sigma试剂公司产品。Thermo Evolution 201紫外可见光分光光度计,美国赛默飞世尔科技公司产品;元素型18120纯水装置,上海摩勒科学仪器有限公司产品;BSA224S-CW型电子天平,德国赛多利斯公司产品;KQ5200B型机械超声波清洗仪器,上海合金超声设备有限公司产品。
2 方法与结果
2.1 山药丸剂制备
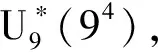
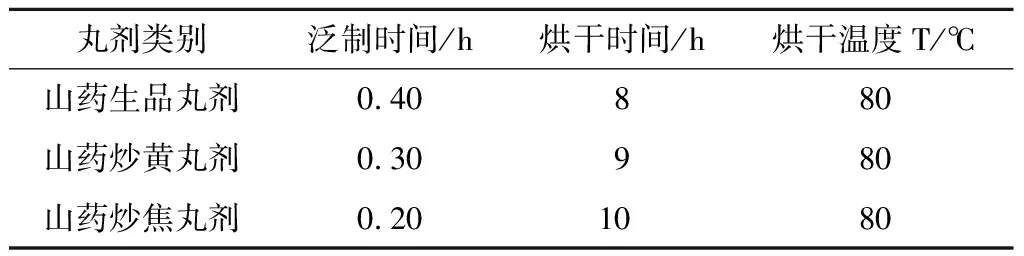
表1 山药丸剂最佳泛制工艺
2.2 山药丸剂物性参数的测定
2.2.1 膨胀度的测定
按照2015版《中国药典》四部通则2101膨胀度的测定方法[8]。
2.2.2 相对密度的测定
按照参考文献[9],精密称取1.00 g山药不同炮制品丸剂,测定山药丸剂相对密度。
2.2.3 pH值的测定
准确称取山药不同炮制品丸剂 1.00 g,加入100 mL纯化水中,室温下浸泡1 h,滤过,取滤液,测pH值,平行测定3次,取平均值。
2.2.4 过氧化值的测定
称取山药不同炮制品丸剂 7.50 g,按照参考文献[10] 测定过氧化值。
2.2.5 物性参数测定结果
见表2。结果表明,经过不同炮制,山药丸剂相对密度、pH值、过氧化值均增大。
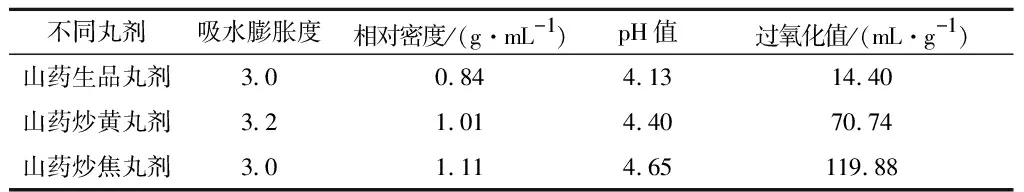
表2 山药丸剂物性参数均值n=3
2.3 主要成分的测定
山药丸剂主要成分为淀粉,采用双波长法[11]检测淀粉中支链淀粉、直链淀粉的含量。
2.3.1 直链淀粉、支链淀粉标准曲线
采用作图法,可确定直链淀粉的测定波长、参比波长分别为604 nm、468 nm,支链淀粉的测定波长、参比波长分别为537 nm、718 nm。直链淀粉、支链淀粉的标准曲线回归方程分别为Y=0.004 5X-0.008 7,r2=0.999 2;Y=0.002 8X+0.005 5,r2=0.998 8。结果表明:直链淀粉、支链淀粉分别在20~90 mg/L、80~200 mg/L范围内呈良好的线性关系。
2.3.2 主要成分测定结果
见表3。

表3 直链淀粉、支链淀粉和总淀粉含量测定结果n=3
2.4 指标成分的测定
山药丸剂的指标性成分为尿囊素和薯蓣皂苷。采用紫外-可见分光光度法测定薯蓣皂苷含量,采用高效液相色谱法测定尿囊素含量。
2.4.1 薯蓣皂苷的测定
(1)薯蓣皂苷含量测定
对照品溶液的制备:精密称取薯蓣皂苷对照品14.09 mg,置10 mL量瓶中,加甲醇溶解稀释至刻度,摇匀,精密吸取该溶液1 mL,置10 mL量瓶中,加甲醇稀释至刻度,得质量分数为0.140 9 g/L的对照品溶液。
标准曲线的制备:精密吸取对照品溶液0.2,0.4,0.6,0.8,1,1.2 mL, 60 ℃水浴加热,挥干溶剂,加入质量分数 50 g/L的香草醛冰乙酸溶液 0.2 mL和高氯酸溶液0.8 mL,于60 ℃水浴中反应 20 min,至冰水浴中冷却,取出,加冰乙酸 5 mL,摇匀,以相应的试剂为空白,按照紫外-可见分光光度法[12],在455 nm处测定吸光度。以吸光度(A)为纵坐标、对照品质量分数(0.004 7,0.009 4,0.014 1,0.018 8,0.023 5,0.028 6 g/L)为横坐标,绘制标准曲线,得标准曲线方程Y=36.689X-0.015 3(r2=0.999)。
测定法:取山药丸剂适量,粉碎,各取约1 g,精密称定,加体积分数 200 mL/L乙醇 20 mL,超声处理60 min,滤过,加体积分数200 mL/L乙醇定容于 25 mL容量瓶中,即得供试品溶液。取供试液1 mL,80 ℃水浴挥干,按“标准曲线的制备”中的方法,自“加入质量分数50 g/L的香草醛冰乙酸溶液 0.2 mL和高氯酸溶液0.8 mL”起,依法测定吸光度,根据标准曲线计算出供试品溶液中薯蓣皂苷的量,测定结果,见表4。
测定波长的选择:取山药薯蓣皂苷对照品溶液,以甲醇为对照,在 400~700 nm波长下进行扫描,455 nm 处有最大吸收,确定样品测定波长为 455 nm。
精密度试验:取山药丸剂粉末按上述方法制备5份供试品溶液,测定结果的RSD值为0.26 %。结果表明:仪器的精密度良好。
稳定性试验:取山药丸剂粉末,制备1份供试品溶液,每隔2 h测定一次吸光度值,计算RSD值为0.38%。结果表明:供试品溶液稳定性良好。
重复性试验:取同一山药丸剂粉末,平行制备6份供试品溶液,测定其吸光度并计算含量,RSD值为1.15%。结果表明:该法重复性良好。
加样回收实验:精密称取已知含量的山药丸剂粉末5份,分别加入薯蓣皂苷适量,按照供试品溶液的制备方法制成加样回收供试品溶液,测定山药总皂苷含量,计算平均回收率和RSD值。结果:平均回收率为100.12%,RSD值为2.03%。结果表明:加样回收方法良好。
2.4.2 尿囊素的测定
色谱条件:色谱柱Agilent ZORBAX SB-Aq(4.6 mm× 250 mm,5 μm ),流动相为甲醇-水(1∶99),流速0.5 mL/min,进样量10 μL,检测波长224 nm,柱温30 ℃[12]。
对照品溶液制备:精密称取尿囊素对照品10.00 mg 于25 mL量瓶中,加体积分数为 200 mL/L乙醇溶解定容,摇匀,即得。
供试品溶液制备:取山药丸剂粉末,精密称量1.00 g,加体积分数为 200 mL/L 的乙醇20 mL,超声(200 W,40 kHz)提取60 min,滤过,加体积分数为 200 mL/L乙醇定容于50 mL容量瓶中,震荡10 min,3 000 r/min 离心20 min,用0.45 μm微孔滤膜过滤即得[13]。
线性关系考察:精密吸取0.1,0.5,1,1.5,2,2.5,3,5,10 mL对照品溶液于10 mL量瓶,加200 mL/L 的乙醇定容。依次进样10 μL,按确定的色谱条件进样测定,记录色谱峰面积。以进样量为横坐标,色谱峰面积为纵坐标,进行线性回归。结果得到标准曲线Y= 9.874X+0.258,r2=0.998。结果表明:尿囊素在4~400 mg/L范围内线性关系良好。
测定方法:取上述尿素囊对照品溶液和供试品溶液各10 μL,进样测定,对照品和不同炮制品的山药丸供试品的色谱图见图1,测定结果见表4。山药经过炒黄、炒焦后制成的山药丸剂尿囊素含量减少,薯蓣皂苷含量增加。由生品到炒黄、炒焦后出现新的色谱峰。

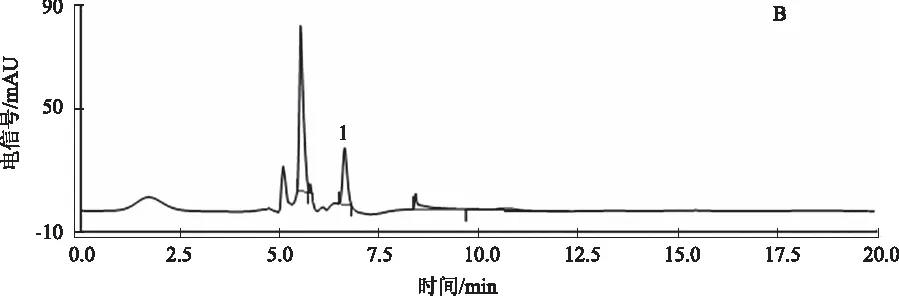
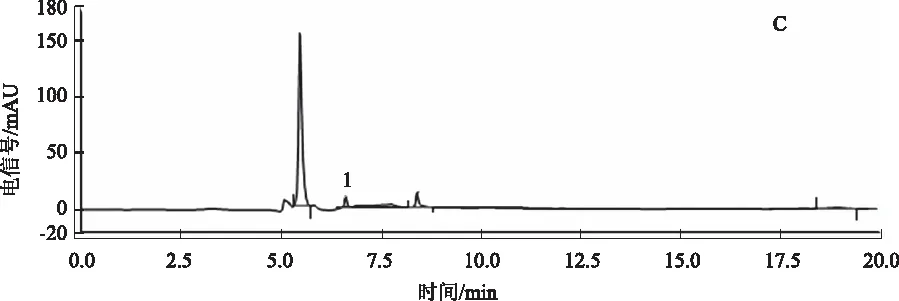

A.尿囊素对照品;B.山药生品丸剂;C.山药炒黄丸剂;D.山药炒焦丸剂;1.尿囊素图1 高效液相色谱图
表4山药丸剂中指标成分含量测定结果
精密度试验:取山药丸剂粉末,按照2.4.2项下“供试品溶液制备”中方法制备供试品溶液,连续进样6次,进行精密度考察,计算峰面积RSD值为0.94%。结果表明:仪器的精密度良好。
稳定性试验:取山药丸剂粉末,按照2.4.2项下“供试品溶液制备”中方法制备供试品溶液,按照2.4.2项下“色谱条件”,在时间点0,2,4,8,12,24 h进样,考察稳定性。结果:峰面积RSD值为0.98%。结果表明:供试品溶液稳定性良好。
重复性试验:取山药丸剂粉末 20.00 g,平行取6份,精密称定,按2.4.2项下“供试品溶液制备”中方法制备6份供试品溶液,进样,考察重复性。结果:含量RSD值为1.41%。结果表明:该方法重复性良好。
加样回收率试验:精密称取已知尿囊素含量的山药丸剂粉末0.5 g,平行取6份,分别加入200 mg/L尿囊素对照品溶液 5 mL,按2.4.2项下“供试品溶液制备”方法制备供试品溶液,计算得出尿囊素的平均加样回收率为99.17%,RSD值为1.46%。结果表明:该方法准确性良好。
2.5 相关性分析
运用统计软件SPSS 24.0进行数据分析,考察物性参数与指标成分、主要成分间相关性。结果见表5。
表5物性参数与主要成分相关性分析结果
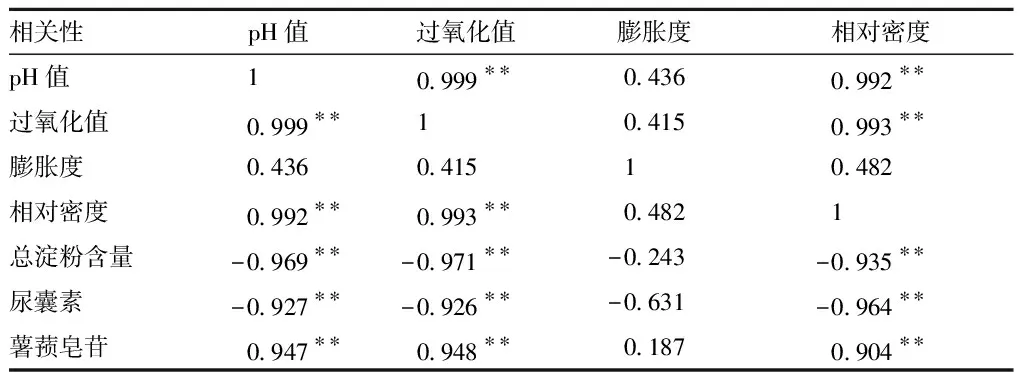
n=3
注:**P<0.01。
3 讨 论
中药炮制是根据中医药理论,依照辨证论治用药的需要和药物自身性质,以及调剂、制剂的不同要求所采取的制药技术[14]。古人已经认识到对中药饮片“制其性、形、色、味”的重要性,现如今将中药饮片炮制归结于其形、色、气、味而的改变。饮片经过炮制后可加工成不同剂型,丸剂有着便于携带、服用方便、保质期长、免煎煮等优点。丸剂的制作过程中存在着饮片物性的变化,而物性是指物质固有的物理和化学属性。对中药饮片及其炮制品,一般从形、色、气、味、质进行评价,而这些评价指标可以通过物性参数(相对密度、过氧化值、吸水膨胀度、pH值)等进行数字化度量,可通过炮制过程中小分子成分含量的变化来优选出符合中药炮制整体现的动态变化指标,利用这些指标控制中药炮制过程,使中药炮制智能化。
本实验通过测定3种山药炮制品丸剂的物性参数发现:随着炮制程度的加深,山药丸剂的相对密度、pH值、过氧化值增大,山药炒黄吸水膨胀度最大。中药饮片在炮制过程中发生美拉德反应,产生褐色成分,同时伴随pH值和过氧化值的变化。随着炮制温度的升高、炮制时间的增加,药材的质地变硬,从而导致吸水减少;随着炒制程度加深,药材粉性增加,从而吸水增加。随着炮制程度的加深,总淀粉含量减少,其中以支链淀粉减少尤为明显,说明炮制的过程加速了淀粉的分解。另外,随着炮制程度加深,尿囊素的含量减少,薯蓣皂苷含量明显增加,说明炮制也会对山药饮片中的小分子成分产生影响。图1中有新的色谱峰出现,表明炮制过程中产生了新的化合物,由此可知,炮制对山药饮片中小分子成分产生了一定的影响。
本次实验可以看出,炮制后的山药丸剂物性参数与有效成分之间具有一定的相关性,山药不同炮制品丸剂物性参数间存在差异(P<0.05)。pH值、过氧化值、相对密度与总淀粉含量均成显著负相关。物性参数和指标成分含量相关性分析表明,pH值、过氧化值、相对密度与尿囊素含量成显著负相关,与薯蓣皂苷含量成显著正相关。从饮片到炮制品再到丸剂以整体观来看,物性和炮制工艺间有着一定的传递性,炮制会改变中药物性参数和小分子成分的含量,可通过物性参数与成分含量间的相关性来更加全面科学地对中药炮制理论进行研究。
中药炮制需要现代化、智能化。山药丸剂有效成分、指标成分及物性参数三者间存在着一定的关联性,可以进一步考察丸剂有效成分的溶出实验,根据指标成分构建一定的线性回归模型,为中药饮片制丸提供一定的数据参数。如何通过物性参数指标的制定使中药炮制标准化,实现中药饮片炮制的智能化、数字化,本实验可为之奠定部分基础。

