响应面优化超声波辅助[Bmim]Cl-K2HPO4双水相提取黄秋葵多糖
何自强,张惠玲,杨正雄
(武汉生物工程学院 化学与环境工程学院,湖北 武汉 430415)
黄秋葵Abelmoschus esculentus,别名咖啡黄葵、秋葵、羊角豆、补肾菜等,为锦葵科Malvaceae秋葵属Abelmoschus1年生药食两用草本植物。目前,全世界均有黄秋葵种植[1-3]。作为一种新型的保健蔬菜,黄秋葵中富含多糖、黄酮、蛋白质、维生素、矿物质以及脂肪等多种生物活性成分,具有较高的食用及药用价值[4-5]。黄秋葵多糖具有抗疲劳[6],抗氧化[7],抗菌,抗癌[8],降血糖血脂,提高机体免疫力及具有体外结合胆酸的能力等药理作用[9]。同时,由于具有良好的增稠、乳化等性能,黄秋葵多糖已广泛用于面制品、肉制品、饮料、冰淇淋等食品的生产中[10-12]。王炜强等[13]研究表明:黄秋葵多糖是一种天然高分子絮凝剂,安全无毒,生物降解性好,在环保领域应用前景广阔。因此,黄秋葵多糖的开发已成为研究的热点。超声辅助提取可加快可溶性黄秋葵多糖的溶出,能避免高温高压破坏黄秋葵多糖的成分,且条件温和、提取时间短、提取效率高[14]。离子液体通常由无机阴离子和有机阳离子组成,室温时呈液态,离子液体不易挥发、稳定温度范围宽、化学稳定性较高、物质溶解性良好、酸性可调[15-17]。离子液体-无机盐双水相萃取技术同时结合了离子液体和双水相的优点,具有分相时间短、无乳化现象、能保持生物分子活性、回收率高等优点,是一种绿色环保的分离方法,已用于生物大分子和天然产物的萃取分离[18-20]。本研究首先采用浊点法分别绘制离子液体[Bmim]Cl与K2HPO4、Na2HPO4、Na2CO3、(NH4)2SO4等4种无机盐组成的双水相体系相图,筛选出[Bmim]Cl-K2HPO4为最佳体系;再利用[Bmim]Cl-K2HPO4双水相耦合超声波提取黄秋葵多糖,通过五因素三水平响应面Box-Behnken设计优化单因素试验,确定黄秋葵多糖的最佳提取工艺条件,以期提高黄秋葵多糖的提取率,为黄秋葵多糖的进一步开发提供试验依据。
1 材料与方法
1.1 材料与试剂
黄秋葵果:产自山东微山;葡萄糖标准品:质量分数(HPLC)≥98%,上海金穗生物科技有限公司批号20170829;1-丁基-3-甲基咪唑氯盐([Bmim]Cl):林州市科能材料科技有限公司,分析纯;三水合磷酸氢二钾:西陇科学股份有限公司,分析纯;十二水合磷酸氢二钠:西陇科学股份有限公司,分析纯;无水碳酸钠:天津博迪化工股份有限公司,分析纯;硫酸铵:国药集团化学试剂有限公司,分析纯;苯酚、浓硫酸均为分析纯。
1.2 仪器与设备
AUY120型电子天平:日本岛津公司;SK3310HP超声波清洗器(53 kHz,180 W):上海科导超声仪器有限公司;TU-1810型紫外可见分光光度计:北京普析通用仪器有限责任公司;SHZ-DⅢ循环水式真空泵:巩义市英峪予华仪器厂;RE-52AAA型旋转蒸发器:上海嘉鹏科技有限公司;TG16-WS型台式高速离心机:长沙湘智离心机仪器有限公司。
1.3 实验方法
1.3.1 标准曲线的绘制 精确称取葡萄糖标准品0.020 2 g,蒸馏水溶解后于50 mL容量瓶定容、摇匀,即得质量浓度为0.404 g·L-1的葡萄糖标准溶液。精确移取0.0、0.4、0.5、0.6、0.7、0.8 mL葡萄糖标准溶液至6支10 mL容量瓶中,依次加入蒸馏水1.0 mL和质量分数为5%苯酚(蒸馏,收集182 ℃馏分)1.0 mL,振荡摇匀后加5 mL浓硫酸,蒸馏水定容后,于92 ℃水浴中加热30 min,流水冷却,于487 nm波长处测其吸光度。用最小二乘法进行回归分析,得到一元线性回归方程:y=15.316x-0.001 9,R2=0.999 0。其中:y为吸光度,x为黄秋葵多糖质量浓度。
1.3.2 黄秋葵多糖提取率的计算 采用苯酚-硫酸法测定黄秋葵多糖质量。该法是先以葡萄糖作标准品做出标准曲线,再通过多糖的显色反应(浓硫酸可使多糖降解为葡萄糖,苯酚再与葡萄糖作用而显色)测定吸光度,然后根据一元线性回归方程和稀释倍数先计算出上相液黄秋葵多糖质量,再计算黄秋葵多糖提取率。
精确移取适量黄秋葵提取上相液于10 mL容量瓶中,其他同1.3.1,测其吸光度。黄秋葵多糖提取率=黄秋葵多糖质量/黄秋葵粉质量×100%
1.3.3 单因素试验 将黄秋葵果于60 ℃下干燥4 h后,粉碎机中粉碎,过80目筛,保存备用。准确称取0.5 g黄秋葵粉,置于50 mL碘量瓶中,加入5 mL不同质量分数的[Bmim]Cl溶液和5 mL不同质量分数的K2HPO4溶液形成的双水相体系中,将5个试验因素K2HPO4质量分数、提取时间、提取温度、液固比、[Bmim]Cl质量分数中的4个固定不变,1个作为变量,超声提取后抽滤,滤液以7 500 r·min-1转速离心10 min,于分液漏斗中分相,上相液待用。
1.3.4 响应面试验 在5个单因素试验得出的最佳条件基础上,以单因素为自变量,黄秋葵多糖提取率为响应值,设计五因素三水平响应面中心组合试验。结果见表1。
1.3.5 数据处理及分析 单因素试验数据采用2010软件处理;响应面试验数据采用Design-Expert 8.0.6.1软件处理,并对数据的显著性差异进行分析。
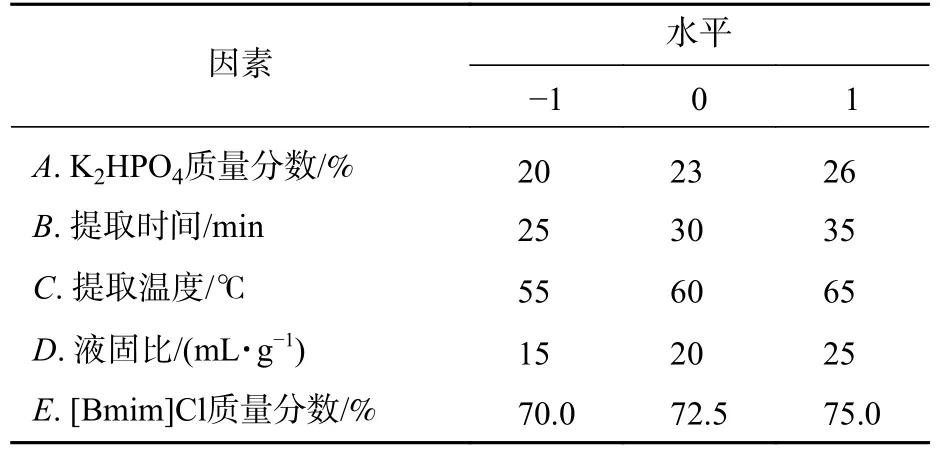
表1 Box-Behnken试验因素与水平Table 1 Factors and levels of Box-Behnken design
2 结果与讨论
2.1 最大吸收波长的确定
分别精确移取葡萄糖标准溶液0.4 mL、黄秋葵提取上相液1.0 mL于10 mL容量瓶,其他操作同1.3.1,可见光区400~800 nm光谱扫描。图1表明:葡萄糖标准溶液和黄秋葵提取上相液在487 nm处均有最大吸收,故选择检测波长为487 nm。
2.2 双水相体系的选取
2.2.1 双水相体系分相能力的考察 采用浊点滴定法绘制各双水相体系相图,考察离子液体[Bmim]Cl与K2HPO4、Na2HPO4、Na2CO3、(NH4)2SO4等4种无机盐形成双水相体系的分相能力[21-23]。室温20 ℃下,分别准确称取一定质量的无机盐于4支试管中,加蒸馏水溶解,再加入一定质量的[Bmim]Cl,直至溶液浑浊,胶头滴管逐滴滴加蒸馏水至澄清,称其质量,反复以上操作。计算每次出现浑浊时,无机盐和[Bmim]Cl的质量分数。分别以无机盐的质量分数为横坐标,[Bmim]Cl的质量分数为纵坐标,绘制相图。
图2的4条曲线均为双节线,曲线上的点为临界点,曲线下方为单相区,不分层,曲线上方为两相区。由图2可知,(NH4)2SO4和Na2HPO4的分相能力较差,仅有3个浊点,继续滴加(NH4)2SO4和Na2HPO4不再出现浑浊,不能与[Bmim]Cl形成稳定的双水相体系;Na2CO3和K2HPO4与[Bmim]Cl能形成稳定的双水相体系,但Na2CO3的溶解度受温度变化影响较大,分相范围较窄,持续时间较短,而K2HPO4分相范围广且持续时间较长。
2.2.2 双水相体系萃取能力的考察 通过相比、分配系数及提取率等物理量,考察[Bmim]Cl-无机盐双水相体系对黄秋葵提取液的萃取能力。准确称取一定质量的黄秋葵粉,分别加入到5 mL一定质量分数的4种无机盐(Na2CO3、NaHPO4、(NH4)2SO4、K2HPO4)溶液和5 mL一定质量分数的[Bmim]Cl形成的双水相体系中,60 ℃水浴中超声提取(超声功率180 W)30 min,抽滤,滤液离心后,在分液漏斗中分相。测定上相和下相中黄秋葵多糖的吸光度,计算4种双水相体系的相比(R)、分配系数(K)及提取率。
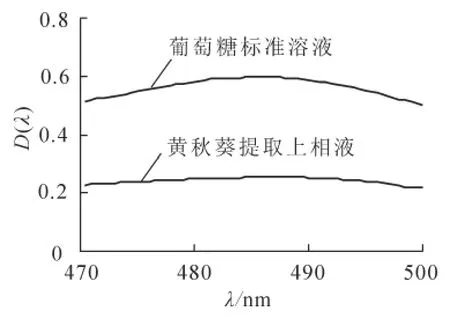
图1 最大波长的确定Figure 1 Determination of maximum wavelength
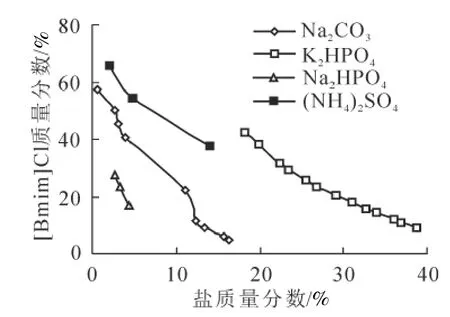
图2 双水相体系相图Figure 2 Phase diagram of two-phase aqueous system

式(1)~(2)中:Vt、Vb分别为上相、下相溶液体积(mL);Ct、Cb分别为上相、下相中黄秋葵多糖质量浓度(g·L-1)。
由表2可知:在[Bmim]Cl-(NH4)2SO4和[Bmim]Cl-Na2HPO4双水相中,提取液不分相;[Bmim]Cl-Na2CO3和[Bmim]Cl-K2HPO4中,提取液分相,但相较而言,[Bmim]Cl-K2HPO4双水相提取率较大,且黄秋葵多糖主要分布在上相。综合以上分析,[Bmim]Cl-K2HPO4双水相有较强的分相能力与萃取能力,因此,选择[Bmim]Cl-K2HPO4为本试验的双水相体系。

表2 不同[Bmim]Cl-无机盐双水相体系萃取能力的比较Table 2 Comparison of extraction ability of different [Bmim]-Clinorgnic salts in aqueous two-phase system
2.3 单因素试验结果
2.3.1 K2HPO4质量分数对黄秋葵多糖提取率的影响 称取0.5 g黄秋葵粉于50 mL碘量瓶中,在5 mL质量分数为70%的[Bmim]Cl溶液、液固比20 mL·g-1、提取温度60 ℃、提取时间30 min,5 mL K2HPO4质量分数分别为20%、21%、23%、25%、27%的条件下进行超声提取(超声功率180 W)。由图3可知:随着K2HPO4质量分数的增大,黄秋葵多糖提取率先增大后减小,质量分数23%时最大。随着盐量的增加,富集盐的下相结构性逐渐增强,容纳黄秋葵多糖的空腔形成越困难,而富集离子液体的上相结构性逐渐减弱,容纳黄秋葵多糖的空腔越易形成,黄秋葵多糖提取率不断增大;但质量分数超过23%时,产生盐效应,黄秋葵多糖提取率逐渐降低。因此,选取23%为K2HPO4适宜的质量分数。
2.3.2 提取时间对黄秋葵多糖提取率的影响
称取0.5 g黄秋葵粉于50 mL碘量瓶中,在5 mL质量分数为70%的[Bmim]Cl溶液,5 mL质量分数为23%的K2HPO4溶液,液固比20 mL·g-1,提取温度60 ℃,分别在20、30、40、50、60 min的条件下进行超声提取(超声功率180 W)。由图4可知:随提取时间增长,黄秋葵多糖提取率增大,30 min时达到最大,但30 min后提取率下降,并趋于平缓。提取时间增长,上相液黏度增大,导致黄秋葵多糖的提取越困难。因此,选取30 min为适宜的提取时间。
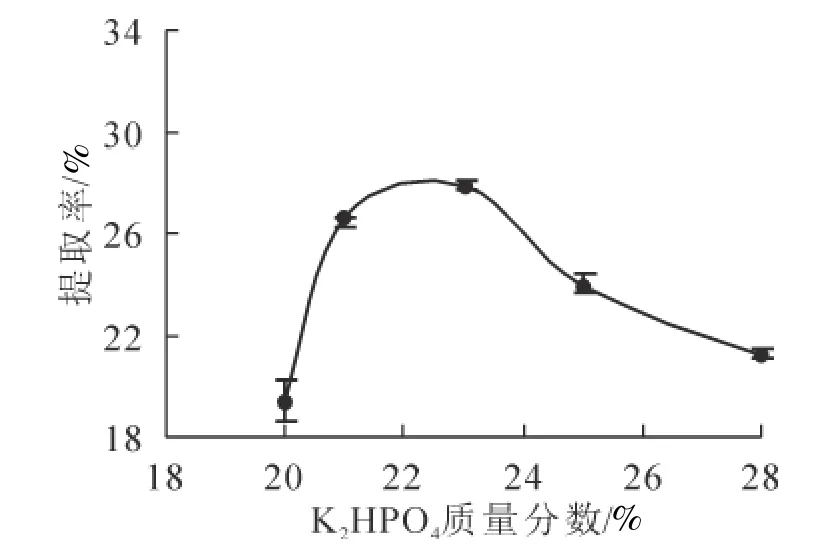
图3 K2HPO4质量分数对黄秋葵多糖提取率的影响Figure 3 Effect of K2HPO4 mass fraction on the extraction rate of okra polysaccharide
2.3.3 提取温度对黄秋葵多糖提取率的影响 称取0.5 g黄秋葵粉于50 mL碘量瓶中,在5 mL质量分数为70%的[Bmim]Cl溶液,5 mL质量分数为23%的K2HPO4溶液,液固比20 mL·g-1,提取时间30 min,提取温度分别为30、40、50、60、70 ℃的条件下进行超声提取(超声功率180 W)。由图5可知:温度升高,促进了黄秋葵多糖的溶出,提取率增大;但温度过高,杂质溶出相应增多,提取率反而下降。因此,选取60 ℃为适宜的提取温度。
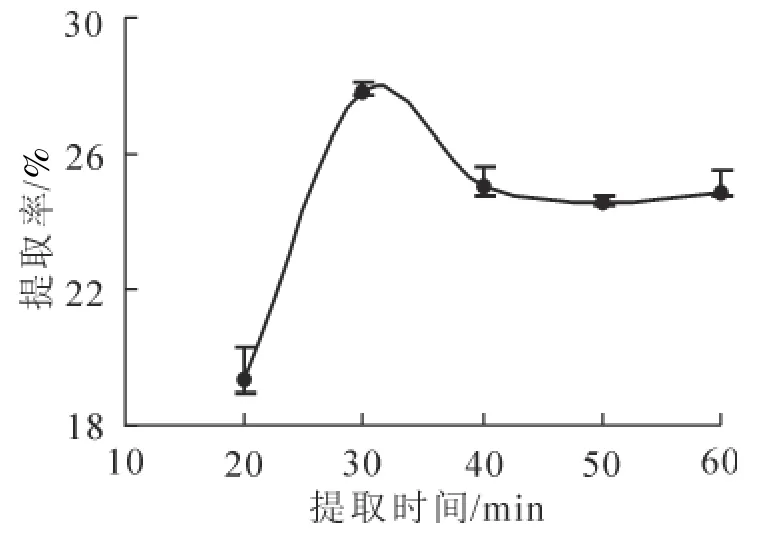
图4 提取时间对黄秋葵多糖提取率的影响Figure 4 Effect of extraction time on the extraction rate of okra polysaccharide

图5 提取温度对黄秋葵多糖提取率的影响Figure 5 Effect of extraction temperature on the extraction rate of okra polysaccharide
2.3.4 液固比对黄秋葵多糖提取率的影响 称取0.5 g黄秋葵粉于50 mL碘量瓶中,在5 mL质量分数为70%的[Bmim]Cl溶液,5 mL质量分数为23%的K2HPO4溶液,提取时间30 min,提取温度60 ℃,液固比分别为17、20、25、30、34、50 mL·g-1的条件下进行超声提取(超声功率180 W)。由图6可知:随着液固比的增大,黄秋葵粉与[Bmim]Cl-K2HPO4双水相接触面积增加,黄秋葵多糖不断溶出。液固比超过20 mL·g-1,黄秋葵多糖提取率下降,可能液固比过大,浓缩等操作时间延长,导致黄秋葵多糖损失较多,提取率下降[24]。因此,选取20 mL·g-1为适宜的液固比。
2.3.5 [Bmim]Cl质量分数对黄秋葵多糖提取率的影响 称取0.5 g黄秋葵粉于50 mL碘量瓶中,在5 mL质量分数为23%的K2HPO4溶液,提取时间30 min,提取温度60 ℃,液固比20 mL·g-1,[Bmim]Cl质量分数分别为65.0%、67.5%、70.0%、72.5%、75.0%的条件下进行超声提取(超声功率180 W)。由图7可知:随着[Bmim]Cl量的增大,黄秋葵多糖在上相的富集增多,[Bmim]Cl质量分数72.5%时最大,之后提取率下降,黄秋葵多糖在上相的富集达到饱和。因此,选取72.5%为[Bmim]Cl适宜的质量分数。
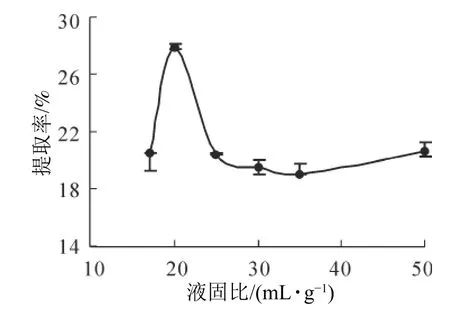
图6 液固比对黄秋葵多糖提取率的影响Figure 6 Effect of liquid-solid ratio on the extraction rate of okra polysaccharide
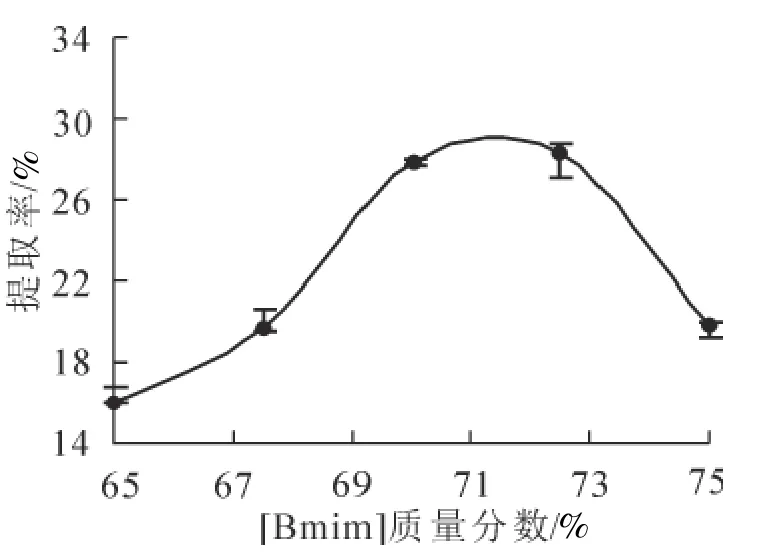
图7 [Bmim]Cl质量分数对黄秋葵多糖提取率的影响Figure 7 Effect of [Bmim]Cl mass fraction on the extraction rate of okra polysaccharide
2.4 响应面优化试验结果
五因素三水平响应面试验共46组,包括析因试验(40组)和中心试验(6组)。析因试验各不相同,6组因素水平均相同的中心试验,是重复6次以估算试验误差。
对试验数据进行回归拟合,得到各单因素与黄秋葵多糖间的二次多元方程:y=27.27-0.13A+0.17B-0.35C+2.99D-1.26E+2.62AB-0.063AC-1.14AD+0.64AE+3.29BC+2.06BD+0.95BE-3.77CD+0.98CE+0.21DE-3.68A2-5.53B2-2.75C2-3.04D2-4.85E2。
分析表3数据可知:模型P<0.000 1(差异极显著),模型对黄秋葵多糖的提取有显著影响,失拟项P=0.909 7>0.050 0(差异不显著),说明模型拟合程度较好;各单因素与黄秋葵多糖提取率之间呈良好线性关系(R2=0.974 2),模型能解释95.35%的黄秋葵多糖提取率的变化;变异系数为4.31%,数据分散程度较小,试验结果可信,因此该模型可分析和预测黄秋葵多糖的提取结果。由F值大小可推断5个单因素对黄秋葵多糖提取率显著性影响的顺序:D(液固比)>E([Bmim]Cl 质量分数)>C(提取温度)>B(提取时间)>A(K2HPO4质量分数);由P值大小可推断:一次项中,D、E对提取率影响极显著;二次项中,A、B、C、D、E对提取率影响均极显著;交互项中,AB、BC、BD、CD之间作用对提取率的影响极显著,AD、BE、CE之间作用对提取率的影响显著。图8为各因素交互作用对黄秋葵多糖提取率显著影响的响应面图。
通过回归模型可预测黄秋葵多糖提取的最佳工艺条件为:K2HPO4质量分数22.31%,提取时间29.36 min,提取温度55.69 ℃,液固比25.00 mL·g-1,离子液体[Bmim]Cl质量分数71.94%。在此条件下,黄秋葵多糖提取率可达29.12%。
2.5 验证试验
为实际操作方便,在K2HPO4质量分数22%,提取时间29 min,提取温度56 ℃,液固比25.00 mL·g-1,离子液体[Bmim]Cl质量分数72%的条件下进行验证试验。5次平行试验的黄秋葵多糖提取率为:30.28%、32.48%、30.24%、32.47%、30.64%,平均值为31.22%,相对标准偏差为3.70%。
3 结论
室温下分别绘制离子液体[Bmim]Cl与4种无机盐[(NH4)2SO4、Na2HPO4、Na2CO3和K2HPO4]形成的双水相体系相图,通过比较提取后黄秋葵多糖在各体系中的相比、分配系数和提取率,确定[Bmim]Cl-K2HPO4为本实验的双水相体系。离子液体-无机盐双水相体系对环境无污染,是一种新型绿色的分析方法。
选取5个因素:K2HPO4质量分数、提取时间、提取温度、液固比和离子液体[Bmim]Cl质量分数进行单因素试验,以单因素最佳提取条件为基础进行响应面试验,超声波辅助[Bmim]Cl-K2HPO4双水相提取黄秋葵多糖的最佳工艺可由回归模型预测。在5 mL离子液体[Bmim]Cl质量分数为71.94%,5 mL K2HPO4质量分数为22.31%的双水相体系中,提取时间为29.36 min,提取温度为55.69 ℃,液固比为25.00 mL·g-1的最佳提取条件下,黄秋葵多糖的提取率为29.12%。在该预测最佳工艺基础上进行5次验证试验,黄秋葵多糖提取率平均值为31.22%,相对标准偏差为3.70%。
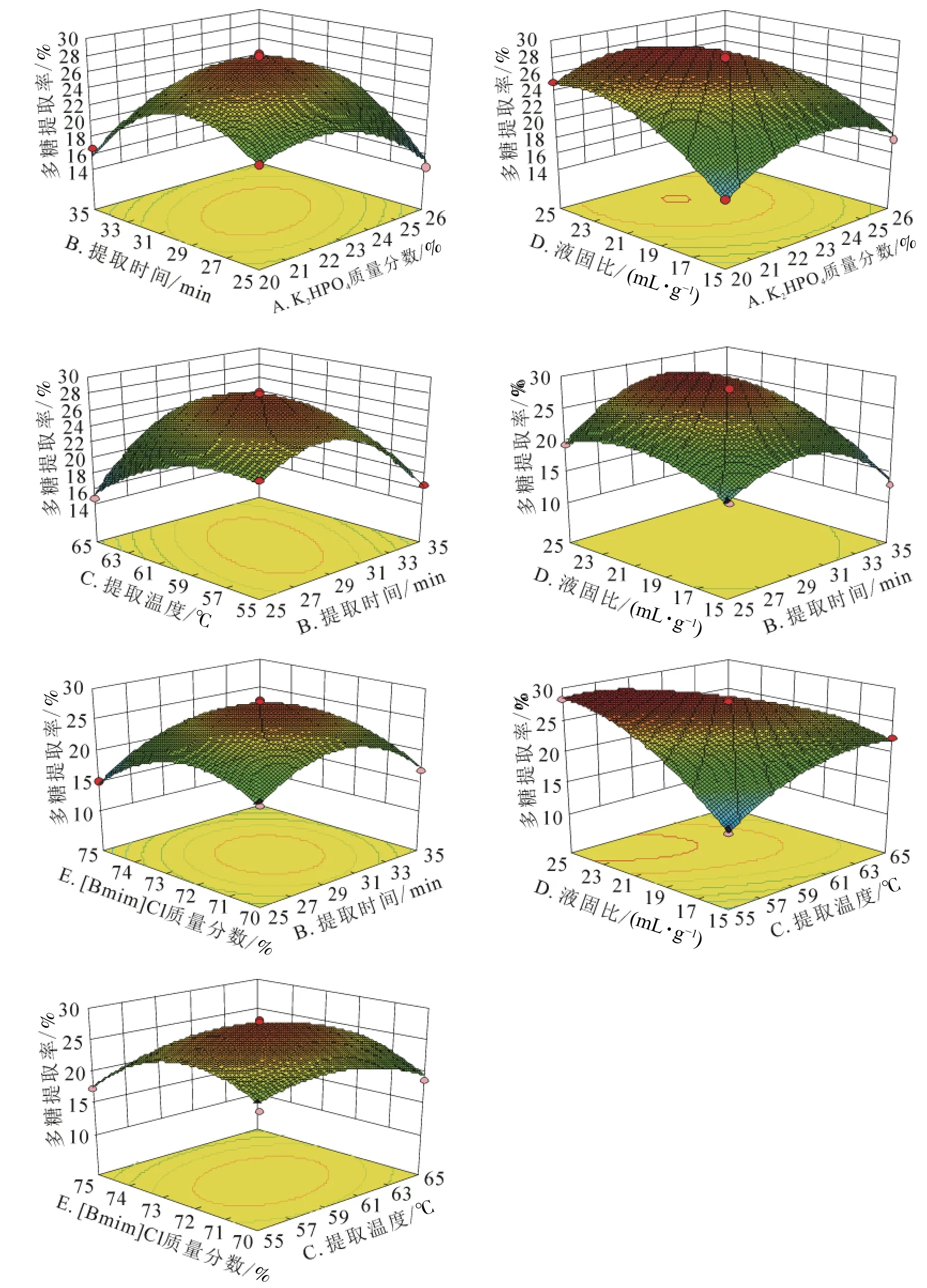
图8 各因素交互作用对黄秋葵多糖提取率交互影响的响应面图Figure 8 Response surface of the interaction of various factors on the extraction rate of polysaccharides from okra

