甲磺酸阿帕替尼联合全脑放疗治疗三阴性乳腺癌脑转移瘤的疗效及安全性分析*
阮寒光, 熊娟, 程晓华, 周学亮
1南昌市第三医院乳腺肿瘤诊治中心(江西南昌 320002); 2江西省肿瘤医院肿瘤放射治疗科(江西南昌 320029);南昌大学第一附属医院 3临床药理研究中心, 4肿瘤诊治中心(江西南昌 320015)
乳腺癌是女性常见恶性肿瘤之一,且发病率呈逐年上升趋势。乳腺癌根据其不同的分子分型其相应预后及复发转移风险亦有差别。其中三阴性乳腺癌(triple negative breast cancer, TNBC)脑转移发病率约高达20%[1-6]。乳腺癌脑转移应用全脑放疗(whole brain radiotherapy, WBRT),尤其在脑部转移病灶大于3个的情况下被认为是脑转移治疗标准,患者中位生存时间可延长4~6个月[7-10]。但由于脑部血脑屏障存在及TNBC患者无相关的靶向药物治疗,该类型患者治疗效果欠佳。采用回顾性队列研究方法对比抗血管生成小分子药物甲磺酸阿帕替尼联合全脑放疗治疗TNBC脑转移瘤与单纯放疗评价该治疗方案有效性和安全性。
1 资料与方法
1.1 一般资料 纳入标准:(1)年龄≥18岁且≤70岁;(2)PS评分≤2分;(3)原发病灶或转移病灶经过病理及免疫组化确诊为TNBC患者;(4)预计生存期≥3个月;(5)脑转移为初次确诊,且病灶≥3个;(6)脑部病灶经外科及放射治疗科医生会诊后不宜行外科切除及立体定向外科放疗(SRS)治疗;(7)除脑转移病灶外,其他病灶稳定且无内脏危象;(8)依从性好,完成既定放疗计划及至少口服药物治疗1个周期。
剔除标准:(1)原发灶为TNBC,而转移后病灶为其他分子类型;(2)因心、肺功能不全无法耐受脑部放疗;(3)未完成既定放疗计划;(4)正接受其他药物全身化疗;(5)原发性或继发性高血压病未得到有效控制;(6)既往接受过其他分子靶向治疗者;(7)多学科会诊后可行外科及SRS;(8)病历及随访资料不全者。
收集2016年10月至2018年9月南昌市第三医院具有完整病历资料及完成随访的TNBC患者46例。其中阿帕替尼联合放疗组21例,单纯放疗组25例。中位年龄48岁(25~67岁),均为女性,其中<35岁20例、≥35岁26例;未绝经24例、已绝经22例;Ki-67表达<14% 27例、≥14%19例;保乳患者5例;临床初始分期为Ⅰ+Ⅱ期25例。两组患者临床特征如年龄、月经状态、病理类型、Ki-67表达、有无家族史等逐一进行配对,差异均无统计学意义(P>0.05),见表1。

表1 两组患者临床资料的比较 例
1.2 治疗方法 研究方案:脑转移灶采用全脑大分割放疗方式。放疗过程中根据脑部病灶及水肿情况可给于甘露醇及糖皮质激素脱水对症治疗。研究主要终点设置为无进展生存期(progression free survival, PFS)。次要终点:(1)近期疗效;(2)总生存期(overal survival,OS);(3)不良反应。
治疗方案:全脑放疗DT:30 Gy/10f,1次/d,5次/周。甲磺酸阿帕替尼剂量为250 mg/次,顿服,餐后半小时,每天连续服用。如出现3~4度不良反应,积极治疗后如再不能耐受或者疾病进展则终止治疗。完成放疗后及口服甲磺酸阿帕替尼至少28 d后评价疗效。
1.3 疗效评价 采用实体瘤治疗疗效评价(RECIST1.1)标准,疗效分为临床完全缓解(complete remission,CR),局部缓解(partial remission,PR):病灶缩小≥30%,疾病稳定(stable disease,SD),疾病进展(progression of disease,PD):病灶增大≥20%。CR和PR之和比例为客观缓解率(ORR)。PFS为患者接受治疗至肿瘤出现进展的时间。OS为患者接受治疗至患者死亡或随访结束的时间。疗效评价影像检查采用MRI平扫加增强。
1.4 不良反应评价 按照《国立癌症研究所不良事件通用术语标准》(CTCAE,version 4.0),每周复查血液分析及每2周查生化评价不良反应。根据患者脑病灶不同情况给于甘露醇及糖皮质激素脱水对症治疗。观察继发性高血压及手足综合征情况,同时关注患者全身其他部位是否出现新的转移性病灶出现。不良反应按分级标准分为0、1、2、3、4级。如治疗过程中出现3、4度不良反应时口服药物剂量减少及进行积极处理并评价。
1.5 随访 采用来院复查、电话访谈及病历资料记录相结合的方式进行。
1.6 统计学方法 使用SPSS 20.0统计软件进行数据处理。两组临床一般资料组间差异采用2检验。疗效差异检查采用Pearson法进行组间检验。无疾病生存率及总生存率,以及生存曲线采用Kaplan-Meier法,组间生存差异采用Log-rank检验,P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效比较 全部患者均可进行疗效评价。如口服甲磺酸阿帕替尼能耐受疗效评价在完成放疗1个周期后进行,不能耐受则立即行疗效评价。全组患者全部完成既定计划放疗,口服药物最少为1个周期。阿帕替尼联合放疗组CR 5例(23.82%),PR 12例(57.14%),SD 2例(9.52%),PD 2例(9.52%),ORR 80.96%。单纯放疗组CR 2例(8.0%),PR 7例(28.0%),SD 9例(36.0%),PD 7例(28.0%),ORR 36.0%(2=9.558,P=0.002)。见表 2。
2.2 两组PFS与OS比较 全组患者均完成随访,全组中位PFS(mPFS)为8.7个月(95%CI:6.433~10.967个月)。中位OS(mOS)为12.7个月(95%CI:10.926~14.474个月)。阿帕替尼联合放疗组mPFS为10.6个月,单纯放疗组mPFS为7.0个月,两组PFS比较差异有统计学意义(P=0.001),见图1。阿帕替尼联合放疗组mOS为14.9个月,单纯放疗组mOS为9.0个月,两组OS比较差异有统计学意义(P=0.001),见图2。

表2 两组患者近期疗效比较 例(%)
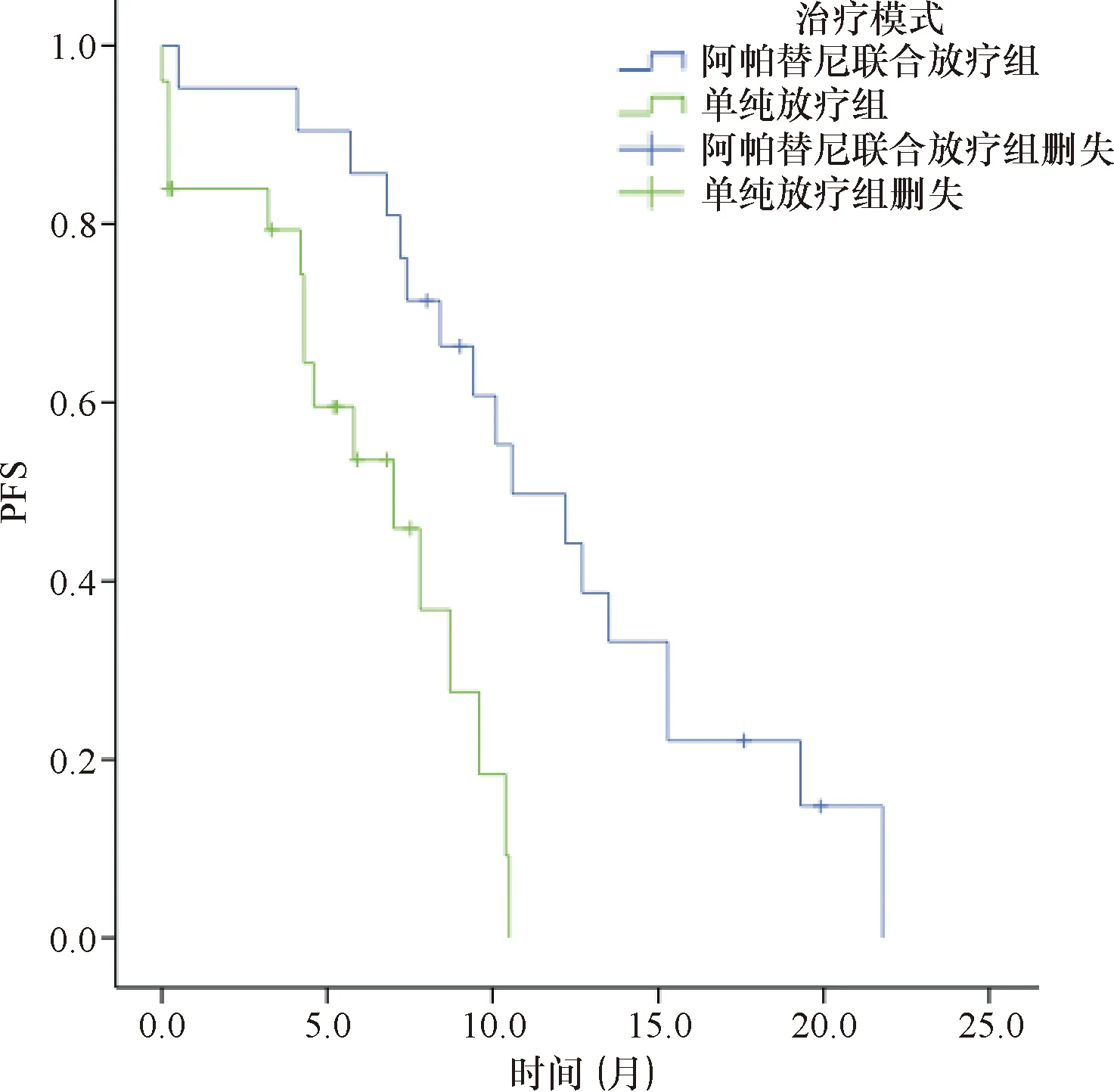
图1 两组患者PFS曲线比较

图2 两组患者OS曲线比较
2.3 不良反应比较 全组46例患者均具有完整病历资料记录,并给予不良反应及安全性评估。不良反应主要包括血液学毒性白细胞下降、血小板下降、血红蛋白下降;胃肠道反应恶心、呕吐、腹泻;继发性高血压;手足综合征、蛋白尿;疲劳等方面进行评估。阿帕替尼联合放疗组出现3~4级血液毒性为2例,单纯放疗组为3例,两组差异无统计学意义(P>0.05)。在胃肠道反应方面两组差异亦无统计学意义(P>0.05)。阿帕替尼联合放疗组出现不同程度的继发性高血压为19例,发生率为90.48%。单纯放疗组出现继发性高血压为3例,发生率为12.0%,且程度均为1~2级。两组间差异有统计学意义(2=28.266,P=0.000)。阿帕替尼联合放疗组均出现不同程度手足综合征,3~4级为4例,其中1例因为严重手足综合征停止服用。单纯放疗组无患者出现手足综合征。阿帕替尼联合放疗组出现1~2级疲劳11例,发生率为52.38%,单纯放疗组仅发生3例,发生率为12.0%,两组差异有统计学意义(2=8.819,P=0.012),见表3。
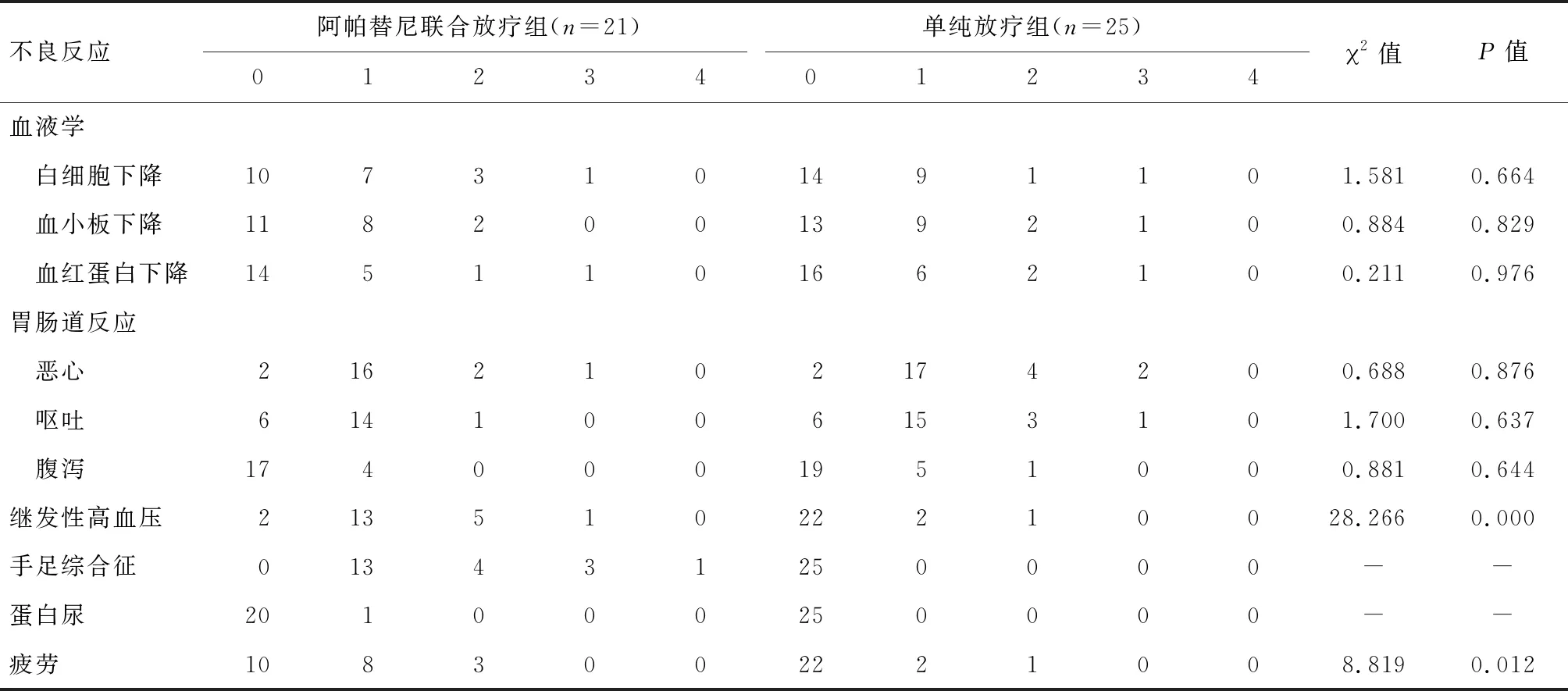
表3 两组患者不良反应比较 例
3 讨论
乳腺癌是女性恶性肿瘤之一,且发病率具有逐年上升的趋势。根据雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体(HER-2)表达状态可分成LuminalA、LuminalB、HER-2过表达及TNBC分子类型[1-3,10-15]。TNBC是一类生物学特性和临床预后较其他分子分型不同且很特殊的亚群。在发病率上,TNBC约占乳腺癌的15%~20%。TNBC类型乳腺癌生物学特性表现为具有高度侵袭性,临床出现内脏转移概率及风险均高于骨转移[16-19]。
TNBC类型乳腺癌脑转移患者通常在内脏转移后出现,恶性程度高。由于血脑屏障存在,细胞毒性化疗药物很难透过血脑屏障达到脑病灶组织。目前临床上尚无针对该类型乳腺癌分子靶向药物,所以脑部放疗成为了该类型患者有效治疗手段。脑转移瘤治疗可根据脑转移瘤位置及数量通常可采用外科手术,SRS及WBRT治疗方式。WBRT作为乳腺癌多发性脑转移瘤的标准治疗。有报道显示乳腺癌WBRT后患者中位生存期提高4~6个月[2-3,20-21]。乳腺癌脑转移后单纯实用WBRT治疗手段后中位生存期达到了11个月[22]。本研究纳入46例TNBC脑转移患者,mOS 12.7个月,mPFS达到了8.7个月,单纯放疗组为9.0个月。本研究报道TNBC类型患者单纯放疗组生存时间较相关文献报道乳腺癌脑转移后经WBRT治疗后时间稍短,可能因素为TNBC分子亚型患者肿瘤恶性程度及预后差于其他分子类型所致。但联合治疗组中位生存期明显高于该文献报道的结果。
甲磺酸阿帕替尼是一种酪氨酸激酶抑制剂,针对血管内皮生长因子受体-2(VEGFR-2)作用的小分子靶向药物。其是我国自主研发并具有自身知识产权新一类口服分子靶向药物。已被CFDA批准在中国上市运用于二线治疗失败后晚期胃癌患者。药物用于晚期胃癌的有效性及安全性已得到证实,明显延长了PFS及OS。TNBC作为乳腺癌特殊分子类型,激素受体及人表皮生长因子受体表达均阴性,内分泌及抗HER-2药物在该类型患者治疗中缺乏有效性。甲磺酸阿帕替尼作为新一代抗肿瘤血管生存药物,具有分子量小,口服易吸收及不良反应轻等优点[23]。Hu等[24]报道一项口服甲磺酸阿帕替尼治疗转移性性TNBC研究,ORR达10.7%,临床获益率为25%。刘凯等[25]在晚期乳腺癌研究中ORR为40.0%,DCR为75.0%,mPFS为12个月。本研究显示阿帕替尼联合放疗组mOS为14.9个月,相比单纯放疗组差异有统计学意义(P=0.001)。PFS阿帕替尼联合放疗组同样显示较单纯放疗组明显延长,mPFS分别为10.6个月与7.0个月,两组差异有统计学意义(P=0.001)。本研究在近期疗效方面,阿帕替尼联合放疗组ORR为80.96%,单纯放疗组ORR为36.0%,两组差异有统计学意义(2=9.558,P=0.002)。
在不良反应方面,全组46例患者观察的不良反应包括血液学毒性、胃肠道反应、继发性高血压、手足综合征、蛋白尿及疲劳等急性不良反应。Hu等[24]报道发生3度以上继发性高血压及手足综合征的发生率分别为20.5%与10.3%。Li等[26]报道不良反应主要以继发性高血压、手足综合征为主。很少发生3度以上的血液学毒性。本研究口服甲磺酸阿帕替尼出现3~4级血液毒性为2例,单纯放疗组为3例,两组差异无统计学意义(P>0.05)。阿帕替尼联合放疗组出现不同程度的继发性高血压为19例,发生率为90.48%。单纯放疗组出现继发性高血压为3例,发生率为12.0%,且程度均为1~2级。两组间差异有统计学意义(2=28.266,P=0.000),该数据明显高于上述文献报道数据。阿帕替尼联合放疗组出现不同程度手足综合征,3~4级为4例,其中1例因为严重手足综合征停止服用。本研究阿帕替尼联合放疗组不良反应较文献报道均较明显,导致的原因可能为本研究纳入人群为TNBC脑转移病例,多数患者为其他内脏转移后出现的进展,治疗耐受力较差所致。
综上所述,口服甲磺酸阿帕替尼联合WBRT提高了TNBC患者治疗疗效,延长了PFS及OS。但口服药物不良反应发生率亦较高。甲磺酸阿帕替尼作为小分子抗血管生成药物在TNBC脑转移患者中的疗效值得进一步期待。由于本研究系小样本回顾性研究,研究结果难免存在偏倚。期待多中心,大样本的Ⅲ期临床试验结果。

