试亚铁灵指示剂用量对CODCr滴定终点影响的研究
赵昌平
苏州国环环境检测有限公司,中国·江苏 苏州 215000
试亚铁灵;CODCr ;邻菲啰啉;线性相关
1 引言
在文明高度发达的今天,人类生产生活为世界带了日新月异的变化。工业文明之后,大量的工业设施崛起,由于技术的弊端和对最大剩余价值的追求,导致了巨大的环境污染。如今,在贯彻科学发展观中,建设环境友好型社会的大前提下,中国对环保方面的重视程度相当高。工业排放的废水在“三废”中占了很大的比重,也对中国的水体质量造成了巨大的威胁。化学需氧量(CODCr)作为反映还原性污染物的指标,能够有效定量的表征水质的受污染程度,为下一步的治理提供理论依据。
对于化学需氧量的测定,中国乃至国际现行最为经典方法仍是GB/T 11914—1989[1]和HJ 828-2017[2]《水质 化学需氧量的测定 重铬酸盐法》。归纳起来说,便是采用过量重铬酸钾为氧化剂氧化水中的还原性污染物质后,用硫酸亚铁铵作为还原剂滴定测量剩余的氧化剂,归一化为氧当量来定量反映水中还原性污染物质的方法。此方法虽然存在含铬、汞等重金属酸废液环境污染隐患的缺点,但由于测定精度和准确度高等优点,得以继续广泛使用。除了高温及强酸性条件下重铬酸钾能够氧化大部分污染物之外,试亚铁灵指示剂(1,10-菲啰啉指示剂)十分灵敏及显著的红褐色终点变化也是CODCr值高精度与准确度的重要保证。
论文通过改变试亚铁灵指示剂的用量,从外观结合CODCr数值的角度来尝试探究了不同指示剂用量对滴定终点的影响规律。
2 实验部分
2.1 实验试剂
(1)硫酸汞(分析纯,国药集团化学试剂有限公司)
(2)含银硫酸溶液
在500 mL 浓硫酸(分析纯,昆山金城试剂有限公司)中加入5 g 硫酸银(分析纯,国药集团化学试剂有限公司),静置3-5 天,待硫酸银完全溶解后使用。使用前摇动混匀。
(3)重铬酸钾标准溶液(c(1/6K2Cr2O7)=0.250 mol/L)
将重铬酸钾(优级纯,国药集团化学试剂有限公司)在105 °C 下干燥2h,于干燥器中冷却后,称取12.2580 g,溶解于去离子水中,转移至1000 mL 容量瓶中,用去离子水定容至刻度线,摇匀。
(4)硫酸亚铁铵滴定溶液(c((NH4)2Fe(SO4)2·6H2O)≈0.10 mol/L)
称取约41.5 g 六水合硫酸亚铁铵(分析纯,国药集团化学试剂有限公司),置于烧杯中,加入去离子水溶解后,缓慢加入20 mL 浓硫酸,待溶液冷却后,加入去离子水至1000 mL。溶液准确浓度每次使用时现标。
(5) CODCr标准溶液(CODCr=200 mg/L)
将邻苯二甲酸氢钾(优级纯,国药集团化学试剂有限公司)在105 °C 下干燥2h,于干燥器中冷却后,称取0.1700 g,溶解于去离子水中,转移至1000 mL 容量瓶中,定容并摇匀(c(HOOCC6H4COOK)=0.8330 mmol/L)。溶液的理论CODCr值为200 mg/L。
(6)试亚铁灵指示剂
将0.6950 g FeSO4·7H2O(分析纯,国药集团化学试剂有限公司)溶于50mL 水中,加入1.4740 g 一水合邻菲啰啉(分析纯,天津市科密欧化学试剂有限公司),搅拌溶解后,转移至100 mL 容量瓶中,加水定容至刻度线后摇匀,装入滴瓶中。
2.2 实验设备
(1)消解及回流装置
COD 标准消解仪(HCA-102 型);冷凝回流管。
(2)其他器材
250 mL 锥型玻璃瓶;50 mL 聚四氟乙烯滴定管;10 mL及20mL 胖肚移液管;10 mL 移液管;100 mL 容量瓶。
2.3 实验方法
2.3.1 消解过程
准确吸取20.0 mL CODCr标准溶液(1.1.5)和10.0 mL重铬酸钾标准溶液(1.1.3)于250 mL 锥形瓶中,加入0.4 g硫酸汞(1.1.1);套于冷凝回流管下,置于标准COD 消解器上,向回流管中加入30.0 mL 含银硫酸溶液(1.1.2),混合均匀后,加热,使瓶中溶液沸腾2 h;冷却至50 °C 以下,向瓶中加入90 mL 去离子水后,取下锥形瓶,摇晃均匀,并继续冷却至室温。取10 份CODCr标准溶液进行消解处理。
同时用20.0 mL 去离子水代替CODCr标准溶液,同样按照上述步骤测定2 份空白平行样品。
2.3.2 滴定过程
CODCr标样:将10 份CODCr标准样品分为5 组,每2 个为1 组平行样品,分别向其中加入1 滴(1 d),3 滴(3 d),10滴(10 d),20滴(20 d),50滴(50 d)试亚铁灵指示剂(1.1.6),用硫酸亚铁铵溶液滴定至终点,记录硫酸亚铁铵溶液消耗量VndmL。
空白样:向2 份空白样品中加入3 滴(3 d)试亚铁灵指示剂,滴定至终点,记录硫酸亚铁铵消耗量为V0mL。
硫酸亚铁铵溶液浓度标定:准确吸取10.0 mL 重铬酸钾标准溶液(1.1.3)至250 mL 锥型瓶中,加入90 mL 去离子水和30 mL 浓硫酸,冷却后,用用硫酸亚铁铵溶液滴定至终点,记录其消耗量V mL,通过计算((2)式)得出CODCr值(mg/L)。

3 结果与讨论
3.1 消解与滴定过程中色彩的变化原理
3.1.1 消解过程
采用氧化还原滴定法测定CODCr,滴定过程从外观上最为显著的便是色彩的变化。
pH 值在2-9 之间时,水中的还原性无机物或是有机物,在消解过程中被重铬酸钾氧化,这部分重铬酸根离子被还原为3 价铬离子,3 价铬离子在此条件下显翠绿色,因存在剩余的呈橙黄色的重铬酸根离子,因此整体色彩介于橙色与绿色之间((3)式),具体由还原性物质的耗氧量决定。
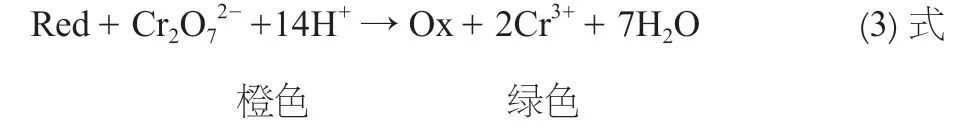
3.1.2 滴定过程
滴定所用的硫酸亚铁铵溶液中存在游离的Fe2+、NH4+、SO42-、H+等离子。滴定过程中,样品中剩余的重铬酸根离子被滴入的亚铁离子还原为3 价铬离子,如(4)式所示。因此,随着硫酸亚铁铵的滴定量增加,样品溶液的色彩由偏橙色逐渐向绿色。
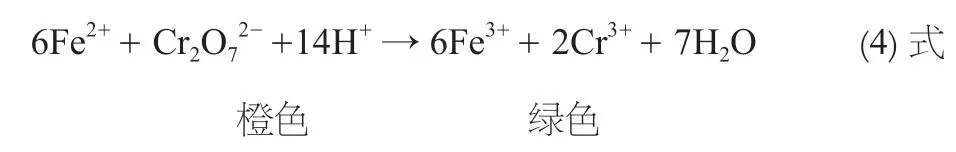
当样品溶液中的重铬酸根离子完全被还原为3 价铬离子时,肉眼上观察,溶液呈翠绿色。由于亚铁离子呈淡绿色,外观上完全被翠绿色3 价铬离子里所覆盖,因此如果此时继续滴加过量的硫酸亚铁铵溶液,从色彩上观察并没有显著变化。如是操作,便会超过滴定终点,使结果与真实值产生偏差。
为了精准确定硫酸亚铁铵的滴定量,在滴定初始时加入试亚铁灵指示剂滴定终点时会出现溶液由翠绿色向红褐色,差异十分显著的色彩变化[3]。
3.1.3 试亚铁灵指示剂
试亚铁灵指示剂是一种配位化合物,化学成分为硫酸三邻菲啰啉合亚铁(II),呈深血红色,其显色基团主要为三邻菲啰啉合亚铁(II)离子,论文中简写为(FeII(phen)3)2+[4]。指示剂配置过程中,亚铁离子以6 配位的形式与3 分子邻菲啰啉(phen)中的6 个N 配位,形成血红色的配合络离子(FeII(phen)3)2+,此反应十分灵敏,色彩变化十分显著,因此,邻菲啰啉也经常被用作于检测Fe2+,和在分析过程中保护和掩蔽Fe2+。
3.2 试亚铁灵指示剂对滴定终点外观的影响
当加入标准的3d 指示剂后,滴定过程中的色彩变化随着硫酸亚铁铵滴加量的增加应当是由橙色到翠绿,再由翠绿瞬变为红褐色,此色彩与指示剂本身相近[5]。
3.2.1 不同指示剂用量滴定终点色彩对比
通过改变试亚铁灵指示剂的滴加量依次为1d,3d,10d,20d,50d,对比了滴定终点色彩的差异,如图(1)所示。
1d:接近滴定终点并未呈现显著的色彩变化,只是翠绿色稍暗,无法准确判断滴定终点。
3d:指示剂加入量为标准值时,滴定终点为显著的红褐色,能够准确判断。
10d:增加指示剂量到10 滴时,接近终点时,翠绿色较3d 时更深,到达终点时,呈血红色,能够判断。
30d:继续增加指示剂的量,到达终点时,色彩较加入量10d 时,更深,呈暗血红色,能够判断。
50d:将滴加量增加到50d 时,在溶液变为翠绿色后,继续滴加硫酸亚铁铵,溶液由绿色变为深蓝色(如图1(a)),继续滴加硫酸亚铁铵数毫升后,溶液由蓝色变为黑褐色(图1(b))。此时滴定终点处色彩变化复杂,滴定终点有待考查。

图1 (a) 不同指示剂用量CODCr 标液滴定终点的色彩对比;(b) 加入50 滴指示剂后,滴定终点的色彩变化
3.2.2 不同指示剂用量滴定终点色彩差异的探讨
加入指示剂为1d 时,(FeII(phen)3)2+浓度较低,红褐色被稀释,终点显色不充分,因此不易判断。
加入量为标准的3d 时,适当提高了(FeII(phen)3)2+浓度,此时终点显色显著,同时溶液透明度较高,此滴加量应为能够正常显色的最少滴加量。
继续增加指示剂量到10d,20d 时,由于(FeII(phen)3)2+浓度的显著增加,使得溶液的透明度降低,终点色彩逐渐由血红色变为暗红色,这时判断溶液的终点变得不易。
当指示剂量增加到50d 时,(FeII(phen)3)2+浓度较高,因此滴定过程中产生的氧化型(FeIII(phen)3)3+的浓度也十分高,此基团显蓝色,其色彩覆盖了Cr3+的翠绿色,十分显著。当指示剂加入量较少时,氧化型(FeIII(phen)3)3+依然存在,但其浓度较低,色彩较淡,被Cr3+的颜色所覆盖,因此之前的变色过程中并未存在此现象。而(FeII(phen)3)2+的色彩强于(FeIII(phen)3)3+,因此当(FeII(phen)3)2+的黑褐色应是其滴定终点,如(5)式所示。

总的来说,不同指示剂滴加量呈现的终点色彩差异是由(FeII(phen)3)2+浓度差异造成的。随着滴加量的增加,(FeII(phen)3)2+浓度提高,溶液色彩变深。当滴加量为50d 时,溶液中出现蓝色,为(FeIII(phen)3)3+颜色,继续滴加至黑褐色,应为滴定终点。
3.3 试亚铁灵指示剂用量与CODCr 值关系的探讨
对试亚铁灵指示剂的滴加量依次为1d,3d,10d,20d,50d 的CODCr真实值为200 mg/L 的10 个标准样品进行了其CODCr实际值的测定,并研究了指示剂用量对CODCr值的影响。
3.3.1 不同指示剂用量时CODCr测定实际值
10 个标准样品的CODCr测定值如表1所示。

表1 不同试亚铁灵指示剂滴加量标准样品的CODCr 实际测定值
从表1观察可知,当亚铁灵指示剂滴加量为标准的3d 时,CODCr实际测定值为200 mg/L,与真实值相同。当加入的指示剂为10d 时,测定值为204 mg/L,偏离真实值+4 mg/L。继续增大指示剂的用量,CODCr实际测定值继续增大,当滴加量为50d 时,偏离值达到+29 mg/L。总的来看,随着指示剂用量的增加,CODCr实际测定的增加值不断增大。
3.3.2 指示剂增加量与CODCr实际测定的增加值的关系
GB/T 11914—1989[1]明确规定了试亚铁灵的指示剂的加入量为3 滴,通过上述实验验证3 滴指示剂的加入量不仅能得到准确的CODCr数值,同时也节省了指示剂的用量,达到较为明显的重点变化。
将3d 指示剂作为试亚铁灵指示剂增加量的零点,其余的增加量(d)分别为7,17,47,作为横坐标;以不同指示剂用量的CODCr实际测定的增加值,0,4,9,29 为纵坐标,绘制散点图。观察发现大致存在线性相关性,因而对4 个散点进行了线性拟合处理,结果如图2所示。

图2 指示剂增加的滴数与CODCr 值增加量的关系图
线性回归方程为y=0.6206x-0.5149,相关系数r=0.9985,线性相关性较好,即在0-47d 指示剂增加量的范围内,指示剂增加滴数与CODCr增加量成正比:
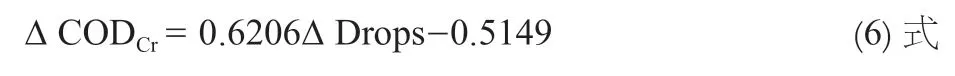
4 结语
论文通过改变亚铁灵指示剂的滴加量,研究了其对滴定终点外观及COD 测定值的影响。随着指示剂滴加量的增加,(FeII(phen)3)2+浓度升高,滴定终点逐渐由红褐色向暗黑色转变。同时,随着指示剂滴加量的增加,CODCr实际测定值与标准值的偏差逐渐变大;在0-47d 指示剂增加量范围内,指示剂增加滴数与CODCr较标准值的增加量成线性关系,为:Δ CODCr= 0.6206Δ Drops-0.5149。

