优化术前肠道准备方案对根治性膀胱全切加回肠通道术患者的影响
刘颖,黎丹,黄燕波,王倩,贯华
(北京大学第一医院 泌尿外科,北京100034)
根治性膀胱全切加回肠通道术是指患者全膀胱切除后,以回肠流出道的方式行不可控尿流改道,该手术方式是目前治疗膀胱癌的主要术式之一[1]。 根治性膀胱全切加回肠通道术涉及肠道重建, 传统的术前肠道准备包括饮食管理、 口服泻药、 清洁灌肠等,以减少术后并发症[2-3]。 然而膀胱癌患者多为老年人,身体虚弱而难以耐受传统的术前肠道准备,易出现不良反应,且术后胃肠道功能恢复较慢。最新的加速康复外科(enhanced recovery after surgery,ERAS)证据指出术前肠道准备并非必须[4-6]。 目前不同国家、不同地区对于根治性膀胱全切加回肠通道术患者的肠道准备做法各异[7-9]。 因此本研究旨在探讨优化的术前肠道准备方案对根治性膀胱全切加回肠通道术患者的影响,为泌尿外科加速康复护理提供参考。
1 对象与方法
1.1 研究对象 本研究为前瞻性对照研究,采用方便抽样法选择2018 年1 月—2019 年4 月在北京某三级甲等医院泌尿外科的膀胱癌患者为研究对象。纳入标准:(1)年龄≥18 岁;(2)经膀胱镜检及病理检查确诊为膀胱恶性肿瘤患者, 其他辅助检查显示无周围浸润及远处转移病灶;(3)择期行全麻下根治性膀胱全切加回肠通道术;(4)知情同意,自愿参与本研究。排除标准:(1)存在其他严重基础疾病,消化道功能障碍,免疫抑制剂使用者;(2)术前1 周使用过抗菌药;(3) 术前1 个月内接受过放疗或化疗;(4)精神或意识障碍;(5)接台手术。 (6)已参加其他临床研究。 本研究通过医院伦理委员会批准(2018R000033),患者均签署知情同意书。 使用随机数字软件生成编码,随机分组编码用不透光信封密封保存。纳入研究对象时开启对号入组,偶数者进入观察组,奇数者进入对照组。最终纳入100 例患者,观察组和对照组各50 例。2 组患者一般资料比较差异无统计学意义,见表1。

表1 2 组根治性膀胱全切加回肠通道术患者基本资料比较
1.2 研究方法
1.2.1 围术期管理 由同一组医护人员按照腹腔镜下根治性膀胱癌切除临床路径对2 组患者进行围术期管理。 2 组患者均在全麻下行腹腔镜根治性膀胱全切加回肠通道术,均为当日首台手术。 参与手术医生不知晓患者的随机分组情况,按照腹腔镜根治性膀胱全切加回肠通道术手术指南实施手术。 术后,患者麻醉复苏后回病室。 由同一组护士进行术后护理。
1.2.2 肠道准备
1.2.2.1 对照组干预方法 采用传统的术前肠道准备方法。 (1)饮食管理:术前3 d 3 餐进食半流质,术前2 d 3 餐进食全流质无渣饮食, 术前1 d 3 餐禁食;(2)口服泻药。 术前1 d 用3 000 mL 温水冲服复方聚乙二醇电解质散(和爽)3 袋, 要求患者于3 h内分次喝完;(3)清洁灌肠。 术前晚20:00 及术日晨6:00,由责任护士用3 000 mL 生理盐水进行大量不保留灌肠,清洁标准为肠道排出物清澈呈水样。
1.2.2.2 观察组干预方法 参考《根治性膀胱切除及尿流改道术加速康复外科专家共识》[3],优化术前肠道准备方法。 (1)饮食管理:术前1 d 3 餐进食全流质无渣饮食,术前晚上22:00 至次日手术前禁食禁饮;(2)无需口服泻药;(3)灌肠:于术日晨6:00,由责任护士进行生理盐水灌肠1 次,清洁标准为无成形粪便。
1.2.3 评价方法 由1 名研究人员独立完成评价指标的收集,其不知晓随机分组情况。 评价指标包括:(1)肠道准备后不适发生率:参考相关文献[7-9],课题组自行设计问卷, 评估患者肠道准备后常见的5种不适症状,包括饥饿感、肛门不适(如肛门胀痛感、坠胀感)、腹痛、腹胀、恶心。 经5 人专家小组评定,问卷内容效度为0.900, 本研究中问卷的Cronbach α 为0.834。于术前1 h 由患者亲自填写或回答。(2)术后并发症发生率。 观察并记录2 组患者术后常见并发症发生率,包括肠梗阻、吻合口瘘、伤口裂开、腹腔感染、伤口感染、尿路感染和菌血症,以医生诊断为准[3]。(3)术后康复情况。 记录2 组患者术后首次排气、排便时间。 上述评价指标情况均由研究人员记入病例报告表, 由课题负责人定期核查数据的完整性和准确性。
1.2.4 统计学处理 所有数据采用SPSS 25.0 进行整理和分析。 计数资料用例数、百分比进行描述;计量资料中正态分布的资料用均数、标准差进行描述,组间比较采用独立样本t 检验、卡方检验。 检验水准α=0.05。
2 结果
2.1 2 组根治性膀胱全切加回肠通道术患者肠道准备后不适发生率比较 除饥饿外, 观察组在肛门不适、腹痛、腹胀、恶心等不适发生率均低于对照组,差异有统计学意义(P<0.05),见表2。
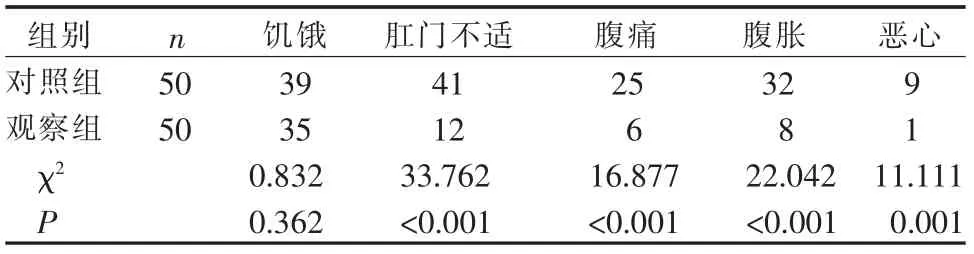
表2 2 组根治性膀胱全切加回肠通道术患者肠道准备后不适发生率比较(例)
2.2 2 组根治性膀胱全切加回肠通道术患者术后并发症情况比较 2 组患者均未发生吻合口瘘、 伤口裂开、腹腔感染和菌血症,均无患者死亡。 2 组患者术后肠梗阻、伤口感染、尿路感染的发生率比较差异无统计学意义(P>0.05),见表3。
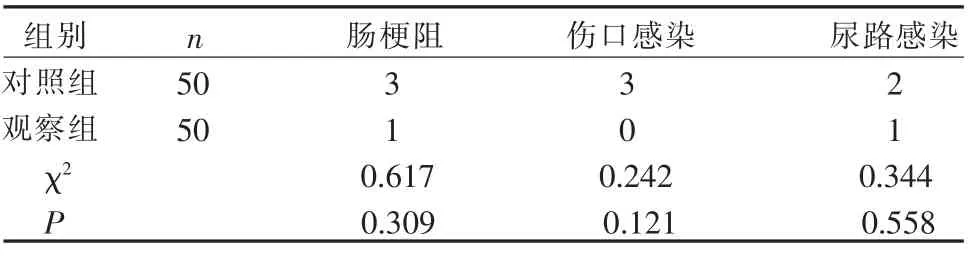
表3 2 组根治性膀胱全切加回肠通道术患者术后并发症发生情况比较(例)
2.3 2 组根治性膀胱全切加回肠通道术患者术后康复情况比较 2 组患者术后首次排气、 排便时间比较差异有统计学意义(P<0.05),见表4。
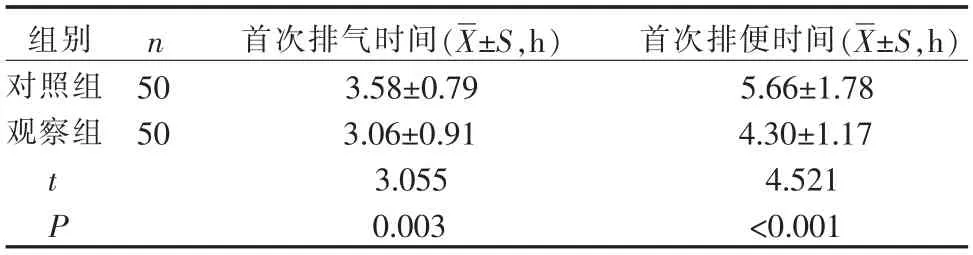
表4 2 组根治性膀胱全切加回肠通道术患者术后康复情况比较
3 讨论
3.1 优化术前肠道准备有助于减少根治性膀胱全切加回肠通道术患者不适 本研究结果显示, 观察组患者肛门不适、腹痛、腹胀、恶心等不适的发生率显著低于对照组(P<0.05),说明优化的肠道准备方式有助于减少患者不适。 传统机械性肠道准备易在短期内引起患者不适, 其中反复灌肠可造成明显的肛门胀痛感或坠胀感, 口服泻药常引起患者恶心呕吐、腹痛腹胀、电解质紊乱等[10]。 而膀胱癌患者大多为老年人,基础身体状况相对较差,且膀胱括约肌松弛,对肠道刺激的耐受性差。目前关于膀胱癌手术患者肠道准备的临床研究数量有限[6,11-12],国内外尚无统一标准。 国内泌尿外科普遍参考胃肠外科传统的术前管理方式,即严格执行多次机械灌肠;术前3 d逐步由少渣、无渣饮食,过渡到术前1 d 禁食,从而达到彻底清洁肠道,避免手术感染的目的。 近年来,在加速康复外科理念指导下, 国内外胃肠外科术前肠道管理方式逐渐革新, 而泌尿外科大多仍沿用传统方式[9-10];在根治性膀胱切除及尿流改道术加速康复外科专家共识中,针对术前肠道准备的方式,也未给出明确的证据等级及相关指导意见[3]。 本研究广泛查阅文献,结合临床实际,对术前肠道准备方案进行优化改良,缩短了饮食管理时间,取消了口服泻药,并将灌肠次数减少至1 次, 有效降低了患者的术前不适。 2 组患者饥饿感比较差异无统计学意义(P>0.05),分析原因,可能与2 组的饮食管理方案有关。 虽然观察组将术前饮食管理的时间由传统的3 d 缩短至1 d,但2 组术前禁食禁饮时间均超过8 h,因而患者都有较强的饥饿感。我国加速康复外科专家共识(2018 版)[13],术前禁食禁饮时间为术前2~8 h,且可以口服清流质,以减少患者术前不适。 在今后围术期饮食管理中,可进一步尝试对现有术前禁食禁饮方式进行优化。
3.2 优化术前肠道准备有助于提高根治性膀胱全切加回肠通道术患者康复效果 本研究结果显示,观察组患者术后尿路感染、伤口感染、肠梗阻的发生率与对照组比较差异无统计学意义(P>0.05),2 组均未发生严重并发症,该结果与既往的研究结果一致[8],提示传统的肠道准备方式在降低患者术后并发症方面并无优势。 根治性膀胱全切加回肠通道术后早期常见并发症(包括发热、不全性肠梗阻和切口相关并发症等)发生率约为38%[14-15]。 理论上传统的肠道准备可以减少肠腔细菌,降低术后并发症,但该方法过度刺激肠道,易造成肠黏膜结构改变,引起菌群移位和失调[16],并造成肠道营养吸收障碍,增加术后感染风险。多项前瞻性随机对照研究已证实术前常规行肠道准备并未降低结直肠手术感染并发症的发生率[17-18]。 就根治性膀胱全切加回肠通道术而言,主要使用回肠进行尿道重建,而回肠黏膜内的细菌菌落总数远远低于直肠和结肠[12]。 术前严格的肠道准备反而会成为应激因素,降低患者手术耐受性,导致术后并发症。 就早期康复效果来看,本研究结果显示,观察组患者术后首次排气、排便时间方面显著早于对照组(P<0.05)。
3.3 研究局限性 本研究的评价指标中未涉及患者术后远期康复情况, 在今后的研究中可进一步跟踪患者,对其远期康复情况进行评估。此外本研究样本数量有限, 仅在单中心进行, 今后还可扩大样本量,开展多中心的研究。

