MnMoO4纳米棒制备工艺的探究及其电化学性能
张利锋, 神克超, 蒋永韬, 宋一飞, 刘 毅, 郭守武
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
0 引言
钼酸锰(MnMoO4)作为一类过渡金属钼酸盐是一种重要的无机功能材料.由于钼、锰资源丰富,价格低廉,以及独特的双过渡金属活性位,MnMoO4在光致发光、变色、磁性等领域应用广泛[1-3].近年来,MnMoO4微纳米结构的制备发展迅速,在催化、储能等方面倍受关注.Srirapu等[4]采用微波辅助共沉淀法制备了MnMoO4纳米粒子,在催化析氧反应方面表现出独特的性能.Kumar等[5]通过水热法制备了微米级MnMoO4块体材料,与石墨烯杂化之后可以有效的光降解甲基蓝.Lee等[6]则通过共沉淀结合煅烧及固相法分别制备了MnMoO4纳米线和纳米粒子,在锂-氧电池上表现出优异的电催化性能.
此外,MnMoO4微纳米材料与CoMoO4、NiCo2O4、石墨烯等组成异质结构或杂化物在超级电容器上也表现出较强的应用潜力[7-9].2001年,Kim等[10]将固相法制备的MnMoO4块首次用于锂离子电池负极材料,证明了其较好的储锂活性,但是充放电仅循环了25次.之后,研究者们陆续采用共沉淀、水热等方法制备了微米级MnMoO4棒[11]、中空MnMoO4微米球[12]等,研究了锂离子在MnMoO4材料中的嵌入和脱出行为,提高了MnMoO4的电化学性能,对MnMoO4在电化学储能上的应用具有十分重要的意义.
在MnMoO4微纳米材料的制备中,水热法相对于其他制备方法能耗适中,晶粒发育较好,粒径分布较窄,避免了固相法中易出现的杂质及结构缺陷[13,14].但是,水热过程中各种工艺参数对产物结构及形貌影响较大.晶粒在形成和生长过程中由于奥氏熟化的作用,经常团聚成大颗粒甚至是大块,不利于MnMoO4微纳米结构的调控,严重影响其光/电催化、电化学储能等性能的发挥.因此,有必要对水热制备MnMoO4微纳米材料的制备工艺进行比较详细地探索.
本文通过对原料配比、水热时间和温度、煅烧温度等工艺参数进行较为详细地探索,制备了直径大约为80 nm的MnMoO4纳米棒,并采用XRD以及SEM对所制备产品的晶体结构及形貌进行了表征.同时考察了制备的MnMoO4纳米棒作为锂离子负极材料的电化学性能,测试结果表明,MnMoO4纳米棒与Li+离子反应活性较高,但是其容量在前期衰减较快.
1 实验部分
1.1 原料与仪器
所用药品及试剂:二水钼酸钠、四水乙酸锰均为分析纯.
所用仪器:HZK-FA210电子天平,SHZ-D循环水式真空泵,DHG-9030A电热干燥箱,DF-101S集热式恒温加热磁力搅拌器,MSK-ES200涂覆机,SKGL-1200-60开启式管式炉.
1.2 MnMoO4的制备
将等摩尔的二水钼酸钠和四水乙酸锰分散到70 mL的水溶液中,搅拌10 min后移入不锈钢水热釜中,140 ℃下反应5 h,制得的样品经过抽滤、洗涤后60 ℃下干燥12 h,最后在500 ℃、氩气气氛下煅烧4 h.
1.3 测试与表征
采用X-射线衍射仪(XRD,D/Max-2200,日本理学)对MnMoO4样品进行晶体结构分析,测试条件为Cu靶Kα线,管电压为40 kV,2θ范围为10 °~70 °,步宽0.2 °;使用SEM(S- 4800,日本日立)观察MnMoO4样品的微观形貌.将制备的MnMoO4样品组装成CR2032型扣式电池,电解液是1 M的碳酸亚乙酯和碳酸二甲酯(体积比1∶1)的LiPF6溶液,隔膜是Celgard 2500.采用恒流充放电仪(CT-3008,深圳新威)进行恒电流充放电测试和倍率性能测试.测试的电压区间是0.01~3 V.并使用电化学工作站(CHI660E,上海辰华)测试其循环伏安(CV)曲线.
2 结果与讨论
2.1 原料配比的影响
图1是不同原料配比在140 ℃下反应5 h水热产物的XRD图.从图1可以看出,三种水热产物均是含一个结晶水的MnMoO4,对应JCPDS标准卡片号为39-0084.
图2为不同原料配比水热产物的SEM图.如图2(a)所示,Mo∶Mn=1∶1时,产物主要呈现出交叉的晶须状形貌,组成晶须的细棒直径大约为100~150 nm(图2(b)).图2(c)、(d)是Mo∶Mn=1∶2时产物的SEM图,从图中可以看出,产物仍有形成晶须的趋势,但是结块程度比较严重,并且晶粒生长的有序度降低.说明增加乙酸锰的原料配比不利于晶粒的均匀生长.同样,增加钼酸钠原料配比的水热产物也发生了比较严重的团聚现象(图2(e)、(f)),虽然在两端可以看出其晶须状形貌,但是细棒之间的团聚使其接近于块状材料.因此,Mo∶Mn=1∶1有利于后期MnMoO4纳米棒的形成.
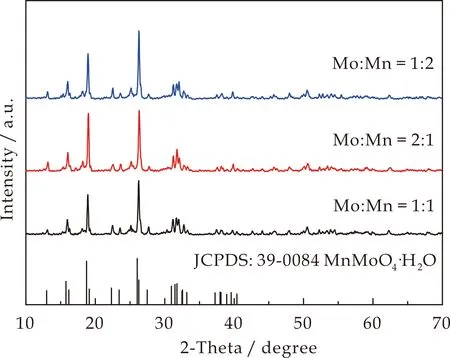
图1 不同配比水热产物的XRD图



(a)、(b)Mo∶Mn=1∶1 (c)、(d)Mo∶Mn=1∶2 (e)、 (f)Mo∶Mn=2∶1图2 不同配比水热产物的SEM图
2.2 水热时间和温度的影响
图3是不同时间和温度水热产物的XRD图.从图3可以看出,调节水热时间和温度不影响产品物相.四种水热产物仍是含一个结晶水的MnMoO4,对应JCPDS标准卡片号为39-0084.
图4为不同时间和温度水热产物的SEM图.如图4(a)所示,缩短水热时间为3 h,产品表面出现大量毛刺状晶体,并伴有不规则的纳米粒子.延长水热时间至7 h(图4(b)),产品团聚形成块状材料,仅在两端可以看到纳米细棒的残留.由此可见,水热时间过短或过长均不利于纳米棒的形成.图4(c)、(d)分别是120 ℃和160 ℃下水热5 h产品的SEM图.在较低的反应温度下,棒状形貌并未出现,形成长度大约为3μm,厚度约为2μm的块状晶体.在较高的反应温度下,同样没有纳米棒,产品晶体不断熔合,形成微米级的大块,且其表面比较光滑.因此,水热5 h和140 ℃是优化的反应时间和温度.
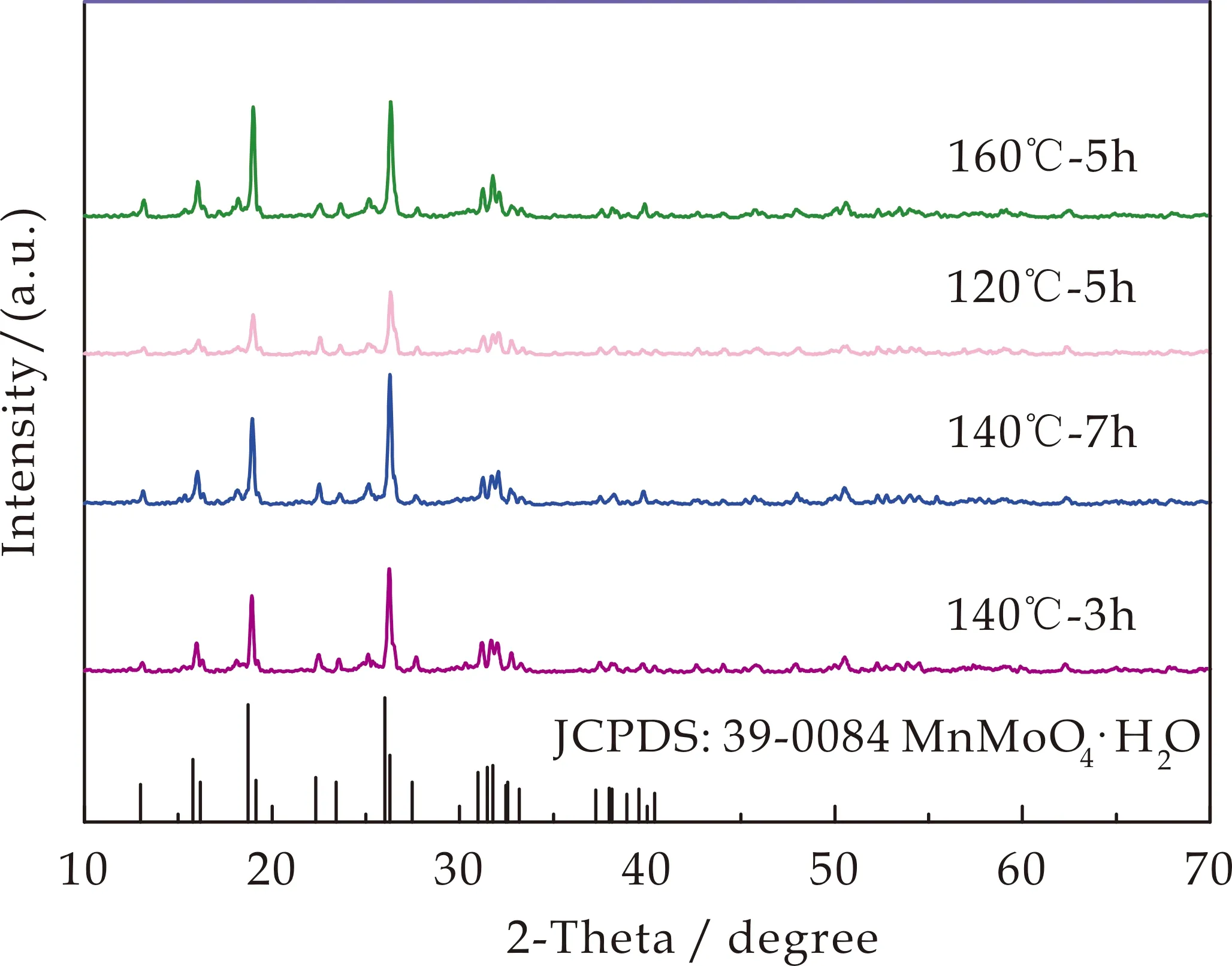
图3 不同时间和温度水热产物的XRD图


(a)140 ℃、3 h (b)140 ℃、7 h (c)120 ℃、5 h (d)160 ℃、5 h图4 不同时间和温度水热产物的SEM图
2.3 煅烧温度的影响
水热生成的MnMoO4晶须由细棒自组装形成,细棒的分散程度不高,且产物带有一分子的结晶水.为进一步提高MnMoO4的结晶性,将水热产物在氩气气氛下煅烧4 h.图5是不同温度煅烧产物的SEM图和XRD图.从图5(a)可见,400 ℃产物由纳米棒和纳米颗粒共同组成,两者相互依附,表明在煅烧过程中经历了熔化再结晶的过程.因此,在此温度下产物的形貌属于过渡状态,并没有转变完全.将煅烧温度提高到500 ℃之后,其再结晶过程转变完全.
从图5(b)可以清晰地看出产物分散良好,形成的MnMoO4纳米棒直径为70 ±20 nm.继续提高煅烧温度到600 ℃时,温度过高导致纳米棒熔融成无规则块体材料(图5(c)).图5(d)是三组样品的XRD图,三条衍射曲线基本一致,2θ在22.8 °和25.8 °有两个显著的衍射峰,对应单斜晶体结构的MnMoO4的(021)和(220)晶面, JCPDS标准卡片号为27-1280.在其它的衍射角范围内并未出现明显的杂峰,说明煅烧之后,水热产物中的结晶水已完全除去.
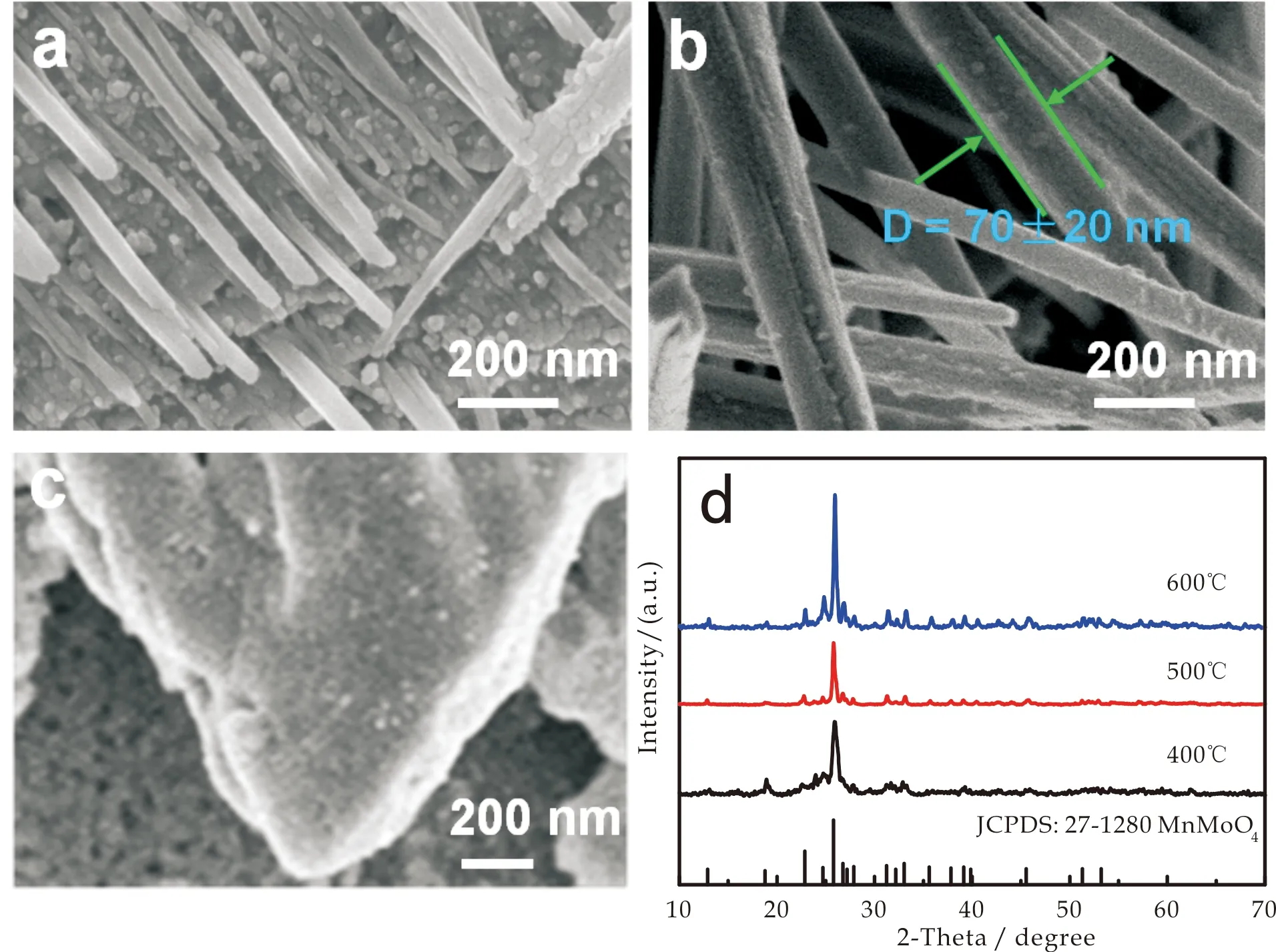
(a)400 ℃时SEM图 (b)500 ℃时SEM图 (c)600 ℃时SEM图 (d)XRD图图5 不同温度煅烧产物的SEM图及XRD图
2.4 MnMoO4的电化学性能
将制备的MnMoO4纳米棒作为活性物质组装为CR2032型扣式电池进行测试.图6为MnMoO4电极的循环伏安曲线(CV),扫描速率为0.1 mV·S-1,电压区间为0.01~3.0 V.从图6可见,MnMoO4电极放电过程中在0.27 V和0.1 V左右出现还原峰,分别对应Mo6+到Mo0和Mn2+到Mn0.充电过程中在1.5 V和1.8 V左右出现Mo和Mn对应的氧化峰,说明了Li+在充电过程可逆地脱出.MnMoO4电极第三次充放电循环曲线与第二次的曲线几乎一致,说明了MnMoO4纳米棒具有较强的稳定性及可逆性.
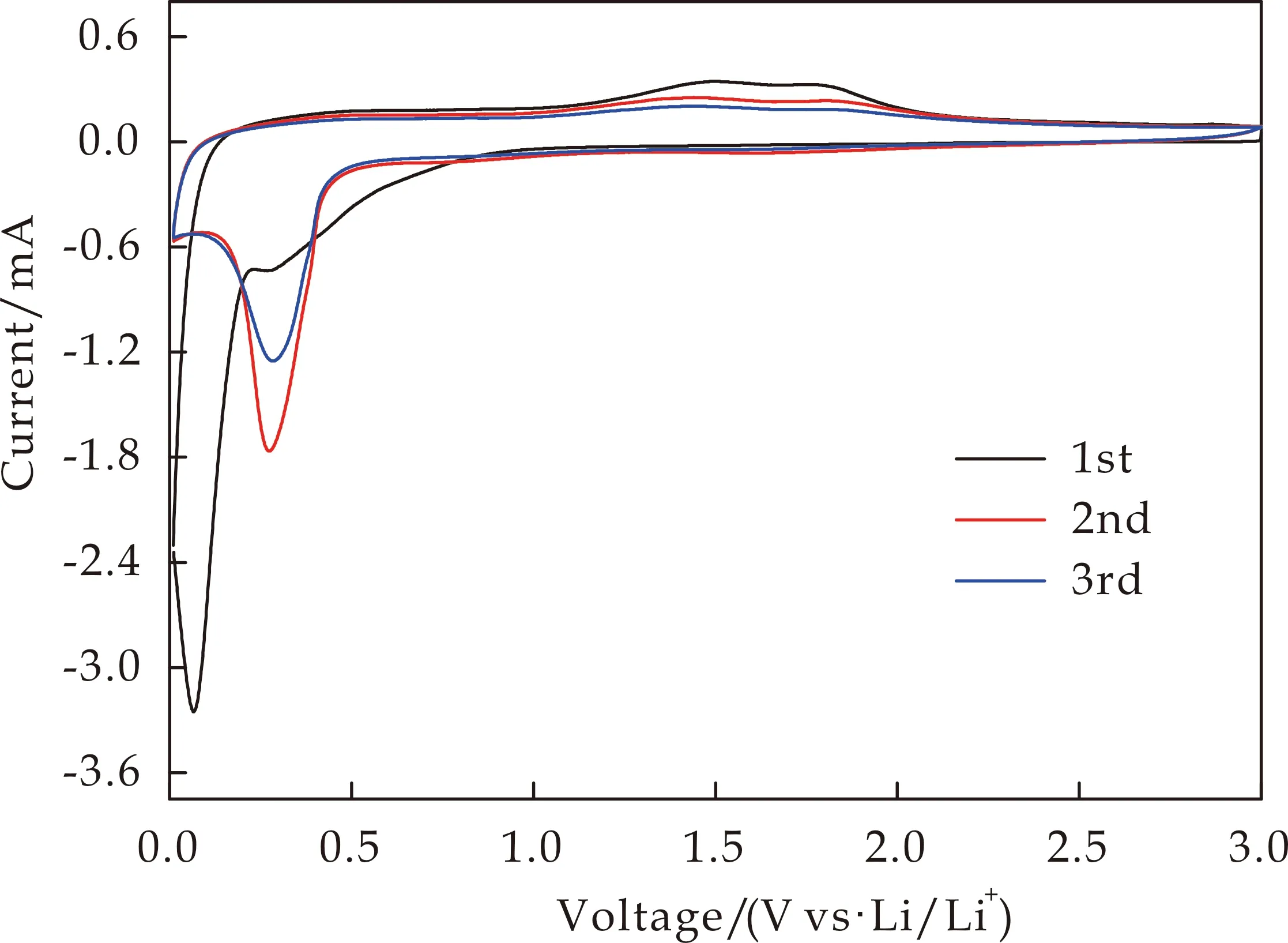
图6 MnMoO4的循环伏安曲线
图7为MnMoO4纳米棒电极在0.1 A·g-1电流密度下的恒电流充放电曲线.从图7可见,MnMoO4电极首次放电-充电比容量分别为1 134 mAh·g-1和849 mAh·g-1,对应的首次库伦效率为74.8%,不可逆容量的产生可能是由于电解液的分解以及Li+在MnMoO4晶体中的不可逆嵌入[10].MnMoO4电极第二次与第三次的充放电曲线几乎一致,说明MnMoO4纳米棒结构较稳定,与Li+反应的可逆性较强.
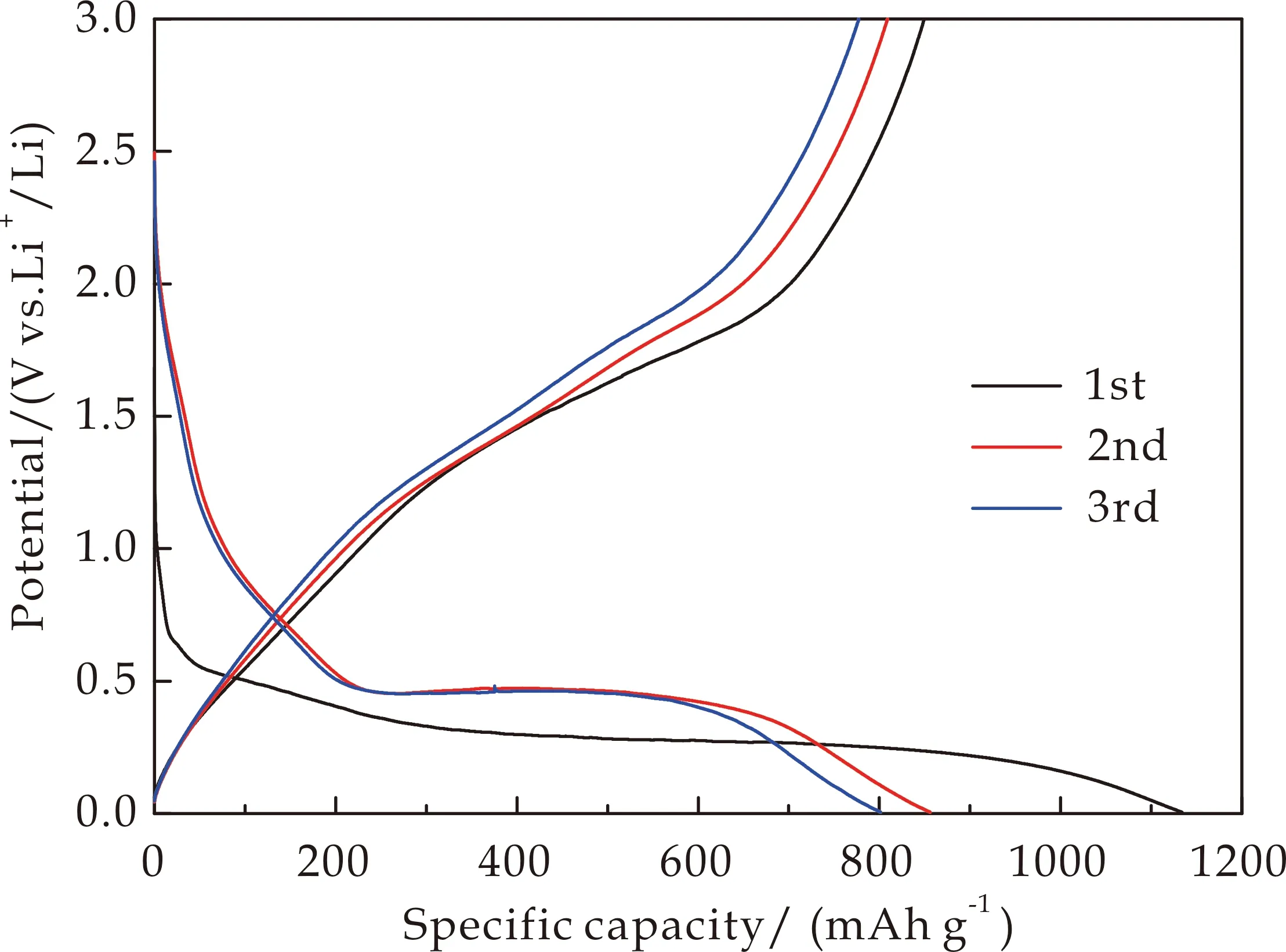
图7 MnMoO4的充放电曲线
图8(a)为500 ℃下煅烧制备的MnMoO4纳米棒电极的倍率性能图,从图中可见,在电流密度分别为0.1 A·g-1、0.2 A·g-1、0.5 A·g-1、1 A·g-1、2 A·g-1、5 A·g-1下,平均充电比容量分别为777.4 mAh·g-1、590.2 mAh·g-1、368.8 mAh·g-1、254.1 mAh·g-1、139.0 mAh·g-1、77.8 mAh·g-1,当电流密度快速恢复至0.1 A·g-1时,其比容量可以恢复至518.7 mAh·g-1,优于400 ℃和600 ℃下煅烧制备的MnMoO4材料,说明MnMoO4纳米棒具有较好的倍率性能.
图8(b)为MnMoO4纳米棒电极在电流密度为0.1 A·g-1下的循环性能图.从图中可见,MnMoO4纳米棒在循环前期容量衰减严重,循环23次之后的比容量为300.3 mAh·g-1,主要原因为MnMoO4纳米棒在充放电过程中存在体积膨胀效应,无法形成稳定的固态电解质界面膜(SEI),导致电解液不断分解,降低了Li+与MnMoO4纳米棒的反应活性.23次之后,MnMoO4纳米棒的充放电反应逐渐稳定,循环300次之后的比容量仍可维持在291.4 mAh·g-1.值得一提的是MnMoO4纳米棒的库伦效率除首次较低外,第二次循环即达到97.4%,之后循环的库伦效率接近99%,说明Li+在MnMoO4纳米棒电极上的嵌入/脱出具有较强的可逆性.
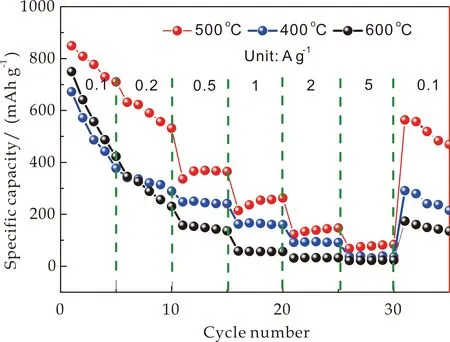
(a)倍率
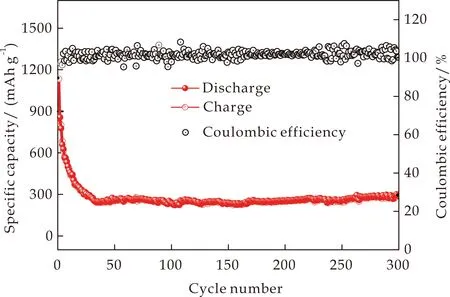
(b)循环图8 MnMoO4的倍率和循环稳定性
3 结论
本文采用水热法结合煅烧处理制备MnMoO4纳米棒.通过对原料配比、水热时间和温度、煅烧温度等工艺参数进行较为详细地探索,在Mo∶Mn=1∶1、水热时间和温度分别为5 h和140 ℃,煅烧温度为500 ℃的优化反应参数下制备了直径大约为70±20 nm的MnMoO4纳米棒.
同时,考察了其作为锂离子负极材料的电化学性能,测试结果表明,MnMoO4纳米棒与Li+反应活性较高,但是其容量在前期衰减较快,循环23次之后充放电反应逐渐稳定.后期拟采用碳包覆改善MnMoO4纳米棒的循环稳定性,但是碳源的选择、包覆方式及碳含量等工艺参数需要进一步探究.

