6种新型冠状病毒核酸检测试剂的检测性能对比观察
李懿,李东晓,王博昊,马红霞,郭万申,黄学勇
河南省疾病预防控制中心,郑州450016
新型冠状病毒(2019-nCoV)是冠状病毒家族中的一种,蝙蝠被认为是冠状病毒的天然宿主,由于外界环境的改变或者病毒的变异,冠状病毒跨越种系屏障传染给人类及其他动物,如鸟类、啮齿动物[1~7]。冠状病毒可以引起呼吸道及神经方面的疾病[8,9]。此次COVID-19具有发热、干咳、乏力、头疼等临床表现及肺部影像学改变[10~14]。自2019年12月武汉市发现多例COVID-19患者以来[15,16],COVID-19疫情在我国其他省份持续扩散。截止到2020年2月17日,全国确诊患者70 639例,疫情形势十分严峻。近日,美国、韩国、日本、新加坡等国家也陆续报出COVID-19患者,COVID-19已经成为世界卫生公共安全所要面对的问题。根据《新型冠状病毒感染的肺炎诊疗方案(试行第六版)》的要求,对COVID-19疑似患者的确诊,需要进行2019-nCoV核酸检测,或者进行2019-nCoV基因测序[17,18]。基因测序成本高、周期长,多数卫生医疗机构不具备开展基因测序条件,因此实时荧光RT-PCR检测2019-nCoV核酸成为COVID-19确诊的主要方法。实时荧光RT-PCR试剂研发和生产速度较快[19],在中国疾控中心公布 2019-nCoV基因序列后,多家试剂公司迅速推出各种2019-nCoV核酸检测试剂。目前仅有少量文献对2019-nCoV核酸检测试剂进行评价[20,21],且涵盖的试剂种类较少。2020年1~2月,本研究采用6种2019-nCoV核酸检测试剂检测了47例COVID-19疑似患者咽拭子样本中的2019-nCoV核酸,对不同试剂的2019-nCoV核酸阳性检出率及CT值进行了对比观察,评价不同试剂的检测性能,为临床及检测部门选取合适的检测试剂提供依据。
1 材料与方法
1.1 检测试剂及受检标本来源 依据国家《新型冠状病毒感染的肺炎实验室检测技术指南》[22]。2019-nCoV核酸检测试剂:试剂A(上海辉睿生物科技有限公司,无批号,无医疗器械注册证书编号)、试剂B(上海捷诺生物科技有限公司,批号:GZTR2020005,国械注准20203400058)、试剂C(上海伯杰医疗科技公司,批号:20200202A,国械注准20203400065)、试剂D(上海之江生物科技股份有限公司,批号:P20200106,国械注准20203400057)、试剂E(圣湘生物科技股份有限公司,批号:2020002,国械注准20203400064)、试剂F(中山大学达安基因股份有限公司,批号:2020008,国械注准20203400063)。咽拭子标本来源于河南省辖市疾控中心送检的47例COVID-19疑似患者标本。6种检测试剂的基本信息见表1。

表1 6种2019-nCoV核酸检测试剂的模板量、PCR反应条件、最低检测限及结果判读标准
1.2 6种2019-nCoV核酸检测试剂对受检标本中2019-nCoV核酸(ORF1ab、N基因)的检测 在生物安全柜内,打开标本运输箱,取出待检咽拭子标本。将咽拭子采样管充分振荡混匀后静置10 min,取上清1 mL转移至2 mL螺口管中。采用西安天隆科技有限公司生产的病毒DNA/RNA提取试剂盒(CDC)(批号:20011010T014 )和NP968核酸提取系统提取咽拭子的RNA,取出适量标本液加入预装病毒裂解液的板中,用封口膜或者盖子盖紧,静置10 min让病毒灭活,具体操作按照试剂盒说明进行。PCR反应体系配制和反应条件均参照各个试剂盒说明。使用Roche公司的LightCycler96实时荧光定量PCR仪进行PCR反应,并参照各个试剂盒检测说明书设置反应程序。结果以CT值表示。在结果判读上6种试剂稍有区别,试剂A、B、C结果为可疑时需要重复检测,若复检结果与初始结果一致可判定为阳性,否则为阴性;试剂D复检时仅ORF1ab为阳性,即可判断为核酸阳性。试剂E、F不需要重复检测。
对47例COVID-19疑似患者的咽拭子标本进行2019-nCoV ORF1ab、N基因检测,取均能检出ORF1ab和N基因的咽拭子标本5份,将5份咽拭子中的核酸进行10倍的倍比稀释,稀释至原液的10倍和100倍后,再用6种试剂分别检测ORF1ab和N基因,取两个基因CT值的平均值作为COVID-19核酸的最终CT值。
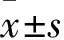
2 结果
2.1 受检标本中6种2019-nCoV核酸检测试剂检测的2019-nCoV ORF1ab基因、N基因CT值及阳性检出率比较 试剂A:2019-nCoV ORF1ab基因、N基因 CT值分别为36.61(26.70~38.89)、33.54(27.19~38.23),阳性检出率为78.7%(37/47);试剂B:2019-nCoV ORF1ab基因、N基因 CT值分别为30.76(24.37~37.00)、33.26(27.34~39.20),阳性检出率为78.7%(37/47);试剂C: 2019-nCoV ORF1ab基因、N基因 CT值分别为31.86(24.10~37.68)、31.63(25.27~37.10),阳性检出率为83.0%(39/47);试剂D:2019-nCoV ORF1ab基因、N基因 CT值分别为34.68(30.84~39.63)、33.33(27.85~39.22),阳性检出率为78.7%(37/47);试剂E:2019-nCoV ORF1ab基因、N基因 CT值分别为31.61(24.61~39.20)、30.21(21.61~38.86),阳性检出率为80.9%(38/47);试剂F:2019-nCoV ORF1ab基因、N基因 CT值分别为33.53(25.92~39.43)、31.92(24.62~38.10),阳性检出率为83.0%(37/47)。试剂A、B、C、E、F对2019-nCoV ORF1ab、N基因阳性检出率及CT值比较,P均>0.05。在对ORF1ab基因的检测中,试剂C、E、F优于试剂A、B、D,但差异无统计学意义。对N基因的检测中,试剂A、B、C、E、F阳性检出率基本一致,试剂D的阳性检出率为74.5%(35/47)。
2.2 6种2019-nCoV核酸检测试剂检测不同浓度2019-nCoV核酸的CT值比较 试剂A、B、C、E、F均能检出5份咽拭子不同稀释浓度的2019-nCoV核酸,试剂D检出率只有60%(6/10)。因为试剂D检出率太低,故未统计试剂D的检测结果。试剂A、B、C、E、F检测2019-nCoV核酸的CT值分别为30.30±2.39、28.68±2.34、27.63±2.14、25.96±2.57、28.43±2.38,试剂A、B、C、E、F检测10倍稀释的2019-nCoV核酸CT值分别为33.75±2.13、32.03±2.56、31.01±2.15、29.28±2.62、31.65±2.44,试剂A、B、C、E、F检测100倍稀释的2019-nCoV核酸CT值分别为37.20±2.13、35.27±1.99、34.35±2.78、32.49±2.54、35.02±2.35。试剂A、B、C、E、F检测3种不同浓度2019-nCoV核酸的CT值比较,P均>0.05。
3 讨论
COVID-19现在已经成为世界公共卫生安全所要面对的问题,准确、快速地对COVID-19疑似患者进行病原鉴定十分重要。准确的2019-nCoV病原鉴定对COVID-19疑似患者治疗方案的确定、感染的控制都起着关键作用[23]。本研究选取了市场上可以购买的6种2019-nCoV核酸检测试剂,3种是《新型冠状病毒感染的肺炎诊疗方案(试行第二版)》推荐使用的试剂,又选取了3种有医疗器械注册证号的检测试剂。目前从国家食品药品监督管理总局的官网上能查到的6种2019-nCoV的检测试剂(实时荧光RT-PCR法),除了华大生物科技的2019-nCoV核酸检测试剂(实时荧光RT-PCR法)我们没有对比到,其余5种试剂均在本次对比中。
我们比较了这6种2019-nCoV核酸检测试剂对COVID-19疑似患者咽拭子标本进行2019-nCoV ORF1ab基因、N基因检测,结果发现试剂C、F对2019-nCoV ORF1ab基因、N基因阳性检出率最高,其次是试剂E、A、B,三种试剂的阳性检出率基本相同。试剂D对咽拭子标本的2019-nCoV核酸检出阳性率处于中等水平,我们根据其说明书判断,重复检查ORF1ab单独阳性,结果也判读为阳性,但是其N基因的检出率最低,仅为74.5%(35/47)。
对比这6种试剂对阳性2019-nCoV核酸原液、10倍稀释、100倍稀释这三个浓度的检测发现,除了试剂D不稳定,不能同时检测出ORF1ab和N基因,其余5种试剂都能同时检出ORF1ab和N基因。试剂A、B、C、E、F检测的不同浓度核酸稀释液CT值比较差异无统计学意义,证明这5种试剂均具有良好的稳定性;而且检测各稀释浓度的CT值差值在3.3左右波动,表明这5种试剂的检测准确性较高,检测的重复性也较好。
综上所述,本研究评价的6种试剂中,除了D试剂对2019-nCoV ORFlab和N基因的检出率较低外,其余5种试剂均能检出ORFlab及N基因。试剂A、B、C、E、F对不同浓度阳性2019-nCoV核酸标本的检出能力差异不明显,均具有较好的稳定性。这5种试剂均可满足实验室及临床检测要求,可作为COVID-19疑似患者的确诊检测试剂。但本研究仍有不足之处。6种试剂各自推荐了不同的核酸提取方法,在样本处理和核酸提取过程中,为尽快完成标本的处理,减少检测人员暴露的机会,要尽量减少离心、开盖等操作步骤,降低风险,所以在检测过程中没有选择各个试剂推荐的核酸提取方法,而选取了操作步骤少、提取时间短和市场上使用较多、较成熟的磁珠法来提取咽拭子标本的核酸。这样有可能会出现核酸提取试剂与检测试剂不太匹配的情况,提取试剂的残留也可能会影响试剂的扩增效率。本研究仅对比47份COVID-19疑似患者咽拭子样本的检测结果,样本数量有限,不能有效地评价试剂的敏感性和特异性。另外,我们仅对比了各试剂的其中一个批号,并不能完全代表各个试剂的整体检测性能。如有条件,需选择同一试剂的多个批次进行有效评价,以满足临床检测所需。

