帕博丽珠单抗治疗晚期黑色素瘤的不良事件及相关性分析
北京大学肿瘤医院暨北京市肿瘤防治研究所肾癌黑色素瘤科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京100142
近年来,随着肿瘤免疫治疗的兴起,免疫检查点抑制剂(immune checkpoint inhibitor,ICI)已经彻底改变了癌症治疗方式并显著改善了晚期肿瘤患者的预后[1]。帕博丽珠单抗作为一种人源化IgG4型抗程序性死亡[蛋白]-1(programmed death-1,PD-1)单抗,已于2014年获得美国食品药品管理局(Food and Drug Administration,FDA)批准用于局部晚期或转移性黑色素瘤患者的治疗;基于一项“帕博丽珠单抗作为二线治疗中国局部晚期或转移性黑色素瘤的Ⅰb期临床研究(Keynote-151)”,该药也在中国获批为经治失败的不可切除或转移性黑色素瘤的适应证。由于其药物特殊的作用机制可能引发非靶组织的免疫活化从而导致免疫相关不良反应(immune-related adverse event,irAE)[2],而这一免疫反应可能发生于全身各个器官,程度轻重不等,甚至危及生命,引起临床广泛关注[3-5];其次,该药物上市时间较短,尤其是国内安全性数据相当缺乏,给广大肿瘤医师的临床决策带来困惑。因此,本研究回顾性分析了入组Keynote-151研究的54例局部晚期或转移性黑色素瘤患者不良事件的临床特征及与预后和疗效的关系,探讨PD-1单抗不良事件发生的预测因子及与预后的相关性,以期为该药今后临床应用提供更多的参考信息。
1 资料和方法
1.1 临床资料
收集2016年8月—2017年7月在北京大学肿瘤医院入组一项“帕博丽珠单抗作为二线治疗中国局部晚期或转移性黑色素瘤的Ⅰb期临床研究(Keynote-151)”的54例患者的临床资料。临床研究入组标准:患者年龄≥18岁;经病理学检查确诊为局部晚期或转移性黑色素瘤一线治疗失败的患者;美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力状况(performance status,PS)评分≤1分;预期寿命≥3个月,且既往未接受过抗PD-1、抗程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)或抗程序性死亡[蛋白]配体-2(programmed death ligand-2,PD-L2)抗体治疗。排除标准:眼部黑色素瘤患者;有症状的脑转移患者;合并自身免疫性疾病且需要治疗的患者;艾滋病毒阳性患者;活动性乙型肝炎或丙型肝炎患者;合并肺炎或既往曾因肺炎需要激素治疗的患者。
本中心入组患者54例,其中男性23例,女性31例,年龄26~77岁,中位年龄53岁,ECOG评分0分24例(44.4%)。原发部位最常见的是肢端型19例(35.2%),其次是皮肤黑色素瘤16例(29.6%)、原发部位不明黑色素瘤10例(18.5%)、黏膜黑色素瘤9例(16.7%)。按疾病分期M1c期患者最多为30例(55.6%),其次分别是M1b期12例(22.2%)、M1a期11例(20.4%)、M0期1例(1.9%)。存在突变基因的患者有14例(25.9%),其中6例为BRAF突变,3例为NRAS突变,5例为其他突变类型,其余40例患者为野生型。既往接受过化疗的患者30例(55.6%),其余患者曾接受靶向治疗、溶细胞性T淋巴细胞相关抗原-4(cytolytic T lymphocyteassociated antigen-4,CTLA-4)抑制剂等其他治疗(表1)。
1.2 治疗及评价
给药方案:帕博丽珠单抗单药治疗,2 mg/kg,每3周给药1次,直至疾病进展或无法耐受毒性为止。研究方案已经伦理委员会审批通过,所有患者均签署知情同意书。中位随访时间为24.5个月(随访数据截至2019年4月19日),不良事件和严重不良事件根据通用不良事件术语标准(Common Terminology Criteria Adverse Events,CTCAE)4.03版评价分为5级,1级:无症状或症状轻;2级:中度;3级:重度;4级:危及生命;5级:死亡。疗效采用实体肿瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors,RECIST)1.1进行评估,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),临床获益是指CR+PR+SD的患者。
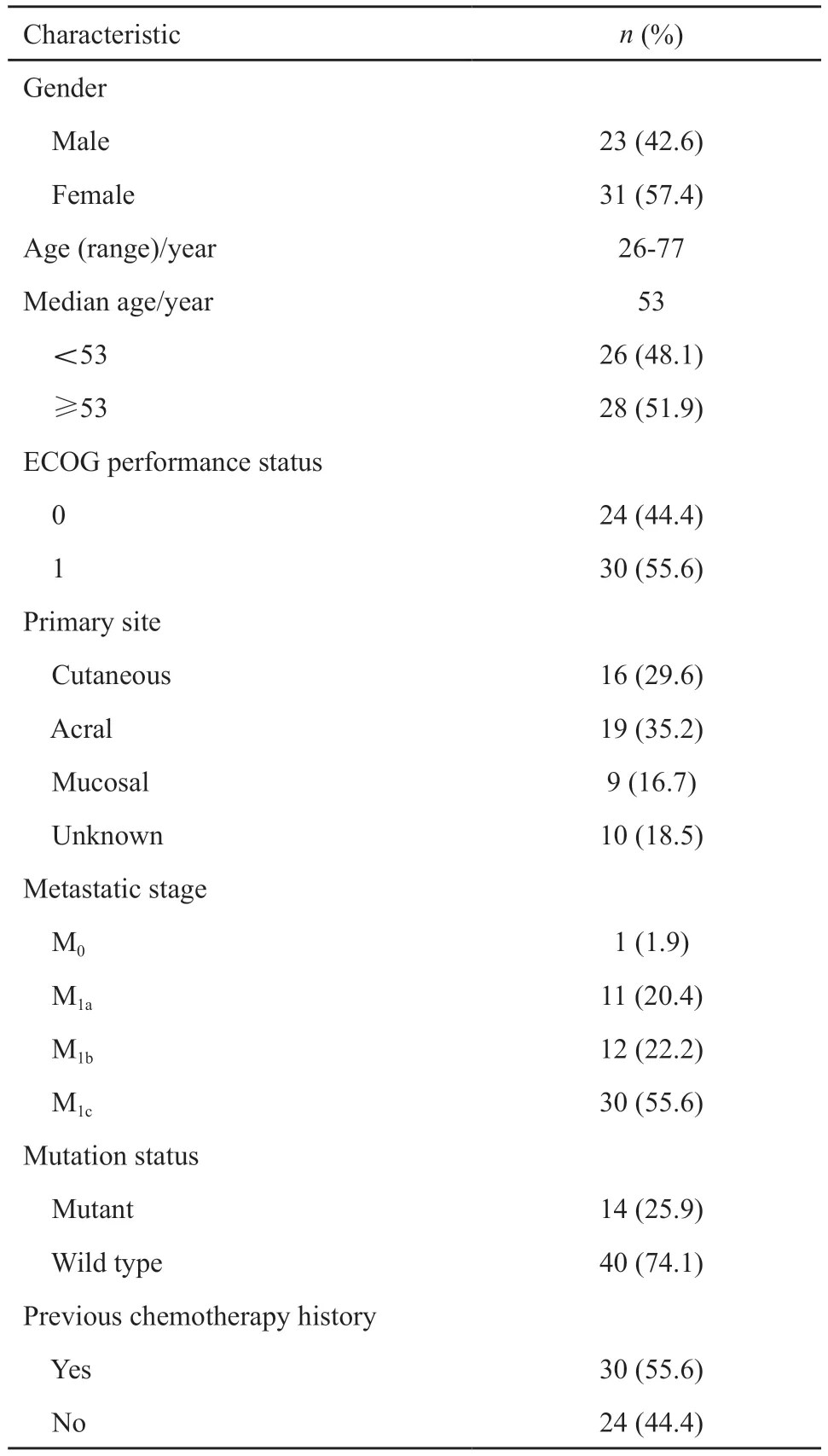
表1 患者临床特征Tab.1 Clinical characteristics
1.3 统计学处理
统计学处理采用R3.5.3进行计算,定量资料采用t检验,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 不良事件及严重不良事件发生率
本组患者药物相关性不良反应发生率高达88.9%(48/54),不良事件种类达51种,累及全身多个系统,其中发生率≥10.0%的常见不良反应24种,前5种依次为:甲状腺功能异常24例(44.4%),高三酰甘油血症22例(40.7%),乳酸脱氢酶升高17例(31.5%),丙氨酸氨基转移酶升高15例(27.8%),血糖升高15例(27.8%)。无治疗相关死亡事件发生,严重不良事件发生率为13.0%(7/54),其中1例(1.9%)4级不良反应为自身免疫性肝炎,其余均为3级不良反应,分别为γ-谷氨酰胺转肽酶升高2例(3.7%)、低钠血症2例(3.7%)、中性粒细胞绝对值减少1例(1.9%)、血糖升高1例(1.9%)(表2)。
2.2 严重不良事件的相关因素分析
将患者分别按性别(男性vs女性)、年龄(≥53岁vs<53岁)、ECOG PS评分(0分vs1分)、既往化疗史(有vs无)、基因突变(有vs无)各分为两组,分别按疾病分期(M1avsM1bvsM1c)、原发部位(皮肤vs肢端vs黏膜vs原发部位不明)各分为4组,采用χ2检验比较组间严重不良事件发生率的差异。上述各临床特征与严重不良事件的发生无显著相关性(P>0.05)。同时,采用两样本均数t检验比较外周血中白细胞计数、中性粒细胞/淋巴细胞绝对值比值(neutrophil-to-lymphocyte ratio,NLR)、嗜酸粒细胞绝对值、血小板计数的基线水平在有无严重不良反应患者组间的差异,结果提示两组之间各指标差异均无统计学意义(P>0.05,表3)。
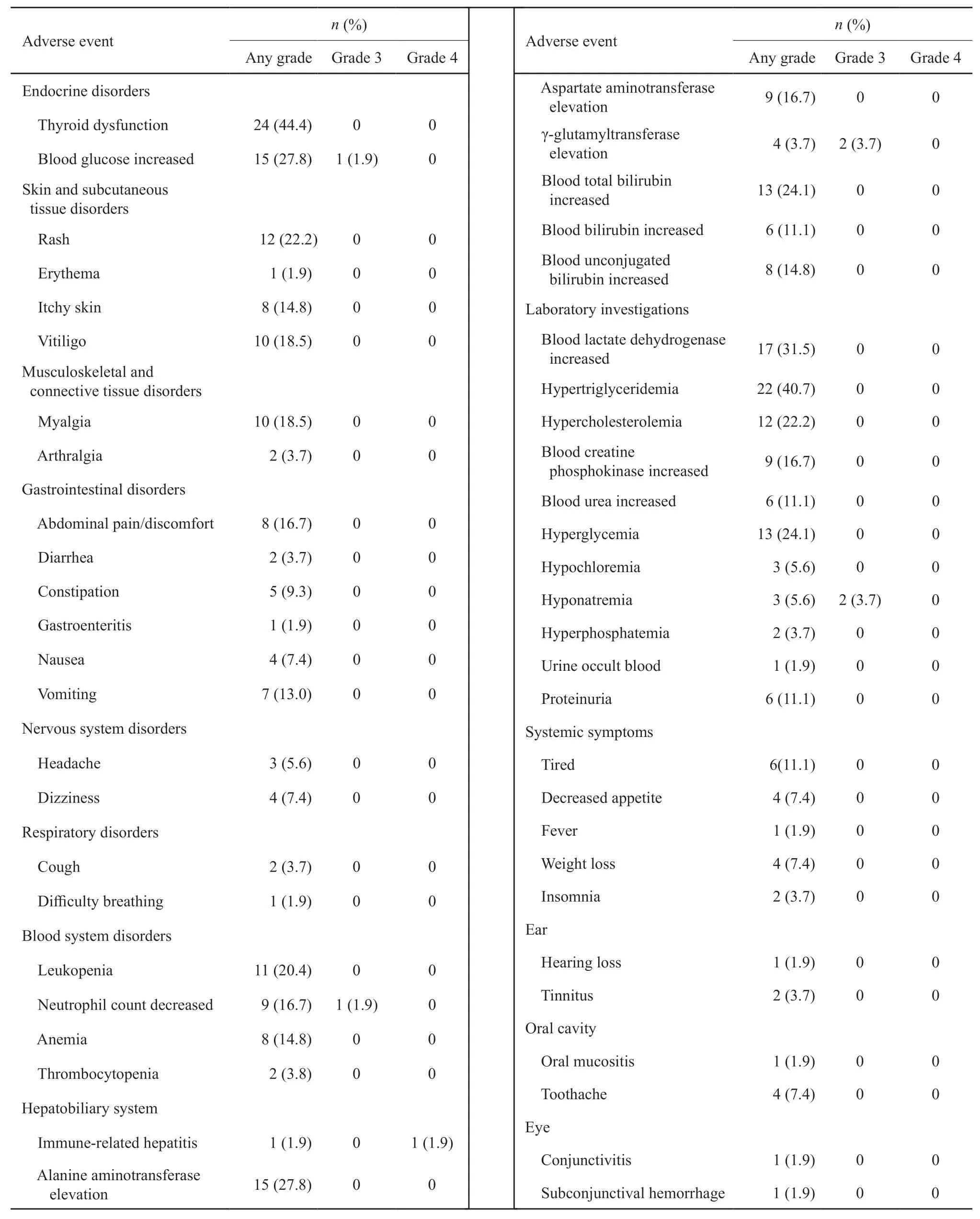
表2 不良事件Tab.2 Adverse events
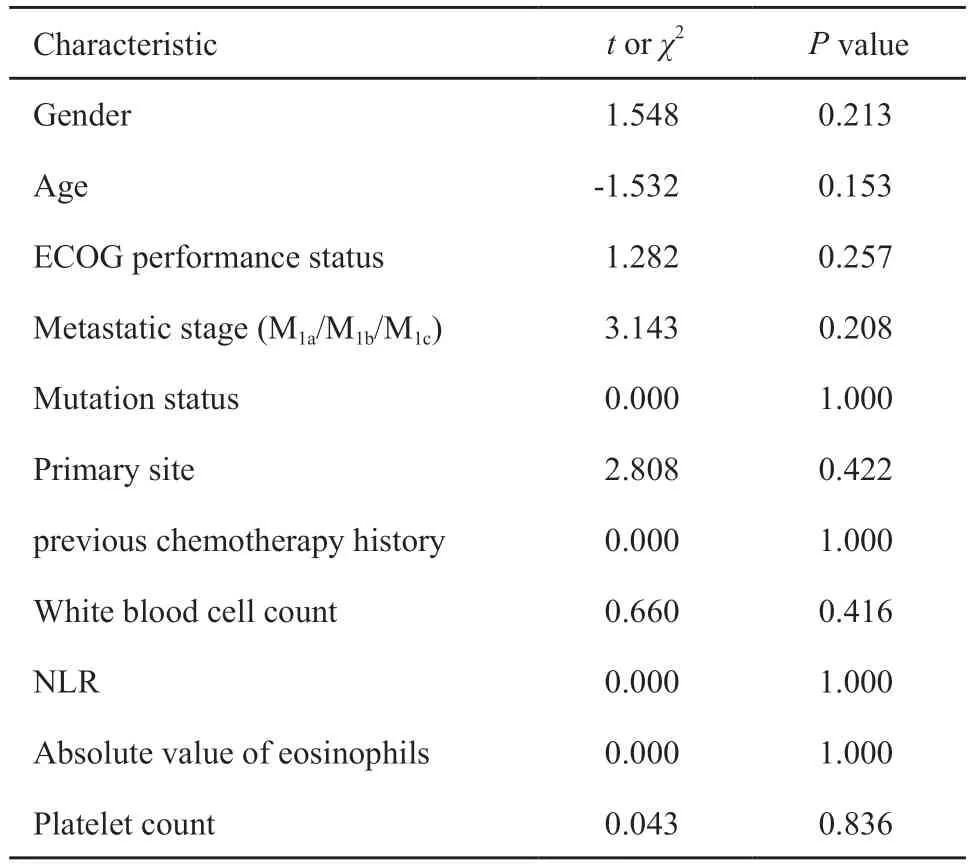
表3 严重不良事件相关因素分析Tab.3 Analysis of factors related to serious adverse events
2.3 不良事件对治疗的影响
本组患者共发生不良事件496例次,其中绝大部分均能通过对症治疗缓解或自行缓解,截止随访日期仍有19.0%(94例次)的不良反应持续未缓解,其中较常见的包括甲状腺功能减退、白癜风、高三酰甘油血症、高血糖、疲劳、贫血、高胆固醇血症、体质量下降等。这些不良事件均未累及重要脏器且绝大部分为1~2级,仅需给予对症治疗,不影响继续治疗。
本研究中因不良事件终止治疗1例次,为4级自身免疫性肝炎,给予大剂量肾上腺皮质激素治疗后缓解;因不良事件暂停治疗8例次,其中1例因3级低钠血症暂停治疗1次;其余7例次均为肝功能异常,主要表现为3级γ-谷氨酰胺转肽酶升高(2例次)、2级丙氨酸氨基转移酶升高(1例次)、2级直接胆红素升高(4例次),经对症处理均可逆转。
2.4 不良事件与疗效相关性分析
5 4 例患者接受治疗后临床获益者(CR+PR+SD)26例,其中10例发生白癜风,而28例未获益患者中无一例发生;同时甲状腺功能异常在获益患者中的发生率为65.4%,而在未获益患者中的发生率为21.4%。采用χ2检验,分析两种不良事件与疗效的关系,说明白癜风(P=0.001)和甲状腺功能异常(P=0.007)可能是两个疗效预测因子,可以认为用药后出现上述两种不良反应提示预后良好(表4~5)。
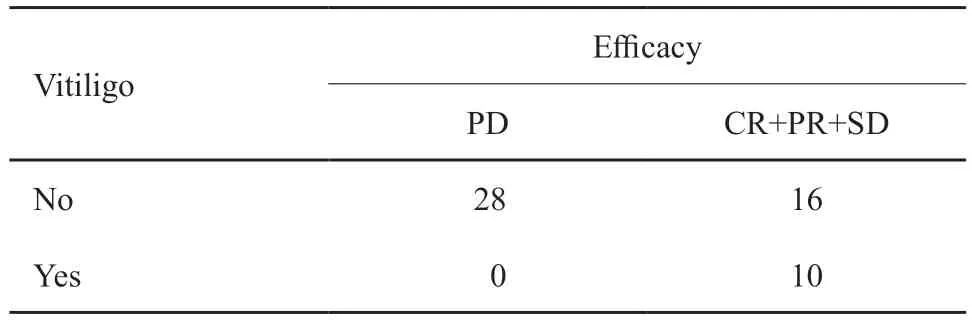
表4 白癜风与疗效相关性分析Tab.4 Correlation analysis between vitiligo and efficacy
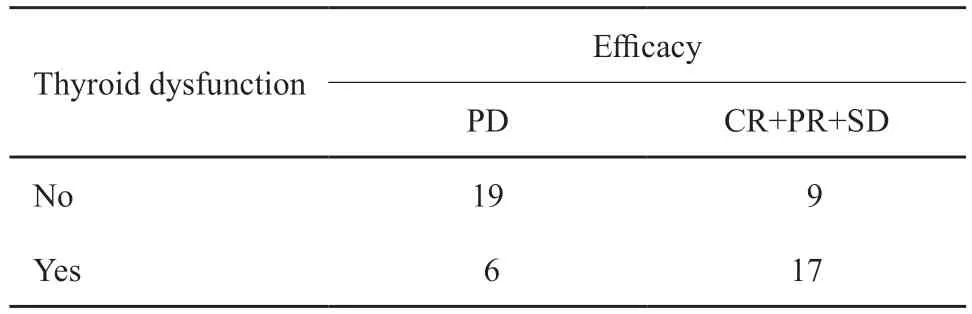
表5 甲状腺功能异常与疗效相关性分析Tab.5 Correlation analysis between thyroid dysfunction and efficacy
3 讨 论
近年来,以ICI为主的肿瘤免疫治疗在临床肿瘤治疗领域取得了突破性进展[1]。帕博丽珠单抗为首个获批用于晚期黑色素瘤二线治疗的PD-1抑制剂[6],基于其显著的疗效很快美国FDA又扩展批准为黑色素瘤一线治疗和多种恶性肿瘤适应证[7]。然而,ICI带来疗效的同时,其不良反应也引起国内外学者的重视。临床研究中ICI总体不良反应发生率为60%~80%,严重不良反应发生率为10%~15%[8-10],并发现不同瘤种不良反应特征不同,如皮肤毒性在黑色素瘤患者中更容易发生,而肺炎更容易在肺癌患者中发生[11]。
Keynote-151研究为一项在既往接受过一线系统性治疗的中国局部晚期或转移性黑色素瘤患者中开展的多中心、非对照、Ⅰb期临床研究。Si等[13]已报道了该研究早期结果,帕博丽珠单抗在中国晚期黑色素瘤患者二线治疗中有较好耐受性及显著的临床疗效,总体安全性特征与全球人群一致。本研究对北京大学肿瘤医院入组该研究54例患者不良反应数据做了进一步分析,发现总的不良反应发生率为88.9%,与早期结果(84.5%)比较基本一致,严重不良事件发生率为13.0%,较前(8.7%)有升高趋势,发生率最高的不良事件仍是甲状腺功能异常,高达44.4%,与早期结果(32.0%)比较也有所升高[13]。分析严重不良事件及甲状腺功能异常发生率较前升高,可能与用药时间延长有关,故提示临床医师用药后期仍要关注严重药物相关不良事件的发生及甲状腺功能的监测。同时发现甲状腺功能异常发生率明显高于国外报告的数据(2%~10%)[14],不能排除这一不良反应存在人种间的差异,有待今后大样本研究进一步证实。
目前对PD-1抑制剂疗效相关标志物的研究较多,而对不良事件发生预测因子的研究相对较少。有学者认为,外周血细胞计数与肿瘤免疫反应有一定相关性,从而进一步探讨是否可将其作为免疫治疗毒性或疗效的生物标志物[15]。Diehl等[16]进行的多变量分析结果表明,外周血淋巴细胞和嗜酸性粒细胞计数与≥2级的irAE发生率显著相关。并有研究发现,较高的嗜酸性粒细胞计数与内分泌irAE的发生有关[17]。本研究就性别、年龄、ECOG评分、原发部位、疾病分期、基因突变、既往化疗史等临床特征及外周血细胞计数进行了分析,探究这些因素对严重不良事件发生的影响,结果显示,严重不良事件的发生与上述因素之间无显著相关性。因此,对于PD-1单抗不良事件发生的预测因子仍有待进一步研究。
同时,本研究观察了不良事件对研究药物的影响,发现大部分不良事件均为1~2级,绝大部分不良反应均能通过对症治疗缓解或自行缓解。导致中断或终止治疗的不良反应共9例次,其中8例次均为肝毒性反应,7例严重不良事件中,3例为严重肝毒性反应,严重肝毒性的发生率为5.6%(3/54),与既往帕博丽珠单抗临床研究报道数据(5.0%~6.0%)基本一致[18-21],提示临床医师用药中应严密监测肝功能并及时给予干预和治疗。
ICI在通过增强免疫应答发挥抗肿瘤作用的同时诱发irAE,故有研究认为irAE与疗效有关,并多提示预后较好。Downey等[22]研究发现,应用伊匹木单抗的患者中,有无不良反应发生的客观反应率分别为26%和2%。Nivolumab治疗转移性黑色素瘤中发现,皮肤不良反应无论是白癜风、皮疹均与总生存率具有显著相关性,预示疗效较好[23],而白癜风与其他非黑色素瘤疗效之间的关系尚不清楚[15,24-26]。此外,Fujisawa等[17]发现内分泌irAE的发生与黑素瘤患者的总生存相关。本研究重点对白癜风和甲状腺功能异常与疗效相关性进行了分析,发现白癜风(P=0.001)和甲状腺功能异常(P=0.007)与疗效有一定的相关性,可能是两个疗效预测因子。
综上所述,帕博丽珠单抗在提高晚期黑色素瘤患者疗效的同时伴随相关不良反应的发生,虽然药物治疗相关不良反应发生率较高,但以1~2级为主,临床耐受性较好;肝毒性是导致停药和中断治疗最常见的不良事件,临床应用中应引起高度重视;白癜风和甲状腺功能异常可能是疗效较好的预测因子。鉴于本研究为单中心小样本回顾性研究,不良反应发生相关因素及与疗效相关性仍需进一步前瞻性大样本临床研究数据证实。

