带血管腓骨移植治疗股骨头坏死中氨甲环酸在腓骨供区的局部应用
陆健 盛加根 陶诗聪 朱振中 张长青
带血管腓骨移植术(FVFG)于20世纪70年代被首次提出,已成功应用于骨髓炎、创伤后骨折不连接、肿瘤切除后缺损重建和下颌骨重建等[1-4]。股骨头坏死(ONFH)是一种机理尚不明确且治疗难度较大的疾病[5],常因股骨头血液供应中断导致骨细胞和骨髓细胞进行性坏死,继而发生股骨头塌陷并最终发展成骨性关节炎,患者因此面临全髋关节置换(THR)。作为针对ONFH的保髋手术,FVFG对缓解关节疼痛、改善髋关节功能和提高患者生活质量均具有重要意义,其有效率可达70%~90%[6]。然而有文献报道,FVFG术后腓骨供区部位的血管损伤与肌肉组织渗血可导致血肿形成,增加软组织张力,进而损伤腓浅神经和腓深神经并引发伤口感染等[7]。因此,控制FVFG围手术期失血量尤为重要。许多临床研究均报道,作为止血药物,氨甲环酸(TXA)已广泛用于骨科手术中,并获得世界卫生组织认可。为探讨局部应用TXA对FVFG围手术期腓骨供区出血量的影响,我们对2016年8月至2017年8月及2017年10月至2018年10月在上海市第六人民医院行单侧FVFG治疗的238例ONFH患者资料进行回顾性分析,评价TXA的应用效果。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①行单侧FVFG治疗的ONFH患者;②有完整的病史资料及术后半年随访资料。
排除标准:①年龄<18岁或>60岁;②有TXA禁忌证:既往有动脉或静脉血栓形成,肌酐清除率<30 mL/min;③术前长期服用抗凝药物或者无抗凝药物服用史但凝血功能异常者;④对TXA过敏;⑤术前贫血(男性为血红蛋白<120 g/L,女性为血红蛋白<110 g/L)。
1.2 研究对象及分组
依据纳入及排除标准,选取2016年8月至2017年8月局部未使用TXA的患者121例,设为对照组;2017年10月至2018年10月局部使用TXA的患者117例,设为TXA组。
1.3 手术方法
所有患者均由同一组医生采用上海市第六人民医院标准FVFG手术方式治疗[8]。患者全身麻醉生效后,于术侧下肢上1/3处用止血带。待驱血及气囊止血带充气后,术者首先于患者小腿外侧沿腓骨轴心线作纵切口,然后从位于小腿后外侧的腓骨长短肌与腓肠肌之间肌间隙进入以暴露腓骨,最后在距腓骨小头远端约6 cm处取长约7~8 cm带腓血管和肌袖的腓骨瓣。经仔细止血,对照组以干纱布填塞至肌肉间隙中,TXA组则以浸有50 mL生理盐水(含2 g TXA)的纱布填塞至肌肉间隙中,并于填塞10 min后取出。松开止血带及仔细结扎活动出血点,两组患者均常规放置负压引流管并分别逐层关闭切口。
1.4 术后处理
术后3 d内常规应用一代头孢预防感染,6周内预防性应用低分子肝素抗凝,引流管放置不超过72 h。所有患者均被告知术后第一天进行足踝和股四头肌主动功能锻炼,术后2周行髋膝主动功能锻炼,术后 3个月扶拐行走并逐渐负重,术后6个月完全负重。
1.5 主要观察指标
①术后第一天小腿引流量;②术后24 h引流管拔除率(引流量<50 mL予以引流管拔除);③术后并发症:术后出现患肢足背麻木感及伸趾、伸踇无力,术后30 d内出现小腿皮肤感染,术后60 d内出现下肢深静脉血栓形成和肺栓塞。
1.6 统计学分析
应用SPSS 24.0统计学软件对相关数据进行分析。经统计学分析,两组患者年龄、引流量不符合正态分布,以均数±标准差表示,并采用Mann-WhitneyU检验比较。两组患者性别、手术侧别、术后24 h小腿引流管拔除率采用卡方检验比较。P<0.05为差异有统计学意义。
2 结果
2.1 患者一般临床资料比较
对照组年龄为(35.3±8.9)岁,TXA组年龄为(36.2±9.0)岁,两组患者年龄无统计学意义(P>0.05)。两组患者性别和手术侧别差异均无统计学意义(P>0.05)(表1)。
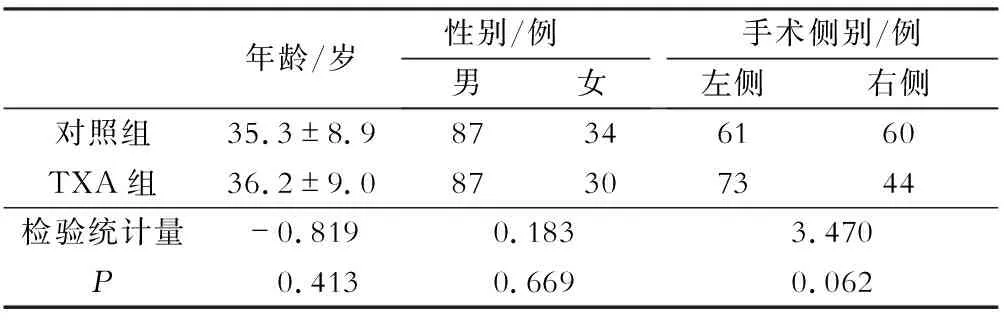
表1 患者一般临床资料比较
2.2 围手术期观察指标比较
TXA组术后第一天腓骨供区负压引流量[(13.0±13.9) mL]明显少于对照组[(36.4±33.4) mL](P<0.05);TXA组24 h小腿引流管拔除率(100%)明显高于对照组(58.7%)(P<0.05)。
2.3 患者并发症情况
所有患者随访超过6个月,对照组和TXA组术后均未出现患肢足背麻木感及伸趾、伸踇无力,也未见下肢静脉血栓形成、肺栓塞、胃肠道反应和低血压等并发症。
3 讨论
FVFG可为股骨头提供良好力学支撑并有利于形成丰富的血运,已成为治疗ONFH的常用方法。腓骨是小腿的非主要承重骨,有研究发现腓骨中上段切取后对下肢负重及踝关节稳定性无影响[9-10]。然而,接受FVFG治疗的患者需要采用全身麻醉,可能会因为毛细血管阻力降低导致腓骨术中出血增加[16],截取腓骨后产生的断端髓腔出血、血管损伤或者肌肉组织的渗血均可能导致短暂的腓神经麻痹、疼痛及血肿等[11];供区切口关闭时皮肤软组织张力过大又会导致伤口感染等并发症[12],发生率为10%~40%[13-14]。引流管放置时间长容易增加逆行感染发生的风险,增加患者的护理负担,影响患者术后的早期锻炼,不利于康复。
TXA是赖氨酸的合成衍生物,通过与纤溶酶原上的赖氨酸位点结合,可减少纤维蛋白溶解和稳定血液凝块,进而减少出血[15]。目前,TXA已经广泛应用于心胸外科、妇产科、整形外科和骨科多种手术学科,可显著减少围手术期的失血量并降低输血率。作为迄今为止最大的创伤试验之一,抗纤溶治疗严重出血临床随机研究(CRASH-2)对来自40个不同国家的274家医院招募来的超过20 000名成年创伤患者进行评估,证实TXA可降低输血率和总失血量[16]。尚无任何研究可以证实围手术期使用TXA与血栓栓塞风险增加相关。
据大量文献报道,切口内局部应用TXA可减少围手术期失血量和输血率[17-18]。Abdel等[19]对640例全膝关节置换术患者予静脉注射和局部应用TXA,发现2种方式均可有效减少失血量并降低输血率。North等[20]在一项双盲随机对照研究中比较THR术中局部应用TXA和静脉注射TXA的效果后发现,TXA作为抗纤维蛋白溶解剂,2种应用方式在减少THR失血方面均安全有效。Drakos等[21]认为,对髓内钉治疗股骨粗隆间骨折的老年患者局部应用TXA,可显著降低失血量、输血量和医疗费用。Gillespie等[22]进行了一项单侧肩关节置换双盲随机对照研究,发现与安慰剂组相比,局部应用TXA的患者术后失血量明显减少,血红蛋白水平变化较小。局部应用TXA的优点是全身吸收范围最小,并可直接应用于出血点。TXA分子可以控制腓骨骨髓腔的活动出血点,削弱纤维蛋白单体和纤维蛋白原的蛋白水解作用,增加纤维蛋白凝血块的稳定性,进而有效减少受损血管和肌肉组织间的血液丢失。本研究结果显示,应用TXA的患者FVFG术后第一天负压引流球内出血量明显减少,术后24 h引流管拔除率为100%。
虽然TXA可减少围手术期失血量已得到证实,但其可能增加血栓形成风险也是不可忽视的重要问题。Huang等[23]对2 689例骨科手术患者应用TXA的安全性进行meta分析发现,TXA的应用并不会增加深静脉血栓形成的可能。本研究也选择了下肢静脉血栓发生率作为观察指标,发现应用TXA不会增加下肢深静脉血栓发生率,这可能由于局部应用的TXA主要分布在组织间隙中,仅在出血部位达到高治疗浓度,且没有广泛的全身分布,有助于降低血栓栓塞风险。
另一常见的TXA不良反应是胃肠道反应,包括术后恶心和呕吐,但其发生率很低。也有报道称,静脉注射TXA可引起明显的低血压。本研究采取的是局部使用,故患者术后未出现低血压情况。
综上所述,TXA局部应用不但能有效减少腓骨供区术后出血量,还提升术后24 h引流管拔除率,且不会出现恶心、呕吐或血栓形成等不良反应。

