低氧对恶性黑素瘤A375细胞中Nodal及细胞迁移相关蛋白表达的影响
谭自敏 杨成莲 钟桂书 曾凡才
1西南医科大学附属医院皮肤科,四川泸州,646000;2绵阳市第三人民医院皮肤科,四川绵阳,621000;3西南医科大学生物化学与分子生物学实验室,四川泸州,646000
众所周知,恶性黑素瘤是起源于黑素细胞的肿瘤,好发于皮肤,因其早期隐匿、病情进展快和致死率高等特点,又有人称其为“皮肤癌中之王”,晚期恶性黑素瘤的有效治疗仍是亟待解决的世界难题[1]。Nodal作为调节干细胞多潜能性、维持胚层发育和建立体轴等胚胎发育过程的关键因子,备受各个领域重视[2]。对比胚胎发育和癌症发生发展,不难发现两者在诸多方面具有相似性[3]。这也为通过靶向抑制Nodal来治疗恶性肿瘤的新思路提供了理论基础。Nodal的信号转导由位于细胞膜上的II型受体(ActR II)和I型受体(ALKs)介导,此后依次磷酸化胞内SMADs并调控相关靶基因表达。SB-431542是I型膜受体ALK5、ALK4和ALK7的有效抑制剂,它通过抑制ALK5/4/7阻断Nodal信号进一步转导的同时也阻断Nodal对自身的正反馈表达,起到“Nodal抑制剂”的作用。近年来,不断有研究表明Nodal能诱导细胞上皮-间质转化(epithelial-mesenchymal transition, EMT)。EMT过程中,细胞内许多分子如E-cadherin、MMP2和Vimentin蛋白的表达明显改变。这些明显变化的EMT标志物与细胞的形态、黏附力和运动能力紧密相关。因此这些分子也常被用于反映恶性肿瘤的迁移及侵袭能力。除此之外,恶性肿瘤的发展过程和其特有的微环境也密切相关。由于恶性黑素瘤体积增大速度快、局部血管生成相对减少等原因,它区别于正常组织的微环境特点之一便是低氧[3]。因此,本实验通过CoCl2体外造模和相关技术检测手段,旨在研究恶性黑素瘤A375细胞内低氧微环境对Nodal和肿瘤迁移及侵袭的影响。
1 材料和方法
1.1 材料 人恶性黑素瘤A375 细胞来源于中国科学院细胞库(上海)。CoCl2·6H2O、 SB-431542购买于Sigma公司(美国)。主要材料包括一抗人抗鼠Nodal抗体(美国Santa Cruz)、人抗鼠Vimentin抗体(美国Santa Cruz)、人抗鼠MMP2抗体(美国Santa Cruz)、人抗兔E-cadherin抗体(美国Santa Cruz)、人抗兔ALK4抗体(英国 Abcam)和人抗鼠ALK7抗体(英国 Abcam)。二抗主要包括HRP标记羊抗兔IgG(美国 Bioworld)和HRP标记羊抗小鼠IgG(美国 Bioworld)。
1.2 方法
1.2.1 细胞培养 取出前期冻存的恶性黑素瘤A375细胞,快速复苏细胞后,于培养瓶中加入新鲜配置的含10% FBS的完全培养基。将培养瓶放置于37℃、含5% CO2的恒温细胞孵育箱中培养。间隔一日更换一次培养液。显微镜下观察细胞均匀铺满瓶壁约80%后,加入0.25%的胰蛋白酶消化并以3000 r/min的速度在4℃下完成离心,视细胞状态以1∶3或1∶2传代继续培养。
1.2.2 氯化钴(CoCl2)诱导细胞内低氧 本课题组前期实验已找到CoCl2诱导低氧所需的最佳时间及浓度,并成功构建低氧模型[4]。本实验将采取前期结论所得,即在孵育时间为48 h,浓度为150 μmol/L条件下进行后续实验。
1.2.3 SB-431542阻断Nodal信号通路 A375细胞培养至第3~8代对数生长期时进行SB-431542干预处理。将SB-431542母液用5%的FBS溶液分别稀释至浓度为5 μmol/L、10 μmol/L、20 μmol/L、30 μmol/L、40 μmol/L。将细胞悬浮后以每孔约5×103个接种于96孔板内继续培养12 h至细胞贴壁。分组加入配置好的SB-431542溶液,每组设置5个复孔,分别继续培养在37℃、5% CO2的细胞孵育箱中24 h、48 h和72 h。采用MTT法探索SB-431542对细胞增殖的影响并确定后续实验所需的适宜浓度和时间。
1.2.4 MTT法检测细胞增殖活力 按实验步骤分浓度、分时间进行SB-431542阻断后,在避光条件下于每孔内加入MTT溶液20 μL,继续培养细胞4 h。吸除培养液并加入DMSO 150 μL,震荡10 min以充分溶解晶体。用波长为490 nm的酶联仪测定各孔的吸光度值(OD值)。
1.2.5 Western Blot方法检测蛋白水平 将A375细胞以约5×105个/孔接种于6孔板内,培养至贴壁后弃培养液。实验按分组分别进行干预(表1)。药物干预后分别提取每孔细胞的总蛋白。利用BCA法计算细胞内所测蛋白的浓度。接下来依次进行SDS-PAGE电泳分离、目标蛋白转PVDF膜、室温封闭1 h(5%脱脂牛奶)处理。加入目标蛋白一抗并于4℃孵育过夜。次日洗膜后用所测蛋白二抗于25℃下孵育1.5 h。最后利用ECL法显影,利用Image Lab软件分析。

表1 实验分组

2 结果
2.1 Nodal抑制剂SB-431542抑制恶性黑素瘤A375细胞增殖 恶性黑素瘤A375细胞被不同浓度及不同作用时间的SB-431542孵育后,MTT法检测结果如图1。差异具有统计学意义(P<0.05)。相同时间下加入的Nodal抑制剂浓度越大,A375细胞的增殖活性越低。相同浓度下Nodal抑制剂对细胞的作用也呈现时间依赖性。当Nodal抑制剂SB-431542的浓度大于30 μmol/L时,其对细胞的毒性作用显著增大,细胞增殖活性显著降低。许多涉及SB-431542处理的文献显示,将其浓度稀释至10 μmol/L并再继续培养细胞48 h,此时测得的增殖活性较低,但毒性作用不显著。这与本实验研究结果一致,故后续实验Nodal抑制剂选择此浓度和时间。
2.2 低氧诱导细胞内Nodal、ALK4和ALK7蛋白表达 构建细胞内低氧微环境模型并加入Nodal抑制剂处理后,分别检测各实验组恶性黑素瘤A375细胞内Nodal和ALK4/7的浓度。结果如图2所示。CoCl2组细胞内Nodal和ALK7蛋白的浓度较空白组增加,而CoCl2+SB-431542组蛋白的表达较CoCl2组明显下降。在本研究的A375细胞株中,多次重复实验均没有检测到ALK4的存在。
2.3 低氧诱导E-cadherin、MMP2和Vimentin蛋白表达 利用免疫印迹法检测与恶性黑色瘤A375细胞迁移和侵袭相关蛋白的表达,检测结果如下图3所示。CoCl2组细胞内MMP2和Vimentin蛋白浓度较空白组增加(P<0.05)。CoCl2+SB-431542组细胞内的蛋白浓度仍高于空白对照组,但低于CoCl2组。本研究小组多次重复实验发现A375细胞内E-cadherin蛋白的各组组间差异不具有统计学意义。

(**P<0.01)
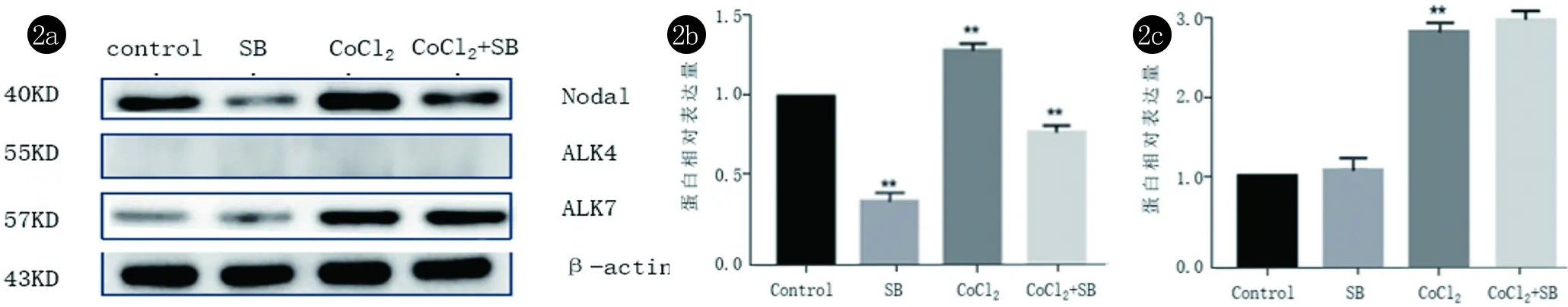
2a:A375细胞经或不经SB-431542和(或)CoCl2干预后用western blot检测Nodal及其受体ALK4/7的条带显示;2b:以β-actin为内参,Nodal在各组中的相对表达水平;2c:以β-actin为内参,ALK7蛋白在各组中的相对表达水平。2b、2c与空白对照组相比,**P<0.01图2 各处理组Nodal及其受体ALK4/7蛋白的表达水平
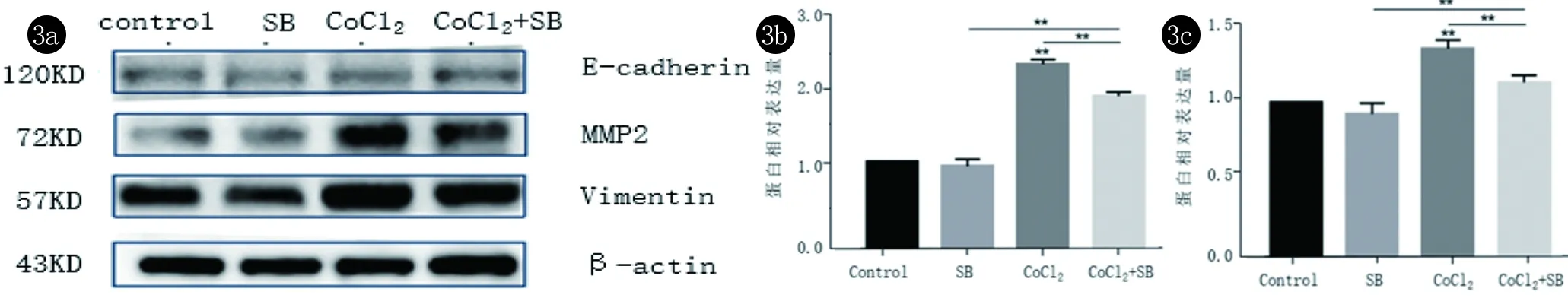
3a:A375细胞经或不经SB-431542和(或)CoCl2干预后用western blot检测与迁移及侵袭相关蛋白的条带显示;3b:以β-actin为内参,MMP2蛋白在各组中的相对表达水平;3c:以β-actin为内参,Vimentin蛋白在各组中的相对表达水平。3b、3c中与空白对照组相比,**P<0.01图3 各处理组MMP2、Vimentin、E-cadherin的表达水平
3 讨论
恶性黑素瘤发生发展过程中的信号级联体系错综复杂,目前机制尚不完全清楚。鉴于胚胎发育过程与恶性肿瘤发生发展过程的相似性,恶性肿瘤研究也越来越多地同胚胎发育联系在一起。Nodal通过诱导干细胞分化、参与原始胚层形成等途径促进胚胎发育已经得到证实,故此猜测Nodal也可能是治疗恶性肿瘤的潜在靶点[6]。Nodal在个体胚胎时期呈现显著高表达状态,随着各个系统逐渐形成和完善,大多数组织和器官的表达逐渐减少直至关闭[7]。根据国内外多项在常氧条件下进行的研究结果表明,Nodal在恶性黑素瘤细胞中已关闭的表达通道再次开启,并被证实其表达程度随着肿瘤细胞增殖和侵袭能力的增加而增加[8]。恶性黑素瘤的分化程度极低,较之其他高分化癌症,其更容易处于低氧状态。因此,在模拟体内的低氧微环境下研究Nodal对恶性黑素瘤细胞迁移及侵袭的影响更加准确客观。
本实验小组延续前期实验中成功构建的低氧模型,通过免疫印迹法检测细胞内Nodal及其受体的浓度。遗憾的是,各实验组通过免疫印迹法没有检测到ALK4蛋白,猜测可能与细胞内ALK4浓度低有关。我们后续将设置不同的实验方案探索原因。与既往研究结果相比,本实验不但同样发现Nodal在恶性黑素瘤A375细胞中呈现再次高表达状态,同时也证实低氧环境能诱导Nodal进一步表达。基于此推测在人体内,由肿瘤细胞高代谢等原因引起的低氧可能会增加Nodal的表达。
为探讨Nodal在肿瘤进展中可能的机制,接下来利用免疫印迹法检测与恶性肿瘤迁移及侵袭相关蛋白的浓度。结果显示,Nodal抑制剂SB-431542可以部分逆转由低氧引起的胞内MMP2的表达。MMP2是重要的降解IV型胶原蛋白的蛋白水解酶。它不仅可以通过降解细胞外基质的方式破坏肿瘤细胞外的第一层屏障[10],同时也可以促进新生血管生成,从而加快肿瘤发展。实验结果表明,低氧诱导的Nodal高表达可能通过增加MMP2蛋白的水平来促进恶性黑素瘤细胞迁移及侵袭。
除此之外,本实验小组还检测了A375细胞内Vimentin蛋白的水平变化。Vimentin蛋白对细胞形态的维持和改变取决于其特殊构象。当Vimentin蛋白上游受刺激而浓度升高时,由于收缩作用增加,细胞逐渐向利于运动的梭形变化,从而加强肿瘤细胞的迁移[12]。本实验所得Vimentin蛋白的变化趋势与MMP2蛋白检测结果相似。即低氧增加胞内Nodal浓度,进而可能通过增加细胞内Vimentin蛋白的浓度来促进恶性黑素瘤细胞的迁移及侵袭。
E-cadherin是判断恶性肿瘤的发生、发展及预后的有效指标之一,其胞内浓度可间接反映细胞间的黏附能力。当胞内、胞外刺激导致E-cadherin蛋白表达受抑制时,恶性肿瘤细胞之间的黏附力随之减弱,细胞的癌旁浸润和远处转移能力随之增强[11]。故此,我们推测低氧诱导下Nodal的促肿瘤机制也与E-cadherin有关。但在实验中我们发现,低氧及Nodal抑制剂对胞内E-cadherin蛋白的表达差异并不显著。究其原因,一可能是A375细胞内E-cadherin蛋白的表达主要受其他途径调控;二可能是恶性黑素瘤的分化程度低,其在A375细胞内的浓度不高,上游的表达变化并不足以引起显著改变。
综上所述,低氧诱导Nodal高表达可能通过上调MMP2和Vimentin蛋白水平,从而促进恶性黑素瘤细胞的迁移及侵袭。我们下一步将继续进行划痕试验和基因水平验证低氧诱导Nodal高表达对A375细胞迁移及侵袭能力的影响。本实验通过模拟低氧微环境,初步探索了Nodal在恶性黑素瘤的迁移及侵袭过程中可能的作用途径,在探索肿瘤进展的生物学标志物以及肿瘤治疗靶点有一定的意义。

