气相色谱-质谱法测定再造烟叶中甲酰胺
张建平,吴清辉,邓其馨,黄朝章,黄胜翰
(福建中烟工业有限责任公司技术中心,厦门361021)
甲酰胺是一种用途极广的化工原料和工业溶剂,具有活泼的反应性和特殊的溶解能力,可作为纸张处理剂[1-2]。但是长期吸入甲酰胺会对人的呼吸系统、神经系统、血管系统、肝脏系统等造成伤害,甲酰胺被欧盟化学品管理局列为生殖毒性物质,被国际癌症研究中心列为1B 类致癌物质[3-5]。再造烟叶在采用造纸法生产的工艺过程中可能引入甲酰胺污染,因此有必要对再造烟叶进行甲酰胺测定,以保证产品质量安全[6-7]。文献已报道的测定甲酰胺的方法均为气相色谱法,检测器主要采用氢火焰离子化检测器(FID)或氮磷检测器(NPD)。这两类方法虽然操作简单,但选择性不强,容易出现假阳性结果[8-12]。气相色谱-质谱法(GC-MS)通过采集离子碎片进行测定,定性的准确性高,是当前研究甲酰胺测定的热点[13-15],但所涉及的对象多为泡沫、塑料、玩具等,再造烟叶中甲酰胺的测定鲜有报道。
本工作采用甲醇涡旋振荡提取的方法,建立了测定再造烟叶中甲酰胺的气相色谱-质谱法,旨在为有效监控再造烟叶中的甲酰胺提供方法参考。
1 试验部分
1.1 仪器与试剂
Agilent GC6890/MSD5973 型 气 相 色 谱-质 谱联用仪;Labnet VX-200 型涡旋混合仪;Sartorius Sigma 1-14 型高速离心机;Millipore Milli-Q 型超纯水仪;有机相滤膜(0.45μm)。
甲酰胺标准储备溶液:1 000 mg·L-1,称取100.0 mg的甲酰胺标准品,用甲醇溶解并定容于100 m L的容量瓶中。
甲酰胺标准品的纯度大于99.5%(避光保存于0~4 ℃下);甲醇、乙腈、丙酮、异丙醇和二氯甲烷均为色谱纯;试验用水符合GB/T 6682-2008《分析实验室用水规格和试验方法》中一级水的规定。
1.2 仪器工作条件
1) 色谱条件 DB-Wax 毛细管色谱柱(0.32 mm×30 m,0.25μm);进样口温度230℃;载气为氦气,载气流量2 m L·min-1;分流进样,分流比10∶1;进样量1μL。升温程序:初始温度80℃,保持2 min;以15 ℃·min-1速率升温至210 ℃,保持2 min。
2)质谱条件 电子轰击离子源(EI);溶剂延迟3 min;接口温度230 ℃;选择离子监测(SIM)模式,SIM 监测离子质荷比(m/z)为45,44,29,17,其中m/z 45为定量离子。
1.3 试验方法
试验所用国内生产的再造烟叶样品共20 个(1#~20#),均为片状。
按YC/T 31-1996《烟草及烟草制品 试样的制备和水分测定 烘箱法》中的方法制备再造烟叶样品并测定水分。
称取1.000 0 g再造烟叶样品于50 m L 具塞三角瓶中,加入15.0 m L甲醇,涡旋振荡5 min。收集上层清液,经有机相滤膜过滤,按仪器工作条件进行测定。
2 结果与讨论
2.1 色谱行为
按仪器工作条件对甲酰胺标准溶液进行测定,其色谱图见图1。按试验方法对再造烟叶阳性样品进行分析,其色谱图见图1。
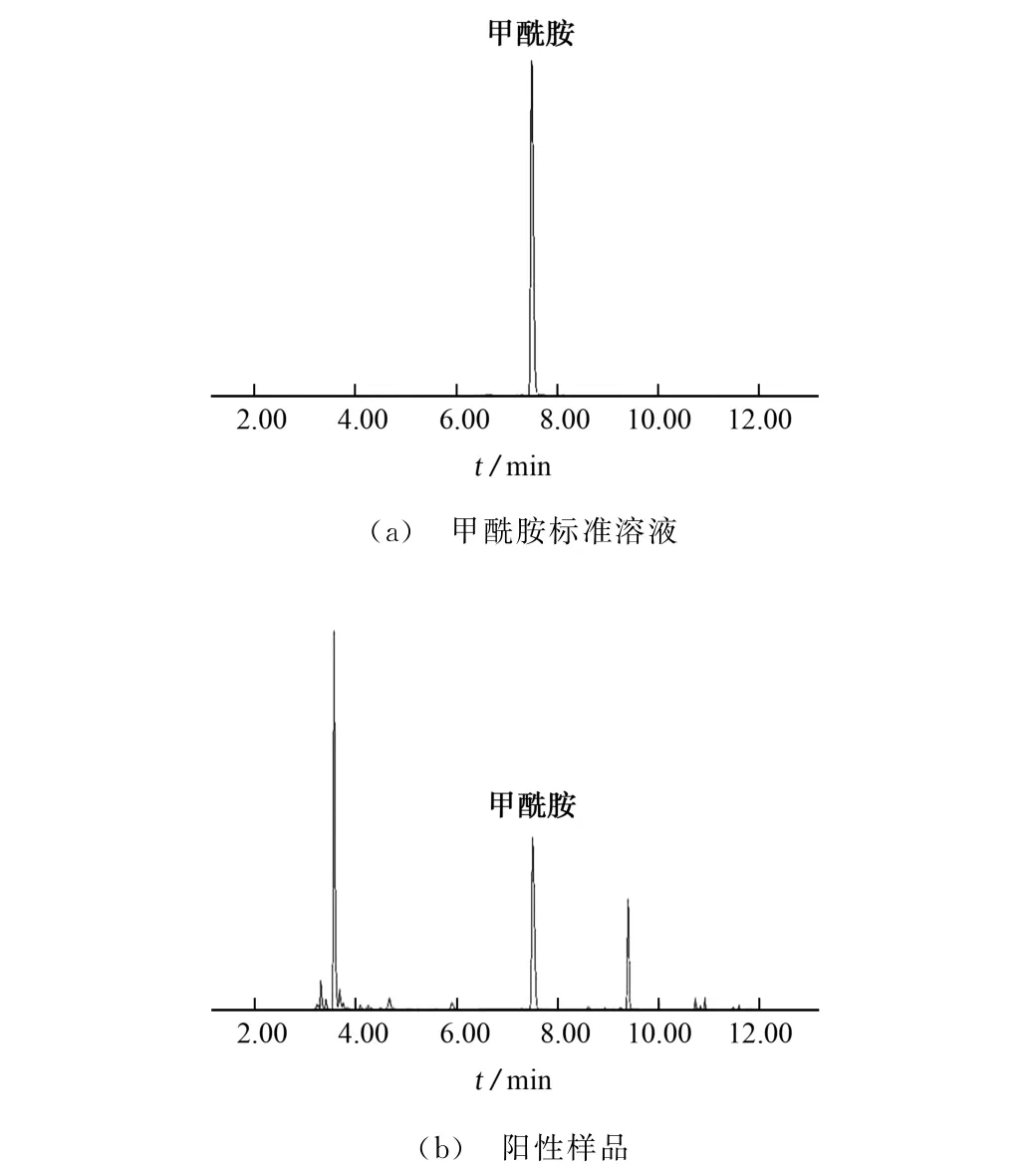
图1 甲酰胺标准溶液和阳性样品的色谱图Fig.1 Chromatograms of formamide standard solution and the positive sample
2.2 仪器工作条件的选择
2.2.1 色谱柱
试验分别考察了 HP-5 毛细管色谱柱(0.32 mm×30 m,0.25μm)、DB-Innowax毛细管色谱柱(0.32 mm×30 m,0.25μm)和DB-Wax毛细管色谱柱(0.32 mm×30 m,0.25μm)对甲酰胺分离效果的影响。结果发现:使用HP-5毛细管色谱柱时,甲酰胺的峰形不对称,不利于定量;使用DB-Innowax毛细管色谱柱时,甲酰胺的峰形稍微改善,但效果不太明显;使用DB-Wax毛细管色谱柱时,甲酰胺的峰形对称,符合定量要求,且能较好地分离甲酰胺和其他未知化合物。试验选用DB-Wax毛细管色谱柱。
2.2.2 质谱条件
在全扫描模式下扫描m/z 16~50内的离子碎片,甲酰胺的质谱图见图2。

图2 甲酰胺的质谱图Fig.2 MS spectrum of formamide
由图2 可知:甲酰胺的主要离子碎片m/z 为45,44,29,17,选择这些主要离子碎片进行选择离子测定,其中响应最强的离子碎片(m/z 45)作为定量离子。甲酰胺在电子轰击电离作用下,C-H、C-N极易断裂,形成CH2NO(m/z 44)、CHO(m/z 29)、NH3(m/z 17)的碎片。试验选择的质谱条件见1.2节。
2.3 样品前处理方法的选择
2.3.1 提取溶剂
甲酰胺是小分子极性化合物,根据“相似相溶”原理及气相色谱-质谱仪的溶剂适应性,并参考文献[16-18],选取甲醇、乙腈、丙酮、异丙醇和二氯甲烷等5种极性溶剂作为提取溶剂进行考察。按试验方法采用上述提取溶剂对再造烟叶样品15#进行分析,平行测定3 次。结果表明:采用甲醇、乙腈、丙酮、异丙醇和二氯甲烷作为提取溶剂时,甲酰胺的测定 值 依 次 为17.20,16.53,13.26,15.74,11.48 mg·kg-1。
对上述5种提取溶剂所得提取液的基质进行考察。结果表明:基质干扰均较小。甲醇对甲酰胺的提取效率最高,试验选择提取溶剂为甲醇。
2.3.2 提取溶剂的用量
试验考察了提取溶剂甲醇的用量依次为5.0,7.5,10.0,12.5,15.0,20.0 m L 时 对 甲 酰 胺 测 定 值 的影响,结果见图3。
由图3可知:当甲醇用量为5.0~12.5 m L 时,随着甲醇用量的增加,甲酰胺的测定值逐渐增大;继续增加甲醇用量,甲酰胺的测定值变化不明显。综合以上结果,同时为了保证提取完全,试验选择提取溶剂甲醇的用量为15.0 m L。
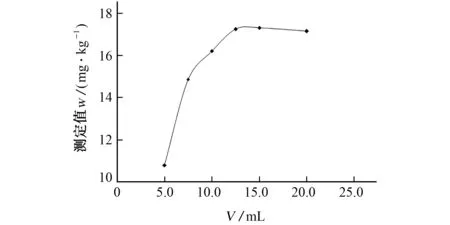
图3 甲醇的用量对甲酰胺测定值的影响Fig.3 Effect of amount of methanol on determination value of formamide
2.3.3 提取方法和提取时间
甲酰胺的提取可采用顶空提取、微波提取、超声波提取和索氏提取。顶空提取适合于提取空气(气态)中的甲酰胺,后3种方法常用于提取固态和液态介质中的甲酰胺[8-18];微波提取和索氏提取易造成目标物损失;超声波提取的效果最好,但需要较长的时间。涡旋振荡提取是一种新兴的提取方法,其振荡频次可达到2 000 r·min-1,是普通旋转振荡的10倍,可极大地缩短振荡时间、提高提取效率。试验考察了提取时间依次为1,2,3,5,7,10,15,20,30 min时超声波提取和涡旋振荡提取对甲酰胺测定值的影响,结果见图4。
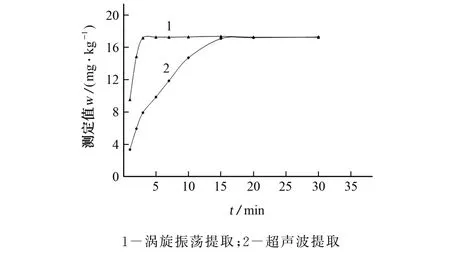
图4 提取方法和提取时间对甲酰胺测定值的影响Fig.4 Effect of extraction method and extraction time on determination value of formamide
由图4 可知:超声波提取的提取时间小于15 min时,甲酰胺的测定值随提取时间的延长而增大;超声波提取的提取时间大于15 min时,甲酰胺的测定值变化不明显;涡旋振荡提取的提取时间小于3 min时,甲酰胺的测定值随提取时间的延长而增大;涡旋振荡提取的提取时间大于3 min时,甲酰胺的测定值变化不明显。为了节省时间,提高提取效率,同时保证提取完全,试验选择涡旋振荡5 min进行提取。
2.4 标准曲线和检出限
用甲醇稀释1 000 mg·L-1的甲酰胺标准储备溶液,得到0.1,0.5,1.0,2.0,5.0 mg·L-1的甲酰胺标准溶液系列,按仪器工作条件对上述甲酰胺标准溶液系列进行测定,并绘制标准曲线。结果表明:甲酰胺的质量浓度在0.1~5.0 mg·L-1内与其对应的峰面积呈线性关系,线性回归方程为y=2.035×104x+7.424×104,相关系数为0.999 0。
分别按3倍和10倍信噪比计算甲酰胺的检出限(3S/N)和测定下限(10S/N),结果依次为0.01,0.04 mg·L-1。
2.5 重复性
为了考察方法的重复性,对再造烟叶样品15#进行重复3 d的分析,每天进行6次平行测定。结果表明:日内相对标准偏差(RSD)为2.5%~3.0%,日间RSD 为4.4%。
2.6 回收试验
按试验方法对再造烟叶样品15#进行加标回收试验,计算回收率,结果见表1。

表1 回收试验结果Tab.1 Results of test for recovery
由表1可知:回收率为92.5%~105%。
2.7 样品分析
按试验方法对20个再造烟叶样品进行分析,在部分样品中检出了甲酰胺,结果见表2。将本方法与常规的气相色谱法(配FID)[7]进行比对试验,结果见表2。
由表2可知:检出率约为30%,测定值在4.11~33.97 mg·kg-1之间。阳性样品的两组测定结果经t检验后发现:t=0.498,小于1.812(置信区间小于0.05)。这说明两种测定方法无显著性差异。
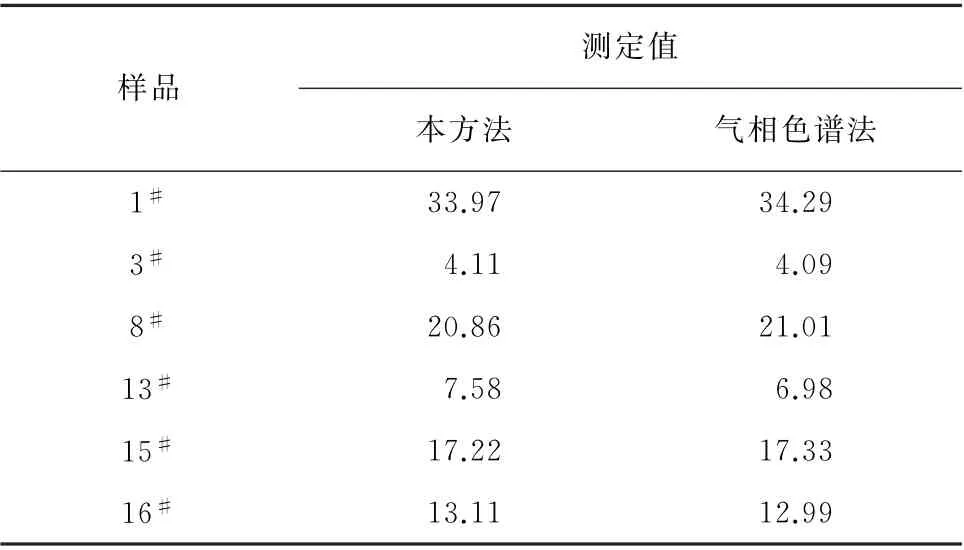
表2 样品分析结果Tab.2 Analytical results of the samples mg·kg-1
在日常的大量样品分析中,发现了常规的气相色谱法假阳性高的问题。气相色谱法和气相色谱-质谱法同时分析的486个样品中有35个样品用气相色谱法分析为阳性,而用气相色谱-质谱法分析为阴性,气相色谱法的误检率为7.2%。这是由于再造烟叶作为植物再加工产品,生产过程中可能在烟叶中加入了助剂、填料、涂布液等物质,导致样品提取液的基质较为复杂,气相色谱法单纯地采用保留时间进行定性,提取液中的色素等可能在相同的时间出峰,造成了分析的假阳性。气相色谱-质谱法在锁定保留时间的同时,还获取了甲酰胺的离子碎片及离子碎片丰度比信息,只有这3个信息均与标准样品一致才会被定义为甲酰胺,因此极大地排除了分析的假阳性。
本工作采用气相色谱-质谱法测定再造烟叶中甲酰胺的含量。本方法操作简单、效率高、适合于再造烟叶中甲酰胺的测定。

