Ce修饰NaY分子筛负载PdO纳米晶催化剂用于苯的催化氧化反应
赵 波,王 卓,叶 娜,左树锋*
(1.绍兴文理学院,浙江 绍兴 312000; 2.台州学院,浙江 台州 318000)
挥发性有机化合物(VOCs)是一类毒性大、污染严重的化学物质,来源广,排放量大,严重威胁人类健康,极大破坏了生态平衡,并制约社会的可持续发展[1]。目前,有许多技术可用于VOCs消除治理,催化氧化技术具有起燃温度低、节省能源、适用范围广、处理效率高、最终产物为CO2和H2O、无二次污染等优点,成为目前最具有应用前景的消除VOCs的方法[2]。
对于VOCs催化氧化反应,高效催化剂的开发极为重要。按照活性组分不同,大致可以分为贵金属催化剂[3-5]、过渡金属氧化物催化剂[6-9]和稀土复合氧化物催化剂[10-12]。贵金属类催化剂具有起燃温度低、低温活性好、催化活性高、催化降解彻底和产物选择性高等特点,在实际处理VOCs过程中一直被广泛使用。其中,Pt[5]、Pd[4,13-15]和Au[3,16]是常用的贵金属催化剂。Liu Ji等[15]采用不同气氛处理Pd/γ-Al2O3,研究其对苯催化氧化的影响。He Chi等[17]采用Pd/ZSM-5/MCM-48催化剂研究其对苯氧化的活性。Wang Yu等[18]在Pt/Al2O3中掺杂少量的钾研究其对二氯甲烷的催化氧化性能。相对于其他贵金属,Pd基催化剂在相对较低温度下具有活性高、热稳定性高、抗失活性能强和耐湿性强。因此,众多研究者致力于Pd基催化剂的研究。由于贵金属稀少且价格昂贵,因此,在保证催化剂高活性和稳定性的条件下,减少贵金属用量是研究的热点。稀土元素特别是Ce具有特殊的外层电子结构(4f)且能够提供活泼晶格氧,使其具有良好的存储和释放氧的能力[19-20]。将稀土与Pd金属结合在一起,降低Pd颗粒尺寸,有利于提高其在催化剂上的分散,同时减少Pd颗粒的烧结和用量,且稀土元素与Pd相互作用,可以增加晶格氧的流动性,有利于VOCs催化氧化。
众所周知,载体对催化剂催化性能有重要影响,特别是氧化过程。目前,研究较多的用于VOCs催化降解的分子筛包括ZSM-5、NaY和MCM[21-25]等。其中,NaY分子筛作为沸石分子筛的一种,具有较均匀微介孔结构、大比表面积和高稳定性,且对各类有机废气具有广谱吸附性等特点。因此,NaY分子筛作为载体,有利于活性组分的分散,减少活性组分用量,降低催化剂成本。
本文通过高温液相还原法制备一系列不同Ce负载量的Pd/Ce/NaY催化剂,该催化剂使PdO以较小的晶粒均匀稳定地分散在载体上,有利于提高催化剂对苯的催化氧化性能。通过活性评价、N2吸附-脱附、XRD、HRTEM-EDS、H2-TPR 、O2-TPD 和 TPSR等,系统探讨该催化剂对苯催化氧化过程中结构与功能之间的关系。
1 实验部分
1.1 原 料
NaY分子筛,南开大学分子筛厂,100%;六水合硝酸铈,分析纯,上海化学试剂公司;H2PdCl4,分析纯,国药集团化学试剂有限公司。
1.2 催化剂制备
Ce/NaY催化剂的制备:将NaY分子筛经压片、粉碎、过筛后,取粒径(40~60)目的NaY于马弗炉中500 ℃空气气氛中焙烧2 h。以焙烧后的NaY分子筛为载体,等体积浸渍定量的Ce(NO3)3溶液,室温放置12 h,110 ℃烘干后400 ℃焙烧2 h。各样品上Ce负载质量分数分别为2%、4%、6%、8%和10%,样品标记为x%Ce/NaY(x=2,4,6,8和10)。
Pd/Ce/NaY催化剂的制备:采用一步高温液相还原法制备Pd/Ce/NaY催化剂。取2.0 g上述Ce/NaY样品和适量乙二醇于三口烧瓶中,搅拌均匀,加入10 mg·mL-1的H2PdCl4水溶液,混合液在高纯氮气保护下搅拌过夜,用NaOH调节混合液pH=11,再将混合液165 ℃搅拌3 h,冷却至室温后离心分离,干燥,400 ℃焙烧2 h。得到不同Ce含量的Pd纳米晶催化剂,催化剂中Pd质量分数为0.2%。催化剂标记为0.2%Pd/x%Ce/NaY(x=2,4,6,8和10)。
1.3 催化剂活性评价
活性评价在天津先权有限公司催化剂评价装置WFS-3010上进行。反应空速20 000 h-1,反应物苯浓度1 000×10-6。反应器进、出口反应物浓度用Shimadzu GC-14C气相色谱仪(FID)在线检测,由色谱工作站记录分析数据,使用质谱(MS,QGA,Hiden,UK)检测最终产物。苯转化率为:
式中,C1为反应器进口苯浓度,C2为反应器出口苯浓度。T50和T90分别表示苯转化率达50%和90%时对应的反应温度。
1.4 催化剂表征
样品比表面积和孔结构采用美国麦克仪器公司TrisStar Ⅱ 3020 apparatus全自动物理化学吸附仪在液氮温度-196 ℃下测定,样品200 ℃真空脱气4 h,然后测定。比表面积采用BET公式计算,孔体积和孔径分布按照BJH模型计算。微孔孔容按照HK模型计算。
催化剂和载体的物相结构在荷兰帕纳科公司EMPYREAN型X射线粉末衍射仪上进行,CuKα,扫描速率0.02°·s-1。扫描范围10°~80°。
样品形貌采用JEM-2100F型透射电镜HRTEM获得,EDS实验利用OXFARD INCA仪器测定,确定样品化学组成。
H2程序升温还原(H2-TPR)在美国康塔仪器公司CHEMBET-3000仪器上测定。将50 mg样品装入石英U型管中,300 ℃空气气氛处理30 min,降温至40 ℃,将气氛切换为5%H2-Ar混合气(40 mL·min-1)。以10 ℃·min-1速率程序升温至850 ℃,用热导检测器(TCD)连续检测尾气中氢气的浓度变化,并记录程序升温还原谱线。
O2程序升温脱附(O2-TPD)在WFS-3010仪器上进行,取350 mg样品置于反应管中,5%O2/Ar(99.99%,60 mL·min-1)气氛中300 ℃预处理30 min,冷却至50 ℃,以7.5 ℃·min-1速率升温至1 000 ℃,采用GC-MS(QGA,HIDEN)在线检测O2浓度的变化。
苯程序升温表面反应(Benzene-TPSR)的反应气路与评价装置相同,取350 mg样品置于反应管中,高纯氮气氛中300 ℃预处理30 min,冷却至50 ℃,对苯进行吸附,平衡后以7.5 ℃·min-1速率将温度升至500 ℃,采用GC-MS在线检测苯和CO2浓度的变化。
2 结果与讨论
2.1 XRD
图1为NaY、0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的XRD图。

图1 NaY、0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的XRD图Figure 1 XRD patterns of NaY,0.2%Pd/NaY and 0.2%Pd/8%Ce/NaY
由图1可以看出,负载PdO和CeO2的催化剂保持NaY的特征衍射峰,表明催化剂制备过程中载体的结构没有被破坏,NaY稳定性良好。与NaY相比,0.2%Pd/8%Ce/NaY的衍射峰强度减弱,这可能是因为活性组分和助剂负载后降低了NaY 在整个催化剂中的相对含量,导致其特征衍射峰降低。此外,图中没有出现PdO和CeO2特征衍射峰,这可能是因为PdO和CeO2的含量低并且高度分散在NaY载体上,从而低于XRD检测限。
2.2 N2吸附-脱附
图2为不同样品的N2吸附-脱附等温曲线和孔径分布。由图2可以看出,等温线均属于具有滞后环的Ⅳ型等温曲线,各样品的滞后环均为H3型,表明样品具有层状结构的微-介孔结构[24],且负载后的催化剂保留载体原有的孔结构特征。与NaY相比,0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的N2吸附能力降低。

图2 不同样品的N2吸附-脱附等温曲线和孔径分布Figure 2 N2 adsorption-desorption isotherms and pore size distribution of the samples
表1为不同样品的比表面积和孔容。由表1可以看出,负载CeO2和PdO后,部分NaY的孔被堵塞,导致催化剂BET比表面积和总孔容均有所下降,使得催化剂物理吸附N2能力降低。结合样品孔径分布可以看出,NaY 分子筛的介孔尺寸分布主要集中在3.93 nm和43.8 nm,负载PdO和CeO2后,催化剂介孔尺寸分布没有改变,表明NaY比表面积较大,且孔结构稳定,是良好的载体材料。另外,结合催化剂活性评价可以看出,催化剂活性高低和比表面积的大小没有必然联系。

表1 不同样品的比表面积和孔容
①相对压力0.99;②Horvath和Kawazoe方法
2.3 HRTEM-EDS
图3为NaY、0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的HRTEM照片,图4为0.2%Pd/NaY 和0.2%Pd/8%Ce/NaY 的EDS谱图。

图3 NaY、0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的HRTEM照片Figure 3 HRTEM images of NaY,0.2%Pd/NaY,and 0.2%Pd/8%Ce/NaY
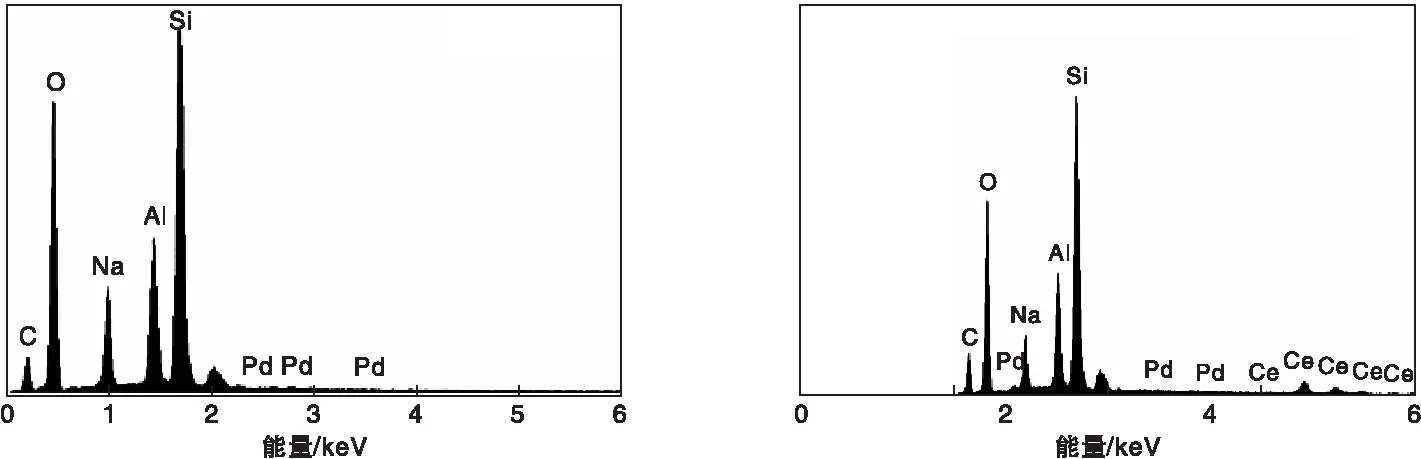
图4 0.2%Pd/NaY 和0.2%Pd/8%Ce/NaY 的EDS谱图Figure 4 EDS spectra of 0.2%Pd/NaY and 0.2%Pd/8%Ce/NaY
由图3可以看出,NaY分子筛具有均匀的层状结构,与N2吸附-脱附表征结果一致。作为载体材料,这种层状结构在催化氧化反应中有利于气体的传输,提高气体传输效率,有利于增加反应效率。负载PdO后,载体保持层状结构,PdO含量较低且分散在载体表面,PdO纳米晶粒直径约(3~5) nm。负载PdO和CeO2后,没有破坏载体的层状结构,进一步证实NaY的稳定性,这与孔分布和XRD表征结果一致。PdO和CeO2以纳米颗粒形式均匀分散在NaY载体表面,结合图4可以看出,PdO以较小颗粒形式分散在CeO2周围,在催化反应过程中可以充分发挥活性组分PdO和助剂CeO2的相互协同作用,因此,0.2%Pd/8%Ce/NaY表现出最好的催化活性。
表2为0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的元素含量。由表2可以看出,0.2%Pd/8%Ce/NaY上含有Pd、Ce和O元素,且Pd质量分数为0.22%,表明活性组分很好地负载于载体上。
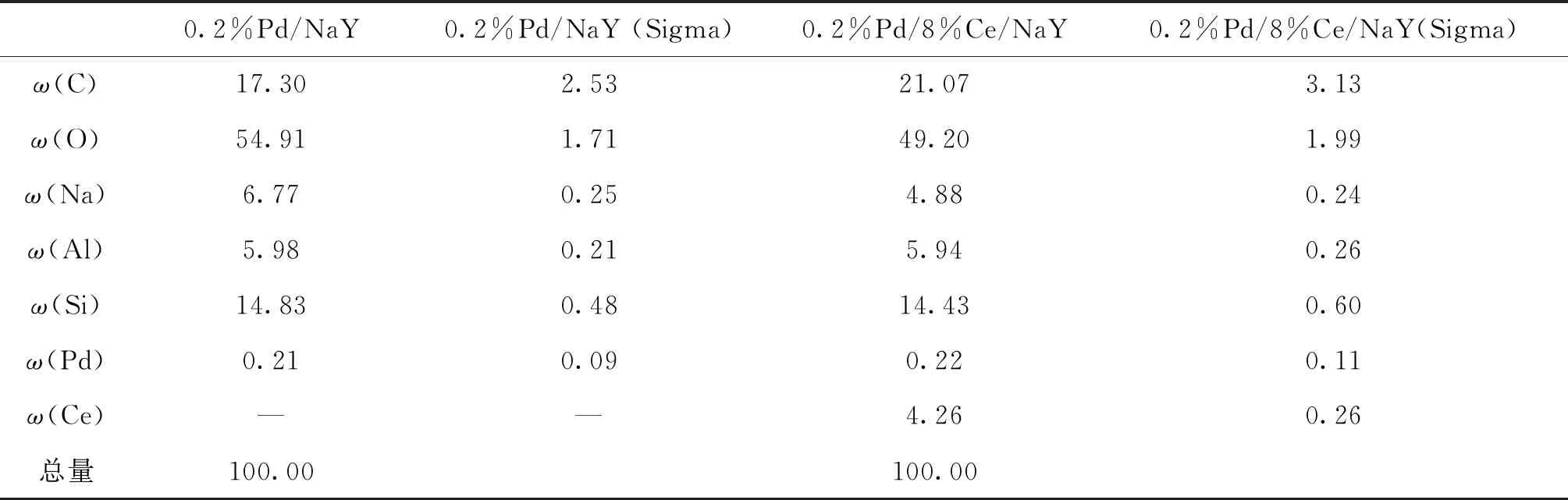
表2 0.2%Pd/NaY和0.2%Pd/8%Ce/NaY的元素含量
2.4 H2-TPR
在测试范围内NaY没有明显的H2消耗峰,PdO的耗氢峰低于100 ℃,且差别不大。耗氢峰仅表明不同催化剂中CeO2的还原性能差别。图5为不同催化剂的H2-TPR谱图。由图5可以看出,8%Ce/NaY出现2个耗氢峰,分别位于548 ℃和753 ℃,分别归属于CeO2表面氧和体相氧的还原峰[26-27]。与8%Ce/NaY相比,加入贵金属Pd后,Pd/x%Ce/NaY(x=2~10)中CeO2的还原性能明显提高,还原温度分别降低至约 525 ℃和620 ℃,特别是难还原的体相氧,温度降低近133 ℃。研究表明,贵金属Pd的存在会有氢溢流现象[28],即活性氢从贵金属表面溢流到和Pd相邻的其他组分表面。因此加入活性组分PdO后,PdO和CeO2相互作用,更多的活性氢存在于CeO2表面,同时CeO2中氧空穴的存在使传输到表面的体相氧能够在较低温度下还原。比较0.2%Pd/x%Ce/NaY(x=2~8)的还原性能可以看出,随着CeO2质量分数由2%增大至8%,催化剂耗氢峰位置没有变化,但是体相氧的耗氢峰强度逐渐增大,并且起始还原温度逐渐下降,由0.2%Pd/2%Ce/NaY的476 ℃降至0.2%Pd/8%Ce/NaY的421 ℃,下降了55 ℃。这是因为在2%~8%范围内,随着CeO2含量增大,催化剂中氧空穴数目增多,并且在这个范围内CeO2和PdO的相互作用增强,因此,0.2%Pd/8%Ce/NaY表现出最好的还原性能。但是,当CeO2质量分数进一步增大至10%时,与0.2%Pd/8%Ce/NaY相比,0.2%Pd/10%Ce/NaY的起始还原温度明显提高,并且体相氧的耗氢峰显著变小,这是因为随着CeO2含量进一步增大,一方面CeO2颗粒的粒径变大,使体相氧的传输阻力增大;另一方面,过多过大的CeO2颗粒包覆PdO粒子,使得CeO2颗粒表面的活性氢数量明显减少,导致0.2%Pd/10%Ce/NaY的还原能力变差。综上所述,可以看出0.2%Pd/8%Ce/NaY氧空穴数目较多,并且和PdO的相互作用最强,表现出最好的还原能力,在催化剂活性评价中表现出最好的苯氧化能力。
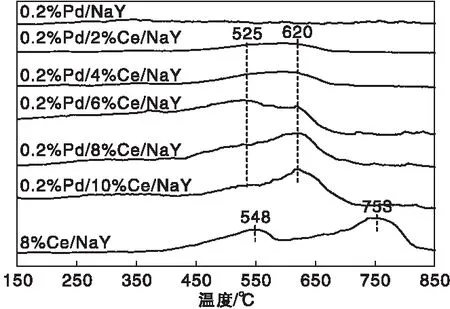
图5 不同催化剂的H2-TPR图Figure 5 H2-TPR patterns of the catalysts
2.5 O2-TPD

图6 不同催化剂的O2-TPD谱图Figure 6 O2-TPD patterns of the catalysts
由图6可见,NaY和0.2%Pd/NaY在低于200 ℃出现物理吸附氧O2(ad)的脱附峰和少量高于500 ℃晶格氧的脱附峰,并且与NaY相比,0.2%Pd/NaY中物理吸附的氧数量明显增多。 负载CeO2后,0.2%Pd/8%Ce/NaY分别在低于200 ℃、(200~400) ℃和500 ℃出现3个氧脱附峰。分别对应于物理吸附的氧O2(ad)、化学吸附的氧和晶格氧的脱附,并且0.2%Pd/8%Ce/NaY晶格氧脱附峰强度大幅度提高。表明适量CeO2的加入在催化剂中引入了大量的氧空穴,再加上PdO的协同作用,促进CeO2表面和体相氧交换能力,从而促进了催化剂中晶格氧的流动性,大大提高了催化剂的供氧能力和氧化性能,这一结果与H2-TPR和催化剂活性评价结果一致。
2.6 苯-TPSR
图7为不同催化剂上苯的TPSR谱图。

图7 不同催化剂上苯的TPSR谱图Figure 7 TPSR spectra of benzene over different catalysts
由图7可以看出,0.2%Pd/NaY对苯的吸附能力大于0.2%Pd/8%Ce/NaY,这是由于0.2%Pd/NaY具有更大的比表面积和孔容,更有利于苯的吸附。与0.2%Pd/NaY相比,0.2%Pd/8%Ce/NaY的脱附峰强度变弱,这与苯的吸附曲线一致,并且0.2%Pd/8%Ce/NaY对苯的脱附温度(194 ℃)低于0.2%Pd/ NaY(258 ℃),表明0.2%Pd/8%Ce/NaY上苯的吸附强度适中,有利于氧化反应进行。对于0.2%Pd/NaY和0.2%Pd/8%Ce/NaY,苯的脱附峰和CO2脱附峰同时出现,表明苯在脱附同时也发生氧化反应,并且这两种催化剂均可以将苯完全氧化为最终产物CO2和H2O。另外,随着反应温度提高,CO2浓度出现突跃式增大,表明随着温度升高,更多的苯发生了氧化反应。与0.2%Pd/ NaY相比,0.2%Pd/8%Ce/NaY在较低温度(约150 ℃)出现CO2脱附峰, 并且0.2%Pd/NaY和0.2%Pd/8%Ce/NaY分别在320 ℃和250 ℃时气相中苯浓度降为零,即苯发生了完全反应,表明0.2%Pd/8%Ce/NaY具有更低的起燃温度和完全转化温度。因此,CeO2的加入明显提高了催化剂供氧能力,从而提高了催化剂对苯的催化氧化性能,这与TPR、O2-TPD和催化剂的活性评价结果一致。
2.7 催化剂活性评价
图8为Ce的添加对0.2%Pd/NaY催化氧化苯性能的影响。

图8 Ce的添加对0.2%Pd/NaY催化氧化苯性能的影响Figure 8 Influence of Ce addition into 0.2%Pd/NaY on benzene oxidation
由图8可以看出,少量Ce的添加可明显提高0.2%Pd/NaY的活性,表明助剂CeO2在苯的催化氧化中起重要作用。添加质量分数2%~8%,随着Ce含量增加,0.2%Pd/Ce/NaY对苯的催化氧化性能提高。0.2%Pd/NaY的T50和T90分别为272 ℃和306 ℃,而0.2%Pd/8%Ce/NaY的T50和T90分别为210 ℃和230 ℃,与未添加相比,当Ce添加质量分数为8%时,T50和T90分别降低62 ℃和76 ℃。由图8还可以看出,当Ce质量分数进一步由8%增至10%时,催化剂对苯的催化氧化能力明显降低。研究表明,CeO2通过CeO2·CeO2(1-x)+xO2的可逆循环而具有氧存储和释放能力[19-20],随着CeO2质量分数增加(2%~8%),催化剂中氧空穴增多,增大了催化剂中氧的流动性,再通过CeO2与PdO的相互作用,使得催化剂具有更强的供氧能力(如O2-TPD),这是0.2%Pd/8%Ce/NaY表现出最佳活性的原因。前期研究表明,适量稀土氧化物的添加能够促进贵金属分散,提高催化剂活性[10]。当Ce质量分数进一步增大到10%时,过高的含量使CeO2粒径变大,可能包覆一部分活性PdO物种,使得催化剂供氧能力变弱(如H2-TPR),因此,导致催化剂活性降低。
2.8 催化剂稳定性
图9为不同温度0.2%Pd/8%Ce/NaY连续反应100 h对苯氧化性能的稳定性影响。

图9 不同温度0.2%Pd/8%Ce/NaY对苯氧化性能的稳定性影响Figure 9 Stability tests of 0.2%Pd/8%Ce/NaY for benzene oxidation at different reaction temperature
由图9可以看出,随着反应时间的增加,不同温度下催化剂活性出现不同程度的变化,反应前20 h,催化剂活性均略降,但随着温度升高,催化剂活性降低的幅度减小。反应50 h后,不同温度下催化剂转化率基本维持不变,均表现出较好的稳定性。连续100 h反应,195 ℃时转化率由30%降至23%,210 ℃时转化率由50%降至45%,230 ℃时转化率由91%降至86%,即当反应温度分别为195 ℃、210 ℃和230 ℃时,连续反应100 h,催化剂活性降低比例分别为23%、10%和5%。因此,0.2%Pd/8%Ce/NaY在不同温度下均表现出一定的稳定性,并且随着反应温度提高,催化剂稳定性提高,在接近完全转化温度时,0.2%Pd/8%Ce/NaY表现出良好的稳定性。
3 结 论
(1) NaY分子筛具有较大的比表面积和孔容,并且负载活性组分PdO和助剂CeO2后载体层状结构和晶相均得以保持,结构稳定,是良好的载体。
(2) PdO和CeO2均匀分散在载体表面,并且PdO以较小的纳米晶颗粒形式分散在CeO2周围,从而在催化反应过程中可以充分发挥活性组分PdO和助剂CeO2的相互协同作用。
(3) 随着CeO2质量分数的增加(2%~8%),催化剂中氧空穴增多,与活性组分的相互作用增强,但过高的CeO2质量分数(10%),CeO2会包覆住部分活性物种,从而使得催化剂供氧能力变弱,还原性能明显变差。
(4) 0.2%Pd/ 8%Ce/NaY对苯的吸附强度适中,催化剂中氧空穴较多,晶格氧的流动性明显提高,供氧性能优异,与PdO有较好的相互作用,从而表现出最好的还原性能和最佳的苯催化氧化反应活性和稳定性。

