吸入用盐酸溴己新溶液的体外评价
施建国 蒋宇丹
摘 要 目的:研究吸入用盐酸溴己新溶液的雾化特性,建立体外评价方法。方法:使用呼吸模拟装置对吸入用盐酸溴己新溶液的递送速率及递送总量进行研究,使用新一代撞击器(NGI)测定空气动力学粒径分布。结果:通过测定递送速率及递送总量、空气动力学粒径分布,表征盐酸溴己新溶液的体外雾化数据。结论:所测定的体外数据描述了吸入用盐酸溴己新溶液的体外特征,可为该制剂的体外评价提供参考。
关键词 吸入用盐酸溴己新溶液 体外评价 递送速率 递送总量 空气动力学粒径分布
中图分类号:R944.9; R974.1 文献标志码:A 文章编号:1006-1533(2020)09-0072-03
In vitro evaluation of bromhexine hydrochloride inhalation solution
SHI Jianguo*, JIANG Yudan**
(Shanghai Harvest Pharmaceutical Co., Ltd., Shanghai 201206, China)
ABSTRACT Objective: To establish in vitro evaluation methods and study the nebulization characteristics of bromhexine hydrochloride inhalation solution. Methods: The delivery rate and delivered amount of bromhexine hydrochloride inhalation solution were measured by breathing simulator and aerodynamic particle size distribution was determined by next generation impactor (NGI). Results: The in vitro nebulization of bromhexine hydrochloride inhalation solution could be characterized by the determination of the delivery rate and delivered amount and the aerodynamic particle size distribution. Conclusion: The in vitro characterization of the nebulization of bromhexine hydrochloride inhalation solution can be described by these methods, which can provide reference for the in vitro evaluation of bromhexine hydrochloride inhalation solution.
KEy WORDS bromhexine hydrochloride inhalation solution; in vitro evaluation; delivery rate; delivered amount; aerodynamic particle size distribution
鹽酸溴己新为祛痰药,具有较强的黏液溶解调节作用,临床上主要用于慢性支气管炎、支气管哮喘、支气管扩张、矽肺等有白色黏痰又不易咳出的患者[1]。肺部吸入制剂目前广泛应用于肺炎、哮喘、慢性阻塞性肺病(COPD)等肺部疾病的治疗[2],因其能直接到达病变部位,较其他给药方式具有其独特的优势[3]。吸入用盐酸溴己新溶液为供雾化器用吸入制剂。吸入制剂的体外评价是为了保证产品在给药后释放的药物剂量的准确、均一,同时保证产品在有效期内稳定。《中国药典》2015年版四部通则0111吸入制剂中收载呼吸模拟装置测定递送速率和递送总量以及使用NGI测定空气动力学粒径分布[4]的方法,评价吸入溶液的体外研究。目前《中国药典》未收载吸入用盐酸溴己新溶液,国内也无相关研究。本文研究了吸入用盐酸溴己新溶液的递送速率及递送总量、空气动力学粒径分布,为其体外研究提供评价方法。
1 材料和方法
1.1 仪器与试药
L1260液相色谱仪,VWD检测器、自动进样器(美国安捷伦科技有限公司);CPA225D 电子天平(德国赛多利斯科学仪器有限公司);BRS2000呼吸模拟器、NGI-1279新一代撞击器(英国Copley有限公司)。
盐酸溴己新对照品(批号100427-201102,中国食品药品检定研究所);吸入用盐酸溴己新溶液(规格2 ml:4 mg,批号Y161201、Y161202、Y161203,上海禾丰制药有限公司);乙腈、甲醇为色谱纯;水为超纯水;其他试剂均为分析纯。
1.2 方法
1.2.1 色谱条件
Welch Ultimate XB-C18色谱柱(4.6 mm×250 mm,5 mm);以磷酸盐缓冲液(磷酸二氢钾1.0 g,加水900 ml使溶解,用0.5 mol/L氢氧化钠溶液调节pH至7.0,用水稀释至1 000 ml,摇匀,即得)-乙腈(20∶80)为流动相;检测波长245 nm;柱温30 ℃;进样体积10 ml。
1.2.2 对照品溶液配制
取盐酸溴己新对照品适量,精密称定,分别用甲醇溶解并定量稀释制成每1 ml中约含盐酸溴己新0.5、15、30 mg的对照品溶液。
1.2.3 递送速率与递送总量
连接呼吸模拟器和滤纸装置。分别精密量取吸入用盐酸溴己新溶液2 ml及生理盐水2 ml,置于雾化器中,混匀。通过适配器将雾化器的喷雾嘴与滤纸装置连接。开启呼吸模拟器,设定呼吸模式。在呼吸循环的起始时启动雾化器,测试60 s,关闭雾化器,收集第一张滤纸;滤纸装置中再装入滤纸,开启雾化器,测试14 min,关闭雾化器,收集第二张滤纸。分别将第一、第二张滤纸浸泡于适量甲醇中,不断振摇10 min。第一张滤纸的浸泡溶液作为供试品溶液1;第二张滤纸的浸泡溶液作为供试品溶液2。第一张滤纸收集的盐酸溴己新的量与时间相比,即为递送速率,所有滤纸收集的盐酸溴己新总和,即为递送总量。
1.2.4 空气动力学粒径分布
本方法参照中国药典方法[4]125-130,将L型连接管及NGI置于5 ℃的恒温冷却柜中,预冷至少90 min。调节L型连接管进口的气体流速为(15±0.75)L/min,组装雾化装置。精密量取本品2 ml及生理盐水2 ml倒入雾化杯中,混匀,将吸嘴通过适配器连接至L型连接管。启动真空泵,打开三通阀,待气流稳定后,打开雾化器,测试10 min;将雾化装置从L型连接管上取下,拆除装置。水洗涤各部件,收集吸嘴适配器、L型连接管、NGI仪器7级收集板的清洁液,分别置于20 ml量瓶中;收集NGI仪器1、2、6级收集板及MOC的清洁液,分别置于50 ml量瓶中;收集NGI仪器3、4、5级收集板的清洁液,分别置于100 ml量瓶中,作为供试品溶液。
2 结果
2.1 递送速率与递送总量
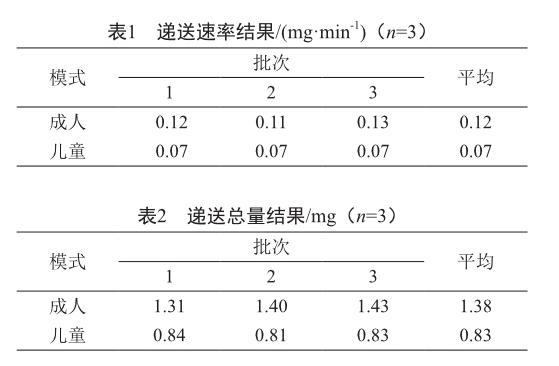
分别采用成人和儿童的呼吸模拟模式对三批样品测定递送速率与递送总量,统计所得平均值。不同批次的样品测定结果显示,各批次的递送速率与递送总量差异不大(表1、2),说明采用的方法可测定吸入用盐酸溴己新溶液递送速率与递送总量、评价该制剂通过雾化器产生药物的速率和总量。
2.2 空气动力学粒径分布
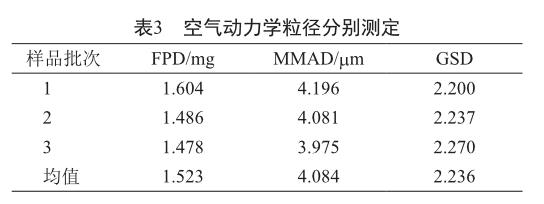
使用NGI分别测定3批样品,统计参数微细粒子剂量(FPD)、质量中间空气动力学直径(MMAD)和几何标准偏差(GSD),结果三个批次产品无显著差异(表3),说明采用微细粒子剂量测定可以评价吸入用盐酸溴己新溶液的空气动力学粒径分布。
3 讨论
3.1 递送速率与递送总量
递送速率是指装有规定体积药液的雾化杯,单位时间内通过雾化系统释出的药物质量或体积,将其转化为雾化药液总量的百分比,可以确定患者预期的治疗时间。递送总量是指装有规定体积药液的雾化杯通过雾化系统释出的药物质量或体积,将其转化为雾化药液总量的百分比,可为患者的预期用药剂量提供指导[5]。递送速率与递送总量测定直观地反映出不同年龄段患者用药的实际剂量,是更为合理评估吸入溶液质量的检测手段[6]。
3.2 空气动力学粒径分布
本研究使用的NGI仪器,经验证在15 L/min的流速下,NGI层级之间的分辨率较高,相邻层级间沉积粒子的粒径几乎无重叠,层级损失较小,数据可靠[7]。空气动力学粒径分布的参数主要选择FPD、MMAD和GSD。FPD是微细粒子剂量,为空气动力学粒径小于5 mm的气溶胶药物粒子的质量,描述了可能进入肺部的药物粒子的质量[8]。MMDA是质量中间空气动力学直径,为和质量有关的空气动力学直径的质量分布的中位值,是控制颗粒沉积在肺部位置的最重要的变量[9]。GSD是几何标准偏差,表征的是药物颗粒粒度分布曲线的形状,越接近1,说明粒度分布越窄[10]。但大多数药物的气溶胶是非均相的,GSD值一般大于1.5。采用以上3个参数可以表征吸入用盐酸溴己新溶液的体外粒径分布情况。
雾化吸入治疗利用呼吸把药物以气雾形式经呼吸道直接到达肺部病变部位,作用直接、起效迅速、避免了对非病变器官的影响;同时用药剂量小,大大减少了不良反应的发生,疗效高并且方便[11]。雾化的气溶胶微粒在肺部沉积的机制包括撞击、扩散、拦截、重力沉降和静电效应[12]。在此过程中,微粒粒径大小及粒径分布很大程度上决定了在呼吸系统中的沉积部位和沉積量,从而影响药物疗效[13]。故采用NGI测定体外吸入溶液的体外粒径分布,为药物进入体内发挥良好提供了保障。
参考文献
[1] 郑凤霞. 盐酸溴己新在小儿支气管肺炎中的临床应用[J/ OL]. 中华肺部疾病杂志(电子版), 2014, 7(3): 347-348. doi: 10.3877/cma.j.issn.1674-6902.2014.03.027.
[2] Kuzmov A, Minko T. Nanotechnology approaches for inhalation treatment of lung diseases[J]. J Control Release, 2015, 219: 500-518.
[3] 周学海, 张成飞, 杨敏, 等. 肺部吸入制剂评价方法研究进展[J]. 药物评价研究, 2019, 42(9): 1891-1895.
[4] 国家药典委员会. 中华人民共和国药典2015年版四部[M].北京: 中国医药科技出版社, 2015: 125-130.
[5] 陈翠翠, 魏宁漪, 周颖, 等. 供雾化器用液体制剂的雾化特性质量控制进展[J]. 中国药品标准, 2018, 19(3): 171-179.
[6] 周颖, 魏宁漪, 林兰, 等. 呼吸模拟装置测定2中雾化器的盐酸氨溴索递送速率及递送总量[J]. 中国新药杂志, 2018, 27(3): 290-294.
[7] Marple VA, Olson BA, Santhanakrishnan K, et al. Next generation pharmaceutical impactor: a new impactor for pharmaceutical inhaler testing. Part III. Extension of archival calibration to 15 L/min[J]. J Aerosol Med, 2004, 17(4): 335-343.
[8] 魏宁漪, 周颖, 陈翠翠, 等. 盐酸氨溴索吸入溶液的空气动力学粒径分布测定[J]. 中国新药杂志, 2018, 27(17): 1994-1998.
[9] 陈桂良, 侯惠民. 吸入用气雾剂雾粒测定方法的评价[J].中国医药工业杂志, 2007, 28(3): 194-199.
[10] 严翠霞, 江文明, 陈桂良, 等. 吸入粉雾剂粒径测定方法的评价: 3种撞击器的比较[J]. 药物分析杂志, 2011, 31(7): 1296-1299.
[11] 李西睦, 喻广娟, 丁志远, 等. 3种不同雾化吸入方式治疗毛细支气管炎疗效比较[J]. 河北医药, 2009, 31(21): 2909-2910.
[12] 陈诗韵, 王伟, 赵新慧. 雾化吸入剂体外粒径分析的研究进展[J]. 北方药学, 2017, 14(10): 142-143.
[13] Newman SP. Can lung deposition data act as a surrogate for the clinical response to inhaled asthma drugs[J]. Br J Clin Pharmacol, 2000, 49(6): 529-537.

