放射性核素锶89(Sr-89)联合放射治疗多发骨转移癌的临床效果
夏林欢
(中南大学湘雅二医院 湖南 长沙 410011)
骨骼是恶性肿瘤转移高发部位,有报道显示,有50%左右的原发性恶性肿瘤患者会发生骨转移癌[1]。疼痛是骨转移癌主要临床表现,于初期疼痛程度较轻且多为间歇性,随着病情加重,逐渐发展为持续性。故必须及时给予有效的治疗措施,以此缓解患者疼痛感,提升其生活质量。Sr-89在转移病灶内的生物半衰期超过50d,其β射线的能量为1.46MeV,Sr-89在原发性骨肿瘤中的分部较为均匀,在骨皮质中的摄取较高。放射治疗是利用放射线对肿瘤患者进行局部治疗的一种方式,也是临床最为常见的一种。故本文此进行分析,阐述如下。
1 资料与方法
1.1 一般资料
使用抽签法对本院筛选的86例多发骨转移癌患者进行分组,分为两组各43例,病例资料来源2019年1月—2020年1月。其中实验组男性27例,女性16例,年龄在34~68岁,平均为(49.62±6.33)岁;12例前列腺癌,13例乳腺癌,15例直肠癌,3例肺癌。对照组男性25例,女性18例,年龄在36~76岁,平均为(48.26±6.41)岁;11例前列腺癌,14例乳腺癌,13例直肠癌,5例肺癌。两组基本资料相比无差异(P>0.05)。
1.2 方法
对照组给予Sr-89治疗。给予患者使用GE Healthcare Limited生产的氯化锶[89Sr]注射液(批号:国药准字H20090880)150MBq(4mCi)/4mL,于开封后3min内将药物缓慢注射至患者体内,用量:1.48MBq/Kg(40μCi/kg)或92.5MBq~137MBq/人(2.5mCi~4.0mCi/人)推荐静脉注射100~150MBq(4.0mCi)/人次。实验组于对照组基础上给予局部放射治疗,依据患者具体病情,采取合适的卧位,将患者固定在专用体板上。依据患者疼痛部位以及图像浓聚位置的体表投影作为放射治疗靶区中心,给予标记;随后使用SPECT/CT行X射线CT定位,并将CT扫描图像导入放疗计划系统(TPS)对病灶进行勾画;给予靶区0gY/3gY/10F,既治疗1次/d,一周治疗5d,共2周。放疗前于模拟定位机(核动力II-B)下校准患者的治疗靶区,以此保证放疗前靶区的准确性,随后使用德国进口IEMENS PRIUMS M 5176直线加速器对靶区实行放疗,放疗:DT30gY/3gY/10F。
1.3 观察指标
对两组疗效进行分析,显效:骨转移病灶完全消失或减轻;微效:骨转移病灶减少至>25%;恶化:骨转移病灶数目减少至<25%或病情完全无改变甚至加重[2]。使用视觉模拟评分法(VAS)对患者疼痛程度进行评分,分值为0~10分,分值越高表明患者疼痛程度越严重[3]。
1.4 统计学处理
本文研究中选择SPSS20.0系统计算数据,其中(x-±s)表达计量数据,选择t检查,而百分比表达计数数据,选择χ2检查,两组数据存在差异后选用P<0.05表达。
2 结果
2.1 两组疗效分析
实验组总有效率95.35%高于对照组79.07%(P<0.05),见表1。
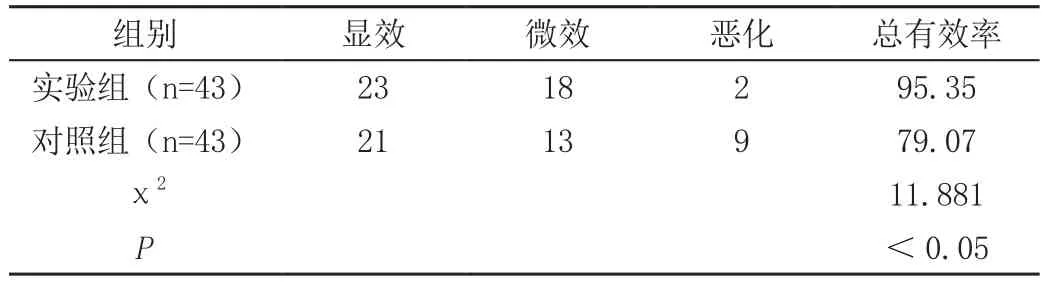
表 1 对两组疗效进行分析 [n(%)]
2.2 两组VAS评分对比
治疗前,两组VAS评分无显著差异(P>0.05),治疗后,实验组VAS评分低于对照组(P<0.05),见表2。
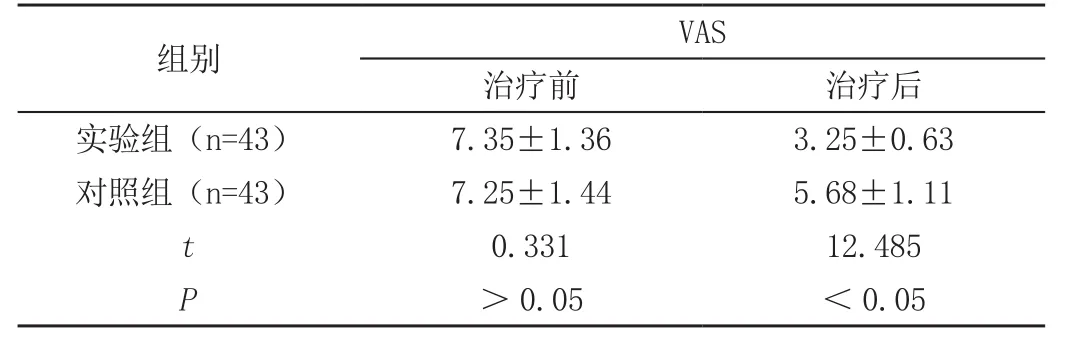
表2 两组VAS、ADL评分对比(x-±s,分)
3 讨论
恶性肿瘤对人类的生命安全造成严重威胁,原发性恶性肿瘤发生骨转移后有一定的疼痛感,这与骨膜遭受肿瘤生长压力以及肿瘤直接浸润累及骨膜密切相关,随着肿瘤不断生长,病情加重,疼痛感会持续加剧。
多项研究表明[4],放射性核素在临床治疗中一直为单一的方式在使用,很少与放射治疗、免疫治疗等联合使用,Sr-89是临床常用的一种放射性药物,该药进入体内后能够与钙一样沉积于骨组织内,于骨转移病灶内的聚集是正常骨的2~25倍,能够有效清除周围肿瘤细胞,并减轻骨膜炎症刺激,以此达到镇痛目的。对于多发骨转移癌患者,临床常给予局部放射治疗,以此抑制骨转移癌生长,且对缓解患者疼痛具有显著效果,对患者身体也不会造成太大的影响。实验组总有效率高于对照组(P<0.05);治疗后,实验组低于对照组(P<0.05)。由此得出,给予患者放射性核素锶89联合放射治疗具有显著疗效,能够缓解患者疼痛。
综上所述,Sr-89联合放射治疗对多发骨转移患者相较于单一使用Sr-89疗效更佳,对改善患者预后具有明显效果,值得推广。

