空心玻璃微珠对聚丙烯酸水凝胶溶胀性能的影响
杨珊,段晓梅
(渭南师范学院化学与材料学院,陕西省煤基低碳醇转化工程研究中心,陕西渭南 714099)
水凝胶是一种亲水却不溶于水的具有特殊三维网络状结构的高分子体系,由于它具有高吸水性和环境敏感性而被广泛应用于工业、农林园艺、医疗和生物工程等[1]。环境敏感的智能型水凝胶要求溶胀平衡快、溶胀比大,而多孔结构是提高水凝胶环境响应速率和响应程度的关键因素之一[2–5]。制备多孔水凝胶方法有发泡法、致孔法、相分离法、前线聚合法、模板法、聚合物互穿网络法、冷冻干燥法、超声法等[1–7]。相比之下,致孔法制备多孔水凝胶有一定的优势,孔径和孔密度可以通过致孔剂的种类和用量来调整,而用作致孔剂的物质种类较多,例如:微粉状的蔗糖,聚乙二醇 (PEG),NaCl,CaCO3,硅胶微粒,活性炭等[3,7–8]。空心玻璃微珠 (HGM)是一种用途广泛的填料,在聚合物基复合材料的制备中常被用于降低材料密度、提高材料力学性能、耐热性、耐磨性等性质[9–10],但目前尚未见其用作水凝胶致孔剂的报道。HGM 因本身有固定的外形和尺寸,且表面带有羟基、亲水但不溶于水,这使其可以作为多孔水凝胶制备时的无机致孔剂。笔者研究HGM作为无机致孔剂对合成水凝胶溶胀性能的影响,以丙烯酸(AA)为单体、HGM 为无机致孔剂、PEG 为有机致孔剂,用自由基溶液聚合法制备聚丙烯酸(PAA)多孔水凝胶,研究HGM 投料量的改变对水凝胶化学组成、热稳定性、孔结构以及吸水溶胀性、耐盐性和pH 敏感性的影响。由于采用单一致孔剂制备多孔水凝胶的报道众多,故笔者期望通过有机、无机两种致孔剂的共同作用来优化水凝胶的孔结构、提高其溶胀性能。
1 实验部分
1.1 主要原材料
AA,PEG ( 分 子 量 为 900~1 000),N,N- 亚甲基双丙烯酰胺(BIS),过硫酸铵(APS),NaOH,NaCl,pH 缓冲液 (pH=4.01,6.86,9.18):分析纯,市售;
实验用水:超纯水,电阻率18.25 MΩ·cm,自制;
HGM:HN60 型,密 度 0.6 g/cm3,粒 径70 μm,河北灵寿县荣盛矿产品加工厂。
1.2 仪器与设备
集热式恒温磁力搅拌器:DF–101S 型,巩义市予华仪器公司;
超声波清洗器:KH–100E 型,昆山禾创超声仪器公司;
超纯水机:GZY–P60–V 型,湖南科尔顿水务公司;
移液枪:大龙实验仪器有限公司;
回旋振荡器:WSZ–100A 型,上海一恒科学仪器公司;
冷冻干燥机:Alpha 1–2 LD plus 型,德国 Christ公司;
傅里叶变换红外光谱(FTIR)仪:Tensor II 型,德国Bruker 公司;
离子溅射仪:EDT–200 型,北京意力博通公司;
扫描电子显微镜(SEM):Sigma500 型,德国Ziess 公司;
同步差示扫描量热(DSC)&热重(TG)热分析仪:STA449 F5 型,德国 Netzsch 公司;
尼龙网袋:120 目(孔径0.125 mm),自制。
1.3 水凝胶的制备
取1.50 mL 单体AA 加入10 mL 离心管,先用等物质的量的NaOH 溶液中和,再加入单体AA 质量80%的致孔剂PEG,0.5%的交联剂BIS 和0.5%的引发剂APS,然后加入不同质量的HGM (HGM投 料 量 分 别 为 AA 质 量 的 0%,0.5%,5%,10%,20%),最后加入5 mL 水,超声混匀后于60℃反应5 h,得到 5 种乳白色固体凝胶 PAA–0,PAA–0.5,PAA–5,PAA–10,PAA–20 (PAA 后数字代表 HGM的投料量)。将凝胶切成约1 cm 厚的圆片并用超纯水浸泡,使PEG 溶于水并使HGM 浮于水面上,通过长时间浸泡、摇振和多次换水可将凝胶中的PEG,HGM 及其它未反应物等杂质除去,得到无色透明的溶胀态凝胶,冷冻干燥后得到白色多孔状干凝胶。
1.4 水凝胶的表征和测试
(1)结构表征。
用FTIR 表征PAA 水凝胶的结构,测试方法同文献[6]。
(2)热稳定性表征。
用同步DSC&TG 热分析仪测试PAA 水凝胶的热行为,测试条件:样品质量5~10 mg,Al2O3坩埚,空坩埚作参比,N2气氛、流速30 mL/min,升温速率10℃/min,温度范围20℃~700 ℃。
(3)表面形貌表征。
用SEM 观察冻干PAA 水凝胶的表面形貌并拍照,测试方法同文献[6]。
(4)溶胀性能测试。
测试冻干PAA 水凝胶在超纯水、生理盐水(质量 分 数 0.9% 的 NaCl 溶 液 ) 以 及 pH=4.01,6.86,9.18 的缓冲液中的吸水溶胀性能,测试方法及水凝胶的瞬时溶胀比(SR)和平衡溶胀比(ESR)的计算方法同文献[4]。
2 结果与讨论
2.1 结构分析
通过FTIR 谱图的比对可获知水凝胶样品的化学组成和结构以及杂质是否被除净等信息。HGM投料量不同的PAA 水凝胶的FTIR 谱图见图1。图1 表明,3 种投料量的 PAA 水凝胶的 FTIR 谱图基本相同,这表明HGM 的添加并未影响水凝胶的化学组成。对PAA 水凝胶的FTIR 谱图归属如下[4,8,11–12]:3 389 cm-1大包峰为羟基和氨基伸缩振动的合并出峰,源于PAA 上羧基、交联剂BIS 上N—H以及样品吸附游离水;2 924,2 886 cm-1两峰为饱和C—H 的不对称和对称伸缩振动峰,1 699 cm-1峰为羧基上C=O 的伸缩振动峰,1 559 cm-1强峰为—COO–的不对称伸缩振动峰,1 407 cm-1处强峰为—COO–的对称伸缩振动峰,1 451 cm-1峰为亚甲基的弯曲振动峰,1 280,1 240 cm-1两峰为 O—H 面内弯曲振动峰,1 111 cm-1处强峰为C—O 伸缩振动峰。笔者制备的PAA 水凝胶的FTIR 谱图与本课题组报道的活性炭致孔的PAA 水凝胶的FTIR 谱图近似[8],但与本课题组报道的PEG 致孔的PAA 水凝胶的FTIR 曲线差异很大[4],该差异是由羧酸盐和羧酸的红外吸收不同所致[11],源于聚合前单体AA 是否被中和。笔者制备的PAA 水凝胶的FTIR 谱图中同时存在C=O 的伸缩振动峰和—COO–的伸缩振动峰,这表明PAA 水凝胶中—COOH 和—COO–同时存在;从峰强度来看,—COO–远多于—COOH。对比文献[4]和文献[8]中PAA 水凝胶的FTIR 谱图可知,笔者制备的PAA 水凝胶在3 389 cm-1处出大包峰,这表明该水凝胶的吸水性很强。
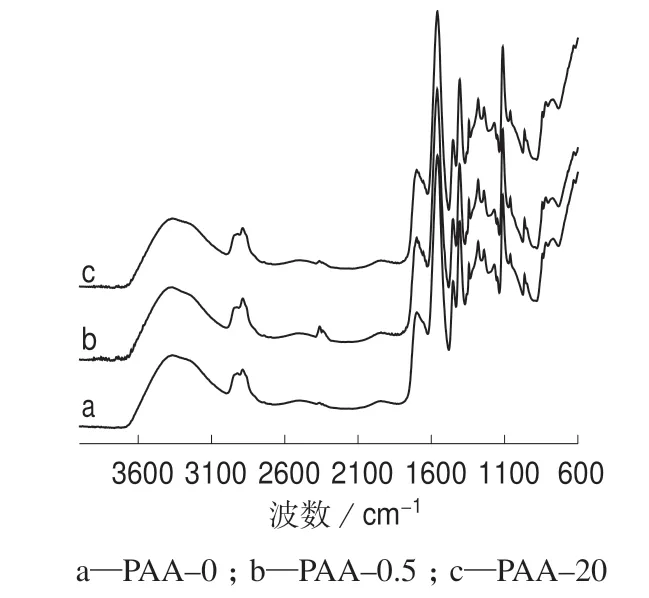
图1 PAA 水凝胶的FTIR 谱图
2.2 热稳定性分析
水凝胶的热稳定性直接关系到其使用的温度范围,而水凝胶的组成和结构的变化可能会引起其热稳定性的变化。HGM 投料量不同的PAA 水凝胶的典型DSC&TG 曲线如图2 所示。图2 显示,HGM 投料量不同的PAA 水凝胶的TG 曲线皆有3段明显失重,对应DSC 曲线上有3 个吸热峰:第一段的最大失重温度在100℃以内,对应水凝胶失去吸附水的过程;第二段和第三段失重源于水凝胶受热分解,5 种投料量的水凝胶初始分解温度很接近,皆在160~165℃。由此可见,HGM 的加入基本未影响水凝胶的热稳定性,这表明制备过程中所加入的HGM 在水凝胶浸泡、除杂过程中被除去。

图2 PAA 水凝胶的DSC&TG 图
2.3 表面形貌分析
HGM 投料量不同的PAA 冻干水凝胶的SEM照片见图3。图3b~图3e 中基本看不到球状物,这表明HGM 在浸泡、摇振过程中被除去。所有样品均为相互贯穿的多孔网络结构,未加HGM 的PAA水凝胶的孔较小、孔壁较厚(图3a),而添加HGM的PAA 水凝胶的孔明显变大、孔壁也变薄(图3b~图3e),这表明HGM 在凝胶制备过程中起到了致孔作用。比较可知,PAA–0 的孔密集、孔壁较厚;PAA–0.5 的孔壁明显变薄、孔的通透性变好;PAA–5的孔壁更薄、孔的通透性更好;PAA–10 的孔比PAA–5 密集、孔壁也增厚,但与 PAA–0 明显不同的是其孔壁布满了孔坍塌褶皱(图4);而PAA–20 的孔明显比PAA–10 缩小,虽然孔壁上也有孔坍塌褶皱,但整体结构与PAA–0 更近似。从水凝胶的孔结构来看,HGM 在水凝胶制备过程中并非添加越多致孔效果越好,HGM 的投料量为单体AA 质量的0.5%~10%时的孔径相对较大、孔结构较丰富,水凝胶中存在孔径为0.3~5 μm 的小孔和10~50 μm的大孔。水凝胶孔径结构的变化也说明了HGM 在水凝胶制备过程中除了致孔作用之外,还可能会限制其附近大分子链的运动范围,尤其在添加量较大时HGM 可能会导致其附近大分子链物理缠结程度增加,从而导致孔径有所减小。

图3 PAA 水凝胶的SEM 照片(放大500 倍)

图4 不同放大倍数下PAA–0 和PAA–10 水凝胶的SEM 照片
2.4 溶胀性能分析
(1)水凝胶对水和盐水的溶胀性能分析。
HGM 投料量不同的PAA 水凝胶在纯水和生理盐水中的溶胀行为见图5,对应的ESR 数据见表1。

图5 PAA 水凝胶在纯水和生理盐水中的溶胀行为
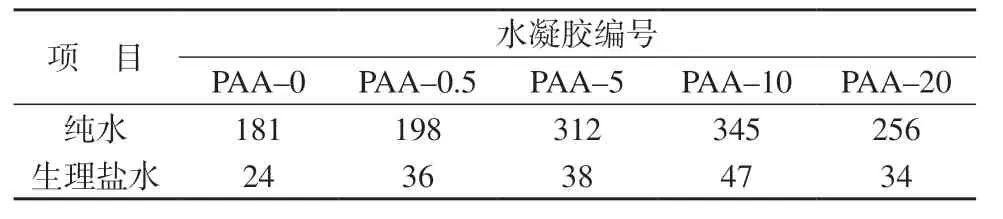
表1 PAA 水凝胶在纯水和生理盐水中的ESR g/g
由图5a 可见,5 种PAA 水凝胶在纯水中的溶胀平衡皆较快,大约2~3.5 h 即达到平衡状态。随着HGM 投料量的增大,水凝胶的ESR 先增大再减小(表1),这与其SEM 照片中的孔结构变化规律相符。5 种凝胶中PAA–10 吸水的 ESR 最大,这表明适量HGM 的添加所引起的水凝胶孔径增大、孔壁褶皱增多有利于吸水溶胀。PAA–20 吸水的ESR 比PAA–10 降低了很多,这也表明了HGM 除了致孔作用之外,HGM 刚性颗粒对周围大分子链段的伸展还有一定的限制作用[13],这可能使大分子链的物理缠结加重以致孔洞减小,所以在HGM 用量较大时会导致水凝胶的溶胀性变差。与本课题组之前报道[4]的 PEG 致孔的 PAA 水凝胶相比,HGM 和 PEG共同致孔的PAA 水凝胶的吸水溶胀平衡更快、ESR更大,这除了HGM 的致孔作用外,还与聚合前单体AA 被 NaOH 中和有关[14]。
对比图5a 和图5b 可知,5 种投料比的PAA 水凝胶在盐水中的SR 远小于在纯水中;由表1 可知,水凝胶在盐水中的ESR 随HGM 投料量的变化规律与在纯水中的基本相同。PAA 水凝胶在盐水中的ESR 较小的现象是由于溶液离子强度的增大降低了凝胶网络的静电斥力和水的渗透压,导致其吸水溶胀能力降低[15–16]。图5b 中5 种投料量的PAA水凝胶在盐水中的溶胀曲线存在先快升、再下降、然后缓慢平衡的现象,溶胀平衡比在纯水中慢得多,这可能是由于PAA 水凝胶的大孔结构导致其开始迅速吸水溶胀,而后由于盐水离子强度的影响导致孔收缩失水,最后才达到平衡。
(2)水凝胶的pH 响应性分析。
HGM 投料量不同的5 种PAA 水凝胶在pH 缓冲液中的溶胀曲线见图6,对应的ESR 与pH 的关系曲线见图7。

图6 PAA 水凝胶在不同pH 缓冲液中的溶胀行为
由图6 和图7 可知,5 种PAA 水凝胶均具有良好的pH 敏感性,添加HGM 的水凝胶对pH 变化更敏感,尤其PAA–10 的pH 敏感性明显优于其它水凝胶,这表明适量HGM 的加入有利于提高水凝胶的pH 敏感性。结合SEM 照片可知,水凝胶的pH敏感性与其孔结构的关系密切。

图7 PAA 水凝胶的ESR 与pH 的关系
5 种水凝胶在不同pH 缓冲液中的ESR 皆小于对应在纯水中的ESR,这是pH 缓冲液的离子强度远大于纯水所致。在pH=4.01 的缓冲液中,5 种水凝胶溶胀曲线的变化趋势类似于在生理盐水中的变化,这是离子强度和pH 共同作用的结果,酸性条件下凝胶中—COO–基团会结合H+导致孔收缩失水。而pH=6.86 缓冲液接近中性,对水凝胶的孔结构影响很小,故而水凝胶能够迅速吸水溶胀平衡。而pH=9.18 缓冲液为碱性,更有利于水凝胶中—COO–基团的充分电离,故而吸水溶胀也很快。与本课题组之前报道的聚合前单体AA 未被中和的、PEG 致孔的PAA 水凝胶[4]相比,笔者制备的PAA 水凝胶在pH 缓冲液中的溶胀平衡时间更短(2~3.5 h),这与本课题组报道的聚合前单体AA 被中和的、活性炭致孔的PAA 水凝胶的溶胀平衡时间相差不大[8]。
3 结论
用HGM 和PEG 为致孔剂制备PAA 水凝胶,研究HGM 的投料量对该水凝胶的吸水溶胀性、耐盐性和pH 敏感性的影响。结果表明,HGM 的加入并不会影响水凝胶的化学组成和热稳定性,但对提高水凝胶的吸水溶胀性、吸盐水溶胀性和pH 敏感性有一定的作用。PAA 水凝胶的SEM 照片表明HGM 有显著的致孔作用,而且HGM 与PEG 复合致孔的PAA 水凝胶的孔结构比单纯PEG 致孔的PAA 水凝胶更加丰富。对比未加HGM 的PAA 水凝胶,当HGM 投料量为单体AA 质量的10%时,PAA 水凝胶的孔结构最丰富,其吸水ESR 由181 g/g 增加至 345 g/g,吸盐水 ESR 由 24 g/g 增加至 47 g/g,pH 敏感性最好。

