右美托咪定对心外科术后患者睡眠质量的改善作用
程 浩,杨心月,李白翎
[海军军医大学(第二军医大学)附属长海医院心血管外科,上海 200433]
心脏病术后患者血流动力学变化大,重症患者因心脏功能恢复缓慢及其他原因可能长期滞留重症监护病房。危重患者的睡眠特征是睡眠片段化,觉醒次数过多,过多的1期睡眠(浅睡眠)、慢波睡眠大幅减少(SWS)[1-5]。而外科手术后患者的睡眠剥夺和忽视睡眠问题可能会引起一系列心脑血管及神经内分泌系统的并发症,从而导致其围术期病死率的增加[2]。本研究探讨右美托咪定的夜间持续静脉注射对心外科术后患者睡眠的影响。
1 资料和方法
1.1 一般资料
本研究于2018年1月至2018年12月间在上海长海医院进行。选取标准:年龄在18~80岁;心脏体外循环手术后,血流动力学趋于稳定;无严重的外周器官功能障碍;试验开始时在心外科重症监护病房时间<30 d;已撤除呼吸机或气管切开可以自主呼吸,或需要呼吸机辅助的模式为持续气道正压(CPAP),支持压力为(9±1)mmHg(1 mmHg=0.133 kPa)的患者。右美托咪定是高选择性α2肾上腺素能受体激动药,通过作用于蓝斑核α2受体及激动内源性促睡眠通路而产生镇静催眠作用,这种镇静催眠状态的特点是患者可以被刺激或语言唤醒,并且在镇静催眠过程中不会产生呼吸抑制[1-2]。右美托咪定经肝代谢,并对部分患者可引起心率减缓、低血压等。鉴于右美托咪定的药理特性和睡眠生理,本试验需排除影响此药物代谢、临床作用,防止副作用发生及任何影响人体睡眠、影响评估睡眠的因素。排除标准:(1)格拉斯哥昏迷评分<11分;(2)试验时间内任何其他镇静药物的应用;(3)心率低于50次/min或三度房室传导阻滞无起搏器;(4)严重肝功能异常(总胆红素>100 μmol/L);(5)使用中枢作用的α-2受体激动剂或在研究开始前24 h内使用其拮抗剂;(6)癫痫病史;(7)任何其他神经疾病或可能对睡眠质量影响显著的病史;(8)睡眠呼吸暂停的病史;(9)持续感染;(10)出现谵妄。剔除标准:(1)术中二次转机;(2)围术期大出血;(3)术后二次手术。本研究符合作者所在单位伦理委员会所制定的伦理学标准,并取得患者的知情同意。
1.2 方 法
试验组患者睡眠数据由多导睡眠仪记录(SOMNOlab V2.17;德国WEINMIANN公司),数据结果为人工统计。试验时间包括连续3个夜晚(10:00 pm~6:00 am)和之间的两个白天(6:00 am~10:00 pm)。从试验开始的第一个晚上10点开始,试验组患者持续静脉注射右美托咪定,其负荷剂量为0.5 μg/kg,时间不超过20 min,然后以0.2~0.7 μg/(kg·h)持续静脉注射。保持镇静水平镇静程度评估表(richmond agitation-sedation scale,RASS)评分-1~2分,至次日6:00 am停止,白天无右美托咪定静脉注射。右美托咪定连续静脉注射3个夜晚。对照组患者整个试验期间均不静脉注射右美托咪定及使用其他镇静催眠药物。多导睡眠仪记录两组患者夜间的睡眠数据。白天由床旁护士记录患者的睡眠次数,统计数据交由试验人员统计。整个试验期间两组患者均可以使用镇痛药物如阿片类及非甾体抗炎药等镇痛剂。不允许使用抗精神病类药物,如病情需要使用,则患者退出试验。在试验过程中,光、噪音、护理操作和其他干预措施在10:00 pm~6:00 am最小化。此外,对于气管切开的患者,如患者因为病情需要更改呼吸机辅助模式,则患者退出试验;夜间有病情变化需要医生实施床旁有创操作的患者亦退出试验;在试验期间的两个白天,需要改变通气模式的患者不退出试验,但睡眠数据只采用夜间数据进行分析使用。具体试验时间分配见图1。
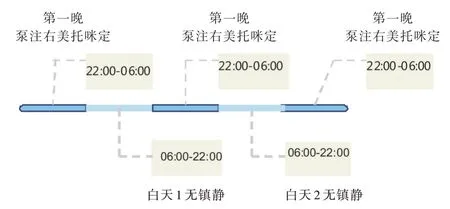
图1 实验组患者静脉注射右美托咪定试验时间图
1.3 观察指标及睡眠效果判定
人的正常睡眠结构包括非快速眼球运动睡眠(NREM)期和快速眼球运动睡眠(REM)期。非快速眼球运动睡眠期睡眠是促进生长、消除疲劳及恢复体力的主要方式,其分为N1(入睡期)、N2(浅睡期)、N3(中度睡眠期)、N4(深度睡眠期)期。快速眼球运动睡眠期睡眠与神经系统记忆力的恢复、体温调节等密切相关[6]。本试验利用多导睡眠仪记录并分析的指标如下:总睡眠时间、睡眠效率、睡眠觉醒次数、各期睡眠的时间等。
1.4 镇静程度评估表及格拉斯哥昏迷评分标准
RASS评分标准:+4为有攻击性,有暴力行为;+3为非常躁动,试着拔出呼吸管,胃管或静脉注射;+2为躁动焦虑,身体激烈移动,无法配合呼吸机;+1为不安焦虑,焦虑紧张但身体只有轻微的移动;0为清醒平静,清醒自然状态;-1为昏昏欲睡,没有完全清醒,但可保持清醒超过10 s;-2为轻度镇静,无法维持清醒超过10 s;-3为中度镇静,对声音有反应;-4为重度镇静,对身体刺激有反应;-5为昏迷,对声音及身体刺激都无反应。格拉斯哥昏迷评分(评估患者昏迷程度的方法,得分值越高患者意识状态越好):最高分为15分,表示意识清楚;12~14分为轻度意识障碍;9~11分为中度意识障碍;8分以下为昏迷;分数越低则意识障碍越重。
1.5 统计学分析
采用SPSS 22统计学软件对试验数据进行处理。正态分布的计量资料采用()表示,组间比较采用成组t检验。计数资料以[n(%)]表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 试验组和对照组患者的基线资料比较
试验过程中,有2例患者因为输注右美托咪定导致心动过缓(心率<50次/min),后停用右美托咪定改用其他镇静剂,患者退出试验;有患者因病情变化等退出试验。最终完成整个试验过程的患者为63例,其中试验组32例,对照组31例。白天的睡眠数据试验组为25例,对照组为26例。所有患者均有应用阿片类镇痛剂(芬太尼、吗啡、哌替啶)和(或)非甾体抗炎药类镇痛剂(氟比洛芬酯50~100 mg/次、丙帕他莫2 g/次)的过程,以确保患者舒适度。睡眠数据符合正态分布。试验组和对照组患者年龄[(55.61±11.37)岁vs.(57.35±11.72)岁,P>0.05]、体质量[(65.15±12.22)kgvs.(67.87±12.52)kg,P>0.05]及其他基线资料比较,差异无统计学意义(P>0.05),详见表1。
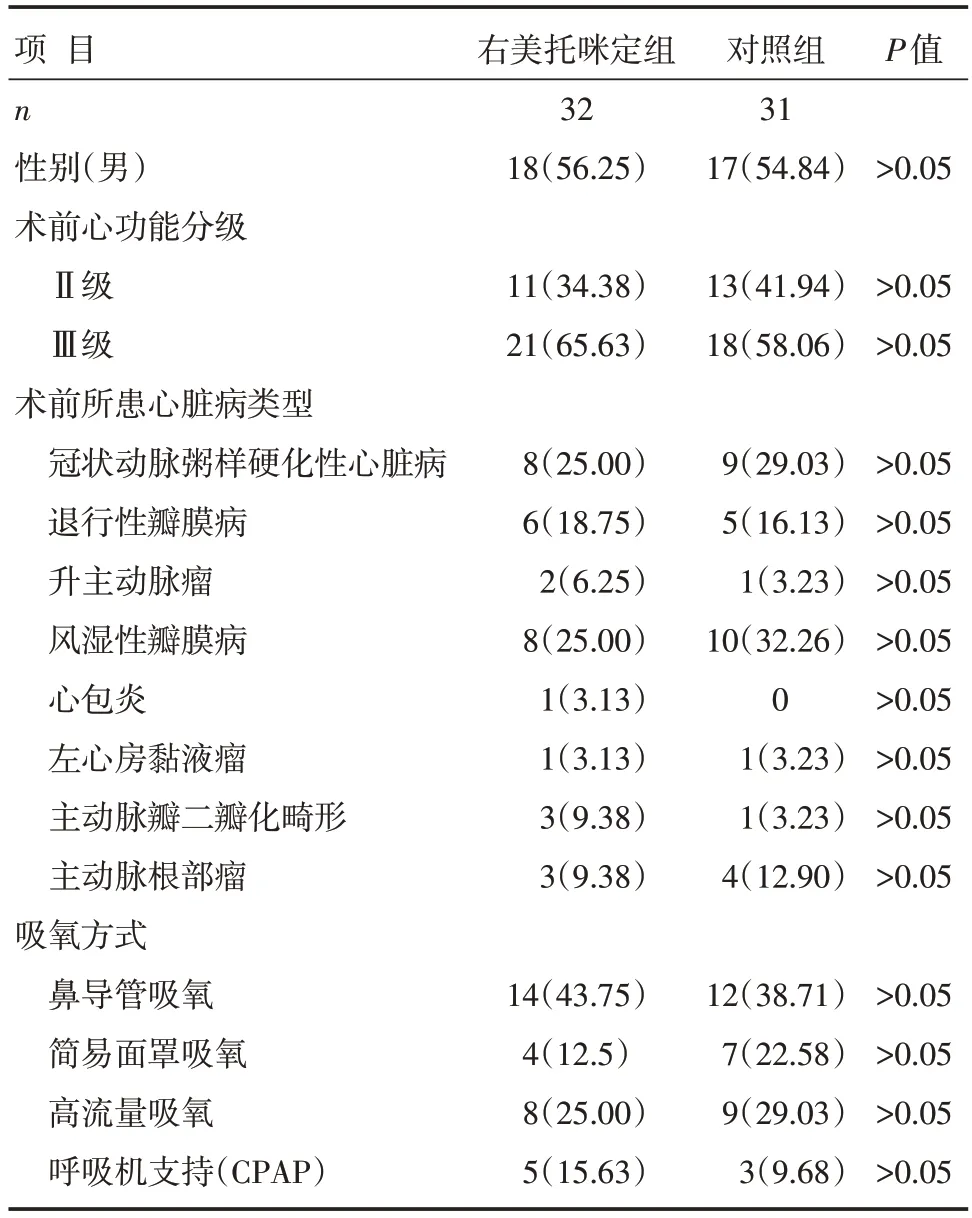
表1 试验组和对照组患者基线资料比较 [n(%)]
2.2 试验组和对照组患者夜晚睡眠数据比较
试验组与对照组比,有更少的觉醒次数[(3.1~3.61)次vs.(8.87~9.77)次,P<0.01],更高的睡眠效率(68%~71.29%vs.25.1%~28.87%,P<0.01),更长的睡眠第二阶段[(249.55~266.89)minvs.(59.12~71.59)min,P<0.01],差异有统计学意义。两组患者睡眠第一阶段比较,差异无统计学意义[(63.61~7.05)minvs.(56.37~63.33)min,P>0.05]。且临床上明显观察到试验组患者睡眠时间更长。慢性睡眠和快速眼球运动睡眠在两组患者中均为少见,没有进行统计分析,试验组也无更好的表现,这也与Alexopoulou[10]的研究吻合。两组患者3晚的夜晚睡眠数据详见表2。
表2 两组患者3晚睡眠数据 []
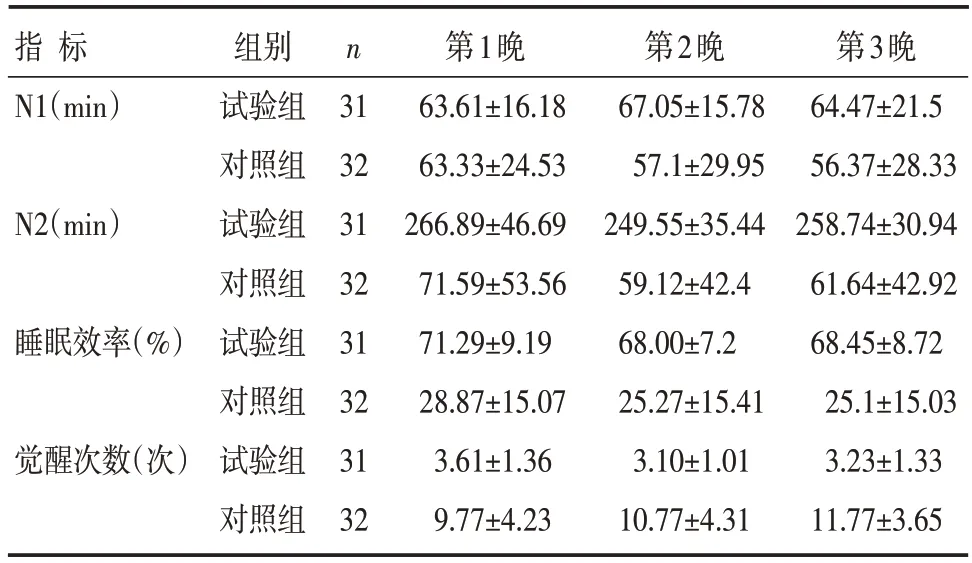
表2 两组患者3晚睡眠数据 []
2.3 试验组和对照组患者白天睡眠数据比较
白天的睡眠因条件所限,无多导睡眠图监测,由护士记录>5 min的睡眠次数。两组患者白天的睡眠次数比较,差异无统计学意义(P>0.05),详见表3。
表3 试验组与对照组白天的睡眠数据比较 []
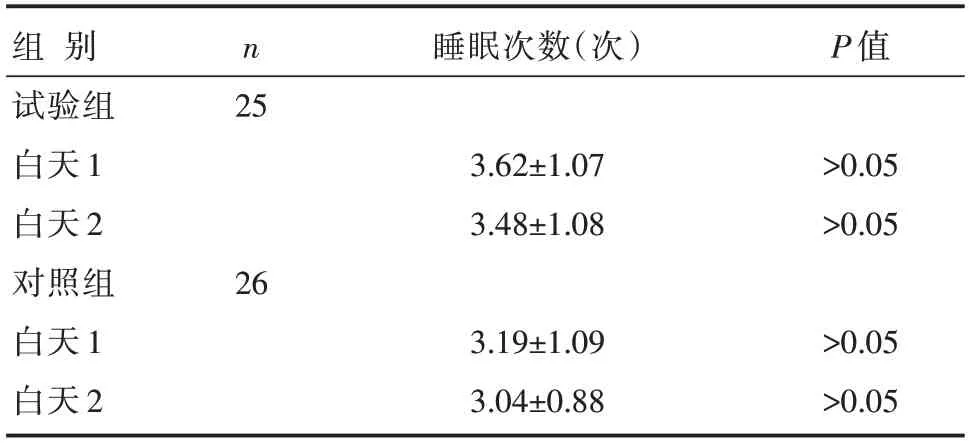
表3 试验组与对照组白天的睡眠数据比较 []
3 讨论
根据本研究白天对患者的观察数据,两组患者均有多段睡眠,对比两组数据的睡眠次数均值有差异,但差异无统计学意义。
有研究表明,无镇静药使用的重症监护病房患者,睡眠是分布在24 h内的,这和对照组数据类似,患者睡眠是多段的、分散的[10]。夜晚持续静脉注射右美托咪定,可以使睡眠集中在夜间,而多天的夜间持续静脉注射,也许可以改善患者在重症监护病房睡眠生物钟紊乱、睡眠分散的问题,使得患者的睡眠更符合人类睡眠为单向性的特点(每天只睡眠1次),这需进一步试验来验证。从患者的基本信息来看,并无性别、年龄、心脏病类型等导致的睡眠差异。
本研究的不足:因试验仪器,试验管理较难,完成整个试验的患者数量相对较少;对于长时间滞留重症监护病房的患者来说,本试验设计为3 d,并无长程的跟踪睡眠试验研究。期待进一步研究试验。
总体来说重症监护病房心脏术后患者的睡眠质量仍偏低,但右美托咪定的持续静脉注射不失为一种更优的选择。期待更接近生理睡眠的镇静药物出现。

