医护-营养师一体化综合管理模式对高磷血症维持性血液透析患者血磷的影响
曾巧 黄江明 石宏斌 钟庆荣
530022 广西壮族自治区南宁市第一人民医院肾内科血液净化室
高磷血症是维持性血液透析(maintenance hemodialysis,MHD)患者发生慢性肾脏病-矿物质骨异常(chronic kidney disease-mineral and bone disease,CKD-MBD)的始动因素与核心环节[1],高磷血症增加MHD患者心血管疾病发病率和死亡率已被广泛认识[2]。根据全球透析预后和实践模式研究(DOPPS4)[3]显示,各国透析患者高磷血症控制率仍较低,而我国血磷控制情况更不理想,是所有参加DOPPS研究国家中最低的。国内多个横断面研究也显示MHD患者高磷血症发病率达55%~80%[4-5]。减少饮食中磷的摄入、使用磷结合剂和充分透析是治疗高磷血症的三大原则。国外多年前已引入营养师参与到透析患者饮食教育中,取得了很好的效果[6-7]。在本研究中,我科首次采用了医护-营养师一体化综合管理模式对30例反复高磷血症的MHD患者进行干预,取得了较好的效果,现报告如下。
对象与方法
一、研究对象
选择2018年9月至2019年3月在南宁市第一人民医院血液透析室治疗的反复高磷血症的MHD患者30例纳入本研究。入选标准:年满18周岁;初中及以上学历,且有较好的理解能力,知情同意自愿参加本研究;维持血液透析治疗3个月以上,透析次数≥5次/2周,且干预期间透析治疗方式不改变;2018年9月至2019年3月至少2次检查血磷>2.0 mmol/L;能与医护进行良好沟通者。排除标准:透析不规律,难以耐受4 h透析,预计存活期不足6个月的患者;有精神障碍、痴呆等不能良好沟通的患者;近期合并严重并发症如心力衰竭、严重感染、恶性肿瘤或其他疾病等。
二、方法
1.干预方法 组建由医生-护士-营养师组成的一体化综合管理饮食教育团队,成员包括2名医生、2名护士和1名营养师。我院血液透析室实行责任医生-护士负责制,医生与护士组成责任小组,分组负责MHD患者的日常管理。本次研究针对反复高磷血症患者,因此特邀1名营养师与医护组成一体化综合管理团队,对30例患者分别进行多对一的综合饮食指导,干预时间为3个月(90 d)[8-10]。
(1)一体化综合管理团队自行设计CKD-MBD高磷血症相关知识问卷:对30例患者进行问卷调查,了解MHD患者对钙磷代谢知识的掌握情况。调查表内容从疾病相关知识、饮食管理相关知识、药物治疗相关知识、自我管理行为4个方面进行,共10题,每题1分。问卷具体内容见表1。根据调查结果针对患者的不足之处反复对其进行宣教。

表1 高磷血症相关知识问卷
(2)由团队自行设计制作“高磷血症透析患者健康宣教手册”:手册内容主要针对“高磷血症相关知识问卷”中的问题,涵盖高磷血症的危害,介绍高磷、低磷食物,合理使用磷结合剂等相关的知识。宣教时将手册发放给患者并进行详细讲解,使患者明确血磷控制的目标,充分认识高血磷的危害、低磷饮食和合理用药的重要性等。
(3)营养师将《中国食物成分表》[11]发给入组患者,指导患者尽可能根据成分表中各类食(谷薯类、蔬菜水果类、豆类、肉蛋奶类、坚果油脂类)磷的含量由低到高进行食物的选择:建议选择低磷尤其是低磷/蛋白比值的饮食,例如:鸡蛋白(磷/蛋白比值 1.6 mg/g)、猪皮(磷/蛋白比值1.4 mg/g)、鹅蛋白(磷/蛋白比值1.2 mg/g)、海参(磷/蛋白比值1.7 mg/g)等。指导患者尽量避免各种高磷食物,例如:蛋黄、动物内脏、坚果类、豆类、乳酪、巧克力以及含食品添加剂多的加工食品和饮料等。建议患者在烹饪肉类食物前先进行焯水处理。饮食的教育对象包括患者以及家属,尤其是为患者做饭的家属。
(4)营养师指导患者进行3 d饮食回顾:3 d饮食回顾需包括连续的一个透析日、一个非透析日、一个周末的饮食情况。记录好后由营养师通过“饮食成分计算软件”计算患者饮食中的热量、蛋白质、磷、钾的摄入量(取平均值),并计算磷/蛋白比值。
(5)由责任医师和护士指导并督促入组患者正确方式服用磷结合剂:避免存在漏服或错误方式服用磷结合剂,强调要餐中或餐后立刻服用,根据服药种类指导药物是否需要嚼服。
2.评价指标
(1)患者对高磷血症知识的掌握情况:干预前、后3个月,应用自行设计的高磷血症相关知识问卷进行调查,了解患者对高磷血症知识的掌握。
(2)患者营养状况:干预前、后3个月营养师对患者进行体重指数(body mass index,BMI)、上臂围、肱三头肌皮褶厚度的测量,并进行主观综合营养评估(subjective global assessment,SGA)[12]。SGA主要包括近半年体质量和营养摄入的变化、胃肠道症状、水肿情况、皮下脂肪和肌肉消耗程度、功能活动情况等内容。
(3)患者实验室检查:干预前、后3个月每例入组患者留取透析前血标本检测血清钙(Ca)、磷(P)、肌酐(Cr)、尿素氮(BUN)、C反应蛋白(CRP)、血红蛋白(Hb)、白蛋白(Alb)、甲状旁腺素(iPTH)等指标,并进行透析充分性(URR)的计算。
(4)患者饮食摄入情况:干预前、后3个月通过对患者“3 d饮食回顾”进行核对与分析,由营养师分别计算出每例患者平均每天饮食摄入的热量、蛋白质、磷、钾的摄入量,并计算磷/蛋白比值。
三、统计学处理
采用SPSS25.0软件进行统计分析,连续性变量符合正态分布采用均数±标准差、不符合正态分布采用中位数(四分位数)、构成比等进行描述性统计。干预前、后3个月的高磷血症知识问卷得分、实验室检查结果、每日饮食的摄入量、上臂围、肱三头肌皮褶厚度等采用配对t检验或秩和检验进行分析。以P<0.05为差异具有统计学意义。
结 果
一、一般资料
本研究共入组MHD患者共30例,其中男性20例(66.7%),女性10例(33.3%);年龄(53.6±10.6)岁;透析龄为4~169个月,中位数35.1个月;平均每周总透析时间(11.0±1.6)h;原发疾病组成:慢性肾小球肾炎12例(40.0%),高血压肾损害9例(30.0%),糖尿病肾病7例(23.3%),系统性血管炎肾损害1例(3.3%),肾小管间质性疾病1例(3.3%)。
二、干预前后患者高磷血症知识问卷得分与患者营养状况的比较
患者高磷血症知识问卷得分在干预后得到明显提高,差异有统计学意义(P<0.01)。干预前后患者营养状况、SGA评分与BMI(因干预时间<6个月,干预后未评价),上臂围、肱三头肌皮褶厚度没有明显变化,差异没有统计学意义(P>0.05)。(表2)
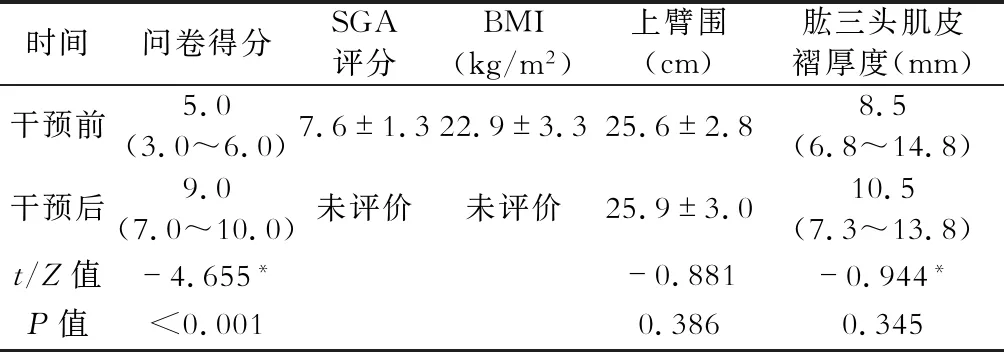
表2 干预前、后患者高磷血症知识问卷得分与患者营养状况的比较
注:*为Z值
三、干预前、后患者实验室检查结果的变化
干预后患者血清磷(P)、钙磷乘积(Ca×P)水平明显下降,差异有统计学意义(P<0.01),血清校正钙(Ca)、肌酐(Cr)、C反应蛋白(CRP)、血红蛋白(Hb)、白蛋白(Alb)、甲状旁腺素(iPTH)、透析充分性(URR)没有明显变化,差异没有统计学意义(P>0.05)。干预后7例患者血磷≤1.78 mmol/L,达标率为23.3%(7/30)。(表3)

表3 干预前、后患者实验室检查结果的变化
注:*为Z值
四、干预前、后患者饮食摄入量的变化
干预后患者饮食中的热量与干预前相比,差异没有统计学意义(P>0.05)。干预后患者饮食中蛋白质、磷、钾的摄入量和磷/蛋白比值与干预前相比,差异有统计学意义(P<0.05)。(表4)
讨 论
目前,国内透析患者的饮食宣教还是以血液透析室护士“口头教育”为主,很难以使患者主动接受,依从性较低[13],能够记住的内容十分有限,因此患者对高磷血症的相关知识掌握普遍较差。本研究中,干预前入组患者高磷血症知识问卷调查得分仅5分(中位数),可想而知患者在日常饮食的实际操作过程中依从性更差。有研究[14]发现,78%的MHD患者知道食用含高磷酸盐食物的危害,但仍有51%喝汽水,39%吃快餐。因此,如何提高患者对高磷血症治疗的依从性是亟待解决的问题。本研究中,我们采用了“医护-营养师一体化综合管理模式”,通过对患者及家属发放“高磷血症透析患者健康宣教手册”、《中国食物成分表》[11],由营养师计算每例患者实际饮食摄入量,及时指出存在问题,给予个体化的指导,推荐患者根据“食物磷金字塔”选择低磷/蛋白比值食物,“食物磷金字塔”以图像的形式涵盖了大量食物磷的信息,更具有科学性、全面性、直观性[15];干预团队及时追踪患者饮食实际操作情况并给予建议,使透析患者及家属依从性明显提高,干预3个月后问卷调查得分升高至9分(中位数),差异有统计学意义。因此,透析患者在饮食教育方面对营养师有更高的依从性,与国内、外研究结果一致[6-7,10]。

表4 干预前后患者饮食摄入量的变化
注:*为Z值
在本研究中,责任医生-护士-营养师的团队合作和及时追踪、反馈是非常重要的。营养师在对每例患者进行饮食分析后,指出存在问题,责任医生和护士会与营养师一起面对面与患者和家属进行反馈,此后至少每1~2周追踪一次患者实际饮食情况,存在问题及时与营养师沟通,营养师根据实际情况对患者进行个体化指导。此外,责任医生、护士积极督促患者正确服用磷结合剂,大大提高患者服用磷结合剂的依从性及正确性,并对在饮食及服药方面有进步的患者给予积极肯定和表扬。通过这种及时关注及给予激励的方式,促使患者更加关注饮食和血磷的变化,达到持续有效的教育目的。在本研究干预3个月后,绝大多数患者(26/30)血磷较干预前有所下降,差异有统计学意义,其中7例患者血磷降至1.78 mmol/L以下,达标率为23.3%(7/30)。
在本研究中,干预3个月后患者饮食中的热量没有明显变化,蛋白质、磷的摄入量和磷/蛋白比值较干预前有所下降,差异有统计学意义。蛋白质摄入量下降可能与部分患者通过减少蛋白质摄入以减少磷的摄入量。干预前、后磷/蛋白比值下降与患者通过饮食教育后更多选择磷/蛋白比值低的食物有关。尽管部分患者长期形成的饮食偏好和烹饪习惯短时间内难以改变,但通过干预团队个体化的教育和低磷/蛋白食物的推荐,患者已有意识的在食物的选择上作出改变。在干预3个月后磷/蛋白比值由21.02降至12.87,达到了磷/蛋白比值(12~14)的理想范围[16]。干预后患者的血清白蛋白、血红蛋白水平和营养状况评估指标(上臂围、肱三头肌皮褶厚度)并没有下降,提示患者选择低磷/蛋白比值的食物不会造成营养状况的恶化,甚至可能会改善,但是其对透析患者长期影响仍须进一步研究。同时,本研究发现干预后患者饮食中钾的摄入量也有明显下降,差异有统计学意义,这可能与推荐的低磷食物中含钾量较低有关。
本研究存在的一些不足之处:首先,本研究是一项单中心研究,样本量较小,且为自身前后对照研究,没有设置平行对照;研究结果可能并不都是干预的效果。但本研究的研究对象都是稳定透析且反复高磷血症的MHD患者(干预前血清磷均>2.0 mmol/L),干预前、后透析次数及充分性也没有变化,说明高磷血症的控制更多和研究干预有关。第二,在饮食调查中,有少量患者饮食磷摄入未超标,但仍有反复高磷血症,考虑不能排除与患者服药有关,近年来越来越多的研究关注透析患者药物含磷情况[17],患者反复高磷血症可能与此有关,在进一步的研究中将考虑分析患者服用药物的含磷情况。最后,此次研究干预随访的时间较短,如何维持干预的长期效果仍须进一步的研究,至此次研究结束时,虽然患者平均血磷水平下降明显,但是仍然有76.7%的患者血磷没有达标,对于这些患者血磷的控制,需要进一步评估干预。
小结本研究显示,医护-营养师一体化综合管理模式能够有效提高MHD患者有关高磷血症知识水平,降低血磷水平,降低饮食中磷摄入量且不影响患者营养状况,是一种有效、可行的管理MHD患者顽固高磷血症的方法。
2017年KDIGO指南[18]建议透析患者血磷目标值控制在正常值范围(0.81~1.45 mmol/L)较2003年NKF/KDOQI指南[19]的目标值1.13~1.78 mmol/L更为严格,表明控制血磷的重要性。然而,目前国内高磷血症MHD患者比例仍很高,如何进一步提高患者低磷饮食的依从性,维持血磷长期达标,仍是一项艰难的挑战,增强营养师在这项工作中的作用将有非常积极的意义。

