具有染料选择性吸附的杂多酸季铵盐制备与性能研究
汤惠睫,韩 哲,俞天寿,张 明,金红晓,葛洪良,王新庆,金顶峰
(1.中国计量大学 材料与化学学院,浙江 杭州 310018; 2.中国计量大学 质量与安全工程学院,浙江 杭州 310018)
种类繁多、成分复杂的染料是印染废水中的主要污染物,一般以芳烃和杂环为母体,属于较难降解的有机污染物且多具有致癌、致畸和致突变作用。其直接排放严重破坏生态环境并威胁人体健康,因此如何有效地处理印染废水成为重要研究方向。目前主要的处理方法包括有混凝沉淀法、化学氧化法、膜分离法及生物法等[1-5],但是存在应用范围窄、投资大、有二次污染等缺点。相比较而言吸附法在印染废水处理中使用得最多,一般采用活性黏土、离子交换树脂、膨润土、硅藻泥、活性炭、粉煤灰和煤渣等作为吸附剂,具有成本低、设备简单和容易再生利用等优点[6,7]。然后,传统的吸附剂因缺乏良好的选择性和不容易解吸附等限制了其进一步发展。
杂多酸(Polyoxometalates,简写为POMs)是由杂原子(如P、Si、Fe、Co等)和多原子(如Mo、W、V、Nb、Ta等)通过氧原子配位桥联按一定的结构组成的一类含氧多酸,是一种多功能的新型催化剂,可作非均相或均相反应,甚至可作相转移催化剂,对环境无污染[8-10]。由于杂多化合物可以通过改变抗衡阳离子来调节其结构,从而改变其性能,使其在新的领域中得到应用。通过季铵盐离子和杂多酸离子生产杂多酸季铵盐,具有良好的染料吸附选择性,可作为吸附剂被应用到水处理行业中[11-14]。
本文采用多种不同浓度比的钼酸钠、磷酸氢二钠、偏钒酸钠和四丁基溴化铵溶液,分别将制得的三种磷钼钒杂多酸季铵盐;通过红外光谱、XRD、氮气吸脱附、SEM等对杂多酸季铵盐进行表征和结构分析。研究了其在模拟废水中对亚甲基蓝(MB)和甲基橙(MO)染料的吸附性能,并通过对两种染料的选择性吸附实验探讨了可能的吸附机理。
1 实验部分
1.1 样品的制备
以NaVO3、Na2HPO4和Na2MoO4为反应物,按P/Mo/V比(P/Mo/V=1∶5∶10、1∶9∶3.2、1∶11∶1)制备样品。首先将NaVO3和Na2HPO4溶于去离子水中,在混合液中加入Na2MoO4·2H2O,调节pH值至2.2,在80 ℃下加热2 h,用乙醚和稀H2SO4(1∶1)混合液萃取,然后加入四丁基溴化铵溶液。让溶液在室温下静置2 h,结晶并纯化。最后,对溶液进行抽滤,滤饼在80 ℃下转移到烘箱中干燥。
1.2 材料测试
本实验中,样品的傅里叶变换红外光谱在FTIR分光光度计(Vertex 70,Bruker German)上测量;X射线衍射(XRD)在日立公司的Smartlab测得,测试的衍射角度范围为5°~60°,步长为0.02°/s;氮气吸附-脱附测试采用美国麦克公司的比表面积及孔径分析仪(ASAP 2020);扫描电镜(SEM)采用冷场发射扫描电子显微镜测试(SU8010 FE-SEM);在Zeta-sizer仪器上测量了样品的Zeta电位;紫外-可见光谱在UV3600分光光度计上获得。
1.3 等温吸附(P/Mo/V=1∶5∶10,1∶9∶3.2,1∶11∶1)
将20 mg吸附剂在25 ℃下放置于含有不同浓度染料溶液的20 mL烧瓶中,在经过吸附、离心、稀释后,取出部分溶液,用UV3600分光光度计测定样品浓度。
Langmuir等温线方程如下:
Freundlich等温线方程如下:
其中:Ce是吸附剂的平衡质量浓度,mg·L-1;Qe是吸附剂的平衡吸附容量,mg·g-1;KL是朗格缪尔平衡常数,L·mg-1;Qmax是染料对样品的最大吸附容量;KF是Freundlich平衡常数;n是描述吸附强度的指数。
1.4 选择性染料吸附(P/Mo/V=1∶9∶3.2)
将样品放入相同质量浓度(30 mg·L-1)的染料混合物(MB+MO)溶液中。通过测定吸附峰的位置和溶液的颜色变化,计算选择性的吸附容量。
2 结果与讨论
2.1 红外光谱分析
C16H36BrN-PMo5V10,C16H36BrN-PMo9V3.2和C16H36BrN PMo11V1的红外光谱如图1。PMo11V1在700~1 100 cm-1有四个特征吸收峰,806 cm-1左右的峰归属于M-Oc-M(M=Mo,V)的拉伸振动峰,880 cm-1左右的峰归属于M-Ob-M(M=Mo,V)的拉伸振动峰,955 cm-1左右的峰归属于Mo=O和V=O的反对称拉伸振动峰,1 062 cm-1左右的峰归属于P-O的反对称拉伸振动峰[14]。在PMo5V10和PMo9V3.2的红外光谱中,相比于PMo11V1,Mo=O和V=O处的反对称拉伸振动峰移动了12~15 cm-1,这表明Mo已被V逐渐取代。同时,P-O键和M-Oc-M也分别有2~5和2~3 cm-1的偏移[5]。
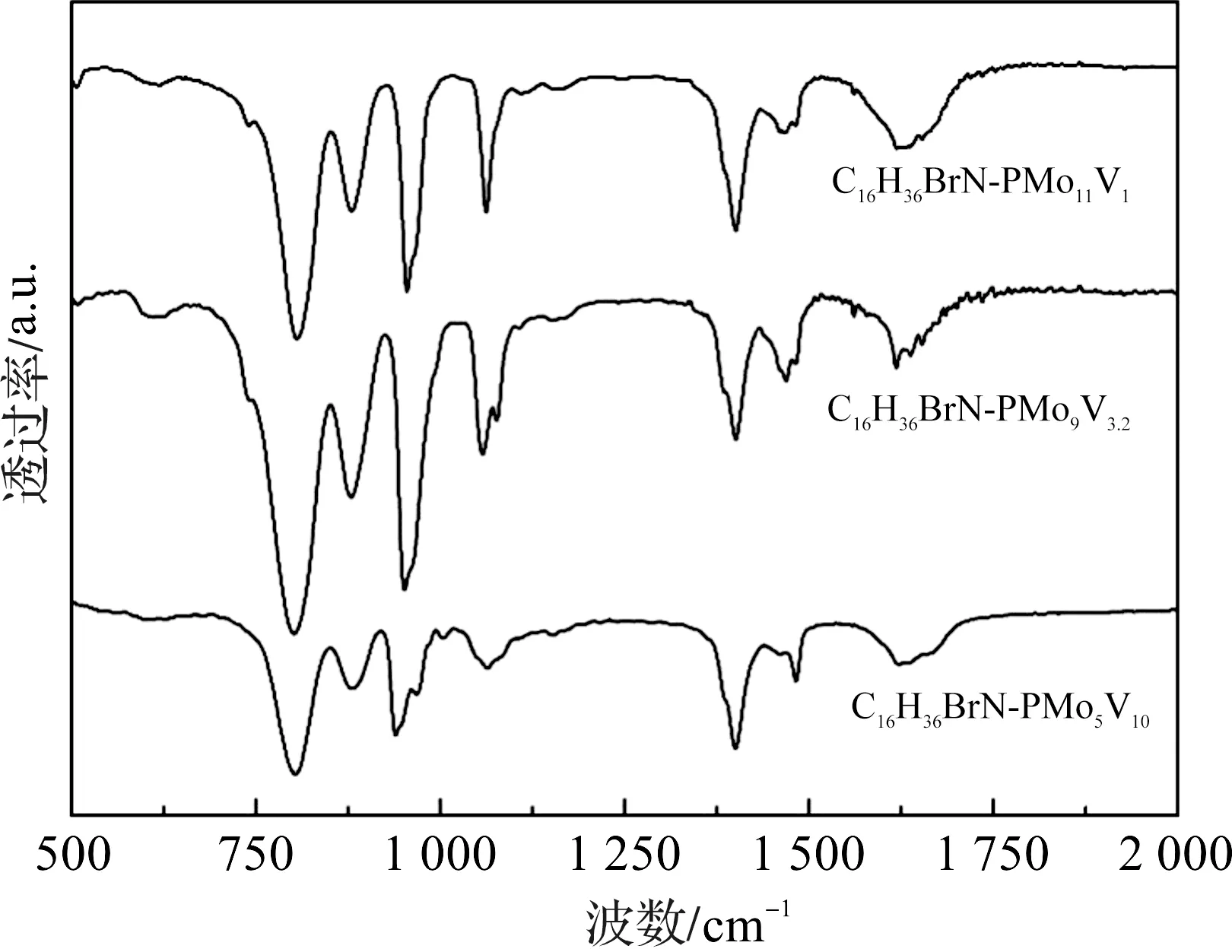
图1 不同磷钼钒杂多酸季铵盐的红外光谱图Figure 1 FTIR patterns of different polyxometalate
2.2 XRD分析
C16H36BrN-PMo5V10、C16H36BrN-PMo9V3.2和C16H36BrN-PMo11V1的XRD结果如图2。从图2(a)(b)(d)可以看出,C16H36BrN-PMo9V3.2和C16H36BrN-PMo11V1在2θ=7.0°,7.7°,8.1°,8.5°,9.3°有5个特征吸收峰,表明样品仍具有Keggin型杂多酸结构[15-17]。C16H36BrN-PMo5V10在2θ=6.64,7.6有2个特征吸收峰,表明样品的Keggin型杂多酸结构仍然存在,但是更多的钒取代使得结构对称性提高,衍射峰的数目得以减少。三个样品在5°~10°的特征峰会发生微量的偏移,这是由于钼原子逐渐取代钒原子,使得衍射角度发生了偏移。另外,三个样品在19°~25°和27°~31°具有较明显的特征峰,是由于引入的季铵盐阳离子与杂多阴离子反应形成了磷钼钒杂多酸季铵盐[13]。
2.3 N2吸附-脱附分析
样品的N2吸附-脱附表征结果如图3,数据结果总结在表1中。由表1可以看出,C16H36BrN-PMo11V1、C16H36BrN-PMo9V3.2和C16H36BrN-PMo5V10的比表面积分别为0.589 9、1.928 4和6.249 2 m2/g,可以看出V原子在取代Mo原子的过程中,样品的比表面积在逐渐增加。另外,从表1中可以看出样品的孔容很小,说明样品在吸附亚甲基蓝和甲基橙染料的过程,微孔吸附作用的染料较少。
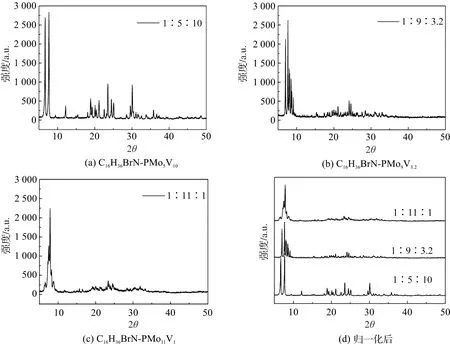
图2 不同磷钼钒杂多酸季铵盐的XRD图Figure 2 XRD patterns of different polyoxometalate
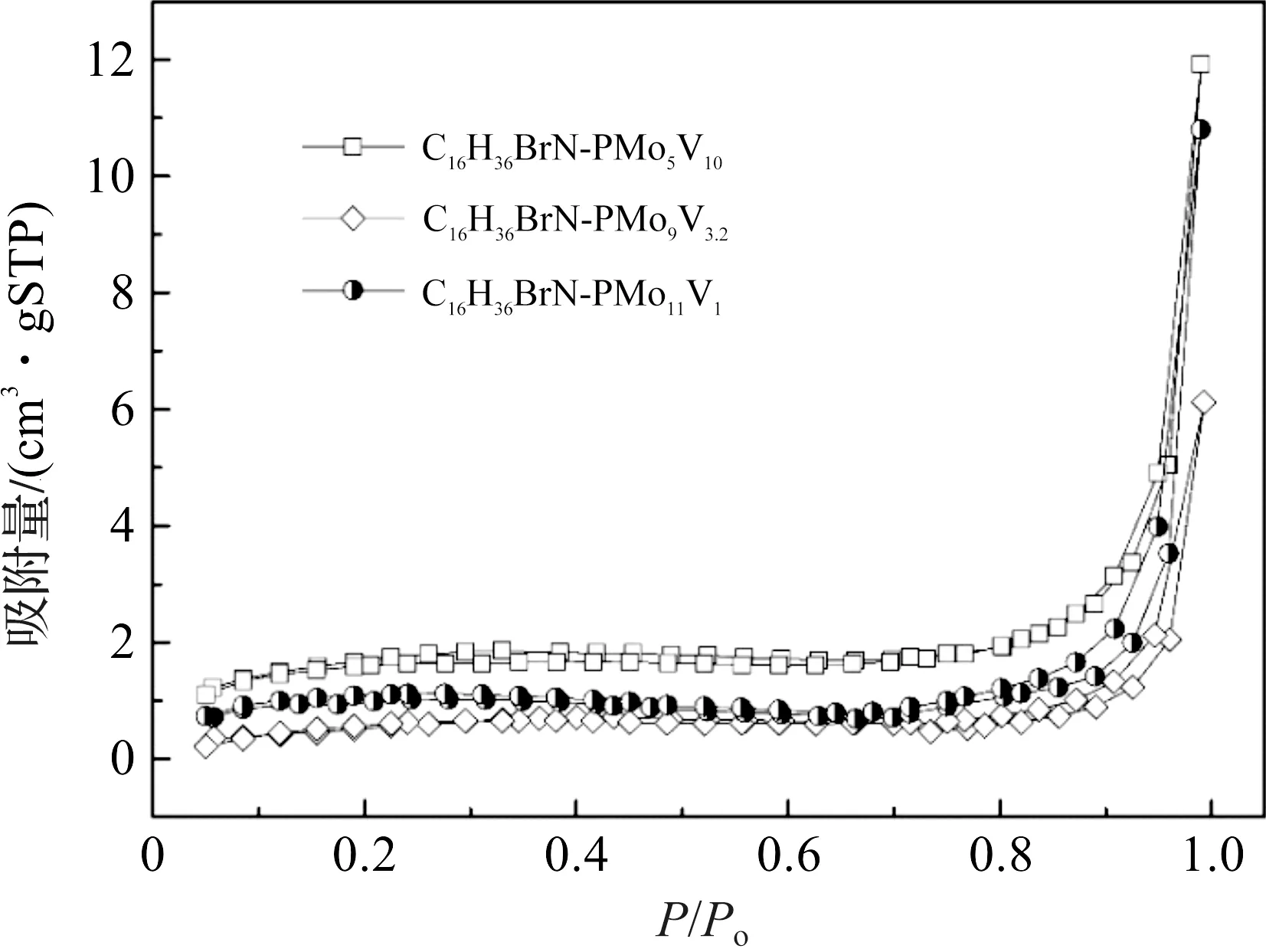
图3 不同磷钼钒杂多酸季铵盐的N2吸附-脱附表征Figure 3 N2adsorption-desorption analysis of different polyxometalate
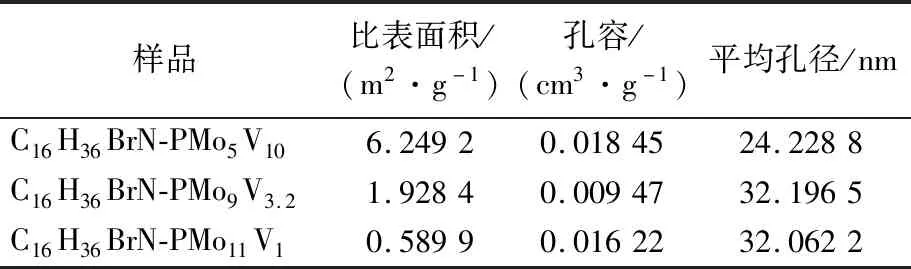
表1 C16H36BrN-PMo5V10,C16H36BrN-PMo9V3.2和C16H36BrN-PMo11V1的N2吸附-脱附数据Table 1 N2 adsorption-stripingdate of C16H36BrN-PMo5V10,C16H36BrN-PMo9V3.2 and C16H36BrN-PMo11V1
2.4 等温吸附(P/Mo/V=1∶5∶10,1∶9∶3.2,1∶11∶1)
以亚甲基蓝为目标吸附质,分析了杂化材料C16H36BrN-PMo5V10,C16H36BrN-PMo9V3.2和C16H36BrN-PMo11V1的吸附性能。不同初始质量浓度下的吸附等温线和相应的亚甲基蓝在样品上的吸附百分率如图4(对于PMo9V3.2,MB的初始质量浓度范围为10~200 mg·L-1,对于PMo5V10和PMo11V1,MB的初始质量浓度范围为10~100 mg·L-1)。对于PMo5V10和PMo11V1,当MB初始质量浓度大于30 mg·L-1时,吸附量分别达到18.98 mg·g-1和14.42 mg·g-1,而PMo9V3.2的吸附量为105.32 mg·g-1。
分别采用Langmuir模型和Freundlich模型来拟合数据分析吸附过程,结果如图5。采用Langmuir模型的拟合结果R2值表明该模型适用于描述磷钼钒杂多酸季胺盐对亚甲基蓝的吸附结果。然而,如表2所示Freundlich模型的拟合结果R2值相对于Langmuir模型较低(PMo5V10为0.745 1,PMo9V3.2为0.927 6,PMo11V1为0.821 9),表明该模型不适用于样品的吸附数据。根据朗格缪尔模型,计算了PMO5V10、PMO9V3.2和PMO11V1对亚甲基蓝最大吸附容量分别为19.326 8 mg·g-1、117.302 6 mg·g-1和14.487 7 mg·g-1,如图4(d)。结果表明,MB在样品上的吸附为单层吸附。
此外,还测试了样品的Zeta电位,如表2。PMo5V10、PMo9V3.2和PMo11V1水溶液的Zeta电位分别为-23.4、-28和-20.1 mV。结果表明,由于样品自身带有负电,而亚甲基蓝带有正电,样品的吸附容量与其电负性有关,吸附结果证明了二者的吸附过程是因为静电吸附作用的结果。
2.5 染料选择性吸附(P/Mo/V=1∶9∶3.2)
本文选用MB(阳离子染料)和MO(阴离子染料)对PMo9V3.2的的选择性吸附进行了评价。图5显示了PMo9V3.2吸附前后混合溶液(MB/MO,v∶v=1∶1,30 mg/L,30 mg/L)的紫外可见光谱,同时显示了吸附前后MB、MO和混合溶液的示例图。此外,用紫外可见分光光度仪测定了MB(665 nm)和MO(465 nm)的特征峰。吸附后,MB在665 nm处的特征峰消失,而MO在465 nm处的峰保留下来,证明样品对阳离子染料的吸附有响应。实验结果表明,该样品对阳离子染料的吸附反应灵敏,可用于废水中阴阳离子染料的分离。C16H36BrN-PMo5V10、C16H36BrN-PMo9V3.2和C16H36BrN-PMo11V1的SEM结果如图5(a)(b)(c)。在图中可以看出三种杂多酸季铵盐均呈现出块状的结构,有部分的块状结构呈现出完整的长条状,部分样品有形成管状的结构,主要是因为四丁基溴化铵为一种模板剂,制备过程中会形成部分的管状模板;随着钒对钼的取代的增加,杂多酸季铵盐的颗粒会变小,使材料的比表面积增大,但其对染料吸附的影响并不是很大。

表2 样品上亚甲基蓝的吸附等温线模型参数及样品的Zeta电位Table 2 Adsorption isotherm model parameters of MB adsorption onto samples and Zeta potentials of the samples
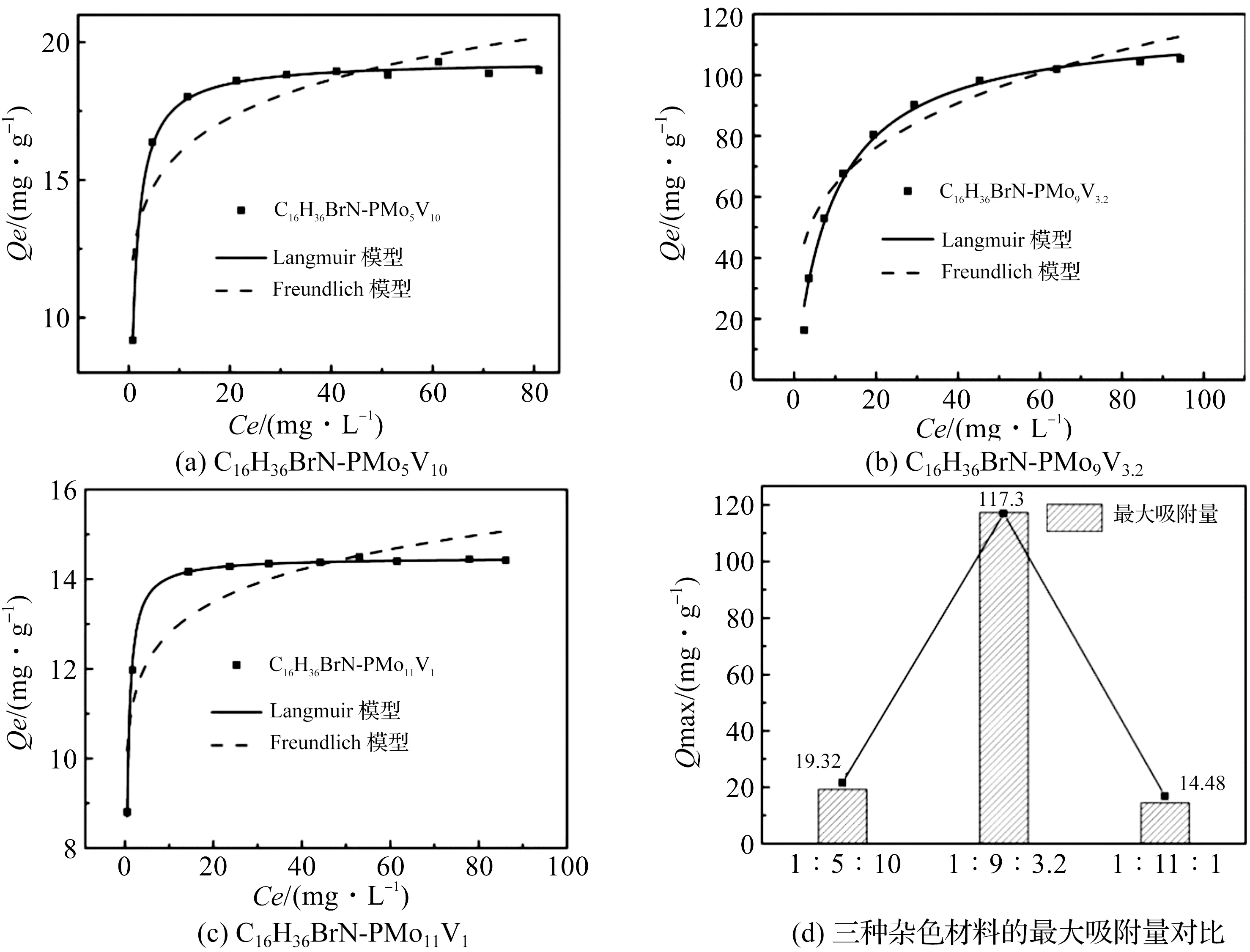
图4 MB的吸附等温线以及用Langmuir和Freundlich模型拟合的曲线Figure 4 Adsorption isotherm of MB andfitting curve by Langmuir model and Freundlich model of sample
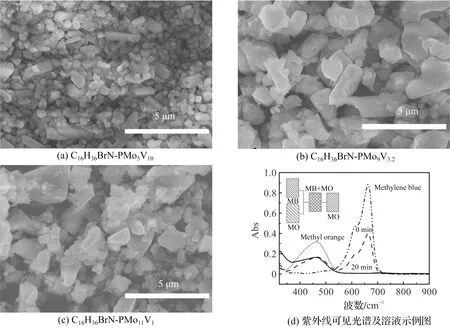
图5 C16H36BrN-PMo5V10、C16H36BrN-PMo9V3.2、C16H36BrN-PMo11V1的SEM表征Figure 5 SEM patterns of C16H36BrN-PMo5V10,C16H36BrN-PMo9V3.2 and C16H36BrN-PMo11V1
3 结 语
采用简单的先合成杂多酸盐再制备得到杂多酸季铵盐的方法,合成了三种具有不同钒取代的季铵盐,并对其进行了表征。结果表明随着钒取代的增加,红外上的反对称拉伸振动峰会有所偏移;XRD结果表明Keggin结构得到保持,同时有季铵盐阳离子与杂多阴离子反应形成了磷钼钒杂多酸季铵盐的特征峰;氮气吸脱附结果表明随着钒取代的增加样品的比表面积在逐渐减小;同时样品的孔容很小,说明样品在吸附亚甲基蓝和甲基橙染料的过程,微孔吸附作用的染料较少。通过吸附实验考察了杂多酸季铵盐的染料吸附结果,并采用Langmuir模型和Freundlich模型来拟合数据,结果表明MB在样品上的吸附为单层吸附,PMO5V10、PMO9V3.2和PMO11V1对亚甲基蓝最大吸附容量分别为19.326 8 mg·g-1、117.302 6 mg·g-1和14.487 7 mg·g-1;样品的Zeta电位结果表明,样品的吸附容量与其电负性有关,由于样品自身带有负电,而亚甲基蓝带有正电,吸附结果证明了二者在吸附的过程是因为静电吸附的作用。最后将亚甲基蓝和甲基橙混合溶液进行选择性吸附,结果表明其具有较好的亚甲基蓝选择性吸附。

