A 型塞内卡病毒研究进展
刘枢清,孙秀峰,何宇乾
(1.青岛市动物疫病预防控制中心,山东青岛 266199;2.青岛市畜牧兽医研究所,山东青岛 266121)
A 型塞内卡病毒(Senecavirus A,SVA),旧称塞内卡谷病毒(Seneca Valley virus,SVV),属于小RNA 病毒科(Picornaviridae)塞内卡病毒属(Senecavirus)成员。该病毒于2002 年在美国马里兰州的“塞尼卡河州立公园(Seneca Creek State Park)”附近的实验室首次被发现,具有偶然性,最初是从被胎牛血清或猪胰蛋白酶污染的PER.C6细胞系中分离到[1],而来自猪胰蛋白酶污染来源的可能性更大,因为大量与SVA 血清学相关的病毒都分离自猪。
SVA 自2007 年逐渐在加拿大、美国、巴西等国家暴发。2015 年我国广东省首次发现该病毒,随后逐渐蔓延至其他省份。猪感染SVA 后的临床表现与感染口蹄疫病毒(foot-and-mouth disease virus,FMDV)类似,通常表现为沉郁、体温升高、厌食、跛行、蹄部和鼻吻出现水疱[2]。水疱是该病的典型症状,蹄部水疱常见于蹄冠带和趾间隙[3]。SVA 感染的诊断目前主要依赖于病原学和血清学方法,防控方面仍无商品化疫苗可用。另外,随着SVA 在我国的传播,其毒力也逐渐致弱,目前国内猪场已频繁出现亚临床感染情况[4]。大量的亚临床感染及无商品疫苗可用,增加了我国对该病的防控及净化难度。
1 分子生物学
1.1 SVA 粒子结构
SVA 结构(图1)与FMDV 类似,为非囊膜正二十面体结构,T 值为3,直径约27 nm,内部为病毒核酸。病毒含4 种结构蛋白,分别为VP1、VP2、VP3 和VP4,其中VP1、VP2 和VP3 构成了病毒衣壳的外层结构,VP4 在衣壳内部。
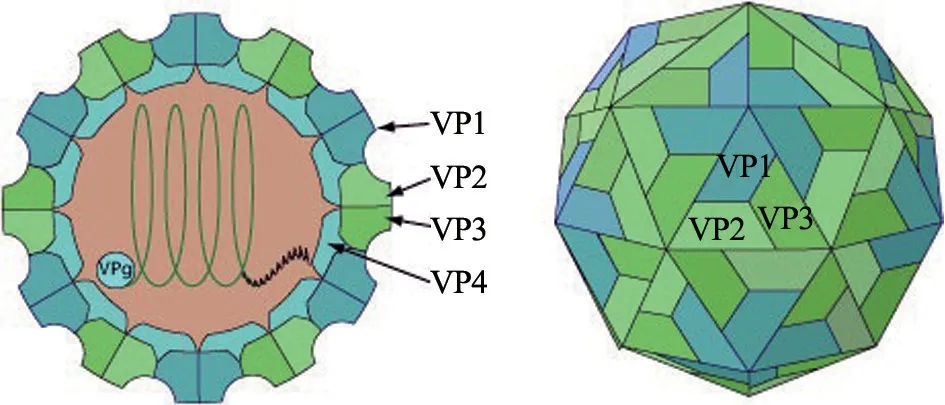
图1 A 型塞内卡病毒结构
1.2 SVA 基因组
SVA 基因组(图2)为单股、线性、正义RNA,长度约为7 300 nt。基因组5'末端结合VPg,为非帽子结构,靠近5'末端为IV 型内部核糖体进入位点(internal ribosome entry site,IRES),为蛋白翻译的上游非编码区域,约666 nt。基因组3'末端为poly(A)结构,长度约为70 nt[5]。SVA 基因组仅含有一个较长的开放阅读框(open reading frame,ORF),编码一个约2 180 aa 的多肽,而后经过进一步加工,形成不同的结构蛋白和非结构蛋白。
各蛋白在基因组中呈“L-4-3-4”样排列(图2),即“Leader-4 个P1 区多肽-3 个P2 区多肽-4个P3 区多肽”。P1 区对应结构蛋白VP0、VP3和VP1,VP0 又进一步加工形成VP2 和VP4。P2和P3 区对应非结构蛋白,主要参与蛋白加工和病毒复制。所有非结构蛋白中,2A 蛋白的形成机制较为特殊,其总长为9 aa,羧基末端为保守基序NPG/P,因此可通过核糖体跳跃机制使蛋白翻译“中止”但不“终止”[5]。
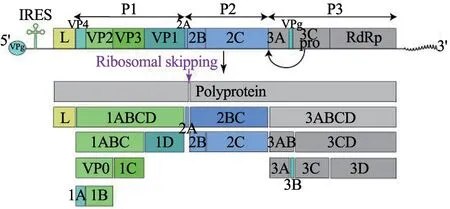
图2 A 型塞内卡病毒基因组结构及多聚蛋白水解图
2 临床症状
2.1 自然感染
高毒力SVA 自然感染猪后会导致典型的水疱型临床症状,与猪的某些其他疫病症状类似,如口蹄疫、猪水泡病及水泡性口炎等。动物感染SVA 后,在鼻吻处会出现水疱性病变,通常为大小不一、充满液体的水疱(图3-A),破裂后可形成溃疡面(图3-B),多日后形成结痂。水疱性及溃疡性病变多出现于蹄冠带和趾间隙,导致边缘上皮疏松坏死,严重者站立及行走困难[6]。患病动物同时伴有厌食、精神沉郁、体温升高等现象。某些患病仔猪3~10 d后,症状可消退并临床康复[7]。
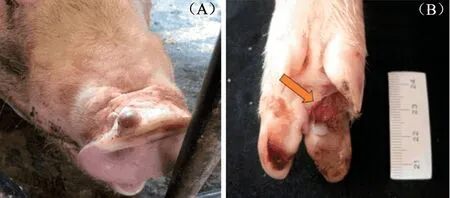
图3 猪感染SVA 的临床症状[8]
2.2 人工感染
国外学者通过动物实验深入研究了SVA 的致病机制[2-3]。通过口鼻途径进行SVA 感染动物实验,4 d 后便可观察到典型的临床症状。病毒血症持续期较短,通常维持在感染后的3~10 d。感染后1~28 d,便可在口鼻及粪便中检测病毒[2]。若为急性感染,1~5 d 后口腔中的病毒分泌量便可达到峰值[2]。2019 年Buckley 等[9]对15 只8 月龄母猪进行了SVA 鼻内感染试验,发现感染2 d 后,4 只母猪的蹄冠带便出现水疱样病变,其他母猪在感染5 d 内在该部位皆出现类似病变;6 只母猪感染4 d后,口吻部出现水疱样病变。病毒血症持续1 周,感染后7 d,出现血清中和抗体。大部分水疱样病变感染2 周后便自行消退。
国内分离株(GD-S5/2018 和GD04/2017)的小鼠感染实验结果显示,通过肌肉、皮下及口服途径感染,GD-S5/2018 株可导致较高的致死率,但GD04/2017 株却未导致明显的临床症状。猪感染实验结果显示,GD-S5/2018 株可导致典型的临床症状,如齿龈和舌部出现溃疡性病变,但GD04/2017株攻毒后,猪仅表现沉郁,未有SVA 感染的典型临床症状。这说明GD-S5/2018 是强毒株,而GD04/2017 的毒性较弱[10]。2020 年Zhang 等[11]比较了另外2 个国内分离株(HB-CH-2016 和CH/AH-02/2017)的毒力,发现CH/AH-02/2017 株可导致明显的临床症状,而HB-CH-2016 株的致病性相对较弱。
3 流行病学
3.1 国际SVA 感染情况
SVA 是一种新发病原体。2007 年加拿大首次报道了SVA 感染病例[12]。2012 年美国报道了猪群中有SVA 流行,但追溯发现2010 年已有猪群发病[13]。2014 年前,除北美地区外,SVA 未在其他地区报道,直到2014 年末,巴西报道了首例SVA感染病例[14],而与美国和加拿大不同的是,巴西的SVA 感染不仅局限于成年猪,新生仔猪亦有感染[7,15]。随后其他国家皆发现了SVA 感染的病例,包括中国(2015)[16]、哥伦比亚(2016)[17]、泰国(2016)[18]和越南(2018)[19]等。
2015—2016 年是全球局部地区的SVA 感染高发期。对此期间的SVA 分离株基因组序列进行遗传进化分析,发现各毒株间的基因同源性较高(95.8%~99.9%),而与历史株SVV-001 的同源性较低(93.8%~94.6%)。基于SVAVP1基因部分序列(541 bp)进行遗传进化分析,可将病毒分为3 个以时间为参考的基因系(Clade),分别为Clade I、Clade II 和Clade III[8]。Clade I 为SVA 原型毒株,如88-23626 株(Genbank:EU271759);Clade II 为历史毒株,如SVV-001 株(Genbank:DQ641257);Clade III 为当前毒株,如CHLX-01-2016(Genbank:KX751945)。Clade III 基因系毒株最多,包括美国、加拿大、巴西、中国和泰国的分离株。
3.2 国内SVA 感染情况
2015 年,SVA 首次传入我国广东省2 个猪场,导致猪群出现水疱型病变及新生仔猪死亡。在排除口蹄疫、猪水疱性口炎等疑似疫病后,最终确诊为SVA 感染[16]。2016 年,湖北省某猪场出现SVA 感染病例[20],其分离毒株(HB-CH-2016 株)与广东省首个分离毒株(CH-01-2015)核酸同源性极高,说明两次疫情具有密切的流行病学相关性。2016年12 月,黑龙江省某猪场的育肥猪经检测感染SVA,其分离株与美国毒株同源性高于其他中国毒株,说明此次黑龙江分离株可能源自美国。2017 年,河南省和福建省几乎同时报道了SVA 感染[6],分离自这两个省份的3 个毒株间具有极高的核酸同源性,说明三者可能源自同一毒株。
近些年,SVA 在我国某些省份再次出现,尤其广东省时常有SVA 感染的报道[21-24],且分离株已呈现出不同的进化分支。张志等[25]将2016—2018 年15 个省份的数百份临床病料进行检测,发现大部分省份皆检测到阳性。结合已有报道,目前SVA 感染的省、自治区和直辖市包括广东、广西、云南、贵州、湖南、福建、四川、湖北、河南、山东、新疆、上海、辽宁和黑龙江等14 个,表明SVA 已在我国不同地域广泛流行。2019 年代蕾等[26]报道了海南省同样存在SVA 感染,应用间接 ELISA 方法,对海南省2 547 份猪血清样品进行SVA 抗体检测,结果抗体阳性率为10.9%。
SVA 自2015 年传入我国后,已进化出5 个遗传分支。遗传进化分析表明,大部分分离株与美国毒株的同源性较高[24]。SVA 在我国正以较快的速度进化,同时不断有报道称,毒株间已发生重组并形成新的重组病毒[27-29]。病毒间的重组,使SVA在我国的遗传多样性更加复杂,因而也增加了潜在的跨物种传播风险。
4 诊断方法
4.1 病原学诊断
因SVA 为RNA 病毒,所以目前建立的病原学检测方法为基于RNA 的检测。针对的检测区域主要为基因组的3D、5'端UTR 或VP1 内部的保守片段,建立的方法为常规RT-PCR[30-31]、定量RT-PCR[32-34]、数字RT-PCR[35-36]及RT-LAMP[37-38]等,另有SVA 和FMDV双重RT-PCR检测方法的报道[39]。病原学检测,尤其定量RT-PCR,其敏感性可达10 拷贝/μL,且与口蹄疫、水泡性口炎等类似疫病无交叉反应,因此是常见的临床核酸检测方法。数字PCR 技术是一种核酸分子绝对定量技术,已应用至SVA 感染的病原学检测。相较于荧光定量PCR,数字PCR能够直接对核酸分子拷贝数进行绝对定量。然而,病原学检测的缺点显而易见,即病毒在不同组织的载量(或排毒量)随时间变化的差异性会导致检测结果出现差异。因此,为保证检测结果的准确性,应尽量采集不同组织的样品用于检测,如血清、淋巴结、粪便、唾液及水疱液等[8]。
4.2 血清学诊断
SVA 血清学诊断主要是基于血清抗体的检测,目前已建立的方法包括间接ELISA[40]、竞争ELISA[41-42]及病毒中和试验[41]等。竞争ELISA 是目前应用最为广泛的血清学检测方法,也有商品化检测试剂盒在售。该方法的敏感性和特异性较为理想,推荐临床检测使用。病毒中和试验的敏感性和特异性皆高于竞争ELISA[41],但操作过程复杂,且需数日才可判定结果,因此不适用于SVA 感染的快速诊断。
5 疫苗研发
SVA 在猪群中流行已有十余年,但仍无商品化疫苗,猪场只能采用生物安全措施对其进行防控,因此开发高效疫苗至关重要。
5.1 活疫苗
SVA 在体内能诱导体液及细胞免疫反应[43]。2019 年Sharma 等[44]通过反向遗传技术拯救了一株重组SVA,并在猪体内评估了重组病毒的免疫原性及免疫保护性。结果显示,重组病毒是一株弱毒株,动物经接种后未出现明显临床症状,病毒血症及排毒现象都相对较弱。虽然毒力致弱,但重组病毒依然维持着较理想的免疫原性。4 周龄仔猪经单次肌内注射及滴鼻免疫后,可在免疫后3~7 d 内产生较高滴度的中和抗体。除了诱导体液免疫反应,重组活病毒还可诱导记忆性T 细胞(CD4+、CD8+及CD4+/CD8+T 细胞)的增殖反应。而且,仔猪经免疫后可以耐受异源SVA 的人工感染,攻毒后并未表现出明显临床症状,且病毒血症、排毒量及组织病毒载量都有所降低,说明该重组SVA 是一株有效的活疫苗候选株。
5.2 灭活苗
虽然活疫苗可以诱导理想的体液及细胞免疫反应,但具有潜在的生物安全风险,如毒力反强。而灭活苗不具有潜在的生物安全风险,因此是另一种理想的候选疫苗。2018 年Yang 等[45]通过二乙烯亚胺将SVA 灭活后,与油佐剂混合乳化制备了灭活疫苗。动物免疫试验显示,该灭活苗可诱导理想的中和抗体反应,且攻毒后动物未表现出明显临床症状,说明该油佐剂灭活苗是有效的SVA 候选疫苗。
6 结语
SVA 是近些年在多个国家出现的一种跨境传播病毒,可导致典型的水疱型临床症状,已对多国养猪业造成了不同程度的影响。SVA 感染目前在国内未像非洲猪瘟那样给养猪业带来毁灭性的影响,但不应忽视的是SVA 属于RNA 病毒,可能具有较强的变异性,因此该病毒未来的流行态势如何演变,目前很难预测。而且,目前仍无商品化疫苗可用,且国内诊断试剂研发相对滞后,这都不利于该病毒的防控。因此,相关工作者应当密切关注SVA 在全球的流行现状,并深入研究SVA 的致病及免疫机理,同时研发有效的疫苗和诊断试剂。

