后腹腔镜肾部分切除术中肾动脉分支阻断与主干阻断治疗肾肿瘤的疗效比较
李升 吴铁林 许建挺 殷民 龙慧民 周立斌
肾肿瘤是泌尿系统常见的肿瘤之一,而保留肾单位手术是目前治疗局限性肾肿瘤的主要术式[1]。传统的保留肾单位手术,通常把阻断肾动脉主干血流作为肾部分切除术的基本步骤,以减少术中出血、降低手术操作难度。但是,这种血流阻断方式在恢复肾脏血供后会导致残留健康肾实质的缺血再灌注损伤[2-4]。为了克服这一缺点,Gill等[5]报道了一种选择性阻断肾动脉分支的肾部分切除术,该术式与肾动脉主干阻断肾部分切除术相比,手术创面无出血,极大地减少了热缺血对正常肾组织的损伤[4,6-7]。近年来,“零缺血”技术不断发展,该技术主张阻断肾的分支血管,不仅能够提供一个相对无出血的手术区域,而且最大限度地减少了热缺血对健康肾组织的损伤。目前关于肾动脉分支阻断与主干阻断对术后短期肾功能影响的报道不多,故本研究比较了后腹腔镜肾部分切除术中上述2种阻断方式治疗肾肿瘤的疗效,现将结果报道如下。
1 对象和方法
1.1 对象 收集2017年1月至2019年1月在本院行后腹腔镜肾部分切除术的43例肾肿瘤患者的临床资料,其中术中采取肾动脉分支阻断[超选择(三级分支)或选择(二级分支)阻断,分支阻断组]20例,肾动脉主干阻断(主干阻断组)23例;两组患者性别、年龄、肿瘤直径、RENAL评分、术前肾小球滤过率(eGFR)比较,差异均无统计学意义(均P>0.05),见表1。排除患有多发肾肿瘤、对侧肾脏病变等其他可能影响肾功能疾病的患者。

表1 两组患者一般资料比较
1.2 手术方法 在全身麻醉下,取健侧卧位,适当抬高腰桥,常规消毒、铺巾。采用3或4通道法(图1a,插页)。根据术前3D肾动脉重建的指导(图1b,插页),找到并游离肾动脉及其二、三级分支(图1c,插页)并使用F8导尿管标记。游离肾周筋膜、肾周脂肪,找到肾肿物,距离肿物0.5~1.0cm用超声刀对肿物进行标记,“哈巴狗(Hemlock Bulldog)钳”阻断肾动脉主干(主干阻断)或者肿瘤部供血的肾动脉分支(分支阻断)(图1d,插页)(计时开始),观察缺血区,可见肿瘤及部分肾周围组织颜色变苍白(图1e,插页)。用剪刀将肿瘤整块切除,倒刺线双层缝合肿瘤基底部及封闭集合系统,关闭肿瘤创面,去除“Hemlock Bulldog钳”(计时结束),恢复肾脏供血,根据需要适当加缝渗血或缝合不牢的部位。检查无出血,留置肾周引流管。将切除的肿瘤放入标本袋取出,送术中快速冷冻病理检查,结束手术。
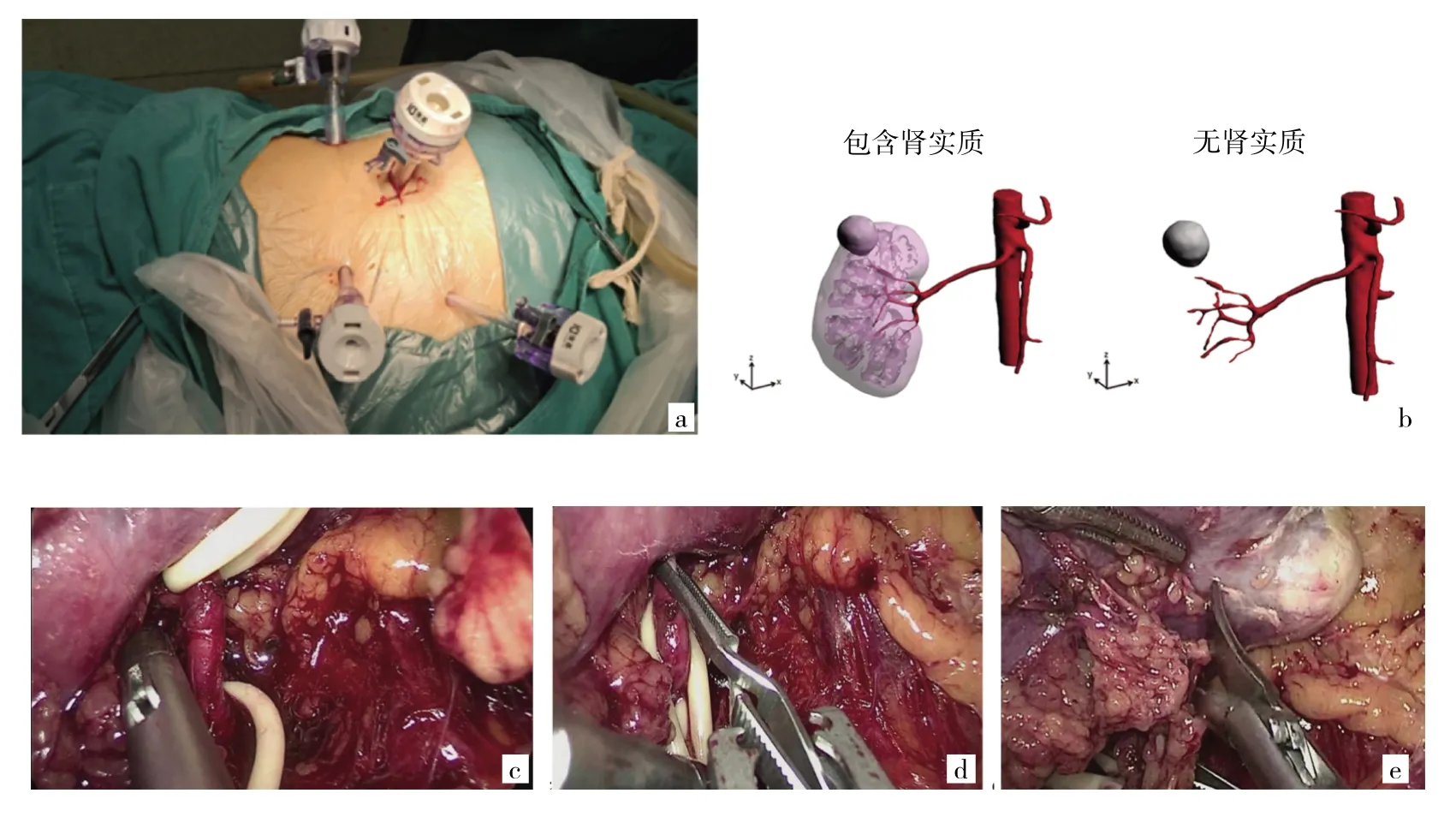
图1 后腹腔镜肾动脉分支阻断肾部分切除术操作过程(a:后腹腔镜4通道;b:术前肾动脉三维重建;c:标记肾动脉及其二、三级分支;d:Hemlock Bulldog钳阻断肿瘤部供血的分支动脉;e:肿瘤及部分周围肾组织颜色变白)
1.3 观察指标 比较两组患者手术一般情况、术中情况(手术时间、阻断时间、术中出血量)以及术后肾功能(手术前后eGFR差值)、并发症、住院时间、病理诊断及随访情况。
1.4 统计学处理 采用SPSS 23.0统计软件。计量资料用用表示,组间比较采用两独立样本t检验;计数资料组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 手术一般情况 所有患者均顺利完成手术,无术中转开放手术。其中分支阻断组1例患者术中出血较多,视野不清,中转肾动脉主干阻断。
2.2 两组患者术中情况比较 分支阻断组手术时间、术中出血量分别为(125.9±11.8)min、(210.4±38.1)ml,较主干阻断组的(110.7±18.3)min、(135.2 ±35.1)ml明显增加,差异均有统计学意义(均P<0.05);阻断时间为(27.2±1.9)min,与主干阻断组的(25.6±2.8)min比较,差异无统计学意义(P>0.05)。
2.3 两组患者术后肾功能比较 分支阻断组手术前后eGFR 差值为(6.1±4.8)ml/min,明显低于主干阻断组的(15.5±10.3)ml/min,差异有统计学意义(P<0.05)。
2.4 两组患者术后并发症及住院时间比较 两组患者发生尿漏、反复大量血尿各1例,经对症治疗痊愈;主干阻断组1例肾下极肿瘤患者术中发生输尿管损伤,行输尿管端端吻合并留置双J管,术后1年内未发生输尿管狭窄及肾积水。分支阻断组与主干阻断组术后并发症发生率(10.0%比13.0%)、住院时间[(8.1±1.1)d比(8.9±2.1)d]的差异均无统计学意义(均P>0.05)。
2.5 两组患者术后病理诊断及随访结果比较 分支阻断组术后病理诊断为肾透明细胞癌16例,乳头状癌3例,嫌色细胞癌1例;主干阻断组术后病理诊断为肾透明细胞癌17例,乳头状癌4例,嫌色细胞癌1例,肾错构瘤1例;两组患者术后病理诊断情况比较,差异无统计学意义(P>0.05)。两组患者手术切缘均为阴性。术后随访3~33个月,复查CT或超声均无肿瘤复发或转移,均未发生肾积水、肾萎缩等。
3 讨论
肾肿瘤手术包括保留肾单位的肾部分切除术、根治性肾切除术等。Gill等[5]认为根治性肾切除术和肾部分切除术的治疗效果无明显差异。有文献报道肾部分切除术安全、有效,已成为治疗早期肾肿瘤的常用术式[8]。而传统的肾部分切除术需要阻断肾动脉主干,为肾脏带来热缺血和再灌注损伤。Gill等[5]认为药物诱导低血压下“零缺血”技术可减轻对肾功能造成的损害。相关研究表明,选择性肾段动脉阻断技术能最大限度地减少热缺血范围,保护残肾功能[9-11]。肾动脉分支阻断通过阻断供应肾肿瘤的肾动脉分支,把缺血范围控制在肿瘤及其周边邻近组织,对剩余健康肾组织影响小,能够很好地解决保持手术视野清楚和保护残留肾脏灌流之间的矛盾[9,12-13]。
本研究结果显示,分支阻断组手术时间较主干阻断组长,差异有统计学意义;这考虑与分支阻断术中寻找及游离肾血管及其分支时间较长有关。但两组术中热缺血时间基本一致,术后手术病理类型、切缘情况、术中输血、术后住院时间及并发症发生率等比较差异均无统计学意义。术后1个月,分支阻断组eGFR改善程度优于主干阻断组,这说明分支阻断在术后保护肾功能方面较主干阻断有优势。关于术中估算出血量方面,分支阻断组出血相对较多,可能由于分支阻断组仅阻断供应肾脏肿瘤动脉,而肿瘤周边肾实质尚有血供所致。两组患者手术并发症无明显差别,术后各有1例患者尿漏,留置双J管治愈;各有1例反复血尿,保守治疗无效,数字减影血管造影介入栓塞治愈。主干阻断组1例肾下极肿瘤,术中输尿管损伤,行输尿管端端吻合,术后随访1年,未见输尿管狭窄及肾积水发生。
笔者结合本中心临床经验,就选择性或高选择腹腔镜肾部分切除术中肾动脉分支阻断术的注意事项归纳如下:(1)术前仔细读片,在3D打印技术或三维血管重建技术辅助下了解各肾段动脉的解剖关系,以选择合适的靶血管[14-16]。(2)采用循血管走行逐级游离的方法,寻找目标分支血管。如术中出血较多、手术视野不清,应及时阻断肾动脉主干,降低手术风险。
综上所述,后腹腔镜肾部分切除术中肾动脉分支阻断,可避免大部分正常肾脏组织的热缺血及缺血再灌注损伤,且不增加术中及术后并发症,是后腹腔镜下肾部分切除术肾动脉主干阻断的有益补充,值得临床有选择性地推广。

