室间隔射频消融术在梗阻性肥厚型心肌病中的应用
叶 菡,王 黎,舒茂琴,蒋周芩,周 杨,周 莲 (陆军军医大学第一附属医院心血管内科,重庆 400038)
梗阻性肥厚型心肌病(hypertrophic obstructive cardiomyopathy,HOCM)是肥厚型心肌病的一种类型,呈非对称性肥厚,常发生在主动脉瓣下区域,因过度肥厚的室间隔导致左心室流出道梗阻(left ventricular outlow tract obstruction,LVOTO),引起疲劳、呼吸困难、胸痛、晕厥甚至猝死等[1-2]。大约70%的肥厚型心肌病患者在静息或运动激发中存在LVOTO[3],而静息时LVOTO可看作是疾病危险进程和死亡的重要独立预测指标[4]。20世纪70年代,症状明显且药物治疗不佳或者不能耐受的患者主要治疗方法是室间隔切除术(surgical myectomy,SM),20世纪90年代开始通过双腔起搏植入治疗以减轻LVOTO[1]。英国医生Sigwart于1995年首次应用乙醇室间隔化学消融术(alcohol septal ablation,ASA)治疗HOCM,该方法逐渐成为替代SM的非药物治疗手段[5]。这些治疗方法的效果各有优劣,SM对术者技术水平要求高、需开胸建立体外循环,手术创伤大,住院时间长,费用高,而ASA常因间隔支动脉位置、大小、走行的不同,治疗效果存在个体差异,且二者均可发生房室传导阻滞等并发症[1,6]。室间隔射频导管消融术(percutaneous intramyocardial septal radiofrequency ablation,PIMSRA)是近年来国内外新兴的治疗方法,其通过超声检测心包及瓣膜情况,三维标测系统确定消融部位,由导管释放射频电流,使组织内温度升高,细胞内外水分蒸发,局部产生细胞凝固坏死,以减轻LVOTO,改善患者临床症状。心腔内超声可以实时监测心包、二尖瓣活动情况;三维标测指导联合压力消融导管可确定消融具体部位、监测局部压力和时间等,合并房颤可同时行房颤环肺静脉消融术,可使HOCM患者左心室流出道压力阶差持续降低,改善临床症状。 PIMSRA具有精确定位、损伤灶局限、易于控制等优点,随着该技术的陆续开展应用,其安全性与有效性已得到初步验证[7-12]。本文回顾性分析我院收治的7例应用PIMSRA治疗的HOCM患者的临床资料,通过回顾手术要点、术后管理重点及随访结果,对 PIMSRA的应用和管理策略进行了探讨和总结。
1 资料与方法
1.1 临床资料
选择2019年6~8月于我院心血管内科行PIMSRA的HOCM患者7例,其中男3例,女4例,年龄49~72岁。合并轻中度冠脉疾病5例,合并心房颤动3例,合并糖尿病2例,有晕厥病史6例(6例患者及家属拒绝ICD治疗)。纽约心功能分级(New York Heart Association,NYHA)Ⅱ级5例,Ⅲ级2例。术前超声提示:非对称性室间隔增厚达15~28 mm,LVOTO明显,静息状态下压力阶差30~110 mmHg,所有患者均存在二尖瓣前叶收缩期前向运动(systolic anterior motion,SAM)现象。
HOCM的诊断依据参照《2014年ESC肥厚型心肌病诊断及管理指南》[1]:①超声心动图示非对称性室间隔肥厚≥15 mm; ②室间隔与左室后壁厚度之比≥1.5,且有SAM现象;③左室流出道压力阶差静息状态≥30 mmHg,或激发状态≥50 mmHg。
1.2 手术方法
患者在1%普鲁卡因局部麻醉下行股动脉、股静脉、桡动脉穿刺后置入血管鞘。经股静脉送入10级电生理导管,记录冠状静脉窦电图;送入4级电生理导管至右心室间隔面备用起搏。经股动脉鞘送入猪尾导管行左心室造影,并测量左心室内压力;经桡动脉鞘管送入多功能导管到达主动脉窦,测量主动脉内压力,记录压力阶差。诱发室性早搏后分别测量早搏激发后左心室内压力及主动脉内压力,记录激发后压力阶差。然后经左侧股静脉送入三维超声导管至右房,在心腔内超声引导下行左心室建模。再经股动脉X射线透视下送入冷生理盐水灌注消融导管至主动脉根部,跨主动脉瓣进入左心室。在左室模内标注His束、束支电位位置,在超声下标记SAM现象区域及室间隔最厚部位。应用STOCKEKT消融系统ST消融导管,在功率35~40 W、温度45 ℃、持续冷生理盐水30 mL/min灌注下,避开His束、束支等正常传导部位,在SAM区域及室间隔最厚区域进行消融,消融大头压力5~20 g,每点消融60~90 s。
2 结果
本组7例患者手术均获成功,术后3~13 d康复出院。患者术中测量激发后压力阶差70~220 mmHg,消融完成后超声提示SAM现象明显减轻,压力阶差降至0~100 mmHg(表1)。合并房颤患者同时在血管内超声指导下行环肺静脉消融术,达到肺静脉电隔离目的(图1)。其中4例患者出现并发症,分别予对症治疗后好转。出院前评估患者主诉症状、NYHA心功能分级、心脏超声等,较术前均有改善,出院后15 d、2个月、3个月门诊随访,监测血压、心率、心律、心功能、心脏超声等,7例患者均生存良好。
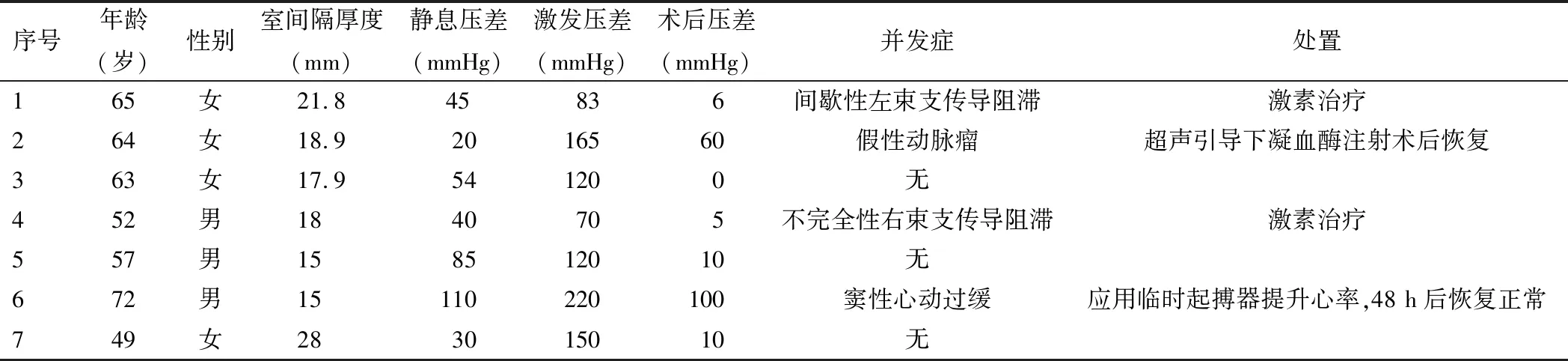
表1 HOCM患者手术前后资料
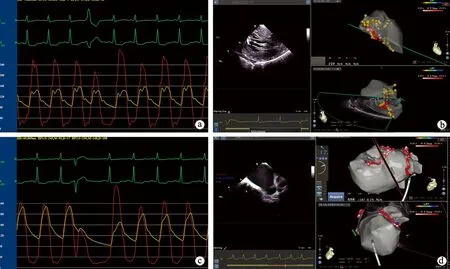
a:术前跨左室流出道压力梯度(静息和激发压差)高;b:在心腔内超声动态实时监测结构变化及三维标测指导下行肥厚的室间隔消融(红点);c:与图a相比,消融室间隔后跨左室流出道压力梯度(静息和激发压差)明显缩小;d:合并房颤时在血管内超声指导下行环肺静脉消融术
图1 肥厚梗阻性心肌病合并房颤导管消融
3 讨论
室间隔射频导管消融术(PIMSRA)是继乙醇室间隔化学消融术(ASA)后另一个非外科治疗梗阻性肥厚型心肌病的新方法,尤其是对药物疗效不佳及靶间隔支血管解剖结构异常的患者可考虑行PIMSRA。首先,术者经股动脉送入猪尾导管,跨瓣膜进入左心室行流出道测压;经桡动脉鞘管送入多功能导管达主动脉窦,测量主动脉内压力;然后,经左侧股静脉送入三维超声导管至右房,在三维标测系统下行左室建模,结果示室间隔明显增厚,可见SAM现象,对SAM对应的室间隔部位标注压力差位置。再经股动脉X射线透视下送入冷生理盐水灌注消融导管到主动脉根部,送过瓣膜,进入左心室内标注HIS束及左前分支、左后分支传导束。在心腔内超声引导下,以SAM对应的室间隔部位作为消融靶点,避开His、束支位置行消融。消融功率为35~40 W、温度45 ℃、冷生理盐水灌注速度为30 mL/min,每次消融时间60~90 s。消融结束后行左室连续测压,可见左室流出道压差下降。该术式术中、术后的并发症主要包括传导束损伤、心室颤动、消融部位组织水肿和腹膜后出血等[7,9-12],这些并发症的发生可能导致需植入永久性起搏器、再次手术甚至死亡。因此,术中精细的操作和术后的严密管理经验都需要逐步探索和总结。
在操作中,PIMSRA需要将导管头端进行跨瓣膜操作、定位消融,导管在狭窄的左心室流出道内操作、操作时间过长以及消融本身对心肌的损伤等,都会增加正常瓣膜结构损伤以及心室颤动发生的概率。术中应使用心腔内超声实时监测心包、二尖瓣活动情况等以确保术中安全。应用三维标测指导联合压力消融导管可精准确定消融具体部位、监测局部压力,以达到左心室流出道压力阶差持续降低、患者临床症状改善的目的[12]。此外,术中应常规监测活化凝血时间,将其维持在250~350 s。房室传导阻滞是术后常见的并发症,且术后24~48 h为炎性水肿最严重的时期,应该严密监测以渡过危险期。术后48 h内要加强对心电图波形的观察,主动关心患者是否感觉不适,出现恶性心律失常时,及时启动应急处置程序。本组有1例患者围手术期出现严重窦性心动过缓,应用临时起搏器提升心率至80~100次/分钟,起搏心室以改善心脏除极顺序,减轻左室流出道梗阻,48 h后心率恢复正常即停用临时起搏;1例患者发生了间歇性左束支传导阻滞,1例患者发生了不完全性右束支传导阻滞,2例患者均给予激素治疗后恢复正常。
容量管理在PIMSRA术后的管理中非常重要,尤其对于LVOTO患者,因为低血容量、扩血管药物或β-受体激动剂等会加重梗阻,所以临床中应充分扩容,避免应用扩血管药物;低血压的患者可用间羟胺或去甲肾上腺素等缩血管药物提升血压。为增加左心室容量,减轻梗阻,术后要早期积极静脉补液,液体选择以晶体为主,补液速度70~80 mL/h为宜。血压和尿量是反映容量状态的2个重要指标,如果收缩压低于90 mmHg或平均动脉压低于65 mmHg,则提示容量不足;结合末梢皮肤颜色与温度、足背动脉搏动强弱等评估全身循环灌注状况,及时调整补液速度。尿量维持在0.5~1 mL·kg-1·h-1为宜,关注患者有无恶心、呕吐、心悸、心累、气促等主观症状,听诊双下肺有无湿啰音以辅助识别容量不足或者容量负荷过重,必要时可使用中心静脉压测定、脉搏轮廓动脉压波形分析法等高级监测手段。通过精细的容量管理,本组患者均未出现血流动力学紊乱的情况。
PIMSRA手术方式经血管入路多,且置入鞘管型号偏大(如超声引导选用11 F鞘管),应加强患者穿刺血管的管理。密切观察伤口局部有无出血、血肿发生,腹膜后血肿是严重的并发症,临床中需提高警惕[11]。结合术中穿刺顺利程度、血管质量及凝血功能评估压迫器压迫时间及患者的术侧肢体制动时间,以及早恢复自主活动,增加患者舒适性。卧床期间需预防下肢静脉血栓的形成,手术当日给予低分子肝素钠4 500 U皮下注射,并指导患者缓慢行踝关节的跖屈运动、下肢的等长运动。本组有1例患者术后第2天出现假性动脉瘤,经超声引导下行凝血酶注射术后恢复。
综上所述,应用室间隔射频消融术治疗梗阻性肥厚型心肌病是近年来新兴的一种安全、有效的介入治疗手段,该方法对心肌细胞损伤较小,术后恢复快,症状改善明显,并发症较少且可控。从目前的研究结果来看,虽然相关数据皆由较大的中心研究和发布,但此技术的应用病例数相对较少,仍缺乏长期的随访数据,且未见与其他治疗方法的病例进行对照研究[6],还将继续追踪远期的效果和安全性,以期形成更加完善的标准化治疗方案。

