天疱疮合并感染患者病原菌分布及耐药性
谢媛媛,陈显侠,郑佳媛,骆志成
(兰州大学第二医院皮肤科,甘肃 兰州 730030)
天疱疮(pemphigus)是一组慢性、复发性、严重的自身免疫性大疱性皮肤病,机体存在针对表皮细胞间桥粒连接的自身抗体(主要为抗桥粒芯糖蛋白Dsg抗体)。主要表现为皮肤黏膜红斑、松弛性水疱及大疱,尼氏征阳性,疱壁破裂易形成糜烂及溃疡,糜烂面不易愈合,疼痛明显;皮损多分布于胸背部、面部、头部、腋窝、腹股沟、臀部等;患者以40~60岁多见;女性较男性易受累[1]。临床主要分为寻常型、增殖型、落叶型、红斑型,其他罕见类型还包括副肿瘤型、疱疹样、IgA天疱疮等[2]。组织病理可见表皮内棘层松解形成水疱,目前治疗药物主要为糖皮质激素及免疫抑制剂。天疱疮患者易继发皮肤黏膜、肺部、泌尿道等部位感染[3],与皮肤黏膜屏障破坏、蛋白丢失及摄入减少、长期使用糖皮质激素治疗、高龄等因素相关[4]。感染显著影响糜烂面愈合及疾病预后,目前为天疱疮患者死亡的主要原因[5]。随着抗菌药物的广泛应用及不合理使用,病原菌耐药性逐渐增强。目前关于天疱疮合并感染的病原菌及药敏分析研究较少,本研究对2014年1月—2019年9月某院天疱疮合并感染患者感染病原菌及其耐药性进行统计分析,以指导临床合理用药及感染预防。
1 对象与方法
1.1 研究对象 回顾性选取兰州大学第二医院2014年1月—2019年9月收治的天疱疮合并感染患者。纳入标准:依据2017年第2版《中国临床皮肤病学》[2],所有患者具有典型临床表现及组织病理学表现,即皮肤松弛性水疱和大疱、顽固性糜烂、尼氏征阳性,可伴有黏膜水疱及糜烂,组织病理为表皮内水疱形成(棘层松解)。排除标准:临床表现为皮肤黏膜水疱及糜烂面,组织病理不表现为表皮内水疱者,或未行组织活检者;有严重免疫系统疾病及恶性肿瘤者。天疱疮病情严重程度依据临床常用划分方法[6]:皮损<体表面积10%为轻度,30%左右为中度,>50%为重度。入院后采集皮肤黏膜分泌物,有相关症状者采集痰、尿行病原学检查,予以皮肤黏膜护理,局部外用抗菌药物及糖皮质激素制剂,视病情予以糖皮质激素及免疫抑制剂等治疗。
1.2 标本来源 标本采集及送检严格遵守无菌操作,标本类型包括皮肤、口腔黏膜的血性及脓性分泌物,及尿、痰,剔除同一患者同一部位重复分离的菌株。
1.3 培养鉴定及药敏试验 将标本及时接种培养,菌株鉴定及药敏试验采用法国生物梅里埃公司VITEK-Compact全自动微生物分析仪,质控菌株为金黄色葡萄球菌ATCC 25923、金黄色葡萄球菌ATCC 29213、大肠埃希菌ATCC 25922、肺炎克雷伯菌ATCC 700603。药敏试验采用K-B纸片扩散法及微量肉汤稀释法,结果判断依据美国临床实验室标准化协会(CLSI)2019年版标准(CLSI M100-S29)[7];头孢哌酮/舒巴坦药敏结果判定参照Barry等[8]的文献。
1.4 多重耐药菌(MDRO)判断标准 参照2014年《MDR、XDR、PDR多重耐药菌暂行标准定义——国际专家建议》[9]中对MDRO的定义与分类。本研究检出MDRO有耐甲氧西林金黄色葡萄球菌(MRSA)、耐甲氧西林表皮葡萄球菌(MRSE)、耐甲氧西林凝固酶阴性葡萄球菌(MRCNS)、产超广谱β-内酰胺酶(ESBLs)肠杆菌科细菌(大肠埃希菌和肺炎克雷伯菌)、多重耐药鲍曼不动杆菌(MDR-AB)、泛耐药鲍曼不动杆菌(XDR-AB)。
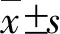
2 结果
2.1 一般资料 共收集天疱疮合并感染患者114例,男性56例,女性58例,平均年龄(50.24±9.12)岁。患者无死亡,均病情好转后出院。
2.2 病原菌分布 114例天疱疮合并感染患者共分离出121株病原菌,其中革兰阳性(G+)菌73株(60.33%)、革兰阴性(G-)菌26株(21.49%)、真菌22株(18.18%)。见表1。G+菌主要来源于皮肤(70株,95.89%),主要为金黄色葡萄球菌(53株)、表皮葡萄球菌(10株)等,来源于口腔黏膜3株(4.11%)。G-菌主要来源于皮肤(14株,53.85%),其次为尿(6株,23.08%)、痰(5株,19.23%)。真菌主要来源于口腔黏膜(16株,72.72%),其次为皮肤(5株,22.73%)。共检出MDRO 37株(30.58%),分别来源于皮肤(30株)、尿(3株)、痰(4株)标本,包括MRSA 23株、MRCNS 7株(其中MRSE 6株)、ESBLs阳性菌株5株、MDR-AB 1株、XDR-AB 1株。
表1 天疱疮合并感染患者检出病原菌分布
Table 1 Distribution of pathogens in patients with pemphigus and infection
病原菌菌株数构成比(%)G+菌7360.33 金黄色葡萄球菌5343.80 表皮葡萄球菌108.26 其他葡萄球菌43.31 其他G+菌64.96G-菌2621.49 大肠埃希菌108.26 肺炎克雷伯菌43.31 鲍曼不动杆菌43.31 其他G-菌86.61真菌2218.18 假丝酵母菌属(未分类)1714.04 白假丝酵母菌32.48 光滑假丝酵母菌10.83 热带假丝酵母菌10.83合计121100.00
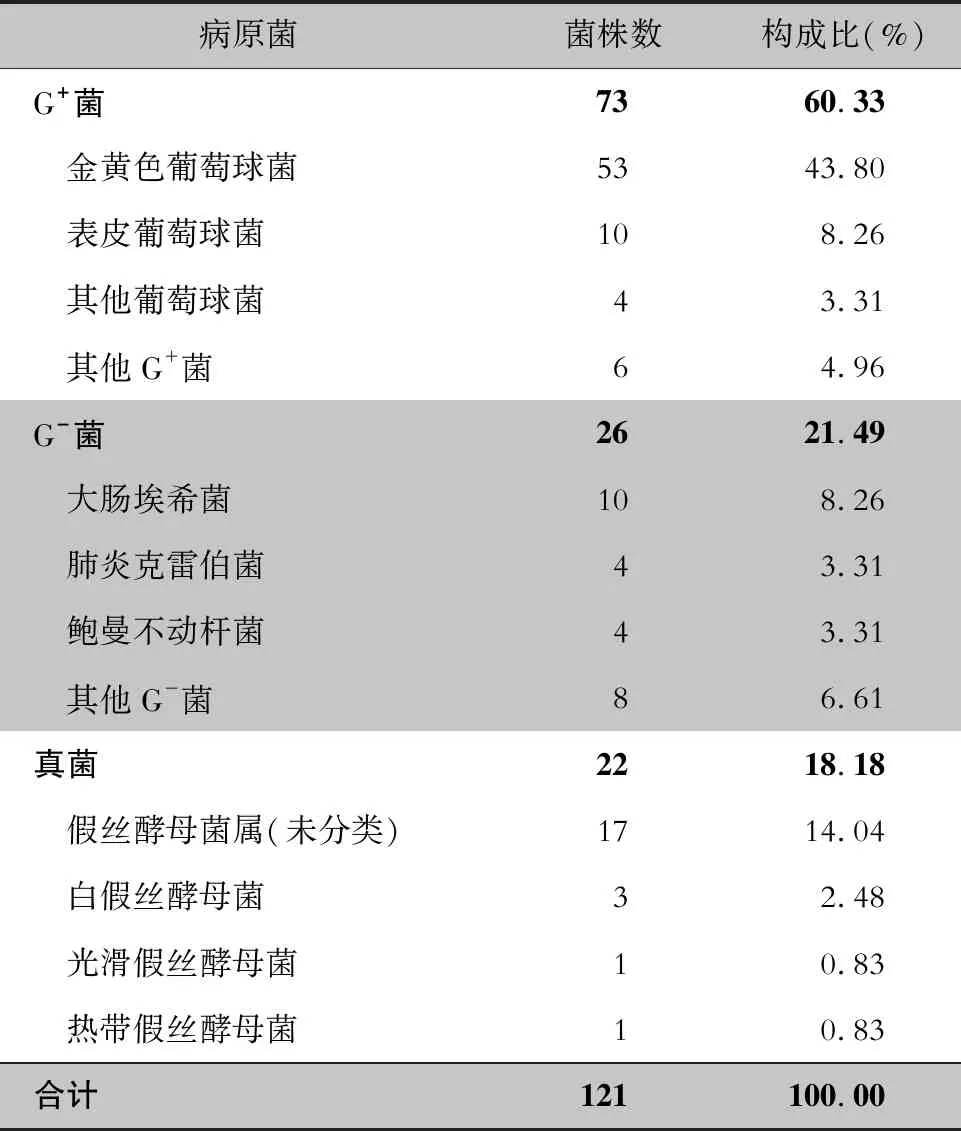
2.3 主要G+菌对常用抗菌药物的耐药情况 金黄色葡萄球菌、表皮葡萄球菌对青霉素的耐药率均为100%;金黄色葡萄球菌对氟喹诺酮类、头孢曲松、氨苄西林/舒巴坦、四环素的耐药率<50%;对克林霉素、红霉素的耐药率>90%。表皮葡萄球菌对氨苄西林/舒巴坦、庆大霉素、四环素、莫西沙星的耐药率<50%。MRSA 、MRSE检出率分别为43.40%、60.00%。未检测出对万古霉素、利奈唑胺、奎奴普丁/达夫普汀耐药的G+菌。见表2。
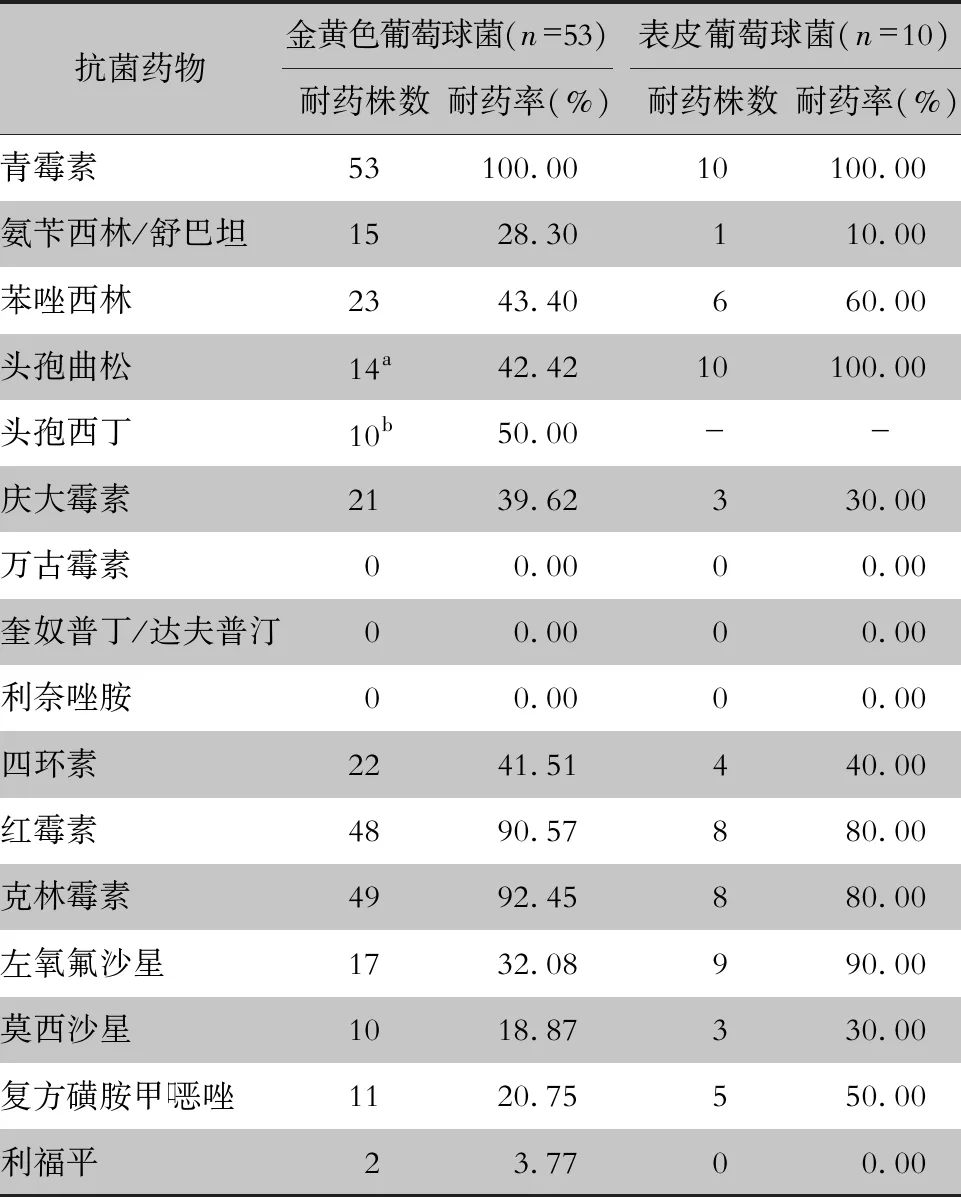
表2 主要G+菌对常用抗菌药物的耐药情况
注:a检测菌株数为33株;b检测菌株数为20株;-表示未检测。
2.4 主要G-菌对常用抗菌药物的耐药情况 大肠埃希菌对大多数临床常用抗菌药物如第三代头孢、氟喹诺酮类、四环素的耐药率≤50%,对氨曲南的耐药率为30%,对头孢哌酮/舒巴坦、亚胺培南均敏感。检出的4株肺炎克雷伯菌对第三代头孢的耐药率≥50%,对氟喹诺酮类、哌拉西林/他唑巴坦均敏感。大肠埃希菌及肺炎克雷伯菌中ESBLs菌株检出率分别为20.00%(2/10)、75.00%(3/4)。检出的4株鲍曼不动杆菌对氨苄西林/舒巴坦的耐药率<30%,对其他多种抗菌药物(包括亚胺培南)的耐药率≥50%,检出 MDR-AB、XDR-AB各1株。见表3。其他G-菌如铜绿假单胞菌、阴沟肠杆菌等,对大多数抗菌药物的耐药率<50%,未检测出MDRO。
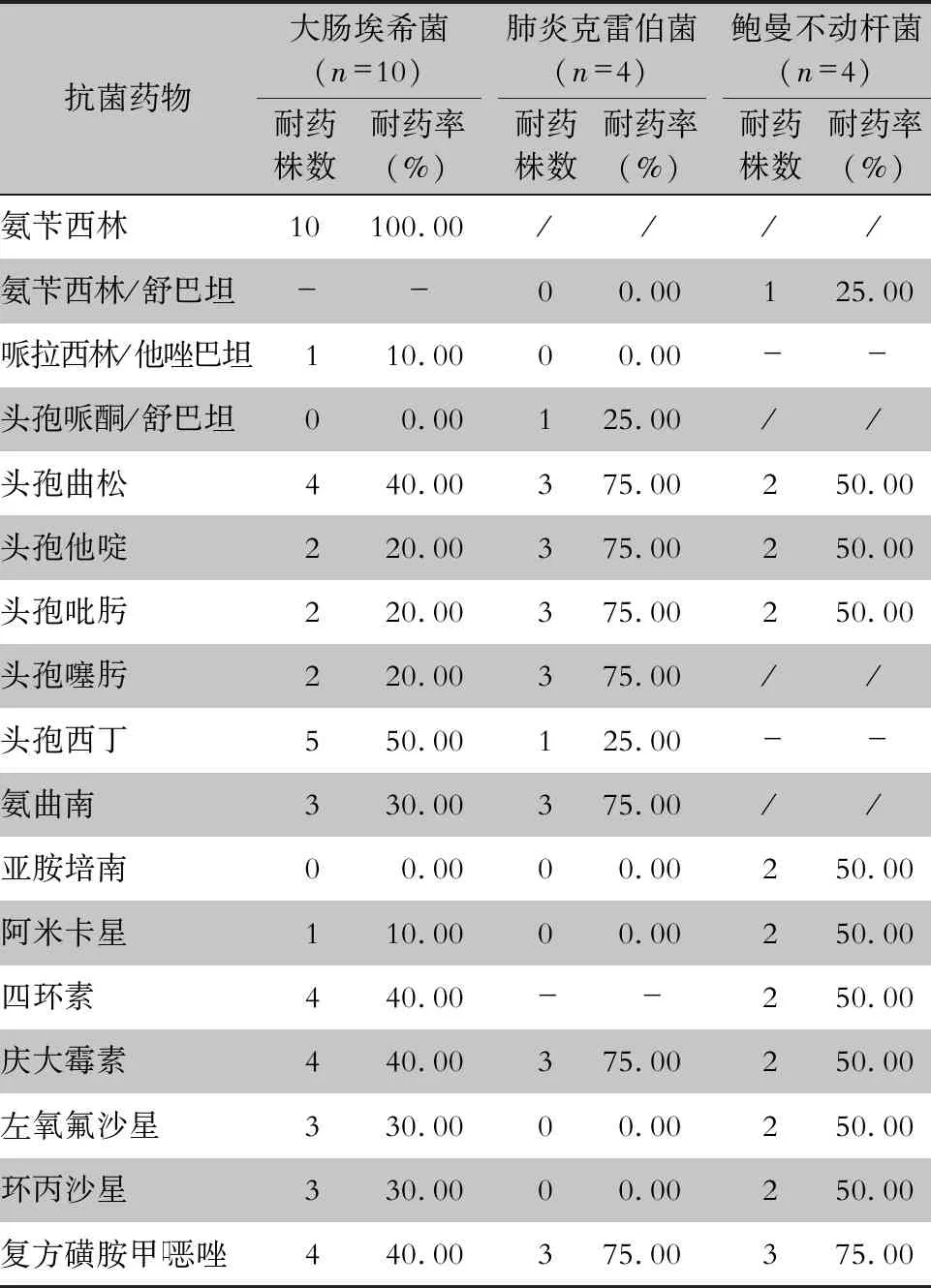
表3 主要G-菌对常用抗菌药物的耐药情况
注:- 表示未检测;/ 表示天然耐药。
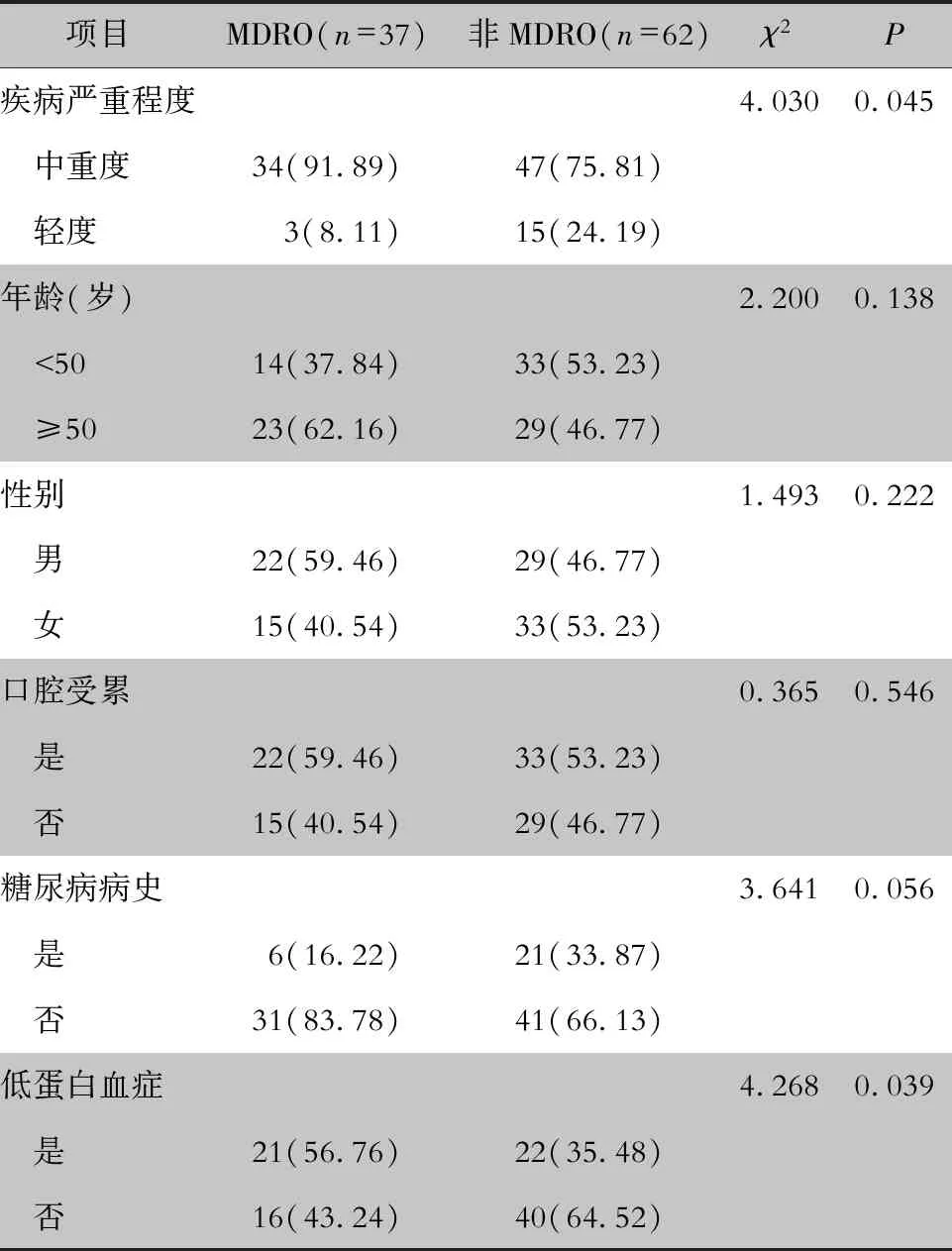
2.5 MDRO感染情况 99株细菌中共检出37株MDRO,主要来源于皮肤(30株)。73株G+菌中检出MDRO 30株(41.10%),其中23株为MRSA;26株G-菌中检出MDRO 7株(26.92%)。疾病严重程度为中重度、伴有低蛋白血症的患者MDRO感染发病率较高,差异均有统计学意义(均P<0.05)。不同年龄、性别、口腔受累、糖尿病病史患者的MDRO感染发病率比较,差异均无统计学意义(均P>0.05)。见表4。
表4 MDRO感染的影响因素分析[例(%)]
Table 4 Influencing factors for MDRO infection (No. of cases [%])
项目MDRO(n=37)非MDRO(n=62)χ2P疾病严重程度4.0300.045 中重度34(91.89)47(75.81) 轻度3(8.11)15(24.19)年龄(岁)2.2000.138 <5014(37.84)33(53.23) ≥5023(62.16)29(46.77)性别1.4930.222 男22(59.46)29(46.77) 女15(40.54)33(53.23)口腔受累0.3650.546 是22(59.46)33(53.23) 否15(40.54)29(46.77)糖尿病病史3.6410.056 是6(16.22)21(33.87) 否31(83.78)41(66.13)低蛋白血症4.2680.039 是21(56.76)22(35.48) 否16(43.24)40(64.52)
3 讨论
天疱疮为自身免疫性大疱性皮肤病,其病理机制由多种因素参与,目前具体发病机制仍不清楚,主要依赖多种靶抗原的协同作用,通过直接干扰桥粒的黏附、影响细胞内信号通路,最终导致角质形成细胞分离、棘层松解[10]。天疱疮为皮肤科的慢性疾病,病情反复,患者皮肤黏膜出现水疱,水疱易破溃形成糜烂面,糜烂面不易愈合,疼痛显著,皮损多位于口腔、胸背部、头面部、臀部等,明显影响患者进食、活动及生活质量。天疱疮的治疗目的在于控制病情,促使皮肤黏膜糜烂及溃疡面尽快愈合,减少并发症,改善患者生活质量,达到长期缓解直至痊愈。天疱疮患者因皮肤黏膜屏障破坏、营养物质不足、大剂量糖皮质激素治疗、长期使用糖皮质激素及免疫抑制剂药物的相关并发症等因素[3],极易继发感染。
皮肤黏膜糜烂面感染明显影响伤口愈合,可延长天疱疮住院时间,增加糖皮质激素使用量和住院费用,预后较差[11],来自多个国家的近十年的研究[12-15]表明,在不同的研究人群中天疱疮患者的死亡风险是对照组的1.7~3倍,感染为天疱疮患者死亡的主要原因[5]。本研究回顾性分析了该院6年间天疱疮合并感染患者感染部位、感染病原菌的分布及耐药性,有助于指导临床合理使用抗菌药物,改善患者预后及生活质量。
本研究中天疱疮感染好发部位主要为皮肤,因其表皮剥脱至皮肤屏障受损、大量体液渗出等。最常见病原菌为G+菌中的金黄色葡萄球菌,与大多文献报道[16-17]一致,但与吴淑萍等[18]研究不一致(主要为铜绿假单胞菌),考虑与样本量较少或不同地区病原菌分布不同有关。金黄色葡萄球菌感染临床较普遍,为心内膜、骨关节、皮肤软组织等部位感染的主要病原菌[19]。金黄色葡萄球菌可以产生表皮剥脱毒素、肠毒素、中毒性休克毒素、杀白细胞素等毒素物质,易引起伤口化脓性感染,并能够通过产生修饰酶,改变抗菌药物作用靶点,降低细胞壁通透性等不同机制,导致对β-内酰胺类、大环内酯类、氟喹诺酮类等产生不同程度的耐药性[20]。文献[21]报道天疱疮抗原Dsg同时也是金黄色葡萄球菌剥脱毒素作用的靶点,后者对前者有直接消化降解作用。感染部位较多的其次为口腔,主要为假丝酵母菌感染,口腔黏膜为天疱疮常见累及部位,口腔内存在大量定植菌,当机体免疫力低下时易发生感染,尤其假丝酵母菌,其在特定条件下可转变为致病菌[22]。因此,使用糖皮质激素治疗天疱疮时应注意黏膜部位真菌感染,注意黏膜护理,防止发生肺部等深部真菌感染。其他部位感染包括泌尿道、肺部感染,主要为细菌感染,考虑与患者使用糖皮质激素、免疫力低下、低蛋白血症等因素引起机会性感染有关。国外一项前瞻性研究[23]表明,初次诊断为天疱疮的患者患病第一年的机会性感染发病率为9.3%。

本研究中MDRO检出率为37.37%(37/99),主要为MRSA、MRSE、产ESBLs菌株,葡萄球菌属来源于皮肤,产ESBLs菌株多来源于尿、痰。本研究结果表明疾病严重程度为中重度、伴有低蛋白血症的患者更易发生MDRO感染。病情严重者皮肤黏膜受损面积大,糖皮质激素剂量大且用药时间长,低蛋白血症者患者免疫力低,营养物质不足,容易继发感染。本研究中未检出对万古霉素、利奈唑胺、奎奴普丁/达夫普汀耐药的G+菌株。目前我国耐药病原菌产生速度远远快于高敏性新药研发速度,在大力推动新药研发的同时,强化临床合理性用药是根治性原则[24]。对于天疱疮合并MDRO感染患者,应予以床旁隔离,加强患者、家属及医护人员手卫生,严格执行无菌操作,规范使用抗感染药物。应注意保护天疱疮皮肤黏膜糜烂创面,给予患者高蛋白饮食。皮肤糜烂处予以油剂纱布换药,可外用抗菌制剂防治感染,外用生长因子凝胶促进伤口愈合。口腔内糜烂或溃疡面可用利多卡因、洗必泰、制霉菌素和生理盐水配成含漱液,以止痛、防治细菌及真菌感染。
天疱疮患者易继发各种感染,主要为皮肤细菌感染,且MDRO感染率高,病原菌及其耐药性具有一定特征。临床医生应结合患者原发病病情及病原菌耐药性特点,针对性地合理选用抗菌药物治疗,提高感染治疗效果,改善患者预后,避免抗菌药物滥用及耐药菌恶性循环,同时做好耐药菌监测及医院感染预防与控制工作,避免MDRO的传播。

