经导管主动脉瓣置入手术在主动脉瓣狭窄合并二尖瓣反流治疗中的疗效分析
王 圣 黄乾海 程兆云 陈现杰 陆国庆 赵 亮
主动脉瓣狭窄为机体心脏主动脉瓣局部钙化、解剖结构异常引发的一种退行性病变。主动脉瓣狭窄多高发于高龄人群中,我国≥65岁的患者中钙化性主动脉瓣狭窄的患病率为0.60%,65~84岁患者中患病率为0.55%,而≥85岁患者中为1.41%[1]。另有报道显示,≥65岁人群中主动脉瓣狭窄的发生率为16.9/1 000,65~84岁人群中发生率为15.7/1 000,而≥85岁患者中为42.6/1 000[2]。
随着病情进展患者的左心室流出道会逐步阻塞,以至于心脏搏出量下降,甚至会发生心力衰竭及其他不良事件而死亡[3]。一旦出现临床症状,该病患者的2年死亡率可超过50%[4],因此及时给予有效地治疗干预具有非常重要的意义。由于主动脉瓣狭窄患者的年龄普遍较高,传统开放性手术的组织创伤大,术中血流动力学波动显著,手术风险性高。随着医疗技术的发展,目前经导管主动脉瓣置入手术为重症高龄高危主动脉瓣狭窄患者的常用治疗方法。
主动脉瓣狭窄患者中二尖瓣反流(mitral regurgitation,MV)的比例处于较高水平,MR通常是由于局部组织钙化、左心室重构或瘤样病变等因素导致的病变,MR会进一步加重患者的主动脉瓣狭窄病情[5]。以往研究者多认为,主动脉瓣狭窄合并重度MR多采用主动脉瓣置换术联合二尖瓣修复/置换术,该类患者不能采用经导管主动脉瓣膜置入术[6]。近年来,有研究发现经导管主动脉瓣膜置入术能够治疗主动脉瓣狭窄合并MR患者[7],但是经导管主动脉瓣膜置入术对主动脉瓣狭窄合并不同程度MR患者的近远期疗效尚没有明确。因此,本研究选取我院自 2017 年5月至2019年5月,就诊的主动脉瓣狭窄合并MR患者,分析经导管主动脉瓣置入手术在主动脉瓣狭窄合并MR治疗中的疗效,为临床中患者治疗方案的确定提供依据。
资料与方法
1.一般资料 选取我院自 2017 年5月至2019年5月,就诊的主动脉瓣狭窄合并MR患者共31例,患者的纳入标准为:①符合《心血管病诊疗标准》[8]中主动脉瓣狭窄以及MR的诊断标准;②经临床各科室会诊后发现患者不适合外科开胸手术或外科手术高风险;③患者或家属对本研究知情同意。本研究经本院医学伦理委员会审核批准。排除标准为:①近期内有心脑血管不良事件或消化道出血等疾病或经导管主动脉瓣置入手术禁忌证者;②对造影剂过敏者;③存在因其他因素影响患者生活质量或伴有恶性肿瘤等致死性疾病者。按照患者的MR严重程度将其分为A组(轻度,18例)和B组(中度、重度,13例)。
2.方法 术前需经实验室和影像学诊断并经各科室会诊确定手术治疗方案,按照每例患者的主动脉瓣瓣膜结构参数分析,确定术中置入心脏瓣膜的规格尺寸,并评估手术风险。所有患者均行经导管主动脉瓣置入手术治疗,手术首选经股动脉入路,如外周血管狭窄或钙化迂曲严重,则选择经心尖入路。在杂交手术室中由心外科医师、心内科医师和麻醉医师共同参与手术过程,入室后常规铺巾,全身麻醉,气管插管,连接呼吸机,并建立深静脉通路,右心室内置入临时起搏导线,并连接临时起搏器备用。根据入路不同手术流程已在其他文献中描述,穿刺左侧股动脉置入6 F猪尾导管,注入造影剂给予主动脉根部造影,导管预装人工瓣膜,首先对主动脉瓣进行球囊预扩张,通过主动脉根部造影反复核查人工瓣膜和瓣叶所在平面的位置,释放人工瓣膜的同时提快心率,手术结束时再通过经食管超声心动图以及主动脉根部造影评估人工瓣膜的位置、形态、瓣周状况和功能情况。最后取出鞘管,缝合切口,常规用药处理。
3.观察指标 记录并比较两组患者的并发症发生率,比较两组在术前、术后1个月的心功能指标LVEF、LVEDD、MR和美国纽约心脏病学会NYHA分级,定期随访观察患者的病情变化,叮嘱患者在术后3个月时入院复查,比较两组患者在术后1个月、3个月时的死亡率和生活质量。LVEF、LVEDD、MR采用超声心动图进行测定;生活质量采用日常生活能力量表(activity of daily living scale,ADL)进行评估,该量表共14项内容,评分为16~64分,分值越低则日常生活能力越好。NYHA分级标准为,①I级:体力活动时没有明显的临床症状;②II级:日常活动时会出现气促、心悸等症状,心脏结构轻微异常;③III级:轻微活动时会出现气促、心悸等症状,心脏结构存在明显病变;(4)IV级:休息状态下出现心衰等严重症状,已经处于终末期。
4.统计学方法 所有数据使用统计学软件SPSS25.0分析。计量资料以均数±标准差表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验。计数资料以频数(百分率)表示,采用卡方检验。以P<0.05为差异有统计学意义。
结 果
1.两组患者的LVEF、LVEDD、MR和NYHA分级比较 术后1个月时的LVEF、LVEDD、MR和NYHA分级同术前相比有统计学差异(P<0.05);A组在术后1个月时的LVEF值明显高于B组(P<0.05);A组在术后1个月时的LVEDD和NYHA分级明显低于B组,A组在术后1个月时的MR程度明显低于B组(P<0.05,表1)。
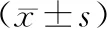
表1 两组患者的LVEF、LVEDD、MR和NYHA分级比较
2.两组患者的死亡率和生活质量比较 A组在术后1个月时的ADL评分均明显高于B组(P<0.05);A组在术后1个月时的死亡率明显低于B组(P<0.05);两组患者在术后3个月时的死亡率和ADL评分均差异无统计学意义(P>0.05,表2)。

表2 两组患者的死亡率和生活质量比较
3.两组患者的并发症比较 各个并发症发生率均差异无统计学意义(P>0.05,表3)。

表3 两组患者的并发症比较[n(%)]
讨 论
本研究中得出两组在术后1个月时的LVEF、LVEDD、MR和NYHA分级同术前相比差异有统计学意义(P<0.05);A组在术后1个月时的LVEF值和ADL评分均明显高于B组(P<0.05);A组在术后1个月时的死亡率、LVED、MR和NYHA分级明显低于B组(P<0.05);两组患者在术后6个月时的死亡率和ADL评分均差异无统计学意义(P>0.05),可见经导管主动脉瓣置入手术可用于主动脉瓣狭窄合并不同程度MR患者的治疗中,能够显著改善患者的心功能,合并重度和中度MR会提高患者术后短期的死亡率,而不会影响患者长期的死亡率,此时MR的严重程度对术后患者远期死亡率和生活质量恢复的影响较小。刘先宝等[9]的临床研究指出,经导管主动脉瓣置入手术可用于主动脉瓣重度反流患者的治疗中,促进患者心功能的恢复。一项国外研究中表明,在经导管主动脉瓣置入手术后,合并重度和中度MR患者的LVEF值比未合并者的明显降低,LVEDI值比未合并者的明显增高[10],这同本文的结果相符,该术式对组织的创伤小,同常规心脏手术相比术中不用进行体外循环,术后可较快改善患者的日常生活能力[11]。
另外,经导管主动脉瓣置换术后多数合并MR患者的反流程度可能会明显好转,因此,临床中考虑是否对主动脉瓣狭窄合并MR患者更适用于该术式,但是仍然有少量患者术后反流加重,本文中1例患者出现重度瓣膜反流而死亡。既往研究指出,经导管主动脉瓣置换术后一个月内,合并中度、重度MR患者的死亡率比合并轻度者明显上升,且两者在一年内的死亡率接近[12],这同本文结果一致。而D’Onofrio 等[10]的文献研究发现,在经导管主动脉瓣置入手术后,合并重度和中度MR患者的院内死亡率和20个月内的死亡率均接近,与本文结果不一致,分析可能同随访时间、病例数目等因素有关。
有研究发现,自膨式经导管主动脉瓣置换术在有症状的重度主动脉瓣狭窄患者治疗中具有良好的疗效[13]。但是,该术式较复杂,患者年龄较高,术后可能会发生房室传导阻滞、脑血管病变、出血和血小板减少症等并发症[14],本文中两组患者术后的并发症发生率均差异无统计学意义(P>0.05),可见合并不同程度MR的主动脉瓣狭窄患者在经导管主动脉瓣置换术后的并发症发生率接近。血小板减少症是为了预防出血使用肝素引发的,及时处理后血小板计数水平恢复,而脑血管病变可能会导致患者死亡[15],术后应注意监控和处理。
综上所述,经导管主动脉瓣置入手术可用于主动脉瓣狭窄合并不同程度MR患者的治疗中,此时MR的严重程度对术后患者远期死亡率和生活质量恢复的影响较小。

