LC-MS/MS快速测定血液中13种安眠镇静类药物及其代谢产物
石银涛,王绘军,王俊伟,郑经,吴玉红
(1.重庆市公安局物证鉴定中心,重庆 400021;2.重庆警察学院,重庆 401331;3.重庆市毒物毒品分析重点实验室,重庆 401331)
安眠镇静类药物具有镇静、催眠、抗惊厥以及中枢性肌肉松弛等作用,并且该类药物具有价格便宜、易得、催眠镇静作用起效快、安全范围大等特点,在临床上广泛使用。而安眠镇静类药物的临床不合理用药、误服误用、自杀他杀、麻醉抢劫和麻醉强奸等导致每年都发生大量的安眠镇静类药物摄毒案(事)件,引发公共安全事件和刑事案件[1-3]。安眠镇静类药物具有用量小、代谢快、半衰期短等特点[4-5],在体内组织和体液中浓度很低。因此,开展安眠镇静类药物及其代谢产物的高灵敏度检测方法的研究对法庭刑事案件侦破和临床诊断治疗具有十分重要的意义。
目前,安眠镇静类药物及其代谢产物的检测方法主要有气相色谱法(gas chromatography,GC)[6]、高效液相色谱法(high performance liquid chromatography,HPLC)[7-8]、气相色谱-质谱联用法(gas chromatography-mass spectrometry,GC-MS)[9-11]、液相色谱-质谱联用法(liquid chromatography-mass spectrometry,LC-MS)[12-19]。GC和LC样品中的基质干扰使检测容易出现假阳性,GC-MS方法检出限高,容易出现漏检。液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)因具有特异性强、灵敏度高、重现性好、线性动态范围宽等特点[20],在安眠镇静类药物检验中应用广泛。然而,现有LC-MS/MS检验方法绝大多数针对安眠镇静类药物中的一种或几种药物进行研究[13,16-17],而且对其代谢产物的研究相对较少。面对多种安眠镇静类药物及其代谢产物的同时检测要求,建立一种灵敏度高、专属性强,快速、准确、能同时检测多种安眠镇静类药物及其代谢产物分析方法显得尤为迫切。本研究旨在建立液液萃取-液相色谱-串联质谱检测血液中多塞平、米氮平、阿米替林、氯氮平、卡马西平、地西泮、艾司唑仑、阿普唑仑、三唑仑、氯氮蓝卓、氟硝西泮、氯硝西泮和代谢产物7-氨基氯硝西泮共13种安眠镇静类药物及其代谢物的方法。
1 材料与方法
1.1 仪器与试剂
Triple Quad 5500 LC-MS/MS系统(美国SCIEX公司),ACQUITY Ultra Performance LCTM系统(美国Waters公司),Allegra X-22R Centrifuge型冷冻离心机(美国Beckman公司),Direct-Q3型纯水机(美国Millipore公司),ML104电子天平(万分之一,瑞士Mettler-Toledo公司)。
乙腈、甲醇、甲酸铵、甲酸(色谱纯,美国TEDIA公司),其他试剂均为分析纯。
多塞平、米氮平、阿米替林、氯氮平、卡马西平、地西泮、艾司唑仑、阿普唑仑、三唑仑、氯氮蓝卓、氯硝西泮、氟硝西泮、7-氨基氯硝西泮和地西泮-d5,纯度≥98.0%,均购自美国Sigma公司。13种安眠镇静类药物及其代谢物标准品和地西泮-d5分别用甲醇配制成10μg/mL的储备液,于-20℃冷冻保存备用。上述储备液根据需要用甲醇稀释成不同质量浓度的13种安眠镇静类药物及其代谢物混合标准品工作液。地西泮-d5用甲醇稀释成1μg/mL的内标工作液。
1.2 样品前处理
取血液1mL置于15mL具塞离心管中,加入50μL地西泮-d5内标工作液(1 μg/mL),加入7 mL乙酸乙酯,涡旋振荡10 min,以离心半径10 cm,9 500 r/min,离心5min,取上清液,于40℃用氮气吹干,用甲醇定容至200 μL,涡旋,离心,过0.22 μm有机滤膜后,供LC-MS/MS分析。
1.3 色谱及质谱条件
色谱条件:ACQUITY Ultra Performance LC®BEH C18(100mm×2.1mm,1.7μm);流动相为甲醇(A)和含20mmol/L甲酸铵的0.1%甲酸水溶液(B)。梯度洗脱程序:0~1.0 min,90%B;1.0~2.0 min,90%~10%B;2.0~4.0 min,10%B;4.0~4.1 min,10%~90%B;4.1~7.0min,90%B;总采样时间为7min;流速0.3mL/min;柱温35℃;进样量2μL。
质谱条件:电喷雾正离子-多反应监测检测;气帘气为20 psi,离子源雾化气为60 psi,离子源加热辅助气为55 psi,碰撞气为8,喷雾电压为5 500 V,加热器温度为550℃。
1.4 方法学验证
1.4.1 选择性
6个不同来源的空白血液样品按“1.2节”方法处理后进行LC-MS/MS分析,观察血液中内源性物质对13种安眠镇静类药物及其代谢物的检测是否有干扰。
1.4.2 提取样品pH值的选择
取空白血液1mL于15mL具塞离心管中,添加的13种安眠镇静类药物及其代谢物混合标准溶液制成50μg/L的样品,用稀盐酸调节样品pH值为3和5,用饱和Na2CO3溶液调节pH值为9和11,空白血液的pH值为7,按“1.2节”方法处理、分析,比较样品pH值分别为3、5、7、9和11时的提取回收率。
1.4.3 线性关系与检出限
取空白血液1 mL于15 mL具塞离心管中,加入13种安眠镇静类药物及其代谢物的混合标准溶液,配制成质量浓度为0.1~200 μg/L系列血样样品,按“1.2节”方法处理、分析。以血液中目标物的质量浓度(x)为横坐标,以血液中目标物与内标的峰面积之比(y)为纵坐标,进行线性回归。
1.4.4 准确度和精密度
取空白血液1mL于15mL具塞离心管中,添加不同量的13种安眠镇静类药物及其代谢物混合标准溶液,分别配制成低、中、高3个质量浓度(10、50、200 μg/L)的血液样品,每个质量浓度点6份样品,按“1.2节”方法处理、分析,连续测定3 d。准确度用偏倚(%)表示,日内精密度(relative standard deviations,RSD)和日间精密度(RSD)计算公式如下:
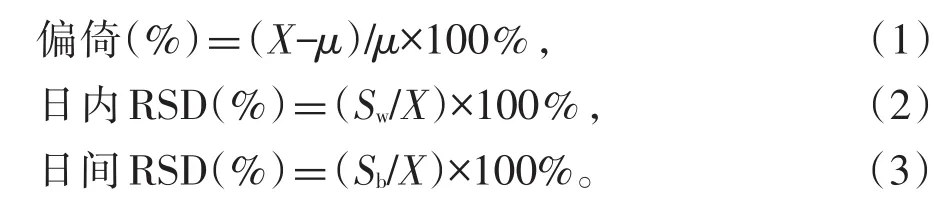
式中,X为平均浓度,μ为标准添加浓度,Sw和Sb分别为日内标准偏差和日间标准偏差。
1.4.5 回收率
取空白血液1mL于15mL具塞离心管中,将13种安眠镇静类药物及其代谢物混合标准溶液分别配制成低、中、高3个质量浓度的血液样品,每个质量浓度点6份样品,按“1.2节”方法处理,按1.3节分析后的色谱峰面积(S3)与空白样品基质提取液添加相应的混合标准溶液后的色谱峰面积(S2)的比值计算回收率(RE)。
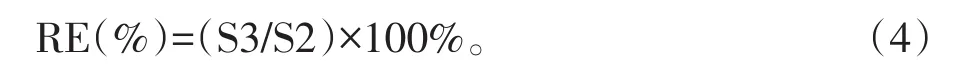
1.4.6 基质效应
基质效应是指基质中的共提取干扰物影响目标物的离子化,从而使目标物在仪器上的响应发生增强或抑制。因此,需要对目标物在不同基质中的基质效应进行评价,并根据评价结果选择适合的方法对基质效应进行抵消[21]。分别测定混合标准溶液的色谱峰面积(S1)和空白样品基质提取液添加标准溶液后的色谱峰面积(S2),以比值S2/S1(%)评价基质效应。
2 结果与讨论
2.1 色谱及质谱条件的选择
2.1.1 色谱条件的选择
本实验选取C18色谱柱作为分析用色谱柱。实验比较了甲醇和乙腈、0.1%甲酸水溶液和含20 mmol/L甲酸铵的0.1%甲酸水溶液、等度洗脱和梯度洗脱对分析结果的影响。实验结果表明:梯度洗脱优于等度洗脱,选择甲醇梯度洗脱分析时,各化合物的分离效果好,响应值高,基质干扰弱。含20mmol/L甲酸铵的0.1%甲酸水溶液优于0.1%甲酸水溶液,加少量的盐后,各化合物的保留时间稳定。因此,选用20mmol/L甲酸铵(含0.1%甲酸)水溶液-甲醇为流动相。
2.1.2 质谱条件的选择
本研究中13种安眠镇静类药物及其代谢物结构中有易于和H+结合的带有孤对电子的N原子,因此选择电喷雾正离子(ESI+)作为电离模式。采用针泵直接进样,确定目标物的母离子,采用子离子扫描方式进行二级质谱扫描,按照响应强度从高到低的原则选取两个以上的碎片作为子离子,并优化各子离子的电压参数。13种安眠镇静类药物及其代谢物、内标的具体质谱参数见表1。
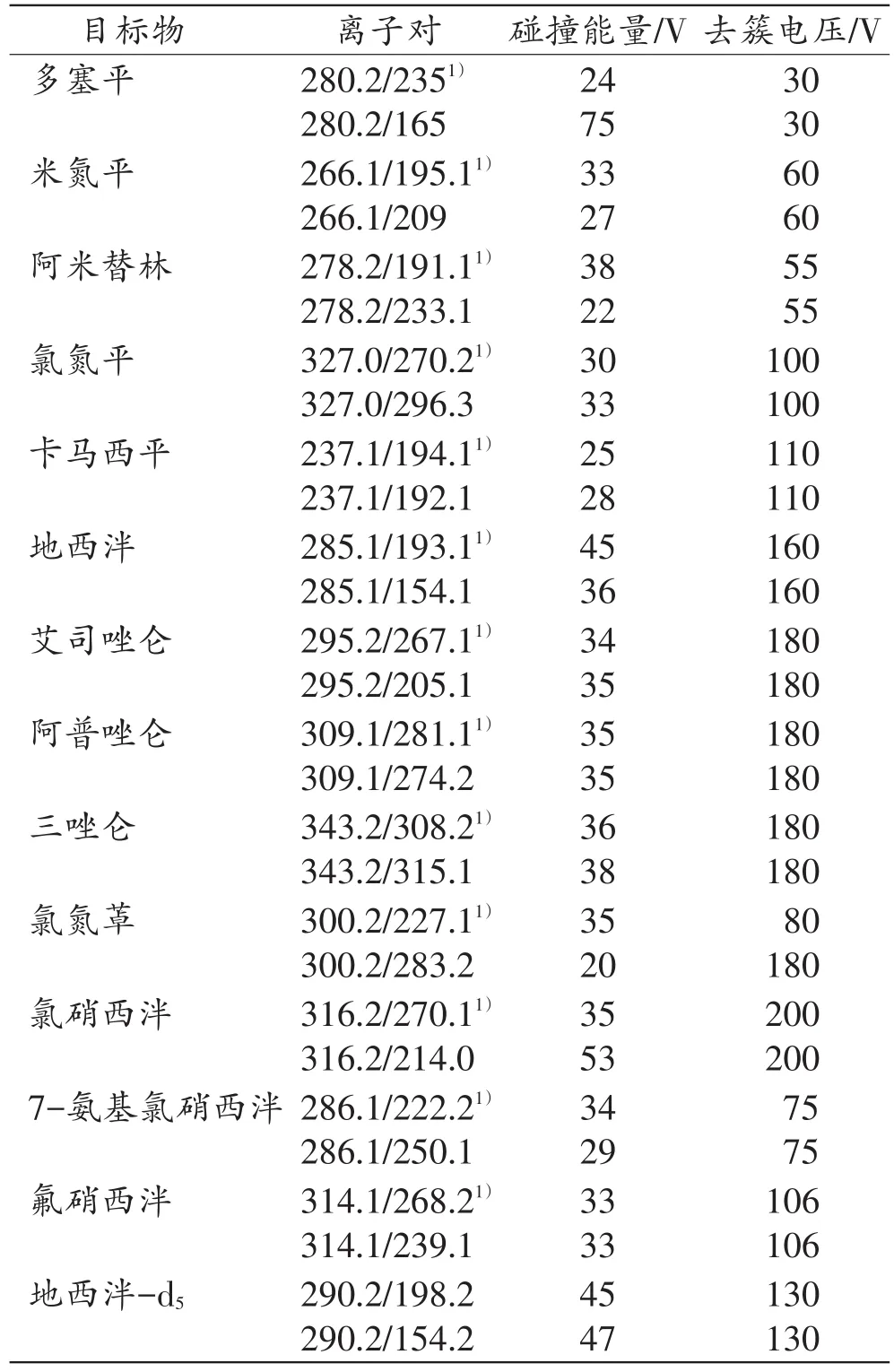
表1 13种安眠镇静类药物及其代谢物、内标的质谱参数Tab.1 Mass spectrum parameters of 13 hypnotic and sedative drugs,their metabolites and internal standards
2.2 方法学验证
2.2.1 选择性
实验结果表明,6个不同来源的空白血液样品的内源性物质不干扰13种安眠镇静类药物及其代谢物的测定,该方法的专属性良好。图1为添加标准品(100μg/L)和添加内标的血液样品的总离子图。
2.2.2 提取样品pH值选择
随着pH值的增加,目标物的提取回收率也逐渐提高,但当pH=9、pH=11时,目标物的回收率依次降低,在pH=7时回收率最高。故样品pH值最终选择为7。
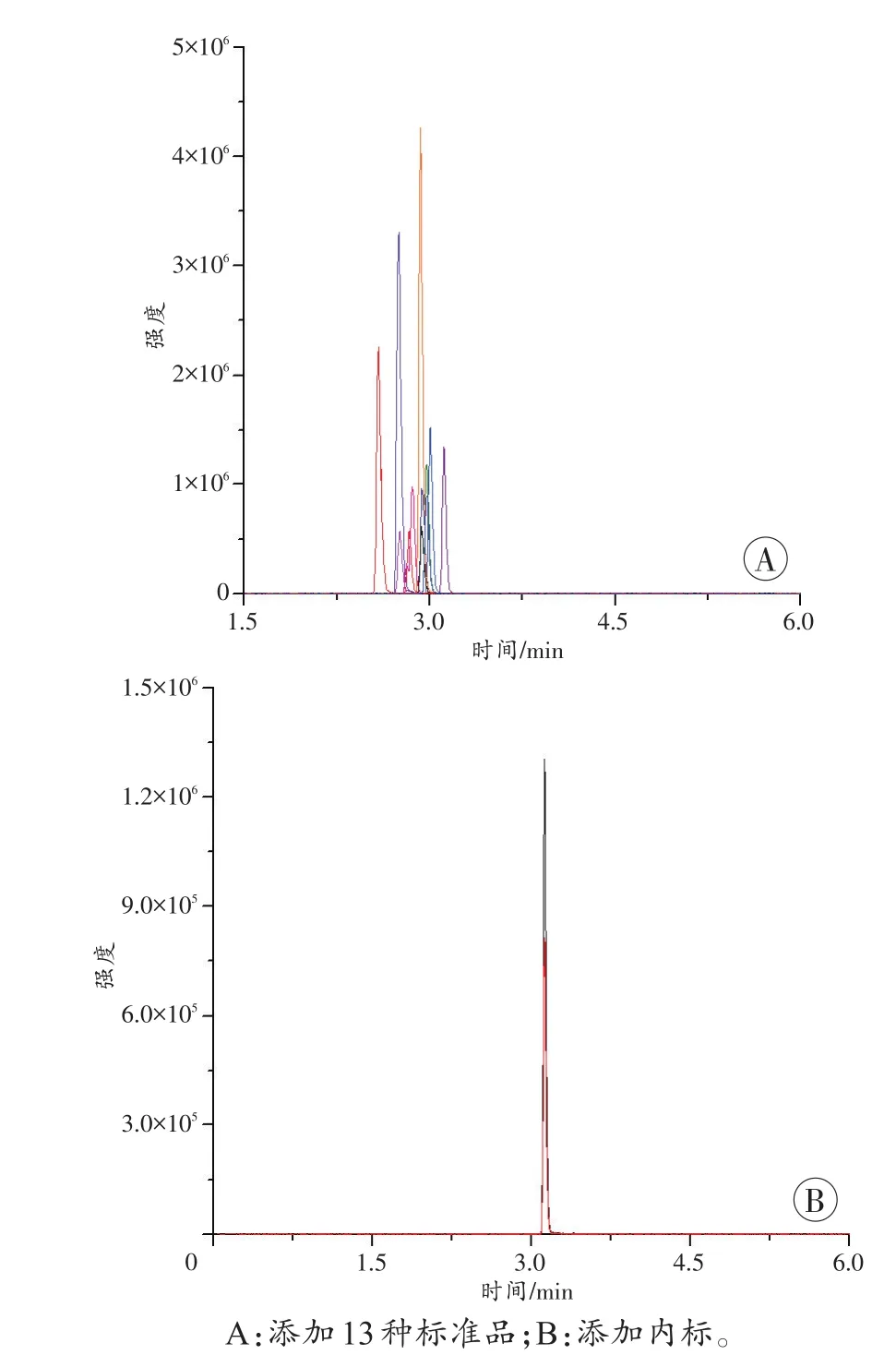
图1 血液样品的总离子流图Fig.1 Total ion flow diagram of blood sample
2.2.3 线性关系及检出限
血液中13种安眠镇静类药物及其代谢物的线性方程、相关系数及检出限见表2。在5~200μg/L质量浓度范围内,血液中13种安眠镇静类药物及其代谢物均呈良好的线性关系。
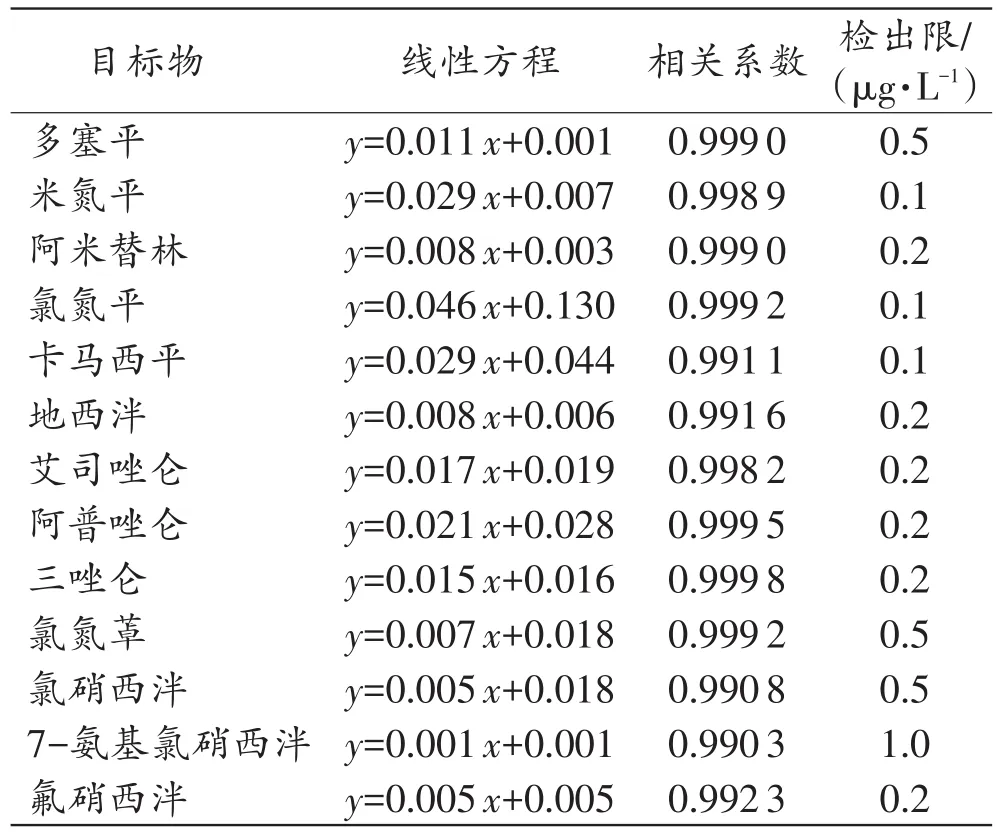
表2 目标物的线性方程、相关系数及检出限Tab.2 Linear equation,correlation coefficient and detection limit of targets
2.2.4 准确度和精密度
配制含13种目标物10、50、200μg/L 3种质量浓度的血液样品各6份,按“1.2节”方法处理、按“1.3节”分析,连续测定3 d。计算各浓度血样测定结果的准确度。用上述3种质量浓度的标准血液样品,1d内分析6次,得日内RSD;连续测定3 d,每天1次,得日间RSD。日内和日间RSD不大于8.6%,准确度(偏倚)在±9.8%范围内(表3)。
2.2.5 回收率
血液中13种安眠镇静类药物及其代谢物在3个添加质量浓度(10、50、200 μg/L)的回收率见表 3。13种安眠镇静类药物及其代谢物的平均回收率在71.2%~93.4%,满足日常检案的要求。
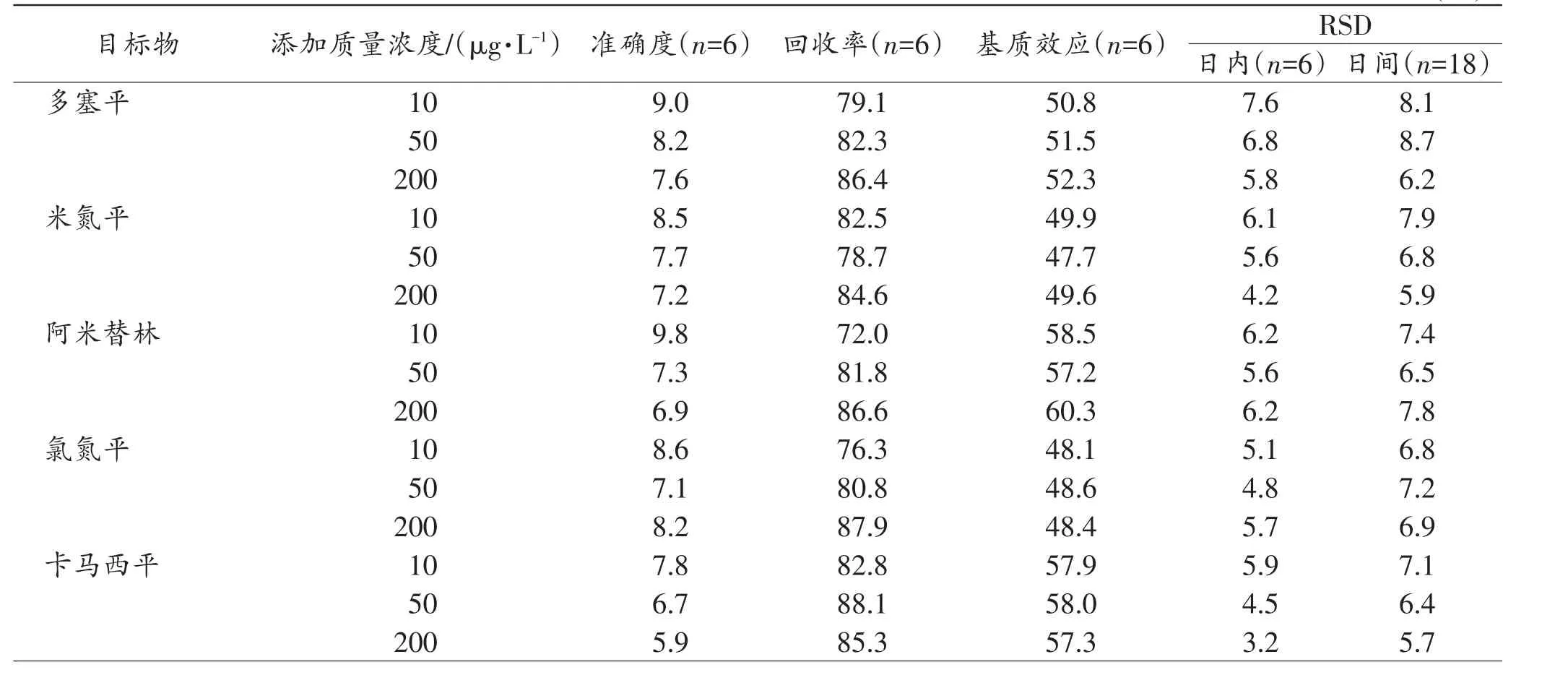
表3 目标物的准确度、回收率、基质效应和精密度Tab.3 Accuracy,recovery,matrix effect and precision of targets (%)
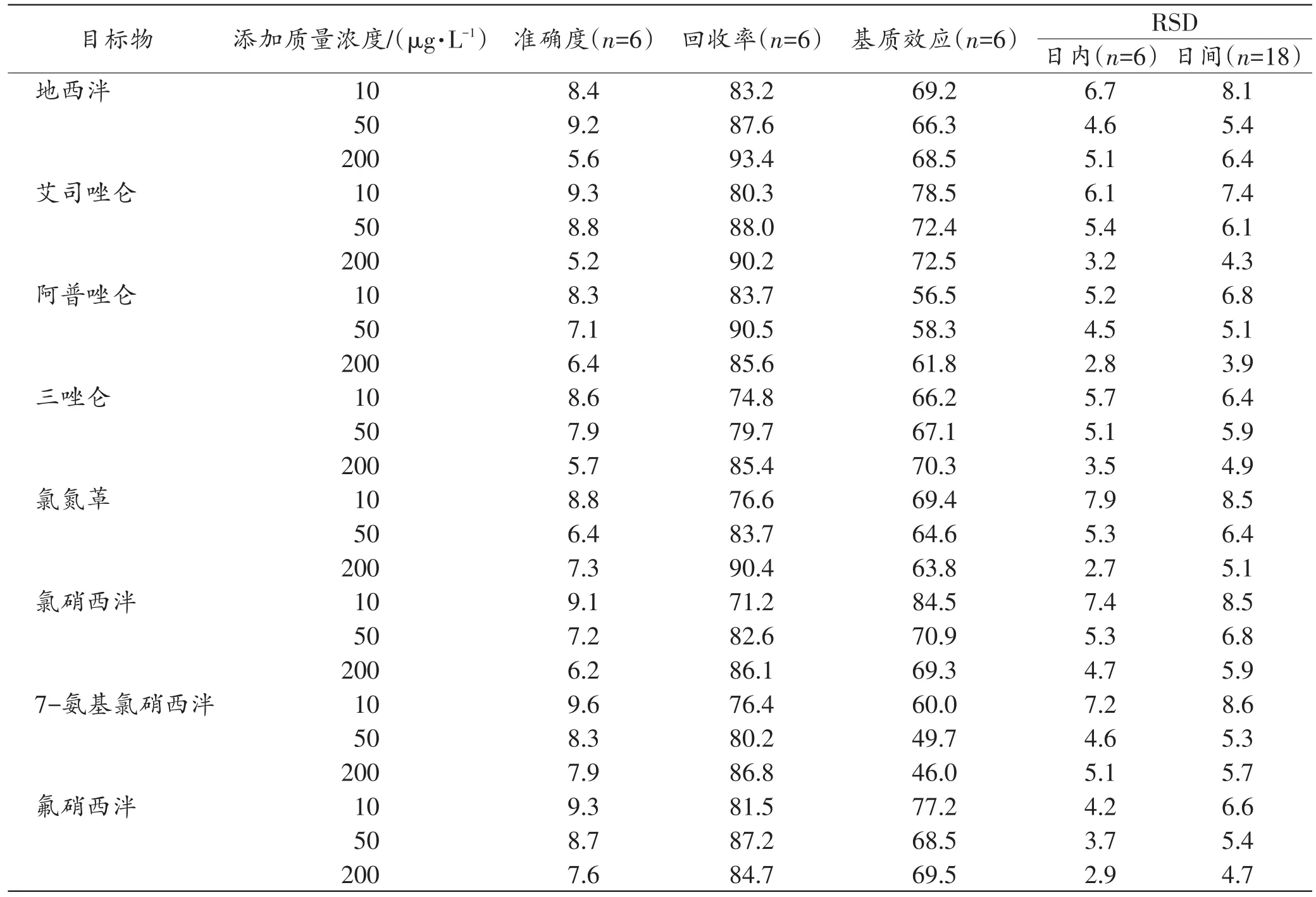
续表3Continued Tab.3
2.2.6 基质效应
目标物在10、50和200 μg/L质量浓度时的基质效应值说明血液中基质对目标物的测定具有较强的抑制作用(表3)。由于基质效应明显,本研究最终采用内标法以降低基质效应的影响。
2.3 实际案例分析
重庆居民谭某于某年12月4日18:00左右在江北区一家火锅店和朋友一起吃饭,吃完饭后和几个朋友打牌,在打牌过程中谭某感觉意识不清、昏昏欲睡,并被诈骗21万元。次日10:00左右提取谭某血液。使用本研究建立的方法对受害人谭某的血液进行13种安眠镇静类药物及其代谢物的定性定量检测,从血液中检出氯硝西泮和7-氨基氯硝西泮,质量浓度分别为 22.3 μg/L 和 196.9 μg/L(图 2)。据犯罪嫌疑人交代,在谭某喝的啤酒中投入了安眠镇静类药物。
CHÈZE等[22]报道的麻醉抢劫案,受害人饮用1瓶含有2.1mg氯硝西泮的啤酒很快入睡,尿液中检出氯硝西泮和7-氨基氯硝西泮的质量浓度分别为17.8μg/L和561.7μg/L,尿液中7-氨基氯硝西泮的质量浓度远大于氯硝西泮的质量浓度。本研究中血液中7-氨基氯硝西泮的质量浓度远大于氯硝西泮的质量浓度,可能与采样时间距离案发时间较长有关。
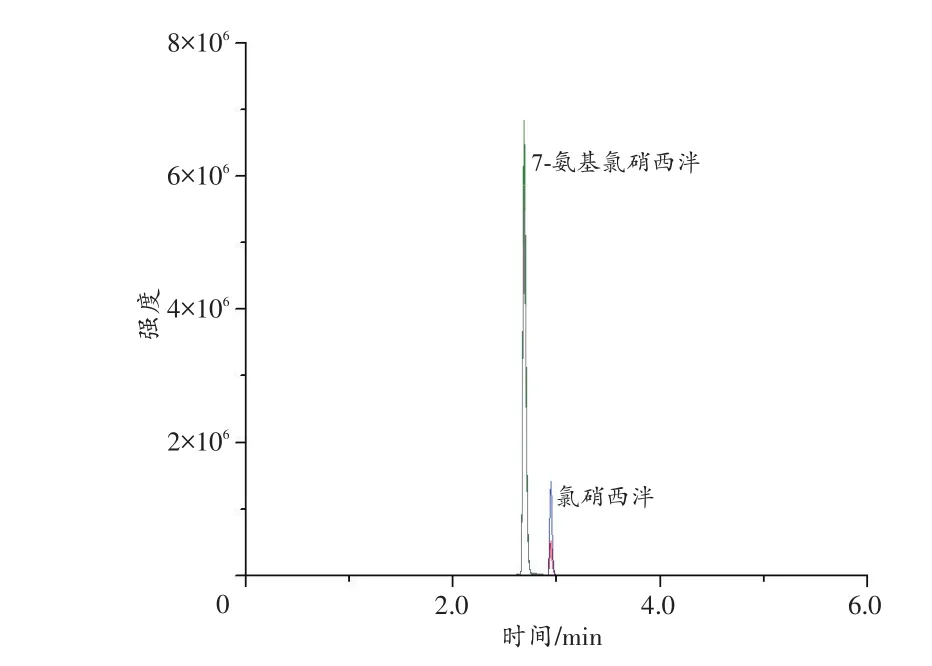
图2 实际样品的多反应监测色谱图Fig.2 Multi reaction monitoring chromatogram of actual sample
3 结 论
本研究结合液液提取与LC-MS/MS技术,建立了同时测定血液中13种安眠镇静类药物及其代谢产物的分析方法。该方法简便快速、专属性强、灵敏度高、重现性好,最低检出限为0.1~1.0 μg/L。实际案例分析结果表明,该法适于分析血液中13种安眠镇静类药物及其代谢产物,在法庭与临床毒物分析中具有重要的应用价值。

