新型吡唑啉衍生物合成与抑菌活性实验研究
罗杰伟,程登龙,钟 月,刘沂明,朱 红*
(1.川北医学院基础医学院,四川 南充 637000;2.川北医学院临床医学系,四川 南充 637000)
传染病仍然是当今严重威胁人类健康的疾病。在抗感染治疗中,抗菌药物的发现及使用为人类的健康带来了福音。但随着细菌耐药性的不断出现,甚至超级细菌的出现,使抗菌治疗不断受到新的挑战,人类生命受到严重威胁,研究者也在不断寻找和研制新的抗菌药物的征途上不断进取。文献表明[1-3],吡唑啉化合物因具有广泛的生物学活性如消炎、止痛、抗菌、抗病毒、抗肿瘤等作用而受到关注,已经成为合成化学杀菌剂的重要研究对象,因此吡唑啉化合物将具有非常好的应用前景。
吡唑啉化合物是一类具有广泛生物活性的物质,此类化合物因具有如抗菌、抗炎、抗肿瘤等活性在医药生产中具有重要的用途,长期以来受到业内关注[4]。早在19世纪后期,Fischer E等采用丙烯醛与苯肼合成出吡唑啉类化合物,在之后的很长一段时间里,采用α,β-烯酮类(醛)化合物与肼类化合物合成了很多吡唑啉类衍生物。自20世纪70年代Ankhiwala M D等[5]报道了某些取代的吡唑啉化合物具有优良的杀菌活性和Makino K等[6]通过实验发现在1-位氮原子上引入磺酰基可筛选出除草活性较强的化合物后,许多新型吡唑啉类化合物在医药中的应用产生了良好的效果。吡唑啉环是不同生物活性的重要结构单元,且取代基在环上不同位置变换可明显影响其生物活性。如杨金美等[7]报道了几种酰代吡唑啉酮金属配合物具有抑菌活性;Turan-Zitounia G等[8]发现含硫杂环2-吡唑啉化合物呈现较强的抗菌活性。此外,王瑾玲等[9-10]报道了一些酰基吡唑啉酮化合物和Yoshioka Koichi等[11]报道了一些吡唑烷酮类化合物也具有杀菌性能,而赵军龙等[12-13]报道了含二茂铁基吡唑啉具有较好的抗真菌活性。基于以上研究,本课题组根据α,β-不饱和醛酮亲核加成反应原理合成化合物L{[3-(4-N,N-dimethyl-pyenyl)-5-Anthracen-9-yl]-Pyrazoline}和化合物M[3-ferroceny-5-(Anthr acen-9-yl)-Pyrazoline],并利用1H NMR、13C NMR对化合物进行结构表征,测定化合物L和化合物M对金黄色葡萄球菌、乙型溶血性链球菌、大肠杆菌、痢疾杆菌、白色念珠菌、新型隐球菌的抑菌效果。
1 实验部分
1.1 仪器和试剂
琼脂粉,分析纯;蛋白胨,北京OXOID公司;酵母提取物,北京OXOID公司;沙保罗氏琼脂,杭州滨和微生物试剂有限公司。其余所用试剂均为化学纯或分析纯,实验用水为二次蒸馏水。
金黄色葡萄球菌(ATCC 6538)、乙型溶血性链球菌、大肠杆菌(8099)、痢疾杆菌、白色念珠菌和新型隐球菌均由川北医学院病原实验中心提供。
恒温空气浴摇床,哈尔滨市东明医疗仪器厂;生物安全柜,美国BIO-RAD公司;SHP-150型生化培养箱,上海精宏实验设备有限公司;标准细菌比浊管,北京哲成科技有限公司。
1.2 合成路线
图1为化合物L与化合物M的合成路线。
1.3 合成步骤
1.3.1 化合物L的合成与结构表征
氮气保护下将化合物1(参考文献[14]的方法合成)(2.55 g、7.1 mmol)加入20 mL无水乙醇与5 mL冰乙酸混合液中,缓慢滴加水合肼(0.82 g、16.4 mmol),常温搅拌30 min使其混合均匀。加热至70 ℃回流8 h,冷却至常温,用CH2Cl2萃取3次,合并有机相,无水Na2SO4干燥,经旋转蒸发仪蒸干得黄色固体,粗品经柱层析纯化(石油醚与乙酸乙酯体积比为4∶1),得到黄色粉末状物质1.02 g,产率为40%,熔点为(180~184) ℃。
将化合物L提纯,充分干燥,选择CDCl3为氘代溶剂,将带有样品的核磁管装入核磁测定仪器中,锁定氘代溶剂吸收峰,扫描并收集信号。1H NMR(CDCl3,400 MHz)δ(ppm):3.0(s,J=5.5 Hz,6H,-CH3),5.25(s,1H,-CH-),6.61(d,2H,-CH2-),7.15(s,1H,Ar-H,),7.28(d,2H,Ar-H),7.42~7.58(m,5H,Ar-H),7.95(d,2H,Ar-H),8.15(d,2H,Ar-H),8.55(s,1H,Ar-H)。13C NMR(CDCl3,400 MHz)δ(ppm):40.07,111.67,121.76,124.31~135.54,149.36,152.27,200.01。
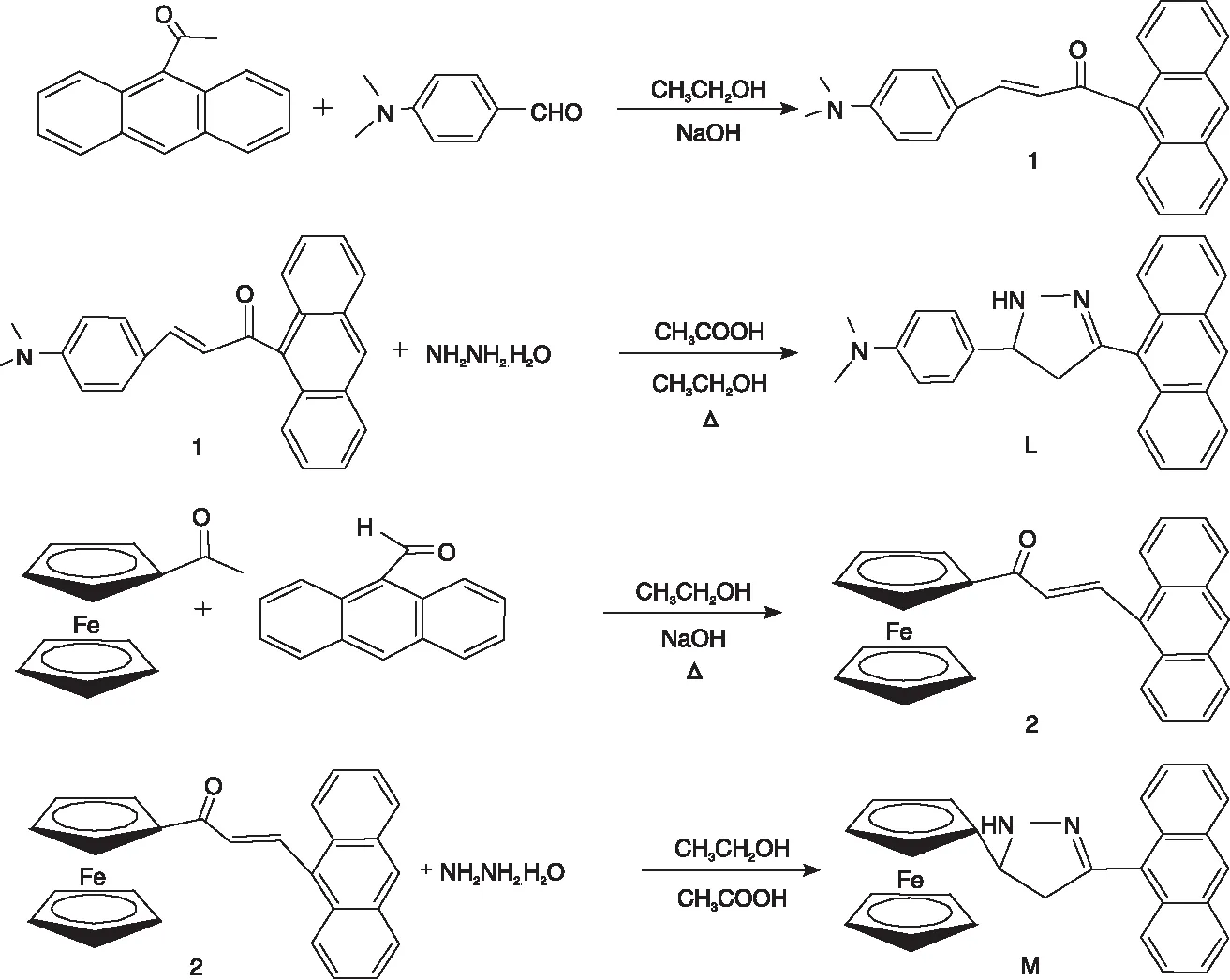
图1 化合物L与化合物M的合成路线Figure 1 Synthesis routes of compounds L and M

1.3.2 化合物M的合成与结构表征
氮气环境下将化合物2(参考文献[14]的方法合成)(2.68 g、7.1 mmol)加入20 mL无水乙醇和5 mL冰乙酸的混合液中,缓慢滴加水合肼(0.81 g,16.4 mmol),常温搅拌30 min使其混合均匀。加热至70 ℃回流8 h,冷却至常温,用CH2Cl2萃取3次,合并有机相,无水Na2SO4干燥,经旋转蒸发仪蒸干,粗品经柱层析纯化(石油醚与乙酸乙酯体积比为3∶1),得到黄色固1.52 g,产率为56.72%,熔点为(250~255) ℃。


1.4 抑菌活性实验
1.4.1 制备LB培养液及LB平板
按照LB培养液的常规制作方法,分别称取蛋白胨和酵母提取物,加入三角烧瓶中,加双蒸水(DW)100 mL加热溶解后,再加双蒸水,调节pH值,按需分装后高压灭菌(15磅,15 min),即制得LB培养液。
称取2 g琼脂粉放入加有100 mL的LB培养液的三角烧瓶中,高压灭菌(15磅,15 min),取出后稍冷倒板,即制得LB平板,备用。相似方法制备沙氏培养基及血清平板。
1.4.2 配备药物溶液
将化合物L与化合物M干燥,称取0.037 5 g化合物L和0.043 2 g化合物M,置于100 mL容量瓶中,加乙腈溶解,制备成浓度1.0×10-3mol·L-1储备液,4 ℃保存备用。
1.4.3 制备菌悬液
将-70 ℃保存的金黄色葡萄球菌、乙型溶血性链球菌、大肠杆菌、痢疾杆菌、白色念珠菌和新型隐球菌菌种取出,室温解冻。接种环焚烧灭菌分别取细菌分区划线接种于适宜平板,37 ℃培养18 h,用无菌接种环取单个菌落接种于5 mL的LB培养液中,37 ℃水浴,180 rpm振摇培养18 h。参照标准细菌比浊管,用无菌pH=7.2磷酸盐缓冲液(PBS液)制备成菌浓度(5.0×105~5.0×106) cfu·mL-1的菌悬液[15]。
1.4.4 抑菌实验
分别取0.1 mL菌悬液均匀涂布于适宜平板表面,自然干燥,每个平板放置两个牛津杯,轻压固定,分别吸取0.2 mL化合物L的乙腈溶液及化合物M的乙腈溶液加入不同的牛津杯中,37 ℃培养20 h后观察细菌生长情况,测量抑菌圈的直径[16]。试验同时设置乙腈溶液作用组、正常LB培养液对照组。实验重复3次,取平均值。
2 结果与讨论
化合物L与化合物M对不同微生物的抑菌效果观察结果如表1所示。

表1 化合物L与化合物M对不同微生物的抑菌效果观察结果
表1的抑菌结果显示,空白乙腈作用组、LB培养液对照组的细菌生长良好,细菌生长未受影响;化合物L对金黄色葡萄球菌、乙型溶血性链球菌、大肠杆菌、痢疾杆菌均有一定的抑菌作用,且对金黄色葡萄球菌、乙型溶血性链球菌的抑菌作用强于大肠杆菌和痢疾杆菌。化合物M对金黄色葡萄球菌、乙型溶血性链球菌和大肠杆菌和痢疾杆菌也有一定的抑菌作用,其抑制金黄色葡萄球菌、乙型溶血性链球菌的作用略强于大肠杆菌、痢疾杆菌。比较两者对细菌的作用结果(抑菌圈直径的大小),化合物L的抑菌作用明显强于化合物M,原因可能是化合物L的吡唑啉环连接N、N-二甲基苯环增强了抑菌活性。两种化合物对白色念珠菌和新型隐球菌(真菌)均无抑制作用。
3 结 论
(1) 吡唑啉化合物对多种细菌均有不同程度的抑制作用,抑菌机理主要是抑制菌体糖及代谢中间产物的氧化和脱氢,并能抑制蛋白和核酸的合成,可避免临床上某些抗菌素的毒副反应及耐药性。抗菌实验显示,化合物L的抑菌作用明显强于化合物M,原因可能是化合物L的吡唑啉环连接N、N-二甲基苯环增强了抑菌活性。
(2) 金黄色葡萄球菌、乙型溶血性链球菌是一种典型的革兰氏阳性菌;大肠杆菌、痢疾杆菌是革兰氏阴性菌的代表;而白色念珠菌、新型隐球菌则是一种单细胞真菌。实验结果显示,化合物L和化合物M对典型革兰氏阳性菌和典型革兰氏阴性菌有一定的抑菌效果,对真核细胞型微生物作用不明显。但由于化合物L的乙腈溶解性及水溶解性均较化合物M差,表明化合物L的实际抑菌效果可能比实验结果还要强一些。

