二氧化锰与二维材料复合应用于超级电容器
王易,霍旺晨,袁小亚,张育新,*
1重庆大学材料科学与工程学院,重庆 400044
2重庆交通大学材料科学与工程学院,重庆400074
1 引言
近几十年来,科技现代化、产业自动化程度不断地进步和革新,同时人口不断增长,能源的需求量也越来越大。然而,数十年大量化石能源的消耗给环境带来了严重影响,并且传统的化石能源有不断消耗殆尽的趋势。能源危机将会制约着现代社会的发展,因此开发和利用可再生能源是人类解决能源问题进而可持续发展的重要举措之一,也成为了当前众多科学家研究的重点课题。高效的能量存储与转换技术成为可再生能源和发展中突出的研究方向。超级电容器功率密度高、循环使用寿命长、倍率性能好,与其他存储系统相比,超级电容器可以在几分钟甚至几秒钟内充电,确保快速存储和交换能量,被认为是一种很有发展前景的能量储存装置1-4。按其储能机理,超级电容器一般可分为两种2,5:双电层电容器、赝电容电容器。双电层电容器是利用电极材料和电解质之间形成的界面双电层来储存能量,主要是双电层理论的机理;法拉第赝电容器是在电极表面或体相中,电极活性物质进行欠电位沉积,发生高度可逆的化学吸附脱附或氧化还原反应来产生电容。
电极材料是决定超级电容器性能的关键因素之一,目前主要分为三大类:碳材料、过渡金属氧化物、导电聚合物。MnO2凭借其低成本(与RuO2相比)、高理论比电容(1370 F·g-1)等优点在过渡金属氧化物中脱颖而出,被广泛用于开发高性能电化学能量存储器件,但与此同时它的导电率低、离子迁移速率低、结构稳定性差5,6,这很大程度上限制了它作为单一电极材料的应用。现在大量研究集中于MnO2与其他材料的复合,以期达到更加理想的储能效果。国内外的大量研究已经表明了石墨烯及其复合物作为储能材料的巨大潜力7-9,正致力于开发同时具有高容量、高功率而且柔性并可实现快速充电的应用石墨烯电极的储能器件。此外,意识到与石墨烯具有相仿的二维结构的其他材料(简称为类石墨烯材料),诸如层状双金属氢氧化物(LDH)、片层状金属氧化物(TMOs)和氢氧化物(TMHs) (如二氧化钌(RuO2)、二氧化锰(MnO2)等、片层状过渡族金属二硫族化合物(TMDCs)和层状金属碳化物/氮化物(MXene)等,也具有成为高能量密度超级电容器电极材料的潜质10,11。随着近些年微小器件的大量使用,超级电容器因此也面临着新的挑战,柔性、可拉伸、轻薄化等高要求的超级电容器研究方兴未艾12-16,对这些二维结构材料的研究也相继展开并取得了快速的进展。将MnO2与上述二维材料进行有效复合,充分发挥MnO2和这些二维材料的优势,不仅能改善MnO2的导电性,同时能为复合材料带来更大的表/界面积,提供更多的电化学活性位点,也将进一步为超级电容器增添柔性、可拉伸、轻便、透明等可贵优势。
关于应用于超级电容器的二氧化锰基材料综述、二氧化锰/二维材料复合物的制备近年来已有很多报道5,17-21,这类材料在能量存储与转换、阻燃、催化等领域表现出重要的应用前景。特别是基于该类材料的超级电容器具有高的比电容和优异的电化学稳定性,从而表现出重要的实际应用前景。然而,MnO2与各类二维材料的复合综述还没有报道。本综述首次系统介绍了以石墨烯为代表的各类二维材料与MnO2纳米复合物在超级电容器中的应用研究,并聚焦于这些二维材料与二氧化锰复合后所展现的优良电化学性能。
2 MnO2基超级电容器研究进展
2.1 MnO2的电化学储能机理
在1999年,Lee和Goodenough22作了一个氧化锰在液相溶液中赝电容行为的指导性研究,初步建立了相关的电荷存储机制。发生在MnO2表面或体相中的赝电容反应是其主要的储能机理,主要包含两类充放电机原理,一种是表面吸/脱附理论,即电解液中的金属离子通过在MnO2表面的吸附和脱附过程。另外一种是本体嵌入/脱出理论,即在充放电过程中,通过电解液中的阳离子在二氧化锰本体内进行嵌入和脱出进行电荷的存储5,23。反应机理如下:
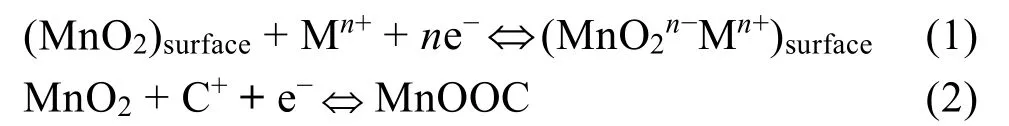
其中,C+代表H+、Li+、Na+、K+等阳离子。
尽管以上两种机理各有不同,但也有相似之处,即都存在三价和四价锰离子间的氧化还原反应。
近些年,二氧化锰电极材料的改性问题一直颇受关注,目前掺杂和复合仍是改性方面较为常用的方法,也有向MnO2基材料中引入缺陷的做法。其中对二氧掺杂后,杂质起到了支撑晶格的作用,使MnO2始终保持一种“敞开”式结构,质子和电子得以在晶格间自由流动,并抑制晶格的膨胀。但物质与复合材料的选择、掺杂和复合方式以及与二氧化锰材料的配比是获得高质量电极的关键。
2.2 MnO2电极材料
作为继RuO2之后被应用于赝电容器电极材料的MnO2,因具有廉价易得、环境友好且电化学活性高等优点一直是研究热点。
1999年,Lee等22首次用无定型的二氧化锰作为超级电容器材料并获得200 F·g-1的比电容,自此以后二氧化锰作为超级电容器电极材料被进一步研究。二氧化锰作为电极材料的优势主要在于:(1)高的理论比电容;(2)有大约0.9-1.0 V的宽电位窗口(相对于在液相电解质中Co3O4和NiO的0.4-0.5 V);(3)采用不具有腐蚀性的中性电解液。另一方面就是得益于MnO2资源较丰富、成本低、环境友好等优势。尽管具有如此多的优势,可二氧化锰在实际应用中的电容性能却远不如理论情况。此外,基于MnO2的电极的进一步发展受到其在高充电/放电速率下比电容低以及由于MnO2的解体导致循环性差的限制。但二氧化锰电容性能的主要制约掣肘在于其电导率差(10-5-10-6S·cm-1),由于其宽带隙、低离子扩散常数、差的结构稳定性。同时,其微观纹理特征(比如尺寸维度、孔隙率等)、晶体结构、缺陷化学也会对电化学性能有一定影响5。现已有较多研究综述系统介绍了二氧化锰基超级电容器,以及影响其电容性能的关键因素5,17,23-26。为获得更高实际比电容,不同形态、多孔结构、高比面积的纳米二氧化锰被合成。合成方法主要有水热法27-29、溶胶凝胶法30,31、电化学沉积法32,33,模板法34-36。

图1 低放大倍数下(a,c)以及不同浓度试剂((1) n(KMnO4) : n(KCl) = 1 : 3; (2) n(KMnO4) : n(KCl) = 3 : 1)高放大倍数下(b,d)异质纳米花状二氧化锰的的SEM图37Fig. 1 SEM images of low-magnification (a, c) and high-magnification (b, d) of hierarchical MnO2 nanoflowers synthesized at different concentration: (1) n(KMnO4) : n(KCl) = 1 : 3; (2) n(KMnO4) : n(KCl) = 3 : 1 37.
例如,Zhao等37通过一步水热法合成了水钠锰矿型MnO2纳米花,如图1所示,探究发现,反应试剂的比例控制是形成纳米花的关键。电化学测试表明,该电极材料有着高比电容(1 A·g-1的电流密度下,比电容为197.3 F·g-1)以及出色的循环稳定性(经1000次循环,仅有5.4%的电容损失)。
Yin等38利用MnCl2-KMnO4水溶液体系中可控的氧化还原反应,设计了一种简单的水热法合成均匀的α-MnO2纳米线,纳米线的长度为数十微米,平均直径为20 nm,观察到的晶面间距为0.489 nm,如图2所示。结果表明,电流密度为1.0 A·g-1,比电容为180 F·g-1。循环2000圈后,电容保持率为78%。Bing等39联用固相反应和湿法化学合成了α-MnO2,并讨论了合成反应时间和酸处理温度对α-MnO2晶体结构,形貌和电化学电容性能的影响。结果表明,样品在25 °C酸处理较长时间后显示出均匀的纳米棒,聚集形成微型建筑的棒表面的精细特征,并呈现出鹿角珊瑚状形貌,如图3所示。该微结构具有大的表面积和更易于电化学接触的活性位点,从而有更好的电化学电容性能。
2015年,单层二氧化锰纳米片被报道40,他们通过十二烷基硫酸钠(SDS)水解获得的十二烷醇将KMnO4还原MnO2纳米固体。结果表明SDS的逐渐水解被认为是成功形成单层纳米片的关键因素。Liu等41通过简单的模板辅助水热法成功设计出了一种具有超薄厚度(约4 nm)的碗状MnO2纳米片的纳米结构,如图4和图5所示。与固体颗粒相比,这种新型纳米结构有望有效地减少空间,为氧化还原反应提供额外的电活性位点,缩短离子/电子转移的反应路径,并最大限度地利用MnO2活性材料。当作为电极材料时,碗状MnO2纳米片在0.5 A·g-1的电流密度下具有379 F·g-1的比电容,电流密度从0.5 A·g-1升至10 A·g-1时的电容保持率为60.5%,经5000次循环后的电容保持率为87.3%。

图2 α-MnO2纳米线的SEM图和TEM图38Fig. 2 SEM and TEM images of the as-synthesized α-MnO2 nanowires 38.
将片状二氧化锰有机组装从而形成优异的结构或形貌是这一领域的又一重点研究方向,当前已被许多学者聚焦42。Gao等43通过剥离又重组二维δ-MnO2的策略来构建三维多孔纳米结构,并研究了伴随不同的pH条件下锰缺陷对赝电容性能的影响。张育新课题组对二维重组三维异质结构也进行了反复的研究44,45,这种结构增大了电解液与电极材料的接触面积,同时也缩短了离子扩散距离。
在当前的研究中,为了进一步改善MnO2的电导率,在纳米化合成MnO2的同时,还将纳米结构的MnO2通过合理设计嵌入到各类导电材料中。一种强大而直接的方法是将MnO2纳米结构均匀地结合到分层多孔和导电材料中以形成异质纳米复合材料。在纳米复合结构中,纳米MnO2结构可缩短用于电荷转移的路径,并为电荷存储提供更多可用的电活性位点,与此同时,导电材料可促进电子收集和迁移,提高机械稳定性,即使在高速充放电条件下也能保证MnO2的高电化学性能。这种复合策略目前已应用在了很多研究当中46-48。

图3 不同反应条件下得到的4个样品的SEM图39Fig. 3 SEM images of fours samples treated at various conditions 39.
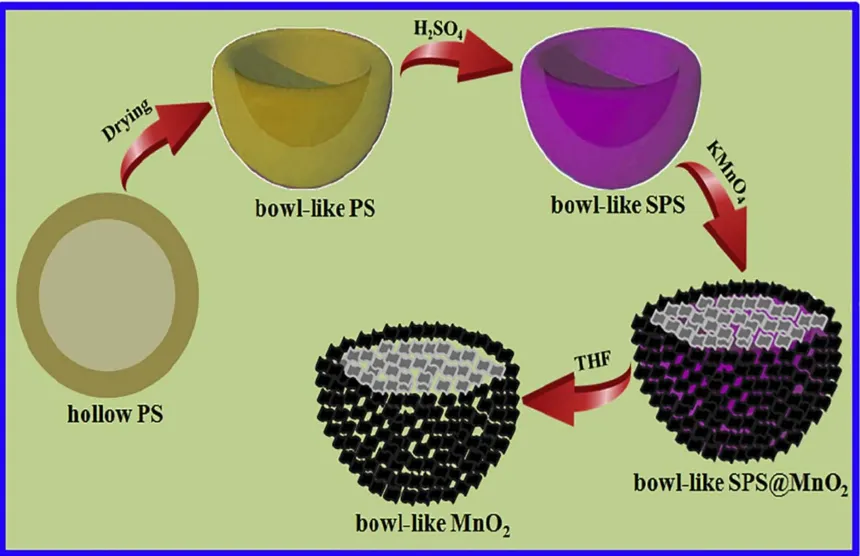
图4 碗状MnO2纳米片的形成示意图41Fig. 4 Schematic illustration of the formation of bowl-like MnO2 nanosheets 41.
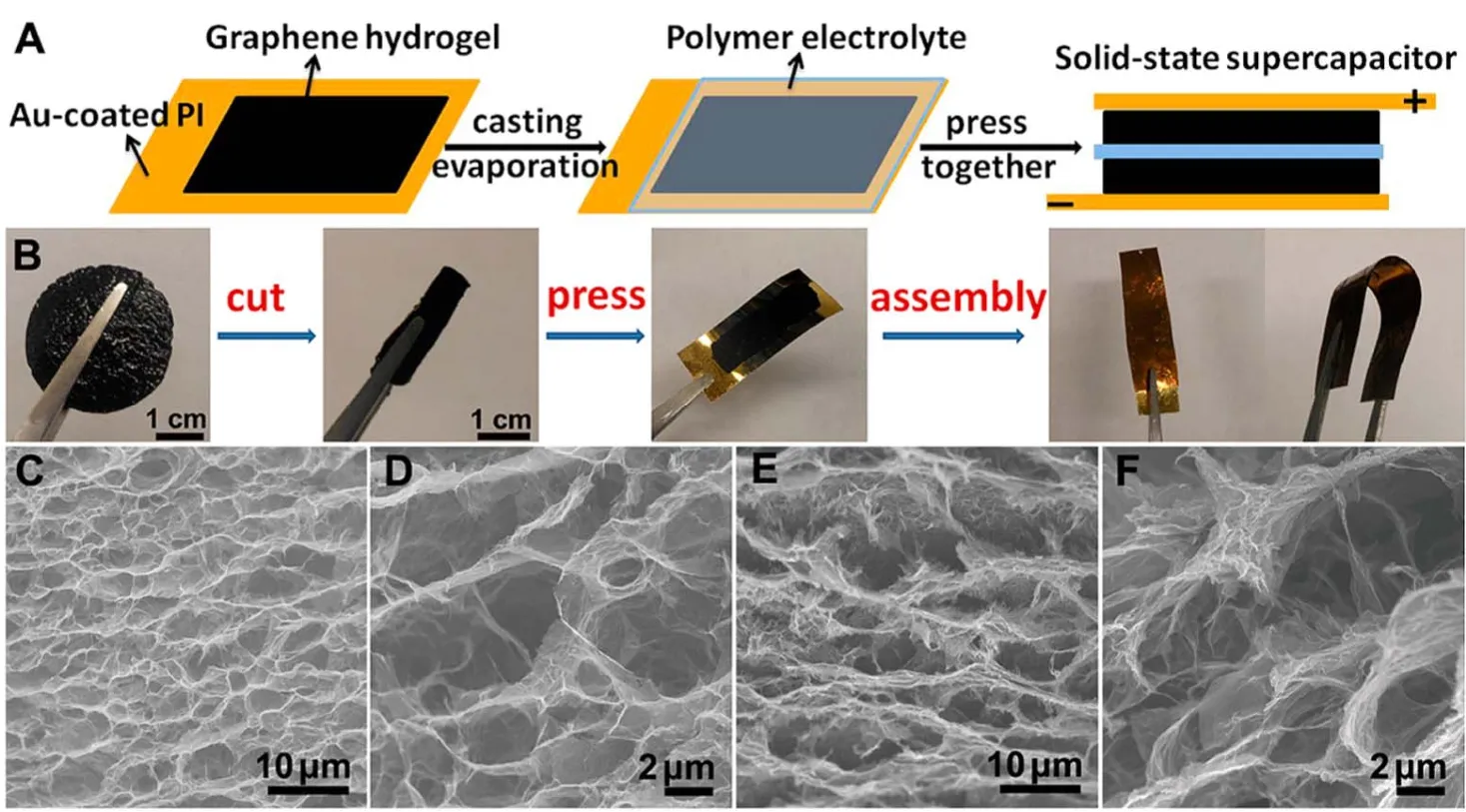
图5 (A)原理示意图;(B)基于石墨烯凝胶薄片的全固态柔性超级电容器的构建过程;(C-F)石墨烯凝胶按压前后不同放大倍数下的SEM图57Fig. 5 (A) Schematic diagram and (B) photographs of the fabrication process of fl exible solid-state supercapacitors based on graphene hydrogel fi lms. (C) Low-and (D) high-magni fi cation SEM images of the interior microstructure of the graphene hydrogel before pressing. (E) Low- and (F) high-magni fi cation SEM images of the interior microstructure of the graphene hydrogel fi lm after pressing 57.
3 二维电极材料在超级电容器中的应用
早期的理论和实验表明,二维结构的晶体材料常温常压下处于热力学不稳定态,其自身会迅速分解,Mermin-Wagner理论也指出晶体表面的起伏会破坏二维晶体的长程有序结构49。2004年曼彻斯特大学的Novoselov等50使用机械解理方法从高定向热解石墨中剥离出单片石墨烯碳层,这一历史性发现,无疑开启了人们对二维材料的认识窗口。
石墨烯材料较大的横向尺寸和原子级厚度赋予超薄石墨烯高的比表面积和活性位点,有研究表明,石墨烯的理论比表面积高达2630 m2·g-1,其作为超级电容器的理论比容量达到21 μF·cm-2或550 F·g-151。可穿戴电子产品是一个具有巨大潜力的新兴产业,有可能彻底改变人类生活互动的方式。因此,开发可穿戴能源设备从而为可穿戴电子设备提供动力越来越重要,此外,微小电子器件的兴起也急需微小型能源装置的构造,这些能量存储设备在过去几年中经历了快速增长,而且在未来大有应用前途。这些促使研究者对具有类似层状结构和多种优异性能的二维材料的大量关注,二维材料在微观上,原子间化学键等其他强键作用的作用力沿着二维的方向延伸,分子间的作用力和其他弱键作用在其他三维方向上,从而形成在二维方向无限扩展同时在第三个维度生长受限的材料;宏观上,二维材料,特别是二维类石墨烯材料,在水平面上具有无限拓展空间同时垂直方向上仅具有纳米级别的厚度,仅有一层或者几层原子层。层层堆叠的二维材料与三维多孔材料一样具有宏观上的高性能和高表面积,同时相比于三维材料具有极佳的柔韧性10,52-55。所以,它可以满足超级电容器柔性化的需要。此外,超级电容轻薄化也被大量研究,实现超级电容器的平面化是超级电容器轻薄化的另一发展方向。平面超级电容器在具有普通电化学电容器的高充放电速率、高循环性等特性的同时,由于其二维空间构型的设计,离子在电解质中沿着平面传输,因此它可以压缩电极材料的空间,在活性材料很少的情况下达到很高的性能,电极材料厚度最薄仅10 nm55,56;更为重要的是,将二维材料作为电极材料的平面超级电容器拥有良好的机械性能,可以任意地卷曲、折叠,而且不会造成电极材料结构的坍塌和超级电容器明显的性能损失,更有前景的是,有望实现超级电容器透明化。因此,它将成为下一代超级电容器的一个重要发展方向。
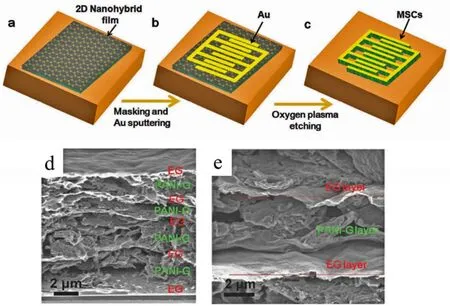
图6 微型超级电容器(MSCs)的构造示意图以及复合物的层片交错SEM图58Fig. 6 Design and fabrication of alternating stacked graphene-conducting polymer hybrid fi lm for in-plane MSCs 58.
二维材料具有前述的诸多优异特点,已广泛应用于能源转换、柔性电子器件等领域,例如层状金属氧化物、层状双金属氢氧化物(LDH)、过渡金属二硫族化合物(TMDCs)、过渡金属碳/氮化物(MXenes)、金属有机框架(MOF)等10。其中石墨烯作为二维材料的典型代表,在超级电容器等储能器件已有广泛应用,在具有柔性化、微型化等新兴特点的储能器件中应用尤为突出。然而,由于石墨烯片层间强的范德华力,实际应用中石墨烯基材料表面积未被充分利用。目前的解决途径是制备多孔石墨烯结构或符合其他物质以充当垫片的作用来防止石墨烯片的堆聚。例如Xu等57报道了一种使用H2SO4聚乙烯醇(PVA)凝胶作为电解质制备基于石墨烯水凝胶薄膜的新型柔性固态超级电容器,如图5所示。该集成器件表现出很高比电容(电流密度为1 A·g-1时,比电容为186 F·g-1)和优异的倍率性能(电流密度增至20 A·g-1,有70%的电容保持率),此外,该器件在正常和高度弯曲的条件下进行测试时显示出很小的电容变化,并且在10 A·g-1的电流密度下,经10000次充/放电循环后仅有8.4%的电容衰减。
Wu等58则提供了一种基于石墨烯材料来构建微型超级电容器(MSC)的通用方案,用于构建交替堆叠的微米厚度石墨烯导电聚合物紧凑型混合薄膜并适用于高能MSCs,如图6所示。该MSC具有里程碑似的高面积和体积比电容,特别是在各种弯曲状态下表现出优异的机械柔韧性和电化学稳定性,如图7所示。
Kim等59用不同重量百分比的PANI (88%,76%和60%)制备了PANI/RGO薄膜,并且根据基材的尺寸(8英寸和13英寸)制备两种不同的尺寸,制备流程如图8所示。值得注意的是,PANI/RGO薄膜(906 S·cm-1)的电导率大于单独的PANI (580 S·cm-1)和RGO (46.5 S·cm-1)组分。该复合薄膜还显示出作为可缩放和柔性电极材料的各种优点(如尺寸可控和高灵活性),如图9所示。电化学测试表明,复合薄膜具有431 F·g-1的高电容,并具有增强的循环稳定性。
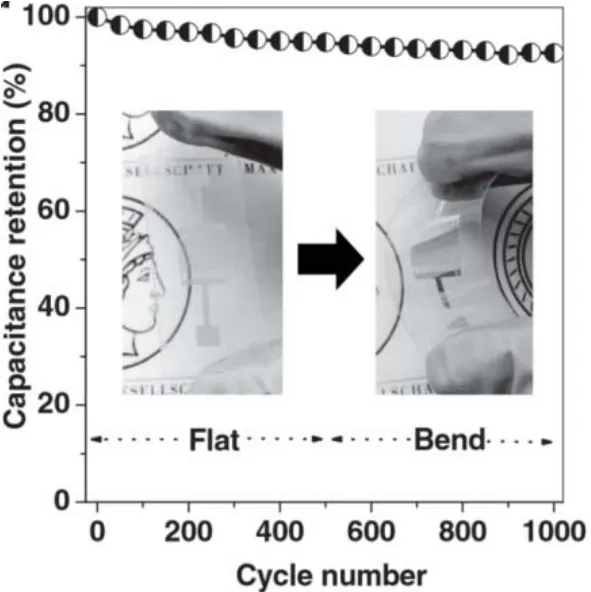
图7 P2G3-MSCs-C不同状态下循环稳定性测试58Fig. 7 Cycling stability of P2G3-MSCs-C 58.
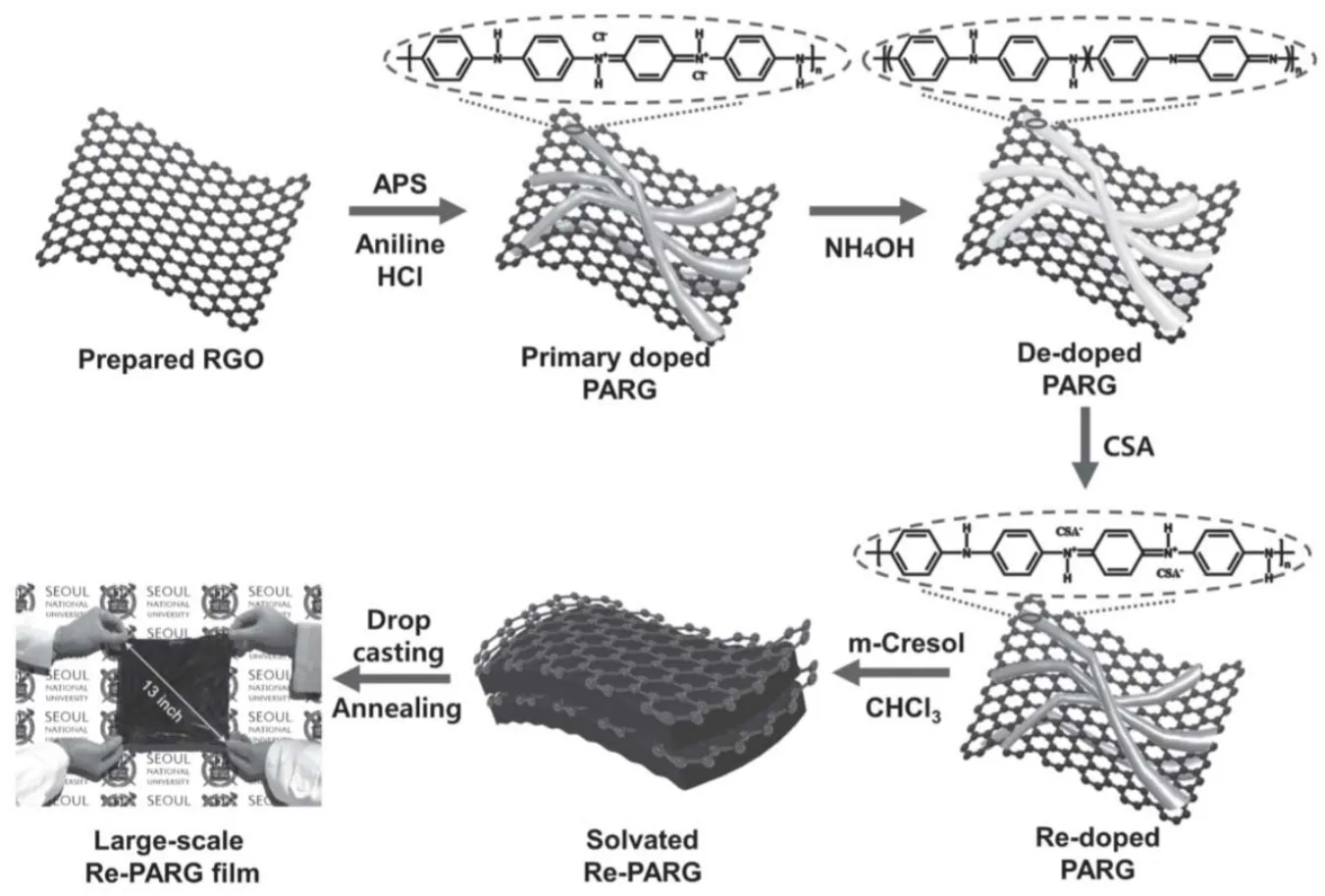
图8 Re-PARG复合薄膜制备流程59Fig. 8 Schematic illustration of the sequential steps for fabricating large-scale Re-PARG fi lm 59.
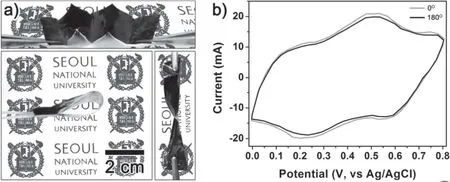
图9 (a)柔性Re-PARG薄片的数码照片。顶部的图像展示了该薄膜的折叠特性,底部图像显示了薄膜的高柔韧性(弯曲和扭曲状态下);(b)不同弯曲角度下测试的CV曲线59Fig. 9 (a) Digital photographs of fl exible Re-PARG fi lm. The top image exhibits the folding characteristics of the fi lm.The bottom images illustrate the high fl exibility (bending and twisting) of the fi lm; (b) CV curves of Re-PARG fi lm electrodes with two different bending angles of 0° and 180° at a scan rate of 5 mV·s-1 59.
此外,过渡金属氧化物或氢氧化物也在超级电容器领域广泛研究。例如,Co(OH)2由于其本身可以被剥离成层状的纳米片等结构,Xia等60以泡沫镍为模板,合成了以Co(OH)2纳米片为微观结构单元的多孔电极材料,所得电极的容量达到了1920 F·g-1(40 A·g-1)。Wang等61制备出单层β-Co(OH)2,并将其与GO复合形成电极,如图10和图11所示,该电极比容量为2080 F·g-1(电流密度为1A·g-1),且具有优秀的循环性能。
探索并制备具有所需组成、尺寸、厚度、晶相、缺陷和表面特性的超薄2D纳米材料对于进一步研究其物理,化学,电子和光学性质从而在超级电容器领域发挥其更大的潜能极其重要,尽管目前有关研究层出不穷,但要达到理想高性能的超级电容器电极材料,该方向仍有很长的一段路要走。
4 二氧化锰与二维材料的复合
二氧化锰本身是一种半导体材料,因具有廉价易得、环境友好且电化学活性高等优点一直是研究热点,但是二氧化锰的导电性较差、可逆性差的特点,极大地限制了二氧化锰用作超级电容器的电极材料时进行大电流充放电,功率密度也受到影响。因此,通过合理的制备工艺对MnO2进行修饰,改变其半导体特性或制备MnO2复合材料,是当下提升二氧化锰基超级电容器性能的最为可行的途径。二维材料的独特结构赋予了其很多优异的性能,如机械稳定性好、强度高、柔韧性、透明、化学稳定性好等。构筑二维材料—二氧化锰纳米复合材料,复合材料具有单一材料各自的优异性能,更重要的是还会产生异质协同效应,这将很大程度上改善二氧化锰基超级电容器用电极材料的电化学性能。在这节内容中,我们总结了纳米二氧化锰与各类二维材料的复合研究进展。
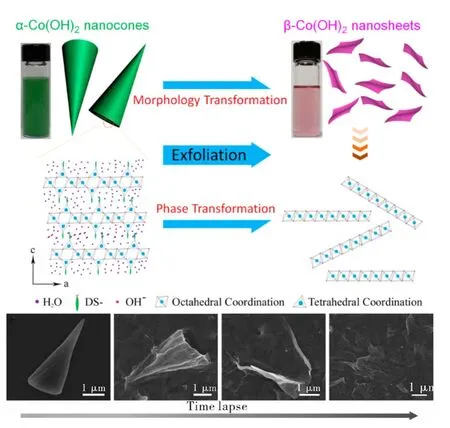
图10 单层β-Co(OH)2纳米片的制备过程示意图以及各个阶段的SEM照片60Fig. 10 Schematic illustration of the process for producing single-layer β-Co(OH)2 nanosheets and SEM images of products after each step 60.
4.1 石墨烯/二氧化锰
由上文叙述,石墨烯与二氧化锰均很适合成为电极材料,但是石墨烯的容量限制了石墨烯的应用,而二氧化锰材料本身虽然有很高的理论容量,但是由于其循环性能差,导电性差,导致了二氧化锰实际容量远远无法达到理论容量。二维石墨烯的高导电率和比表面积,再与纳米MnO2比电容量高特点结合,两者取长补短,可以有效的改善石墨烯材料的容量不足,以及二氧化锰导电性较差这些问题,从而使得石墨烯/二氧化锰复合材料成为一类具有吸引力的超级电容器材料。受到成本等条件所限,完美的石墨烯晶体并不适合用作超级电容器电极,现有的研究除少数理论研究以外,多数立足于以还原氧化石墨烯(rGO)为代表的易量产的类石墨烯材料。石墨烯/二氧化锰复合材料的合成方法主要有:溶剂热(水热)法、电化学沉积法、氧化还原法、自组装法等。
4.1.1 溶剂热(水热)法
溶剂热(水热)法是以高压反应釜作为反应器,以溶剂 (水)作为反应介质,在高温高压环境下利用金属盐类的水解结晶所进行的合成过程。
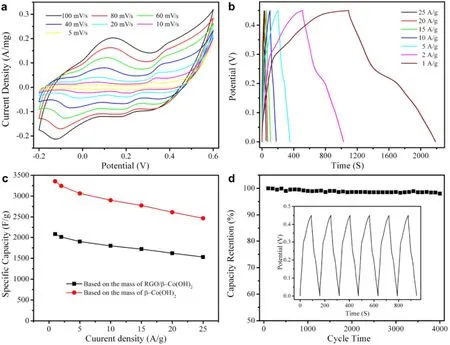
图11 β-Co(OH)2电极的不同扫描速率下的CV曲线(a)、不同电流密度下的充放电曲线(b)、倍率性能(c)及在10 A·g-1电流密度下测试的循环性能(d) 60Fig. 11 Electrochemical properties of RGO/β-Co(OH)2 NS composite-based electrode. (a) CV curves at different scan rates, (b) charge-discharge curves, (c) speci fi c capacitance at different current densities, and (d) speci fi c capacitance vs cycle number of the composite at a current density of 10 A·g-1 (inset of panel disgalvano static charge-discharge curves with time) 60.
Li等62先以Mn单质作为GO的还原剂得到片状石墨烯,然后再与KMnO4混合,水热制备颗粒状MnO2/石墨烯复合物,并对其组成的三电极体系进行电化学测试,结果表明,该复合物的最大比电容值为325 F·g-1。2014年,Dai等63首次以石墨烯和KMnO4为原料,在160 °C的酸性环境中水热处理12 h,成功制备了纤维状的MnO2/石墨烯复合物(图12),并考察了MnO2和石墨烯的不同含量对复合物电化学性能的影响。该复合物中一维纤维状的MnO2不仅能够防止二维片状石墨烯的团聚,也优化了复合物的电化学性质。结果显示,石墨烯含量为90%的复合物电化学性能最优(在三电极测试体系中,复合物最大比电容值为 170 F·g-1,充放电循环1000次后的电容保持率为97.1%)。
二维片状石墨烯易团聚问题的解决除了通过上述复合途径外,另一个主流的方法就是设计合成三维石墨烯。比如Le等64创造性地采用基于硅藻土生物模板的化学气相沉积法合成了三维多孔石墨烯(3DG),这种方法合成的3DG是由无缝互连的石墨烯片组成,厚度可控,纯度高。随后他们还对其进行了异质氮掺杂,最后在这基础上水热合成了氮掺杂三维石墨烯/MnO2复合物(N-G@MnO2),并探究了不同反应时间对电容性能的影响,如图13所示。经测试发现,水热反应3 h的多孔NG@MnO2电极电容性能最好,有411.5 F·g-1的比电容,经4000次的充放电循环后仍有88.3%的电容保持,表明其循环稳定性也好。组装双电极非对称超级电容器的结果表明,N-G@MnO2达到了1.8 V的宽电位窗口时,能量密度高达46.1 Wh·kg-1,测试结果如图14所示。
4.1.2 电沉积法

图12 纤维状的MnO2/石墨烯复合物的(a) SEM、(b) TEM和(c)放大的TEM图63Fig. 12 (a) SEM, (b) TEM and (c) high-magnification TEM image of MnO2 nanofiber/graphene composites 63.

图13 (a)硅藻土@石墨烯,(b)三维石墨烯,(c-f) 不同反应时间合成的N-G@MnO2的SEM图64Fig. 13 SEM images of (a) diatomite@graphene, (b) 3D graphene,(c-f) N-G@MnO2 synthesized with different reaction time (1, 3, 5 and 7 h) 64.
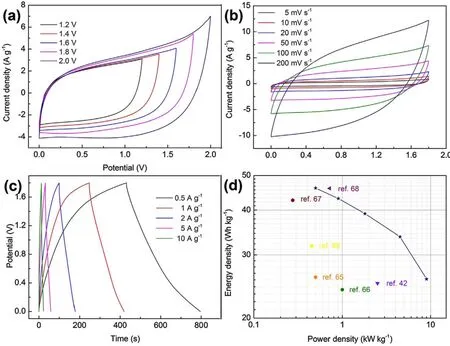
图14 N-G@MnO2//AG 非对称超级电容器的电化学性能64Fig. 14 Electrochemical properties of N-G@MnO2//AG ASC 64.
目前电沉积法主要分为电化学沉积和电泳沉积。电化学沉积法是指利用电场作用使金属氧化物从其水溶液中沉积的过程。电泳沉积是指在外加直流电源的作用下,胶体微粒在分散介质里向阴极或阳极作定向运动,从而沉积在两极上。Chan等65用电化学沉积法得到了颗粒状MnO2/石墨烯复合物,并研究了不同沉积时间对金属氧化物颗粒尺寸的影响。结果表明,沉积时间过短不利于氧化物颗粒的形成,时间过长会导致氧化物负载过多,影响复合物的稳定性。经过多次测试后确定了最佳沉积时间,并在三电极体系进行了电化学测试,测试表明生成的复合物在1 mV·s-1扫描速率下的最大比电容值可达378 F·g-1。Liu等66以GO和MnSO4为原料,采用电化学沉积法制备了花状MnO2/石墨烯复合物,在三电极体系中,该复合物在电流密度1 A·g-1时,比电容值可达到595.7 F·g-1。Amir等67着眼于通过提高电极电势窗口来提高其电容量,他们以制得的多孔还原氧化石墨烯和MnO2纳米片为原料,采用电泳沉积的方法将其层层组装到基底上。最后将所得样品高度压缩到密度为0.2到2.5 μm不等,以PVA-LiClO4凝胶作为电解液,组装成非对称超级电容器。该电容器电极电势窗口宽至0.0-1.6 V,有着高达5000 mV·s-1的超高充放电速率;更重要的是,达到高的工作电势窗后,该超级电容器显示出意外的高体积能量密度,功率密度为8.34 W·cm-3,体积能量密度高达48.8 mWh·cm-3。
也有将电化学沉积和电泳沉积两种方法相结合使用来合成此类复合物68,69,比如,Xiong等69首先结合这两种方法合成了3D GO/MnO2复合物,在氢气和氩气氛围下热还原成3D GR/MnO2。以加热600 °C热还原的GR/MnO2-600为例,采用三电极体系,以1.5 mol·L-1Li2SO4溶液为电解液,在电化学工作站进行各项电化学性能测试。CV曲线如图15,通过计算在200 mV·s-1的扫描速率下,该复合材料比电容为266.75 F·g-1,相比GO/MnO2的比电容量(125.25 F·g-1)有了大幅度的提高。电容量提升的关键因素在于石墨烯的高导电率和大比表面积为电子传输提供了快速通道,此外石墨烯在复合物中充当导电通道,同时二氧化锰作为复合物中的垫片不仅仅提供了额外的赝电容量,而且也防止了石墨烯片的堆叠。
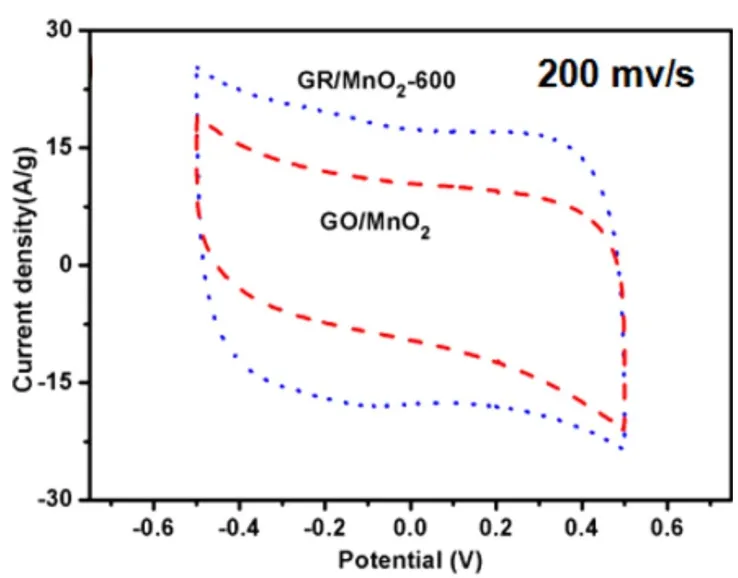
图15 200 mV·s-1的扫描速率下GR/MnO2-600和GO/MnO2的循环伏安曲线69Fig. 15 CV curves of the GR/MnO2-600 and GO/MnO2 hybrids at 200 mV·s-1 69.
4.1.3 氧化还原法(化学反应法)
在众多的氧化还原反应中,最直接的方式莫过于KMnO4与碳进行反应。如图16所示,Zhao和Zhang等70直接将所合成的aMEGO与KMnO4在室温的条件下混合搅拌,反应结束后样品经过蒸馏水反复洗涤过滤,在80 °C下干燥24 h,在400 °C锻烧3 h。将材料组装成对称的电容器,以H2SO4为电解液,比容量为256 F·g-1,经过1000次循环后比容量保留率为87.7%。Zhang等71首先采用湿法纺丝制得了中空还原氧化石墨烯(HRGO),然后向体系中滴加高锰酸钾溶液进行化学反应后,制得了MnO2/HRGO纳米复合纤维电极,并探究了MnO2的不同负载量对电容性能的影响。结果表明,加入反应的KMnO4为4.0 mmol·L-1,即MnO2(4.0)/HRGO有着更大的比电容(在1 mol·L-1Na2SO4电解液中,电流密度为1 A· g-1时,比电容为245 F·g-1)。鉴于全固态超级电容器具有重量轻、柔性、安全性高,环保等优点,更适合开发具有柔韧性和重量轻的光纤超级电容器,为此他们特意构造了柔性纤维状全固态超级电容器,测试发现,该纤维超级电容器在保持柔性的同时,电容性能也有所提高。
4.1.4 自组装法
Cheng等72用膨胀石墨为原料,在表面活性剂十二烷基苯磺酸(SDBS)的辅助下得到了带负电荷的石墨烯片层,表面活性剂的加入不仅使石墨烯表面带有负电荷,也对金属氧化物的负载起到了一定的导向作用。然后与带正电荷的片状MnO2胶体进行自组装,也成功制备了MnO2/石墨烯复合物,在三电极测试体系中最大比电容值为280 F·g-1。Feng等73以石墨烯和不同形貌的MnO2为原料,利用液相自组装法制备了MnO2/石墨烯复合物,并研究了不同形貌的MnO2对复合物性能的影响。在三电极体系中研究发现花状MnO2/石墨烯的电化学性能优于纳米线状MnO2/石墨烯(电流密度1.0 A·g-1时,两种复合物的比电容值分别为405和318 F·g-1)。
图16 复合物合成示意图70Fig. 16 The figure of Composite Synthesis 70.
制备石墨烯/二氧化锰的方法除了以上四种常用方法外,还有共沉淀法46、超声合成法74、微波辐射法75、阳极沉积76等、石墨烯/二氧化锰基超级电容器具有优良的功率和能量密度使得其应用于未来能源存储系统大有希望。然而,探索出一种简单、价廉、适用范围广的方法来构造电容器仍然是很大的挑战。除此之外,柔性和轻量化能源储存装置也越来越受到研究者们的关注,当然,同时电极要具有足够好的电化学性能是重中之重。现在研究者们也不仅仅局限于这两种材料的复合。2016年,Pan等77实现了新型的嵌有MnO2的一维聚苯胺(PANI)纳米线和石墨烯片的有效复合。PANI@MnO2/GN((PMGNs)复合材料在4 A·g-1的电流密度下,循环1000次后,仍然有695 F·g-1的可逆比电容。Huang等78则制备了Cu/RGO/MnO2复合纤维电极,并以此创造性地构造了线缆型柔性全固态超级电容器,如图17所示。电化学测试结果表明,在0.1 mA·cm-2电流密度下,该纤维超级电容器的比电容高达140 mF·cm-2;以大角度120°作弯曲500次,还有97%的比电容,此外,循环5000圈后,仍有初始电容值的88%,说明循环稳定性也较好。
4.2 TMOs/TMHs@MnO2
过渡金属氧化物(TMOs)/氢氧化物(TMHs)是赝电容电容器电极的热门材料。由于赝电容器存储电荷的机理相比电容器而言更接近电池,这样机理上的差别使得此类超级电容器有着与双电层电容器不同的性能限制因素。一方面,受到电子传导和离子扩散等过程的速度限制,电极材料的表面以下一定深度的原子参与氧化还原反应的速度很慢,甚至无法参与反应,这严重限制了材料的倍率性能和比容量。另一方面,由于在充放电过程中电极材料经历的反复相变对其结构有着不可逆的破坏作用,电极的循环寿命也无法与依靠静电力存储电荷的EDLC相比。这二者是现今限制赝电容电容器的性能进一步优化和实用化的瓶颈,也是困扰研究者们已久的难题,而这类材料的二维形式的出现和使用似乎在解决以上问题上开了一个窗口。
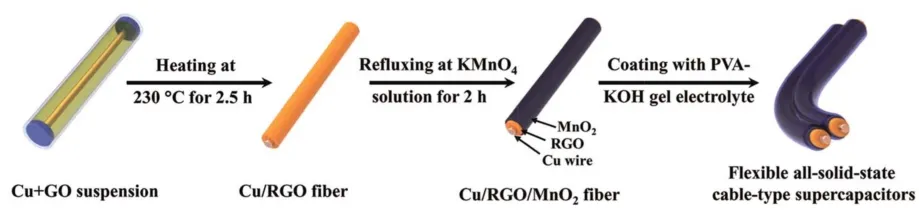
图17 基于Cu/RGO/MnO2纤维电极的全固态电缆型超级电容器的原理图78Fig. 17 Schematic preparation representation of the all-solid-state cable-type supercapacitor based on the Cu/RGO/MnO2 fi ber electrode 78.
由于MnO2自身是一种赝电容材料,但其差的导电性、尺寸稳定性导致其低的比电容,限制了其进一步的实际应用。将它与其他二维过渡金属氧化物/氢氧化物复合,再加上MnO2自身也可被合成为二维片状材料,这将大幅度提高电容性能。通过可控的制备来得到倍受研究者们青睐的核壳结构被广泛研究,并且此种结构朝着更加新颖且优异的方向发展79。例如,现有大量研究关于其他过渡金属氧化物与片状MnO2复合以构建优异的核壳结构80-82。也有将不同晶型的MnO2彼此复合83,84,比如,Ma等84采用简便实用的溶液相技术制备了异质α-MnO2纳米线@超薄δ-MnO2纳米片核壳纳米结构(图18),在20 A·g-1的电流密度下,该异质核壳纳米结构的比电容达到了153.8 F·g-1,循环10000圈后,仅有1.9%的电容损失,电化学性能测试如图19。如此优良多的电化学性能归功于复合后的结构优势以及复合产生的协同效应:一维α-MnO2纳米线核心作为稳定的结构骨架、二维δ-MnO2纳米片壳体提供大表面和更具反应性的活性位点。
值得注意的是,TMOs一般不具有层状结构,因此其二维结构较难直接得到,目前很多关于此类材料大多是纳米颗粒或纳米线等0D和1D材料与MnO2的复合82,85-87,制备理想的核壳结构或阵列。还有研究者提出的替代方案是合成纳米尺度的TMOs并将其附着于石墨烯等二维材料的表面。这一方案一方面通过将材料的厚度控制在纳米尺寸来解决高电阻和体相原子利用效率等问题,另一方面也降低了TMOs等在电极材料中的占比,从而减轻电极质量和降低材料成本。
二元金属氧化物是在一种金属氧化物结构中添加其他组分,使氧化还原电对可同时进行多电子反应,赋予其高的电化学活性,同时,各组分利用协同效应优势互补,可获得兼有高容量、优异的循环稳定性与倍率性能的复合材料。所以除了研究MnO2与一元金属氧化物复合外,目前对片状二元金属氧化物/二氧化锰复合的研究也多了起来。有研究表明,纳米结构的二元过渡金属氧化物(1D NiCo2O4纳米线88,2D CuCo2O4纳米片89)有着优异的导电性、电化学活性和大比表面积。二氧化锰对此类二元金属氧化物有很强的粘合能力,所以此类二元金属氧化物是生长MnO2的良好基底物。Gao等90通过恰当地控制水热反应条件成功制备了在泡沫镍上生长的FeCo2O4@MnO2核鞘纳米架构(图20),超薄纳米片状FeCo2O4的平均厚度在10 nm左右,复合物的厚度可以通过改变水热反应时间进行调节。电化学测试表明,在复合物最优厚度400 nm,电流密度为2 mA·cm-2时,复合物电极面积比电容为3.077 F·cm-2。以该复合材料为正极,活性炭为负极构造了FeCo2O4@MnO2//AC非对称超级电容器。电容器的功率密度为0.061 mW·cm-2的同时,能量密度达到了28.6 mWh·cm-2,而且在经历5000圈的循环后,电容保持率为99.1%。Chu等91基于化学溶液和煅烧路线以MnOOH@NiMo为前驱体制备了以MnO2纳米线为核,NiO/NiMoO4纳米片为壳的三组分异质核壳结构(图21),可通过控制反应时间从而达到对整个结构的控制。所得电极材料的电化学性能测试如图22。
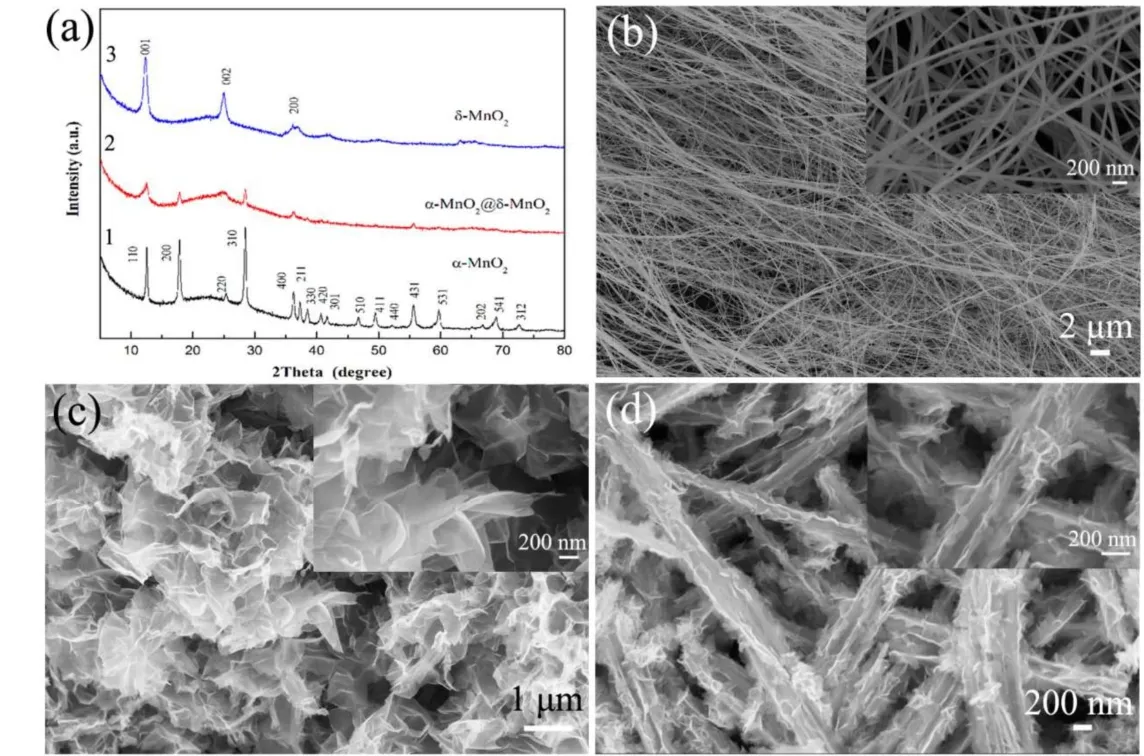
图18 XRD图(a)以及超长α-MnO2纳米线(b)和δ-MnO2纳米片(c)和α-MnO2纳米线@超薄核壳纳米线(d)SEM图84.Fig. 18 XRD patterns (a) and SEM images of the ultralong α-MnO2 nanowires (b), δ-MnO2 nanosheets (c) and α-MnO2 nanowires@ultrathin δ-MnO2 nanosheets core-shell nanowires (d) 84.
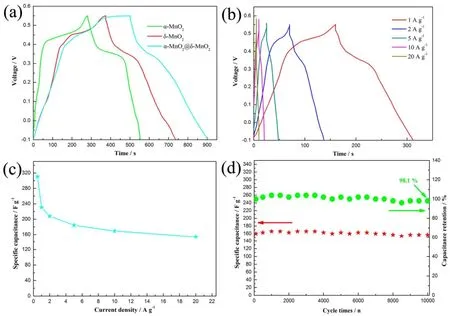
图19 (a)超长α-MnO2纳米线,异质α-MnO2纳米线@超薄δ-MnO2纳米片核壳纳米线和δ-MnO2纳米片的恒电流充放电曲线; 异质α-MnO2纳米线@超薄δ-MnO2纳米片核-壳纳米结构在不同电流密度下的恒电流充放电曲线(b)和比电容(c); 异质α-MnO2纳米线@超薄δ-MnO2纳米片核壳纳米结构在20 A·g-1的长期循环性能(d) 84Fig. 19 (a) Galvanostatic charge-discharge curves of the ultralong α-MnO2 nanowires, the hierarchical α-MnO2 nanowires@ultrathin δ-MnO2 nanosheets core-shell nanowires and δ-MnO2 nanosheets. (b) Galvanostatic charge-discharge curves and (c) specific capacitance of the hierarchical α-MnO2 nanowires@ultrathin δ-MnO2 nanosheets core-shell nanostructure at different current densities. (d) Long-term cycle performance of the hierarchical α-MnO2 nanowires@ultrathin δ-MnO2 nanosheets core-shell nanostructure at 20 A·g-1 84.

图20 泡沫镍上的FeCo2O4@MnO2典型核壳纳米结构SEM图90Fig. 20 SEM images of typical FeCo2O4@MnO2 CSN on Ni foam 90.
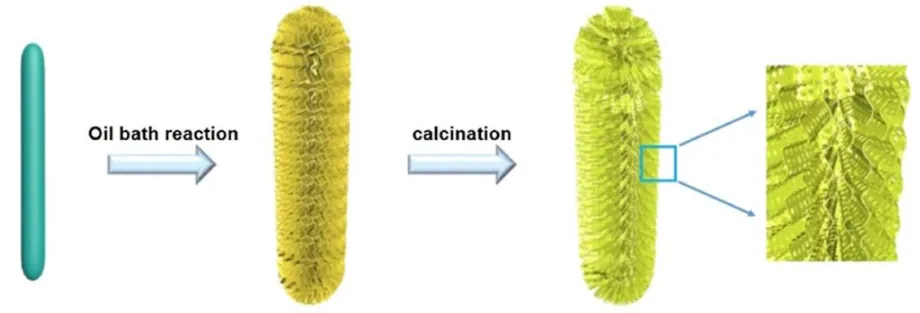
图21 MnO2@NiO/NiMoO4 异质多孔复合结构合成工艺示意图91Fig. 21 Schematic illustration of the synthetic process of MnO2@NiO/ NiMoO4 HPCSs 91.
图22B中在不同扫描速度下,CV曲线形状几乎没有发生变化,表明该复合电极极好的电化学可逆性。采用该复合材料所构造的非对称超级电容器,Ragone图(图23)反映了尽管能量密度从26.5 Wh·kg-1下降到了17.2 Wh·kg-1,但同时功率密度从401 W·kg-1增加到了4010 W·kg-1。
Co(OH)2、Ni(OH)2等的晶体结构具有层状排列的特征,其本身常常可以被剥离成层。关于片层状Ni(OH)2与MnO2的复合研究也较丰富92-96。质量和体积能量密度的提高往往受到正极材料大负载下,有效利用率低和负极材料劣等的电容行为的限制。Shen等94为了克服这道难关,采用简易的水热法设计并制备了三维核壳结构的Ni(OH)2/MnO2@CNT纳米复合材料。在高负载密度(6.52 mg·cm-2)之下,电流密度为1 A·g-1时,所得复合电极的比电容为 2648 F·g-1。他们还制备了活性聚苯胺衍生碳(activated polyaniline-derived carbon,APDC),并与之前所得复合物一起共同构造了Ni(OH)2/MnO2@CNT//APDC非对称超级电容器,其质量能量密度和体积能量密度分别为126.4 Wh·kg-1、10.9 mWh·cm-3。Xi等95则借助于由PVDF-乙炔黑(AB)种子层组成的导电粘合剂通过一步可扩展的水热路线合成了以泡沫镍为基底的三维脊柱状MnO2-Ni(OH)2纳米复合材料(图24),该纳米结构具有多孔、互连的活性纳米片等特征,能有效减少二氧化锰基电极材料由于体积膨胀而诱发的材料粉碎现象。
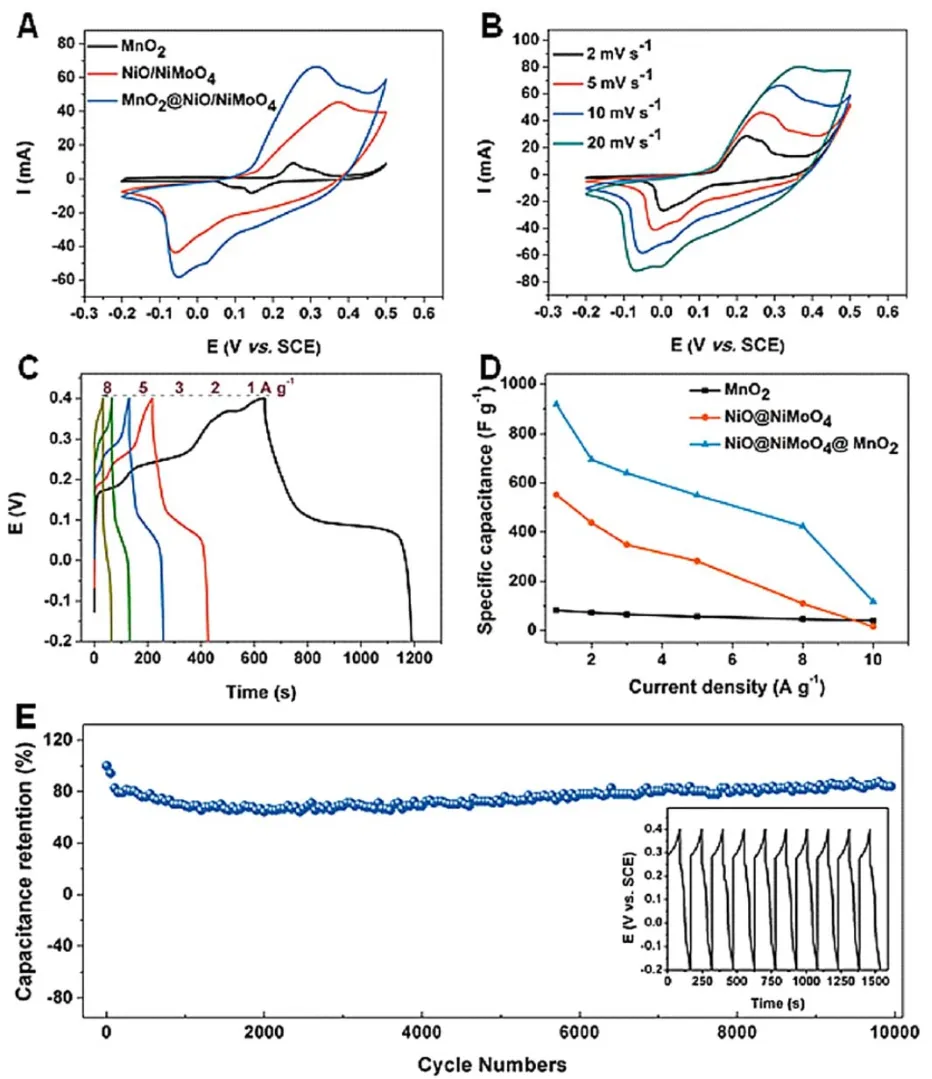
图22 室温下在5 mol·L-1KOH水溶液的电化学表征91Fig. 22 Electrochemical characterizations in 5 mol·L-1 aqueous KOH at room temperature91(A) CV curves of different electrodes at a scan rate of 10 mV·s-1.(B) CV curves at different scan rates and (C) charge-discharge curves at different current densities for the MnO2@NiO/NiMoO4 electrode.(D) The specific capacitance of different electrodes at different current densities. (E) Cycling stability and CE of the MnO2@NiO/NiMoO4 electrode at a current density of 3 A·g-1; inset: the galvanostatic charge-discharge curve for the first ten cycles.
在响应当前环保低消耗等理念的背景下,Wang等96采用细菌纤维素来制备碳气凝胶,随后通过电化学沉积和氧化还原将Ni/MnO2/Ni(OH)2复合物嵌于其上。复合电极的能量密度和功率密度分别为9.4 Wh·kg-1、4 kW·kg-1。此外,他们基于此复合材料构造了柔性全固态超级电容器,并试探性地用于了一LED灯的能量源,充电到3 V后,接上LED灯大约能亮2 min。这充分显示了该类新型复合材料未来应用于超级电容器的潜能。
4.3 LDH@MnO2
LDH中含有过渡金属元素,其作为赝电容材料具有很大优势。首先,它们具有很高的可逆氧化还原活性;其次,内部灵活的离子交换对电解液中离子的深度扩散有很强的促进作用,也便于充分利用材料的活性位点;更为重要的是,高取向的2D层状结构有利于活性材料与集流体间的电子传输。MnO2同样作为一类非常理想的赝电容材料,但是相对低的导电率和循环周期是其严重的发展瓶颈。因此,从理论上设计研究两者的异质复合材料具有重要意义。比如层片状LDH不仅是一种赝电容电容材料,而且由于其层状结构为MnO2提供了支撑。
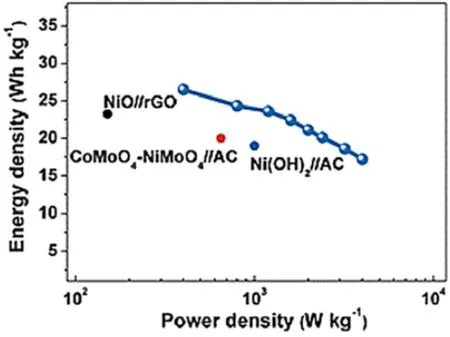
图23 与CoMoO4/NiMoO4//AC,Ni(OH)2//AC相比,MnO2@NiO/NiMoO4//AC非对称超级电容器和NiO//rGO装置的将功率密度与能量密度联系起来的Ragone图91Fig. 23 The Ragone plot that relates power density to energy density of the MnO2@NiO/NiMoO4//AC ASC compared with CoMoO4/NiMoO4//AC ,Ni(OH)2//AC, and NiO//rGO 91.
Diao等97联合改进了的共沉淀法和简易的氧化还原反应等合成了CoAl-LDH/MnO2纳米复合物,经电化学测试发现该纳米复合电极有着比电容高、倍率性能好、长期循环稳定性好等诸多优点,如在1 A·g-1的电流密度下,比电容高达1088 F·g-1。Gu等98制备了CoAl-LDH/rGO/MnO2三元纳米复合材料,与不含MnO2的CoAl-LDH/rGO相比有更高的比电容。然而,这种CoAl-LDH/rGO/MnO2纳米复合物制备方法复杂,而且不得不用粘结剂将其涂覆在泡沫镍上以便进一步的电化学测量。Wang等99则作了进一步的发展研究,他们采用一步电化学沉积的方法直接在泡沫镍上垂直生长MnO2/NiAl-LDH复合物。所制得的复合物呈现出多孔花状纳米结构(图25),用作超级电容器无粘结剂电极材料在1 A·g-1的电流密度下,有着1554 F·g-1的比电容,远远高于单独的MnO2(439 F·g-1)和NiAl-LDHs (742 F·g-1)。这得益于二者复合产生的协同效应,包括MnO2均匀分散于层状NiAl-LDHs之间以及二者紧密接触促使电荷转移速率的提高。
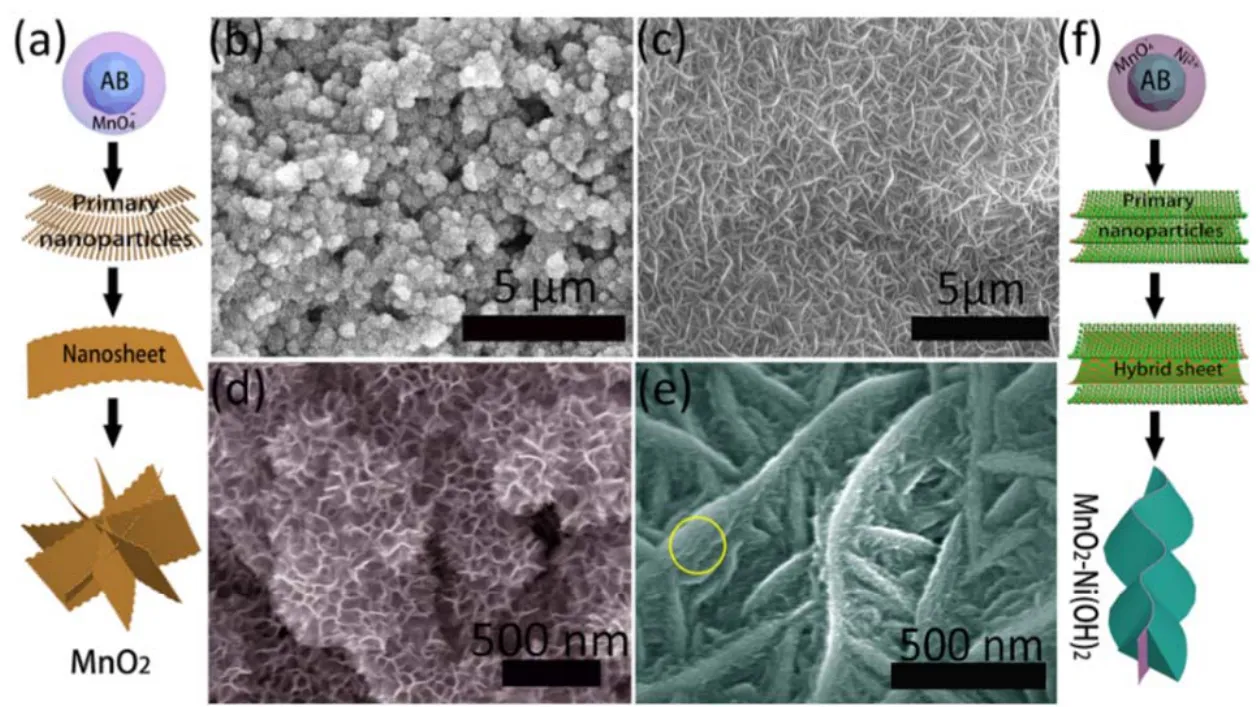
图24 MnO2 (a)和MnO2-Ni(OH)2 (f)的合成示意图(分别在M-NF/AB和MN-NF/AB电极中);M-NF/AB (b,d)和MN-NF/AB (c,e)在不同放大倍数下的SEM图95Fig. 24 Schematic diagram illustrating of the fabrication process of MnO2 (a) and MnO2-Ni(OH)2 (f) in the M-NF/AB and MN-NF/AB electrodes, respectively; the SEM images of the M-NF/AB (b and d) and MN-NF/AB (c and f) with different magnifications, respectively 95.

图25 (a)不同样品的泡沫镍光学图形(c)泡沫镍上的MnO2@NiAl-LDH复合物的SEM图99Fig. 25 (a) Optical graphics of Ni foam with different samples(c) SEM images of the MnO2@NiAl-LDH composites grown on Ni foam 99.
上述复合材料都是在传统三电极体系下用作电极材料,当它们用于对称超级电容器时,工作电压相当低,扩展工作电压的另一种方法是设计不对称超级电容器。例如,Zheng等100通过简易的水热法以及温和的氧化还原负载MnO2的方式分别制备了NiAl-LDH/MnO2和NiFe-LDH/MnO2纳米复合物(图26),并用于构建非对称超级电容器。结果表明NiAl-LDH/MnO2-6//AC非对称超级电容器在1 A·g-1的电流密度下,比电容为87.6 F·g-1,且有着30.4 Wh·kg-1的高能量密度,以及好的循环性能(10A·g-1电流密度下循环10000圈,有90.1%的电容保持),如图27所示。NiFe-LDH/MnO2-16//AC装置性能也较好,在1 A·g-1的电流密度下,比电容为81.7 F·g-1,能量密度为27.3 Wh·kg-1,在10 A·g-1电流密度下循环10000圈后,有80.5%的电容保持率。
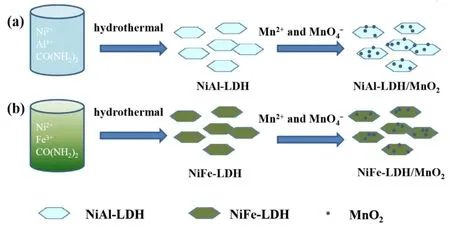
图26 NiAl-LDH/MnO2和NiFe-LDH/MnO2复合材料制备工艺示意图100Fig. 26 Schematic illustration of the fabrication process of NiAl-LDH/MnO2 and NiFe-LDH/MnO2 composites 100.
自组装法是片层状材料复合常用的方法之一,Quan等101通过剥离处理获得的NiMn-LDH和MnO2纳米片的重新堆叠制备NiMn-LDH/MnO2纳米片复合物(图28)。与原始各组分相比,无论是单组份还是简单的混合物,它都具有改进了的表面积和孔径的准无定形结构。这点可从其BET吸附方式的变化看出,如图29所示。这种新型复合材料用作碱性和中性含水电解质中的电极材料,电化学测试结果证明了其良好的协同效应,复合物有着更可观的能量密度(16 Wh·kg-1)和功率密度(15 kW·kg-1),尤其是很好的循环稳定性,经5000次循环后,电容保持率为87%。如图30所示。同样构建了非对称超级电容器,但该复合物制备方法没有上面提到的水热合成后再沉积方法简便。
4.4 TMDCs@MnO2
TMDCs 的层状结构有利于锂离子在电极中快速扩散,同时少层 TMDCs因为堆积结构非常松散,在嵌锂前后可以极大地适应结构变化,体积膨胀率低,被认为是理想的LIBs负极材料,被广泛应用于锂离子电池中。目前应用于超级电容器中较多的有MoS2、VS2。
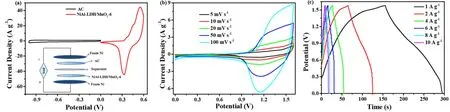
图27 (a)活性炭(AC)和NiAl-LDH/MnO2-6的循环伏安曲线,插图显示了其工作原理。(b) NiAl-LDH/MnO2-6//AC非对称超级电容器在不同扫描速度下的循环伏安曲线。(c) NiAl-LDH/MnO2-6//AC非对称超级电容器在1.58 V电压范围内的不同电流密度下的充放电曲线100Fig. 27 (a) CV curves of AC and NiAl-LDH/MnO2-6 at 10 mV·s-1, and the inset shows the schematic of the NiAl-LDH/MnO2-6//AC ASC. (b) CV curves of NiAl-LDH/MnO2-6//AC ASC at different scan rates.(c) GCD curves of NiAl-LDH/MnO2-6//AC ASC at different current densities within a voltage of 1.58 V 100.
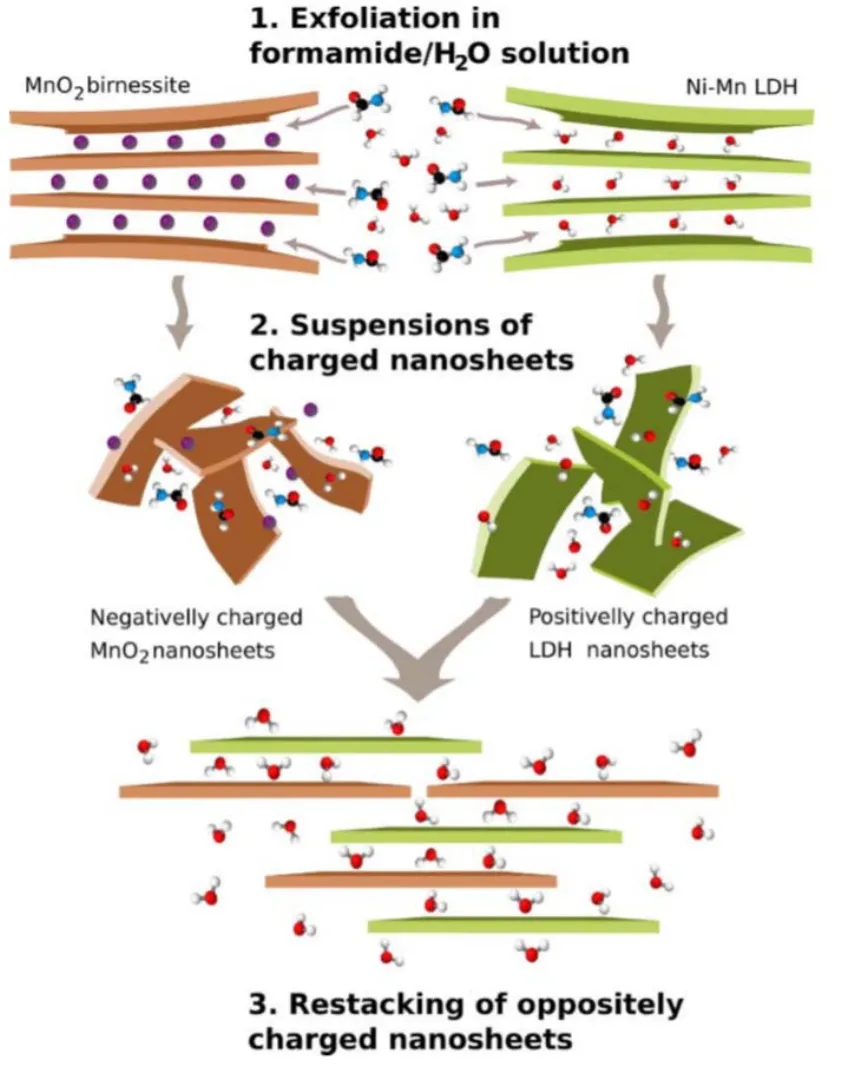
图28 制备NiMn-LDH/MnO2复合材料的一般方案,该复合材料是通过在甲酰胺/水中剥离NiMn-LDH和MnO2得到的带相反电荷的纳米片而得到的101Fig. 28 General scheme for the preparation of the NiMn-LDH/MnO2 composite obtained by restacking of oppositely charged nanosheets obtained by exfoliation of NiMn- LDH and MnO2 in formamide/water solutions 101.
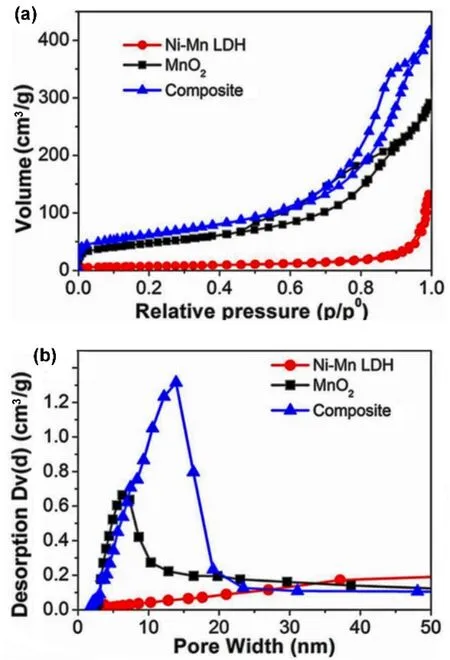
图29 样品的氮气吸脱附等温线(a)和孔径分布图(b) 101Fig. 29 Nitrogen adsorption-desorption isotherms (a) and pore size distribution (b) of the samples 101.
MoS2纳米材料具有巨大的比表面积和层间空间,并且Mo原子在氧化还原过程中有多种价态,因此,以MoS2作为电极材料兼具双电层和法拉第赝电容器的特点102,103。另有研究表明,MoS2作为电极材料时,比氧化物具有更快的电子传输能力104,比石墨烯有更高的理论比电容,展现出优异的性能。Liao等105先水热合成MnO2纳米线,然后采用电化学沉积方法制备了MoS2纳米片/MnO2纳米线异质结构复合材料,拉曼光谱显示MoS2/MnO2接触界面上无新的化学键形成,表明在线状MnO2上垂直堆积的层状MoS2过程是物理性的。他们还以此构造电极,探究其电化学性能,测试结果显示用MoS2代替金属集流体与MnO2复合接触后大约提高了一倍的电容量。该复合材料充分体现了二维异质结构作为电极材料所具有的优越性。Yang等106也注意到了MoS2材料比金属氧化物更高的本征离子导电率,还有比石墨更高的理论比电容,但单一的MoS2材料用来构造电极的研究却很少。他们探究了MnO2/MoS2复合物的微结构和电化学性能,如图31所示。在一开始的扫描速度下,CV曲线显示出很基本的矩形状,表明主要是双电层电容,随着扫描速率增加到50 mV·s-1,曲线有略微的变形,说明此时MnO2贡献了部分赝电容。恒流充放电测试显示随着电流密度的增加,电容量有相应的降低,但总体来看,MnO2/MoS2复合物有着相当好的倍率性能。
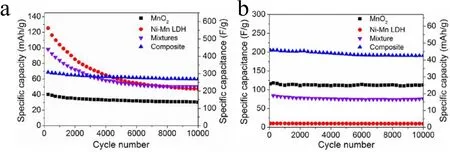
图30 所得样品整个系列的在10 A·g-1电流密度下容量保持率和循环稳定性101Fig. 30 Capacity retention and cycling stability at 10 A·g-1 of the whole series of prepared samples 101.
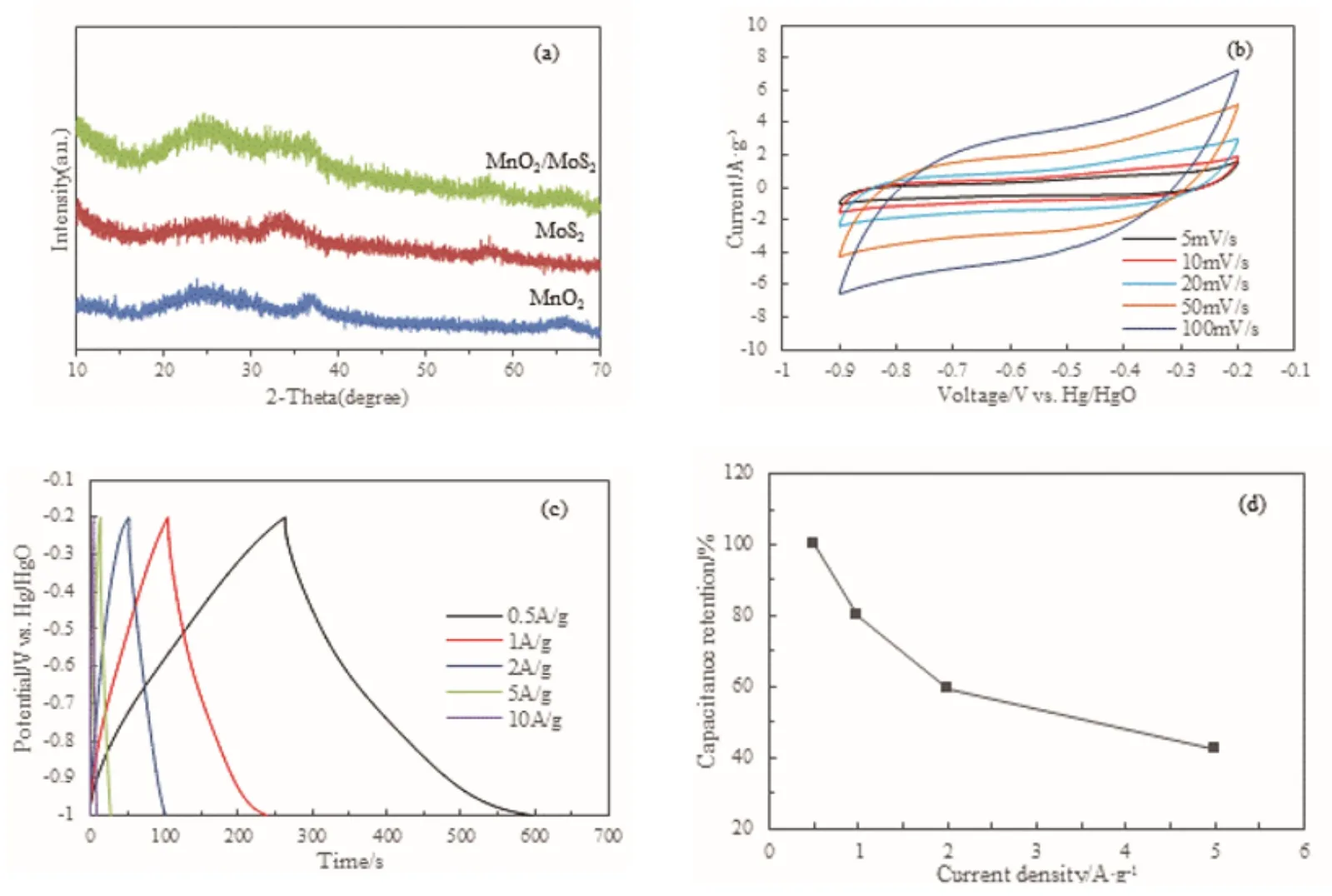
图31 MnO2/MoS2复合材料XRD以及电化学表征图106Fig. 31 XRD patterns,cyclic voltammograms and Galvanostatic charge/discharge properties of MnO2/MoS2 composites 106.
4.5 MXenes@MnO2
MXenes类材料,是一系列二维过渡金属碳化物,正在作为独特的层状化学新兴改性碳材料,其具有有高平面导电性,大表面积和具有金属导电性的亲水表面的优越特性,从而大有电化学能量存储装置应用的潜力107-110。其中最具代表性的当属Ti3C2Tx,一种具有金属导电性和亲水性的二维过渡金属碳化物,将其与赝电容材料MnO2等复合可取得更好的电容性能。Raghavan等111通过化学合成法在MXene纳米片表面上形成了纳米ε-MnO2晶须(ε-MnO2/Ti2CTx和ε-MnO2/Ti3C2Tx) (图32),并用于水性赝电容器复合电极材料。与纯MXene基对称超级电容器相比,ε-MnO2纳米晶须增加了复合电极的表面积,并将比电容提高了近三个数量级。该电容器有着良好的循环稳定性,经10000次循环后,有88%的电容保持率,远高于纯ε-MnO2基超级电容器(74%)。

图32 Ti3C2Tx_Ar (a)和 ε-MnO2/Ti3C2Tx_Ar (b)的 SEM 图以及 Ti3C2Tx_Ar (c)和 ε-MnO2/Ti3C2Tx_Ar (d)的 TEM 图 111Fig. 32 SEM images of stacked multilayer sheets of Ti3C2Tx_Ar (a) and ε-MnO2/Ti3C2Tx_Ar (b);TEM images of Ti3C2Tx_Ar sample (c) and ε-MnO2/Ti3C2Tx_Ar (d) 111.
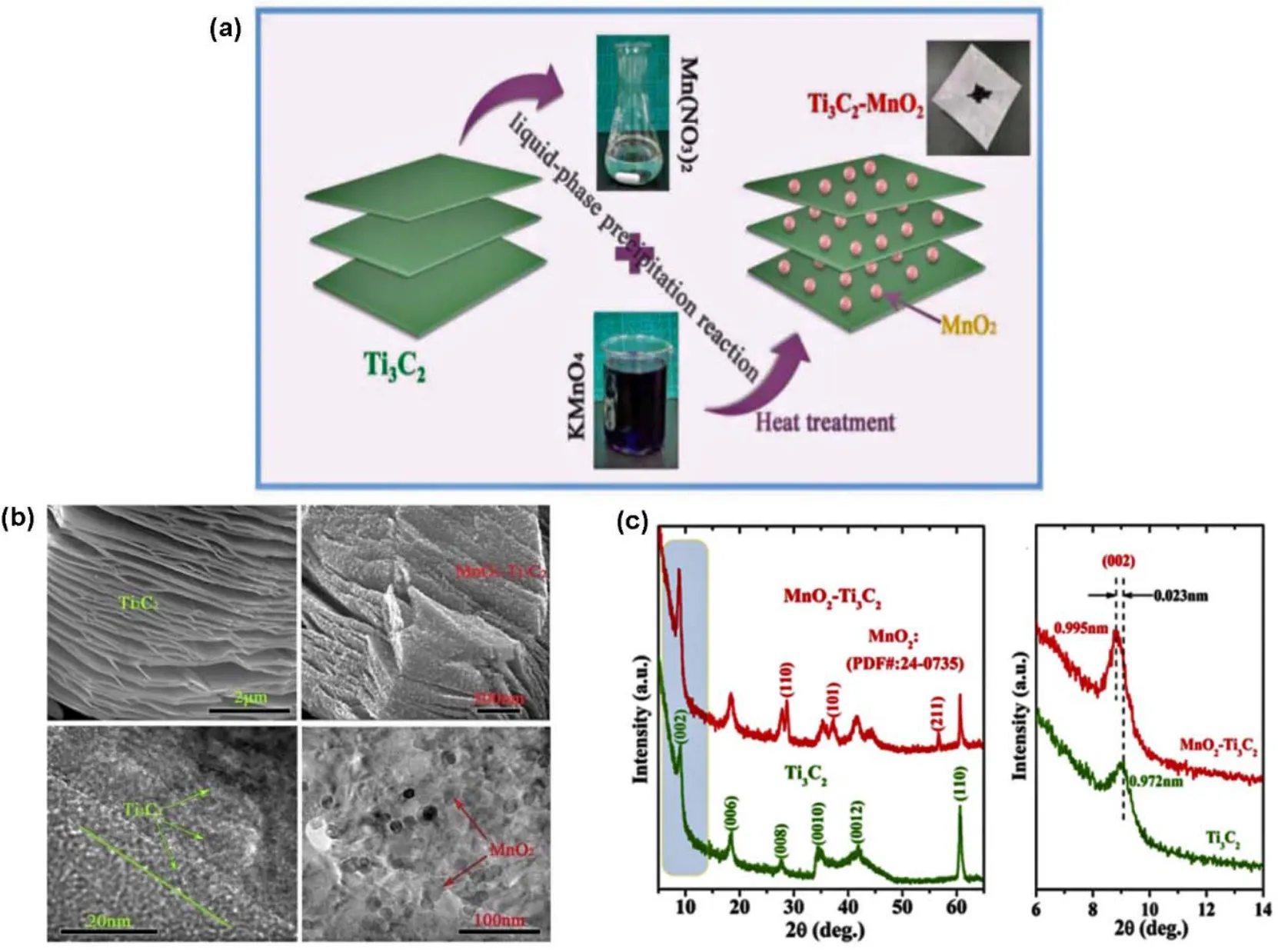
图33 (a) MnO2/Ti3C2纳米复合材料合成工艺示意图(b)典型Ti3C2 和MnO2/Ti3C2纳米复合材料的SEM图以及分别的TEM图(c) Ti3C2和MnO2/Ti3C2纳米复合材料的XRD图113Fig. 33 (a) Schematic illustration of the synthesis process of MnO2/Ti3C2 nanocomposite; (b) SEM images of typical as-fabricated Ti3C2, and MnO2/Ti3C2 nanocomposite; TEM images of Ti3C2, and MnO2/Ti3C2;(c) XRD patterns of Ti3C2 and MnO2/Ti3C2 samples and magnification of XRD patterns 113.
Jiang等112同样采用化学方法合成了新型的MnO2/Ti3C2Tx纳米复合物,除了采用三电极体系测试电极材料的电化学性能外,他们也另外组装了柔性的超级电容器,经过1000次循环后,该电容器没有电容损失,表现出了超强的循环稳定性。Tang等113则联用液相沉淀法和热处理法将MnO2纳米颗粒与Ti3C2纳米片复合,如图33a所示。TEM和XRD图(图33b,c)表明粒径约在20-40 nm的MnO2纳米颗粒Ti3C2均匀地插入到了Ti3C2基质的层间,用于阳离子嵌入。得益于MnO2和Ti3C2基质之间的协同作用,该纳米复合材料在5 mV·s-1的扫描速率下具有优异的面积比电容377 mF·cm-2,高于纯Ti3C2(306 mF·cm-2),此外,循环5000圈后,仍有95%的电容保持率,表明有着优异的循环稳定性。
Liu等114首次报道了组装MnO2和Ti3C2纳米片用于高性能柔性轻薄超级电容器,充分利用了二者相似二维几何特征、相容性以及二氧化锰的高电容和Ti3C2片的优秀的导电性。MnO2和Ti3C2单片层带负电而且液相可溶,它们的胶体混合物已提前制备,然后将其通过醋酸纤维素薄膜过滤便得到了分子堆叠结构的MnO2/Ti3C2片状复合物(图34a)。采用三电极体系,其中中性溶液Na2SO4为电解液测试复合物的电化学性能,得到了CV曲线、GCD曲线、循环寿命图等,如图34b所示。在10 mV·s-1的扫描速率下,比电容为390 F·g-1。而且经过6000次的循环后,电容保持了93%。此外,他们还将测试效果最好的复合比例材料用于构造实际的对称超级电容器(图34c),测试了其电化学性能以及机械可弯曲性。功率密度为221.33 W·kg-1时,能量密度为8.3 Wh·kg-1。
Yuan等115通过水热法合成了Ti3C2/MnO2复合材料,其中二维Ti3C2作为基底,这不仅仅提高了电子传导性,也防止了MnO2结构的破坏,还能让MnO2暴露更多的活性表面区域。测试计算发现,该复合物电极0.5 A·g-1的电流密度下,比电容为254 F·g-1,经过5000次循环后,只损失了4.5%的电容。
4.6 MOFs@MnO2
二维MOF纳米片展现出很多不同于传统块体MOF材料的独特性质。比如具有大比表面积、孔洞可调、表面含大量可氧化还原活性中心以及垂直于水平面的有序孔隙等优点,其应用在超级电容器电极材料中的优势越发明显。
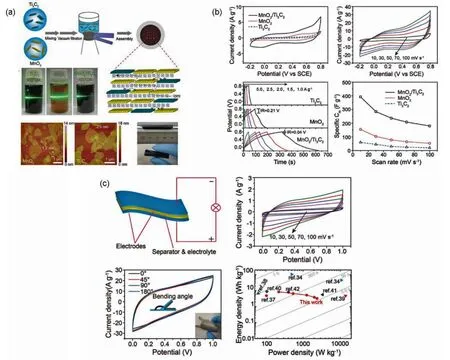
图34 (a)制作混合薄膜的过程示意图;(b)复合薄膜的电化学性能测试;(c)双电极性能114Fig. 34 (a) Illustration of the process for making the hybrid film, (b) Electrochemical performance of the hybrid film, (c) Two-electrode performance 114.
MOFs作为电极材料的途径有三种:(1)直接制备MOFs材料116,通过电解质离子的物理吸附存储电荷,或利用金属中心的可逆的氧化还原反应储存电荷;(2)在惰性气体条件下热解MOFs材料从而得到多孔碳材料117,并将其作为双电层电容器的电极材料;(3)通过破坏MOFs结构,得到金属氧化物或者是金属氧化物和碳材料的复合物118,将其作为法拉第赝电容器的电极材料。在此,我们重点论述直接制备得到的MOFs材料与二氧化锰的有效复合。2018年,Xu等116成功合成了Cu-MOF@δ-MnO2纳米片复合材料(图35),比表面积为1055.2 m2·g-1,显著高于超薄MnO2的比表面积(203.5 m2·g-1),也高于Cu-MOF纳米片的比表面积(1041.1 m2·g-1)。以该材料构造的非对称超级电容器(液相电解液)在0-2.0 V的工作电势窗口下,电流密度为1.0 A·g-1时,有着340 F·g-1的高比电容。同时,循环6000圈后,仅有5%的电容损失。
4.7 g-C3N4@MnO2
石墨化碳化氮g-C3N4由于低成本、化学和机械稳定性好、本征含氮量高等特点,已成为双电层电容器电极材料碳基材料后又一可替代的材料。存在于g-C3N4环结构上的N原子的孤对电子会诱发分子内产生更多极性以及提高材料的可润湿性和电荷载流子的迁移率。但是不论是块体抑或层片状的g-C3N4,其双电层比电容都较低,原因可能是比表面积或导电率较低。有报道表明,在g-C3N4中嵌入赝电容材料,利用复合后异质结构的协同效应可加快电荷传输119。过渡金属氧化物MnO2作为典型的赝电容材料,与g-C3N4复合,复合材料将比单一材料显示出更好的储能特性。例如,Kavil等120分别合成了g-C3N4/MnO2和g-C3N4/SnO2纳米复合材料,并用这两种材料构造了对称超级电容器。他们比较了两种电极材料与纯的g-C3N4的电化学性能。结果表明,g-C3N4/MnO2复合电极比电容(174 F·g-1)有了相当大的提高(纯g-C3N4电极只有50 F·g-1)。Sun等121研究了三类材料的复合,基于之前的MnO2基超级电容器电极材料的研究,再结合新型二维材料g-C3N4的优异结构,他们创造性地合成了二维g-C3N4纳米片为基底,导电聚合物PPy包覆MnO2的新型三元复合物。电流密度为2 A·g-1时,复合物电极的比容量为274 F·g-1,几乎是MnO2@PPy复合电极(比电容为69 F·g-1)的两倍。这是由于(1) g-C3N4纳米片的存在有效防止了MnO2颗粒的团聚,从而颗粒状的MnO2有着更多的电化学活性位点参与到电荷储存的过程。(2)额外的MnO2和g-C3N4界面的产生,有助于电荷传输。(3)除了导电聚合物外,g-C3N4能提供充放电过程中另外的电荷传输通道。
除了复合之外,目前对g-C3N4进行原子掺杂(尤其是金属原子,比如Ag、Ti、K等)也有研究,以解决单一g-C3N4光吸收能力弱和易重新团聚的缺陷。Shan等122采用水热法合成了K/Na掺杂的g-C3N4与MnO2的复合物(分别记为K-CNM、Na-CNM),电镜分析发现纳米盘状的MnO2是垂直均匀地分布在g-C3N4的表面,形成了2D-2D结构。电化学分析结果表明K-CNM在电流密度为0.2 A·g-1条件下,有着373.5 F·g-1的高比电容,比Na-CNM的比电容更高(0.2 A·g-1的电流密度,比电容为294.7 F·g-1),如图36所示。
4.8 其他MnO2基二维异质结构研究展望

图36 K-CNM, Na-CNM在1 mol·L-1 Na2SO4电解质溶液中测电化学性能。(a) 100 mV·s-1扫描速率下的循环伏安曲线;(b) 0.5 A·g-1电流密度下的充放电曲线;(c)在不同电流密度下的比电容(d)在开路电位下的阻抗谱122Fig. 36 The electrochemical performance of K-CNM, Na-CNM and CNM measured in 1 mol·L-1 Na2SO4 (a) CV curves at the scan rate of 100 mV·s-1; (b) GCD curves at 0.5 A·g-1; (c) speci fi c capacitances under different current densities; (d) EIS patterns at open circuit potentials 122.
由于二维材料在超级电容器储能这一领域的巨大潜力,上述只是总结了几大类二维材料与MnO2复合应用于超级电容器电极材料的相关研究,还有许多已开发或正在待开发的二维材料未被提及。比如Choi等123采用化学氧化聚合法(冰作为硬模板)合成了二维聚苯胺纳米片。这种新型的二维导电聚合物有着35 S·cm-1导电率的独特导电通路,而且比表面积(面积比体积)大,这些特征将赋予它比其他形貌的导电聚合物不一般的电化学性能,如果将其再与赝电容材料(如MnO2)复合,将极大幅度地提高电容性能。
近年来,将元素二维纳米材料应用于超级电容器也屡被提出124,比如硅烯、锗烯、锑烯。这类材料有着大比表面积和好的导电性,应用未来高性能超级电容器大有潜能。早些年发现的黑磷(BP)在超级电容器中也广为研究125-127。Sajedi-Moghaddam等128探究了BP纳米盘/PANI在赝电容器中的应用,在电流密度为0.3 A·g-1下,该纳米复合电极的比电容为354 F·g-1。通过层状BP形成的大表面可供PANI形核,从而产生大量离子通道以促进储能的提升。Liu等129通过水热法将MnO2纳米结构直接沉积在鼠尾草衍生的GPCNs (GPCNSS)表面。一系列测试表明,他们所制备的MnO2/GPCN-SS复合材料具有较高的比表面积(483 m2·g-1)和合适的中孔尺寸(2-5 nm)。此外,由于GPCN-SS和MnO2纳米结构的协同作用,MnO2/GPCN-SS复合电极在0.5 A·g-1时的比电容为438 F·g-1(几乎是原始GPCN-SS的两倍),在Na2SO4电解质中具有较高的倍率性能(在50 A·g-1时的容量保持率为67.8%)。
5 结论与展望
二氧化锰基超级电容器在最近几年经历了快速发展,表明其作为高效能量存储装置的巨大潜力,但是二氧化锰的导电性较差的特点,极大地限制了二氧化锰用作超级电容器的电极材料时进行大电流充放电,功率密度也受到影响。二维材料也继石墨烯后被相继用作超级电容器电极材料,具有二维特殊结构特征材料在提高双电层电容器的能量密度、改善赝电容电容器方面发挥出重要作用。本文综述了用于超级电容器电极材料的多种二维材料,以及其中某些二维材料与二氧化锰的纳米复合物构建高性能超级电容器,系统并深入地分析了各类二维材料的结构特点和应用于超级电容器的优势,并阐明了它们与二氧化锰复合缘由以及复合后的效果等。
构筑二维材料-无机纳米二氧化锰复合材料,复合材料具有单体材料各自的优异性能,更重要的是还会产生异质协同效应。尽管在提高电容器性能方面,采用二氧化锰与二维材料纳米复合物作为电极材料所制得的超级电容器相比于其与三维结构材料复合的超级电容器没有绝对优势,但在超级电容器需要高柔性、平面、轻薄甚至透明的情况下,采用二维材料作为电极材料的柔性超级电容器或者微小型超级电容器相比于其他非二维材料更有优势。表现为循环次数更高、柔性化程度更高,并且在折叠几千次后性能不发生明显的变化。这种复合设计带来了诸多优势,为未来发展大规模柔韧微小型电子器件奠定了基础。寻求与二氧化锰复合的二维材料,应基于二氧化锰作为电极材料的不足,以及未来超级电容器所面临的挑战(如微小型、柔韧性、轻薄化等)。同时还应进一步探究复合途径以进一步优化纳米复合物的电化学性能,比如设计复合路径时,应充分考虑导电性能,比表面积,界面结合,MnO2晶型和相貌控制等因素的影响。

