腹主动脉瘤腔内修复术后髂支闭塞的危险因素分析
雍恒,方青波,王斌,慈红波,管圣,戈小虎
多数腹主动脉瘤(abdominal aortic aneurysm,AAA)病因不明[1],无特异性的药物可预防AAA发生、扩张、破裂[2],AAA腔内修复手术(endovascular repair,EVAR)有效改善病人生存情况[3],但晚期并发症,如内漏,复发性动脉瘤,支架迁移,髂支闭塞,移植物感染,使得EVAR术后病人需终生随访[4-6]。EVAR相关二次干预成为影响病人术后生存质量的重要因素[5-7],针对此类情况的早期监测和原因分析,对指导适当干预至关重要。髂支闭塞是EVAR术后常见的严重并发症,可使EVAR治疗复杂化。Conrad等[5]报告832例EVAR术后病人髂支闭塞率2.9%,占全部并发症的18%。髂支闭塞涉及单或双侧髂动脉[8],病因复杂,常需紧急腔内或外科干预。解剖、支架、人为因素均可导致髂支闭塞,主流支架材料的普及、种类、配套设备、操作流程成熟,支架源性髂支闭塞的风险有所减少,人为因素常随着复杂解剖条件和操作者经验差异而有所不同,亚洲人群可能具有挑战性的主动脉解剖结构和更高手术和器械相关并发症风险[9],对髂支闭塞的潜在解剖学危险因素加以总结,可为减少髂支闭塞提供理论支持。
资料与方法
一、研究对象及方法
回顾性收集2008年1月至2018年3月于新疆维吾尔自治区人民医院血管外科诊治肾下型腹主动脉瘤(infrarenal abdominal aortic aneurysm,IAAA)行EVAR治疗病人。依据CT血管造影(CTA)随访结果,按髂支闭塞情况划分髂支闭塞组和非闭塞组,详细整理各项临床资料,进行单因素和多因素分析探寻髂支闭塞的危险因素。
二、诊断标准
AAA指主动脉的最大直径超过3 cm或局灶性扩张≥正常邻近动脉段直径的1.5倍[1]。髂支闭塞最常定义为髂支闭塞(iliac limb occlusion,ILO)[10]或移植物支架内闭塞(endograft limb occlusion,ELO)[8,11],指髂支支架内血栓形成和闭塞后下肢动脉血流受限或中断,通过相关病史采集,临床表现、症状、体征,结合CTA或数字减影血管造影(DSA)检查即可确诊。
三、纳入标准和排除标准
纳入标准:①行EVAR治疗IAAA;②临床资料及手术信息完整;③术前病人充分知情同意,依从性好,随访配合。排除标准:①腹主动脉瘤破裂;②假性腹主动脉瘤;③感染性腹主动脉瘤;④胸腹主动脉瘤;⑤合并主动脉夹层,主动脉壁间血肿,腹主动脉穿透性溃疡;⑥合并下肢动静脉瘘;⑦非“Y”型支架手术;⑧杂交手术或复合手术;⑨相关资料不全;⑩无有效随访。
四、解剖因素测量
影像科医师导出DICOM格式主动脉CTA资料,采用Braco Voxar 3D 6.4 Workstation 影像工作平台(TOSHIBA 公司,日本)行二维、三维显像,观察AAA一般形态学特征,运用Voxar 3D Vessel Metrix 血管专用插件测量EVAR及支架选择相关解剖参数,测量标准参考文献[12-13]。
五、统计学方法
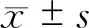
结 果
一、EVAR术后髂支闭塞单因素分析
IAAA行EVAR手术146例,发生髂支闭塞17例(11.6%)。单因素分析显示,两组在一般临床指标即合并慢性支气管炎、高脂血症方面差异有统计学意义(P<0.05),见表1。术前实验室检查,中性粒细胞百分比(NEUT %)、活化部分凝血酶原时间(APTT)、凝血酶原比率(PA %),组间差异有统计学意义(P<0.05),见表2。手术操作相关指标:手术入路,手术时间,组间差异有统计学意义(P<0.05),见表3。手术相关解剖测量因素:右髂总动脉直径分层(≤12 mm、12~16 mm、≥16 mm),组间差异有统计学意义,见表4。手术相关解剖学因素:髂动脉扭曲成角≥60°(图1~图3),髂动脉狭窄或钙化≥50%(图4~图6),术后髂动脉流出道狭窄,髂内动脉流出道闭塞、支架远端延伸到髂外动脉等因素闭塞组与非闭塞组间差异有统计学意义(P<0.05),见表5。
表1髂支闭塞组与非闭塞组一般临床指标分析
变量名称闭塞组(17例)非闭塞组(129例)t(z、χ2)值P值年龄(岁)a68.9±7.269.9±8.60.4410.660男性[例(%)]b15(88.2)108(83.7)0.0160.900病程(d)c22(10,60)7(3,30)1.5260.127合并症[例(%)]b 高血压12(70.6)91(70.5)0.0000.997 动脉硬化10(58.8)93(72.1)1.2730.259 冠心病10(58.8)50(38.8)2.4980.114 慢性支气管炎2(11.8)51(39.5)3.8800.049 脑卒中7(41.2)23(17.8)3.6870.055 2型糖尿病3(17.6)23(17.8)0.0001.000 高脂血症5(29.4)8(6.2)7.3200.007髂动脉瘤[例(%)]b 双髂总动脉瘤9(52.9)41(31.8)2.9860.084 右髂总动脉瘤10(58.8)54(41.9)1.7560.185 左髂总动脉瘤10(58.8)56(43.4)1.4410.230 右髂内动脉瘤4(23.5)19(14.7)0.3390.560 右髂外动脉瘤09(7.0)0.3460.557 左髂内动脉瘤3(17.6)30(23.3)0.0450.833 左髂外动脉瘤3(17.6)6(4.7)2.4270.119 梭形动脉瘤16(94.1)126(97.7)-0.394 附壁血栓13(76.5)96(74.4)0.0001.000
注:a.正态分布的计量资料,行t检验;b.使用χ2检验;c.非正态分布,数据以中位数(四分位数间距)表示,行z检验
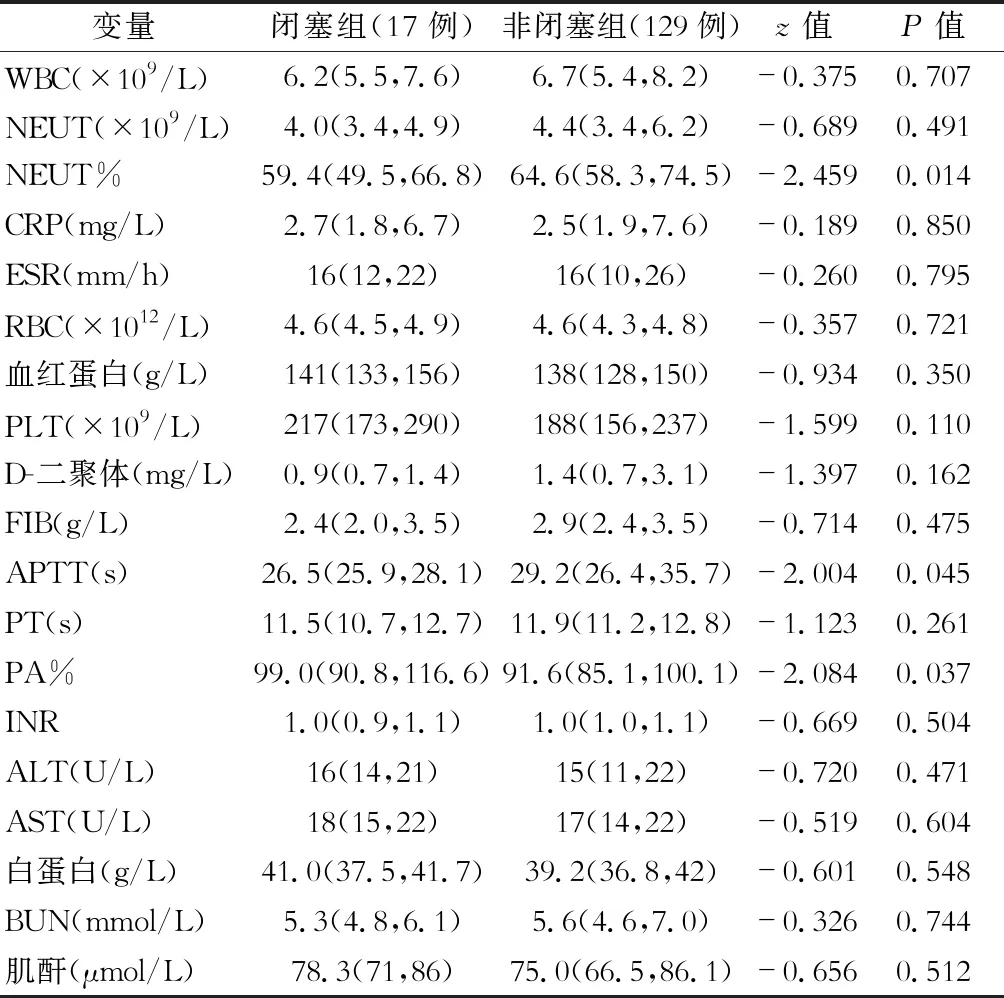
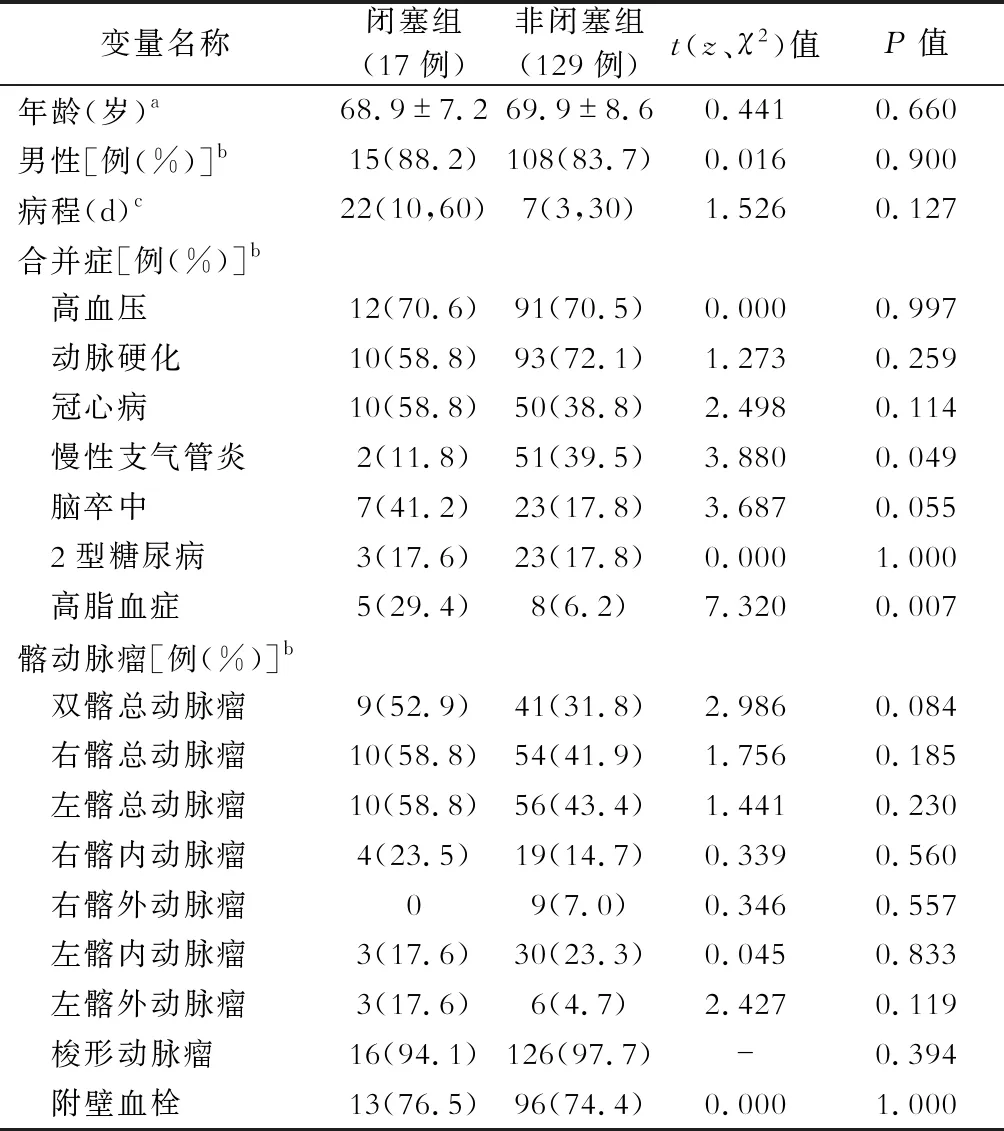
表2 髂支闭塞组与非闭塞组术前实验室检查分析
注:WBC.白细胞计数,NEUT.中性粒细胞计数,NEUT%.中性粒细胞百分比,CRP.C反应蛋白, ESR.红细胞沉降率, RBC.红细胞计数, PLT.血小板计数, FIB.纤维蛋白原, APTT.活化部分凝血活酶时间, PT.凝血酶原时间, PA%.凝血酶比率,INR.国际标准化比值, AST.天冬氨酸转氨酶, ALT.丙氨酸转氨酶, BUN.血尿素氮;数据以中位数(四分位数间距)表示
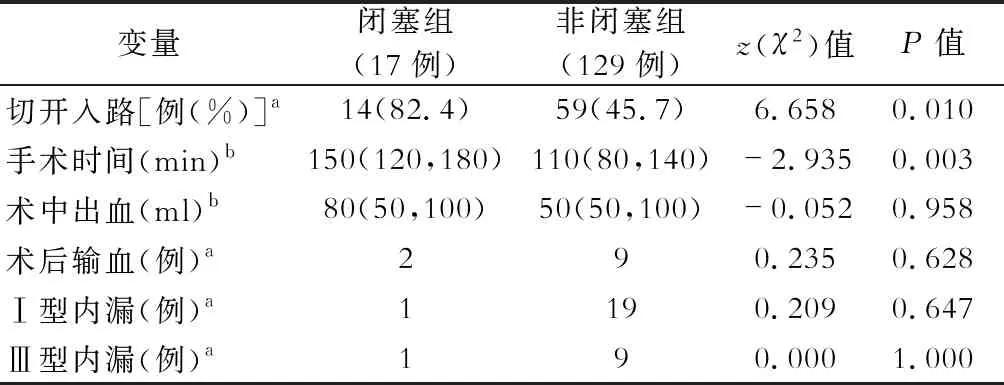
表3 髂支闭塞组和非闭塞组手术相关指标分析
注:a.使用χ2检验;b.非正态分布,数据以中位数(四分位数间距)表示,行z检验
二、影响髂支闭塞相关因素Logistic回归分析
将髂支闭塞作为因变量逐个筛选相关显著变量(P<0.05),进行多因素Logistic回归分析显示:髂动脉狭窄或钙化≥50%、髂动脉扭曲成角≥60°、术后髂动脉流出道狭窄、手术入路为切开显露等因素为EVAR术后发生髂支闭塞的相关危险因素(均OR>1),见表6。
讨 论
有报道髂动脉严重扭曲成角[7,11],髂动脉钙化或狭窄≥50%[8,11],支架远端延伸到髂外动脉[7]与髂支闭塞有关。Carroccio等[10]报道按髂动脉直径14 mm,支架远端延伸到髂外动脉分组,亚组间髂支闭塞率差异有统计学意义,但未行危险因素相关性分析。本研究AAA病人合并髂动脉瘤或瘤样扩张率高,但多因素Logistic回归分析发现术前髂动脉狭窄或钙化≥50%、髂动脉扭曲成角≥60°、术后髂动脉流出道狭窄才是髂支闭塞的危险因素,支架远端延伸到髂外动脉、切开显露和髂支闭塞应当是髂动脉复杂解剖条件结果,二者非导致髂支闭塞的原因。Woody等[14]报道特殊剖特征可致髂动脉扭曲、髂支支架受压或狭窄,血栓负荷增加,支架内血栓形成;腹主动脉分叉处的钙化或狭窄≥50%、股动脉狭窄和扭曲也会对髂支闭塞产生影响,但本研究未能发现后两者对髂支闭塞的发生有关。Carpenter等[15]报道髂支支架与动脉直径不匹配,移植物缺乏支撑,支架径向力不足,可导致支架扭结,这与支架投送特征有关。Mantas等[11]总结技术源性失误是髂支闭塞的主要原因,20例髂支闭塞病人,12例系支架放大率过大,支架定植于髂动脉扭曲部位致流出道受限,未发现髂动脉处血流限制性狭窄而导致支架受压,2例合并髂动脉严重迂曲或腹主动脉分叉狭窄,6例原因不明,特殊解剖条件和违反操作规范是髂支闭塞的主要因素。

表4 髂支闭塞与非闭塞组相关解剖学测量结果分析
注:a.非正态分布,数据以中位数(四分位数间距)表示,行z检验;b.使用χ2检验,单位均为“例(%)”
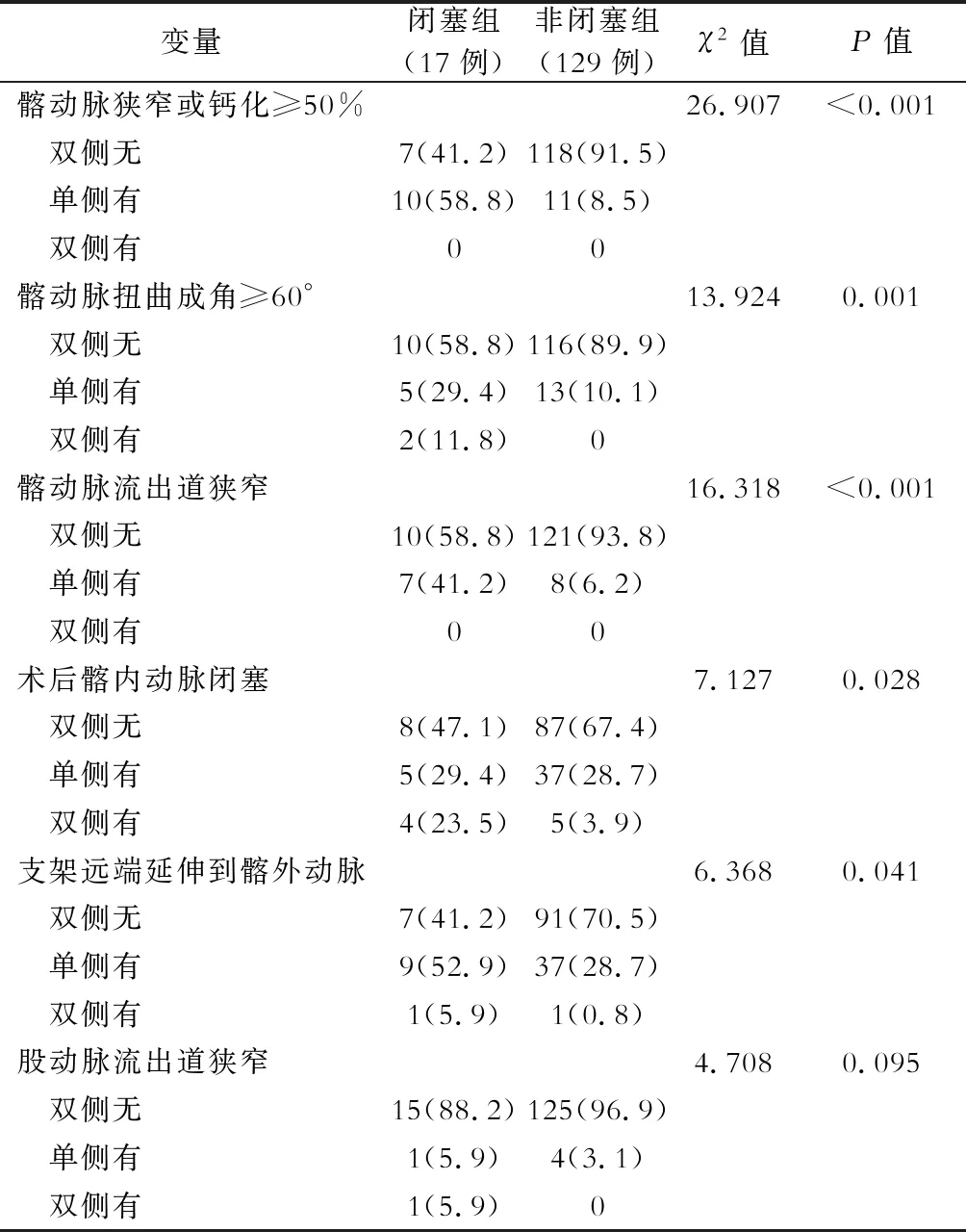
表5 髂支闭塞与非闭塞组在EVAR手术相关解剖学 因素比较[例(%)]
注:双侧无为0,单侧有为1,双侧有为2
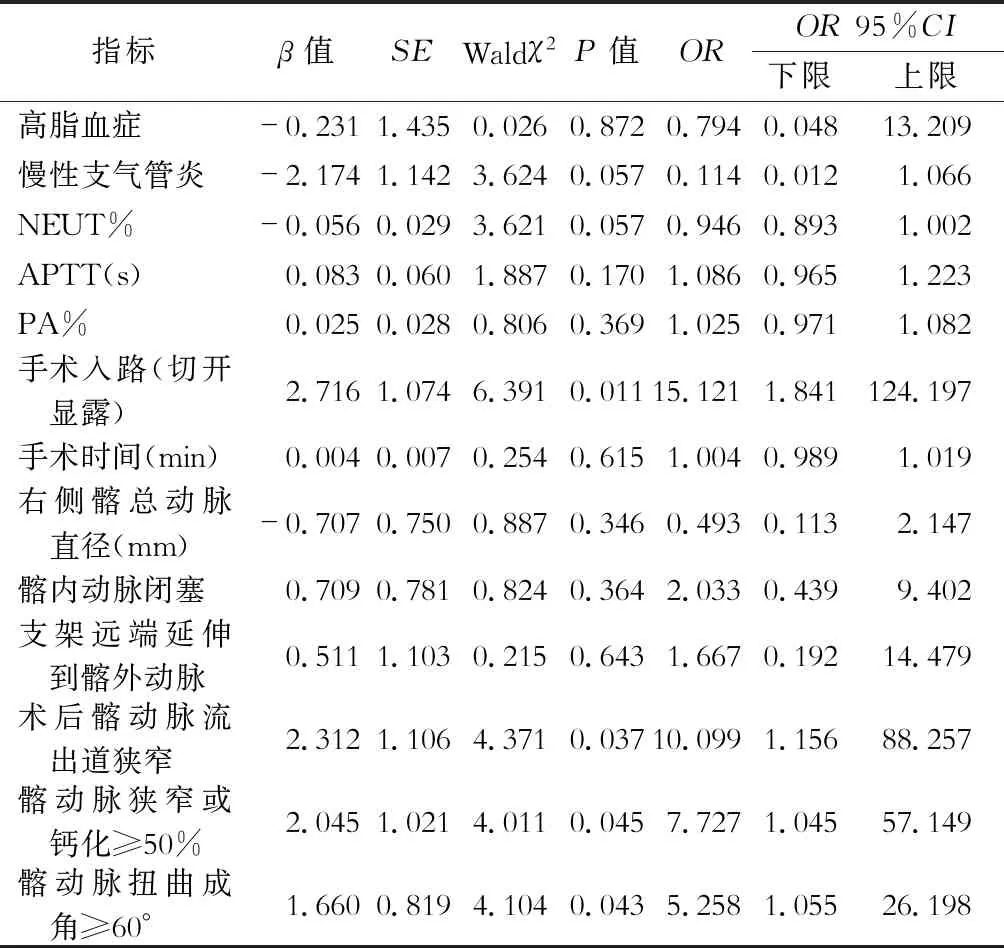
表6 影响髂支闭塞相关因素多元Logistic回归分析
注:NEUT%.中性粒细胞百分比;APTT.活化部分凝血活酶时间;PA%.凝血酶比率
髂动脉解剖结构不良,将增加EVAR手术复杂性,具有潜在并发症隐患。既往注重瘤体破裂、内漏、复发性动脉瘤、支架迁移、移植物感染预防,对远端流出道(锚定区)如髂动脉解剖特异性缺乏应有重视。Henretta等[16]报道74例病人有40例(54%)存在髂动脉扭曲、血管纤细或钙化狭窄、髂动脉瘤样扩张或动脉瘤等挑战性髂动脉解剖结构,对手术策略有直接影响,由于髂动脉瘤或瘤样扩张,需经髂内动脉介入栓塞和支架延伸到髂外动脉及远端喇叭口技术解决支架放置问题,因髂支扭曲而采用肢体交叉技术;支架输送问题原因包括髂动脉扭曲或动脉硬化闭塞,3例需左肱动脉辅助入路,3例因髂动脉硬化行球囊及支架成形,5例行外科重建,3例髂外动脉损伤行腔内重建,髂动脉解剖结构复杂性造成了EVAR治疗的复杂性,对治疗策略和手术相关并发症产生直接影响。现有覆膜支架系统部署需通过大口径鞘管并通过股动脉及髂动脉通路,AAA病人常伴有动脉粥样硬化性血管钙化或狭窄或髂动脉扭曲,经皮腔内血管成形术(PTA)和支架成形可以在一定程度上缓解这一问题[17],而针对髂动脉扭曲病人,除强调避免支架远端植入髂动脉扭曲段外,髂支交叉技术(crossed-limb technique)[18-19]有助于改善瘤颈过于扭曲及髂总动脉成角过大,已在血流动力学、安全性及可靠性上得到验证[20-21]。
髂支闭塞最佳治疗方法是预防。术前CTA及术中多角度血管造影可明确部分髂支闭塞高危因素。若术中造影显示支架流出道狭窄或扭曲,可行球囊成形,再次造影提示限制性血流,可行辅助性支架植入。对流出道条件不佳,术后密切随访,必要时早期重建。ENGAGE研究中[7],依据髂支闭塞的危险因素建立预测决策树,可明确危险分度,为髂支闭塞预防策略选择提供支持,以改善EVAR的总体结果。Lee等[22]依据动脉扭曲指数行解剖特征分类,行辅助性金属裸支架植入(adjunctive iliac stent,AIS)以预防髂支闭塞。唐骁等[23]总结一期裸支架植入适应证:术前CTA显示腹主动脉分叉部或髂动脉锚定区存在中度以上狭窄或钙化,术中造影显示髂支内部或支架远端与髂动脉交界段存在明显狭窄或扭曲且影响血流;相对适应证:DSA虽未见髂支狭窄,但术前CTA提示髂动脉存在中度以上扭曲(“S”形或“Q”形)且扭曲段位于髂支支架内;支架型人工血管远端锚定区位于髂外动脉。合理的一期自膨式裸支架置入确有减少EVAR术后髂支闭塞。髂支交叉技术[18-19]可改善瘤颈扭曲及髂总动脉成角过大情况,当髂动脉成角≥40°使用髂支交叉技术,既降低髂支扭曲风险,又缩短分腿支架长度,降低髂内髂内动脉开口覆盖、支架远端延伸到髂外动脉率[20]。
复杂髂动脉解剖条件是EVAR术后髂支闭塞不确定性增加的主要原因。髂动脉显著扭曲成角≥60°、髂动脉狭窄或钙化≥50%、术后髂支流出道狭窄是髂支闭塞的解剖学危险因素。支架远端延伸到髂外动脉和手术入路选择(切开显露),应当视为AAA髂动脉复杂解剖条件的结果而非导致髂支闭塞的原因[17]。加强髂动脉解剖条件评估,针对髂动脉显著扭曲成角、髂动脉重度狭窄或钙化等因素合理设计手术入路,术中即刻造影,采取一期个体化辅助干预,加强随访管理将有助于降低EVAR术后髂支闭塞的发生。

