2型糖尿病并发高眼压症危险因素分析
高惠娟,胡艳滨,刘永盛,牛淑玲,张明,王永起,杜金金
天津市第三中心医院分院,天津300052
高眼压症是指多次眼压测量双眼数值均在正常人群眼压的高限或高限以上,房角开放,经多年随访仍不引起青光眼视乳头改变或视野损害的一种状态。正常人眼压为10~21 mmHg,眼压>21 mmHg即可判定为高眼压症。高眼压症在普通人群中的发生率约为2%,而在40岁以上人群中的发生率为4%~10%,并且每年0.5%~1%的患者可发展为原发性开角型青光眼。糖尿病是一种以高血糖为特征的代谢性疾病,长期高血糖或血糖控制不佳可引起眼底出血、白内障以及眼底病变等,如果并发高眼压症则会进一步加重视功能损害。有研究报道,糖尿病人群并发高眼压症的风险为非糖尿病人群的1.5~3倍[1]。如能早期识别糖尿病并发高眼压症的危险因素,及时采取有效的干预措施,则能延缓视功能损害。但目前关于糖尿病并发高眼压症的危险因素尚不明确。为此,我们分析了2型糖尿病并发高眼压症的危险因素。现报告如下。
1 资料与方法

1.2 临床资料收集 收集两组人口学资料、物理检查和实验室检查资料。人口学资料包括性别、年龄,物理检查资料包括血压(收缩压、舒张压)、角膜厚度,实验室检查资料包括FPG、糖化血红蛋白(HbA1c)、TG、TC、LDL、HDL、纤维蛋白原(FIB)、全血黏度(低切、高切)、红细胞变形指数和刚性指数。
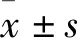
2 结果
2.1 两组临床资料比较 高眼压组男17例、女13例,年龄(53.5±5.4)岁;糖尿病组男29例、女31例,年龄(48.5±6.3)岁。两组性别比例、年龄比较P均>0.05。两组物理检查和实验室检查资料比较见表1~3。

表1 两组物理检查资料比较
注:与糖尿病组比较,*P<0.05。
2.2 2型糖尿病并发高眼压症的危险因素 以是否合并高眼压症为因变量,以两组上述有统计学差异的指标作为自变量进行多因素Logistic回归分析,结果显示,角膜厚度、HbA1c、TG、TC、全血低切和高切黏度为2型糖尿病并发高眼压症的危险因素(P均<0.05)。见表4。

表2 两组糖脂代谢相关指标比较
注:与糖尿病组比较,*P<0.05。

表3 两组FIB、全血黏度、红细胞变形指数和刚性指数比较
注:与糖尿病组比较,*P<0.05。

表4 2型糖尿病并发高眼压症的危险因素分析结果
3 讨论
眼压是眼内容物对眼球壁的压力,眼内容物有房水、晶状体和玻璃体。其中,房水是影响眼压的主要因素。正常状态下,房水的产生和重吸收保持动态平衡,当房水产生过多或排出通道受阻,就会导致眼压升高。有研究表明,遗传因素、性别、年龄、种族、角膜厚度和体位也是影响眼压的重要因素。眼压>21 mmHg即可判定为高眼压症。高眼压症在普通人群中的发生率约为2%,而在40岁以上人群中的发生率为4%~10%,并且每年0.5%~1%的患者可发展为原发性开角型青光眼。临床研究发现,绝大多数青光眼患者眼压明显升高,尤其是原发性开角型青光眼患者,但其发展缓慢,较少引起视盘和视野损害。在40岁以上普通人群中,原发性开角型青光眼的患病率为1.76%,而糖尿病患者原发性开角型青光眼的患病率为5%~12.4%,远高于普通人群[2~4]。Xu等[5]研究认为,糖尿病、高血压、高胆固醇血症等与高眼压症密切相关。Salim等[6]对原发性开角型青光眼患者连续10年跟踪发现,与原发性开角型青光眼相关的系统性疾病中,糖尿病居第三位。糖尿病患者存在高血糖、脂代谢紊乱、血液黏滞性升高等状态,而这些因素对眼压均有一定影响[7]。有研究报道,糖尿病患者眼压比非糖尿病患者高2~3 mmHg[8]。这些研究结果提示,糖尿病患者更易并发高眼压症。糖尿病患者长期高血糖或血糖控制不佳,可引起眼底出血、白内障以及眼底病变等,如果并发高眼压症则会进一步加重视功能损害。
糖尿病患者体内超氧化物歧化酶和谷胱甘肽过氧化物酶活性降低,可导致组织缺氧[9];而组织缺氧会引起糖尿病患者眼内氧化应激反应[10]。小梁网细胞氧化应激损伤产生的活性氧会通过Schlemn′s管及相应集液管使房水流出减少。活性氧还可诱导小梁网细胞骨架重构、凋亡以及炎症因子释放,引起细胞外基质异常沉积和细胞坏死[11]。有研究证实,小梁网细胞骨架老化、细胞骨架成分改变、细胞外基质异常沉积等在原发性开角型青光眼发病过程中具有重要作用。糖尿病并发高眼压症同青光眼一样能够影响视网膜内层[12],且视网膜神经节细胞层厚度与糖尿病病程密切相关[13]。因此,与组织缺血缺氧相关的因素可能也是糖尿病并发高眼压症的危险因素。
糖尿病患者如血糖控制不佳,房水中含糖量增加,引起小梁网胶原纤维和弹力纤维变性,内皮细胞脱落或增生,小梁网增厚、硬化,网眼变窄或闭塞,Schlemn′s管内斑状物沉着,导致房水排出系统阻力增加,引起眼压升高。与非糖尿病患者相比,糖尿病患者视网膜和视盘上小血管硬化阻塞多见,视神经供血不足,更易导致视网膜神经节细胞及其轴突等损害,从而诱发原发性青光眼,引起视野缺损、视力下降,甚至视神经萎缩。糖尿病患者在糖代谢出现异常之前就存在脂代谢紊乱,而脂代谢紊乱能够加重和促进血管动脉粥样硬化,从而加重糖尿病视功能损害。
高黏滞血症是一种常见而多发的代谢性疾病,多发于中老年人,主要表现为血浆脂质中的一种或多种成分含量升高,是导致动脉粥样硬化性心脑血管疾病的重要因素。有文献报道,原发性开角型青光眼与闭角型青光眼患者均易并发高黏滞血症,而血液流变学改变是原发性青光眼发病的重要机制之一[8]。Bojic等[14]研究表明,进展期开角型青光眼患者血小板黏附率明显增高,并认为血小板黏附率增高是原发性开角型青光眼发病的危险因素。葛坚等[15]研究发现,原发性开角型青光眼患者全血黏度、红细胞压积、红细胞聚集指数等血流变学指标均明显高于正常人,并认为高黏滞血症是诱发原发性开角型青光眼的重要原因之一[11]。
肖明等[16]认为,高眼压症患者角膜中央厚度与眼压呈正相关关系,眼压每变化1 mmHg,角膜中央厚度相应变动23.6 μm。吴玲玲等[17]研究报道,高眼压症患者中央角膜厚度较正常人明显增加。殷鸿波等[18]观察了169例正常人中央角膜厚度与Goldmann压平眼压的关系,结果发现中央角膜厚度变异是眼压测量误差的主要来源。中央角膜厚度较厚的正常人可能因“眼压增高”而被误诊为高眼压症,中央角膜厚度偏薄的原发性开角型青光眼患者则可能因“眼压正常”而被误诊为正常眼压型青光眼。在诊断青光眼或高眼压症时,特别是在眼压值与其他临床表现不符时,应考虑中央角膜厚度有无变异[19,20]。
本研究单因素分析显示,2型糖尿病并发高眼压症可能与角膜厚度、HbA1c、TG、TC、全血低切和高切黏度有关,而与性别、年龄、血压、FPG、LDL、HDL、FIB、红细胞变形指数和刚性指数无关。进一步多因素Logistic回归分析显示,角膜厚度、HbA1c、TG、TC、全血低切和高切黏度为2型糖尿病并发高眼压症的危险因素。
综上所述,角膜厚度、HbA1c、TG、TC、全血低切和高切黏度为2型糖尿病并发高眼压症的危险因素。及早对这些危险因素进行有效干预,能够延缓2型糖尿病并发高眼压症的视功能损害。但由于本研究样本量较小,其结论的准确性尚需扩大样本量进一步研究验证。

