类沸石咪唑酯骨架材料ZIF-67对重金属离子镉、铜和铅的吸附性能研究
杨清香,陈从涛,赵翠真,孙梦磊,陈志军
(1.郑州轻工业大学 材料与化学工程学院,郑州450002;2.湖北英特吉新能源科技有限公司,武汉430000)
0 引 言
水体污染是指排入水体的污染物在数量上超过该物质在水体中的本底含量和水体的自净能力,从而导致水体的物理、化学及卫生性质发生变化,使水体的生态系统和水体功能受到破坏。水体污染物种类繁多,尤其是重金属污染已经成为水体污染中危害最大、对环境影响最大的污染源之一[1]。水体中重金属离子污染主要包括Hg2+、Cd2+、Pb2+、 Cu2+、Cr6+等[2],这些重金属离子能够渗入土壤[3],影响植物的生长,并通过食物链最终进入人体内,因其无法在人体里代谢而会集聚在人体软组织,即使在痕量下也会对人类健康造成极大危害[4]。因此,有效防控水体重金属污染已成为影响我国社会经济可持续发展的重大战略问题之一。
治理重金属污染的方法主要有生物处理法[5]、化学沉淀法[6]、离子交换法[7]及吸附法[8]。在这些方法中,吸附法因可以一次性移除水体中重金属离子,且不会造成二次污染而备受人们的关注。传统的吸附剂普遍存在吸附量小和去除效率低等问题[9],研制吸附量大且吸附效率高的吸附材料成为材料领域的研究热点之一。在这些新兴的吸附材料中,金属有机骨架材料(metal-organic frameworks,简称 MOFs)由于具有超高的比表面积、较大的孔隙率以及规整的孔隙结构[10]而成为提高吸附量和吸附效率的新的方法[9,11-14]。在已报道的文献中,MOFs材料用于Pb2+、Cr3+和Hg2+吸附的较多,Huang等[15]通过使用不同的前体成功地制备了Fe3O4@SiO2@UiO-66及其氨基衍生物,其中MFC-N表现出最高的Pb2+(102 mg/g)。Tahmasebi E等[16]将TMU-5用于Cu2+(57 mg/g)、Pb2+(251 mg/g)和Cd2+(43 mg/g)的吸附,但是,这些已报道用于水体中重金属离子吸附的MOFs材料均存在制备过程复杂、吸附量偏低、吸附速率慢等缺点。
本文用ZIF-67(沸石咪唑酯骨架结构材料)可进入孔结构约为1.0 nm左右[17],比表面积大,制备过程简单,可大批量合成,作为水体中重金属离子Cd2+, Cu2+和 Pb2+离子的吸附研究,与传统材料相比,具有独特的优势。
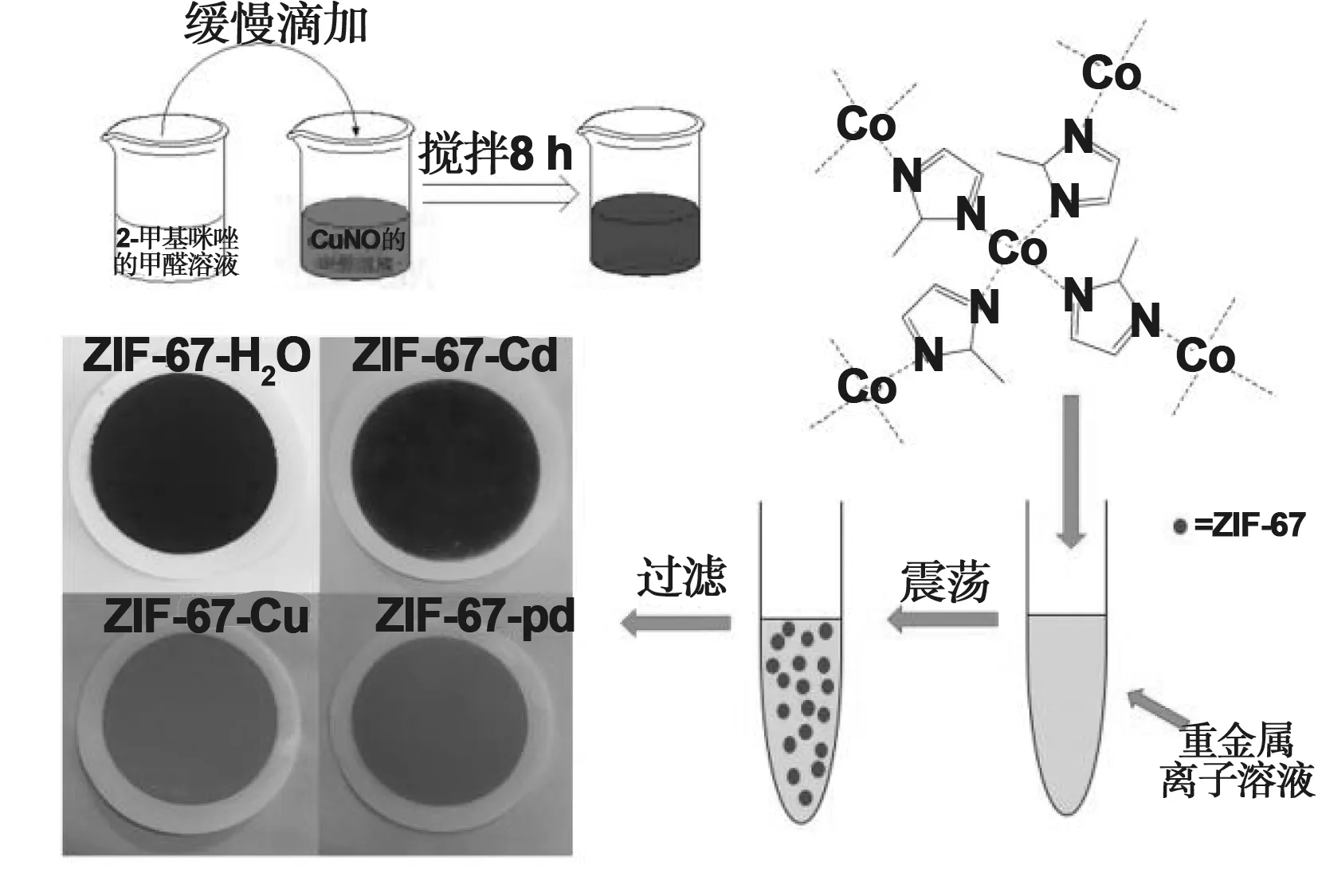
图1 ZIF-67的制备及其吸附过程示意图
1 实验部分
1.1 实验试剂
无水甲醇、硝酸钴、硝酸铅、硝酸钴均为分析纯,购于天津市风船化学试剂科技有限公司;硝酸镉、硫酸铜均为分析纯,购于天津市科密欧化学试剂科技有限公司;2-甲基咪唑为分析纯,购于上海达瑞精细化学品有限公司;去离子水自制。
1.2 ZIF-67的制备
6.489 g 2-甲基咪唑 (79.04 mmol) 与200 mL无水甲醇混合、超声至形成透明的溶液 (记为: 溶液A);2.933 g六水硝酸钴(10.01 mmol) 和200 mL的无水甲醇混合、超声至形成透明的溶液 (记为:溶液B)。将A溶液缓慢滴加到溶液B中,磁搅拌8 h。8 500 r/min离心分离得到粗产品,用甲醇洗涤3次,至清洗液无色透明,60 ℃真空干燥12 h。
1.3 样品的表征
物相分析用X-射线衍射仪(D8-ADVANCB,德国布鲁克),工作电压40 kV,管流30 mA,Cu靶Kα射线入射,2θ范围从5°~50°。材料的热分解温度用综合热分析仪(TG/DTA Diamond),以α-Al2O3为标样,其测量的温度范围是室温至800 ℃,测试条件是气体氛围,升温速率为10 ℃/min。红外光谱分析用红外光谱仪(Nicolet 5700),样品的结构及骨架振动采用KBr做支撑片,在400~4 000 cm-1范围内,记录样品的骨架振动红外吸收峰。产物的形态用扫描电子显微镜(SEM,JSM-6490LV,JEOL,日本),加速电压5 kV。水体中吸附前后的离子浓度用原子吸收光谱仪(contr AA 700,耶拿,德国) 测量。
1.4 吸附性能测试
将一定量的吸附剂分别加入到一定浓度的Cu2+、Pb2+和Cd2+溶液,充分混合一定时间,离心取上清液,稀释一定倍数,再用原子吸收光谱仪测定溶液中离子浓度。
按照式(1)计算吸附剂对重金属离子的单位吸附量。
(1)
其中q为单位吸附量 (mg/g);C0为吸附前重金属离子的浓度(mg/L);Ci为吸附一定时间后溶液中重金属离子的浓度 (mg/L);V为离子溶液的体积(L)。
2 结果与讨论
2.1 物相测定(PXRD)
图2是制备的ZIF-67和模拟ZIF-67的PXRD图。实验制备的ZIF-67样品在7.39°,10.36°,12.79°,14.71°,16.45°,18.01°,22.19°,24.64°和26.72°存在衍射峰,分别对应(011),(002),(112),(022),(013),(222),(114),(233)和(134)晶面[18],与模拟ZIF-67的衍射峰位一致,属于十二面体结构。
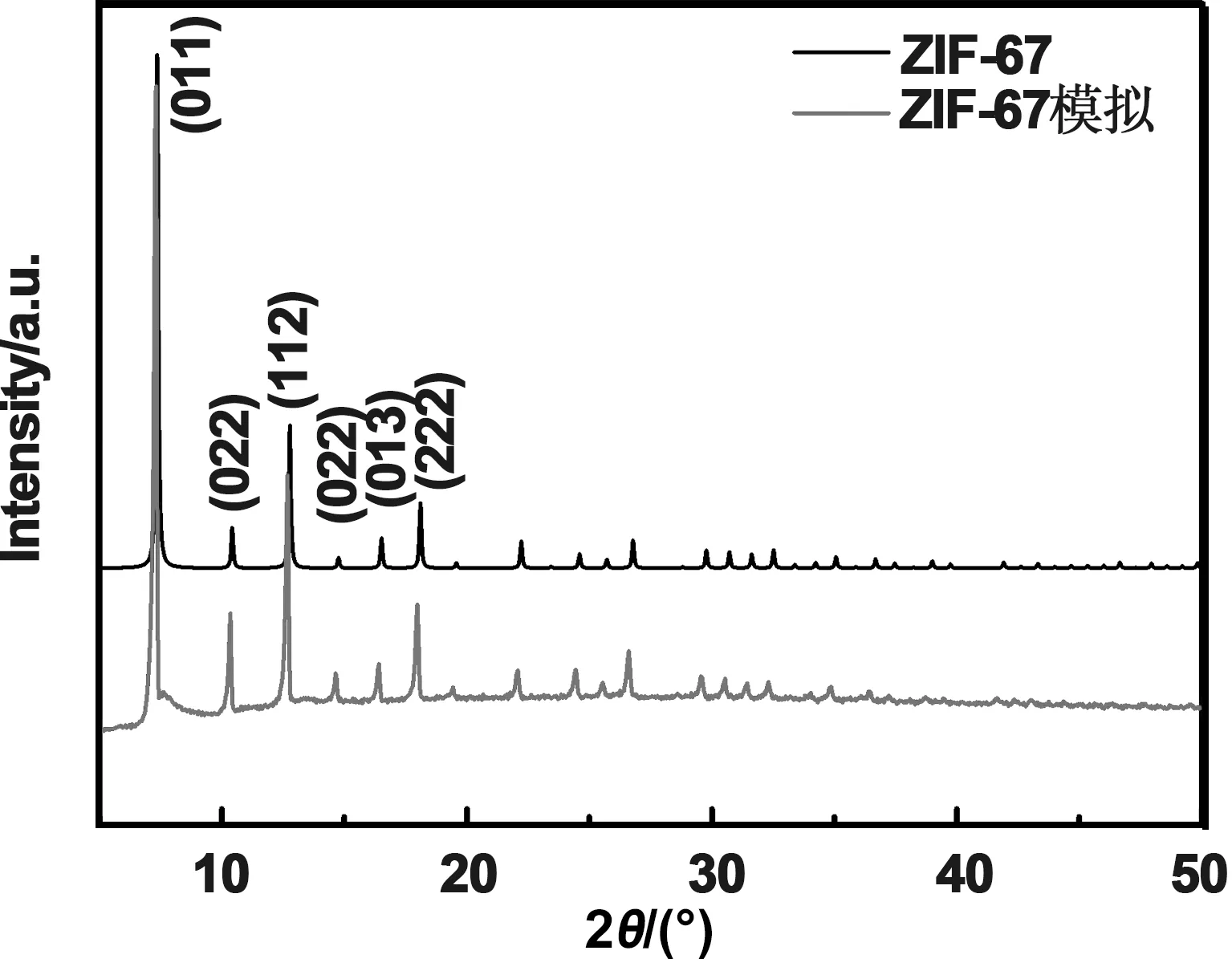
图2 ZIF-67的PXRD图
2.2 ZIF-67的SEM图
图3(a,b,c)是ZIF-67的SEM图。从Fig 3(a)可以看出,可以看出所合成的ZIF-67样品尺寸分布均匀,主要以菱形十二面体单晶体结构为主 (Fig 3(b): A),颗粒直径约为1.5 μm,也存在少量的多晶结构,其尺寸在2.2 μm左右 (Fig 3(a): B, C, D)。图3 (d) 为ZIF-67的EDX图,检测到C,N,Co这3种元素。

图3 (a, b, c) ZIF-67的SEM图,(d) ZIF-67的EDX谱图
2.3 红外分析(FT-IR)
图4为ZIF-67的红外光谱图。2 924 cm-1处的吸收峰是2-甲基咪唑上芳香环的伸缩振动引起的[19],1 612 cm-1处的吸收峰对应于C=N双键伸缩振动,1 350~1 500 cm-1处的谱带可归因于咪唑环的伸缩振动,900~1 350 cm-1的谱带源于咪唑环的平面振动,500~800 cm-1处的谱带由咪唑环的平面外振动引起。红外光谱结果表明:所制备的ZIF-67是由2-甲基咪唑与中心离子配位形成的。
2.4 XPS分析
为了进一步说明所得ZIF-67的化学构成及元素价态,对ZIF-67进行了XPS分析。图5(a)为ZIF-67的全谱图,C(282.6 eV)、O(529.1 eV)、N(397.6 eV)和Co 2p峰均能清晰显示。图5(c)为ZIF-67中咪唑基团对应的N 1s在398.6 eV处的结合能。图5(d)是Co 2p的谱图,796.4 eV和780.7 eV处两处分别对应Co 2p1/2 和Co 2p3/2。XPS结果表明,所制备的ZIF-67中存在2-甲基咪唑和Co2+离子。PXRD、电镜、红外光谱及XPS结果表明所制备的材料为中心离子为Co2+离子,有机配体为2-甲基咪唑的晶体材料。
2.5 吸附性能
本实验通过改变pH、吸附时间和重金属离子浓度等因素,研究ZIF-67对Cd2+、Cu2+和Pb2+的吸附性能,所有的吸附实验均在室温25 ℃进行。
2.5.1 pH对重金属离子的吸附影响
溶液的pH对吸附材料的吸附性能具有显著影响,因此,我们研究了pH值与吸附剂吸附量的影响。溶液的pH用1 mol/L的盐酸或者1 mol/L的氢氧化钠溶液调节(pH: 3、4、5、6、7、8和9),吸附剂的量为5 mg,离子浓度为250 mg/L,吸附时间为24 h。如图6所示,随着pH的增大,ZIF-67对Cd2+、Cu2+和Pb2+的吸附量逐渐增大。其中,pH值对Pb2+的吸附量的影响最小,615.7~831.7,变动范围为:216 mg/g,而Cu2+为743 mg/g,Cd2+为716 mg/g,我们推测这可能是由于在形成金属有机框架结构ZIF-67中,有机配体2-甲基咪唑上的-NH-基团没有参入配位,主要配位基团可能是=N-,因此,在pH较低的酸性条件下,2-甲基咪唑上的-NH-形成了-NH2+1-使吸附量降低,除了静电引力外,还存在配位作用,而且对于铅离子配位作用是吸附剂与铅之间的主要作用力,因此,随着pH的增大,吸附量变化较小,而对于Cd2+和Cu2+之间的作用力主要是静电吸引力,因此,随着pH增大吸附量增加显著。考虑到pH对重金属离子在水中存在形式的影响,研究其他影响因素时,选用pH=5作为实验条件。
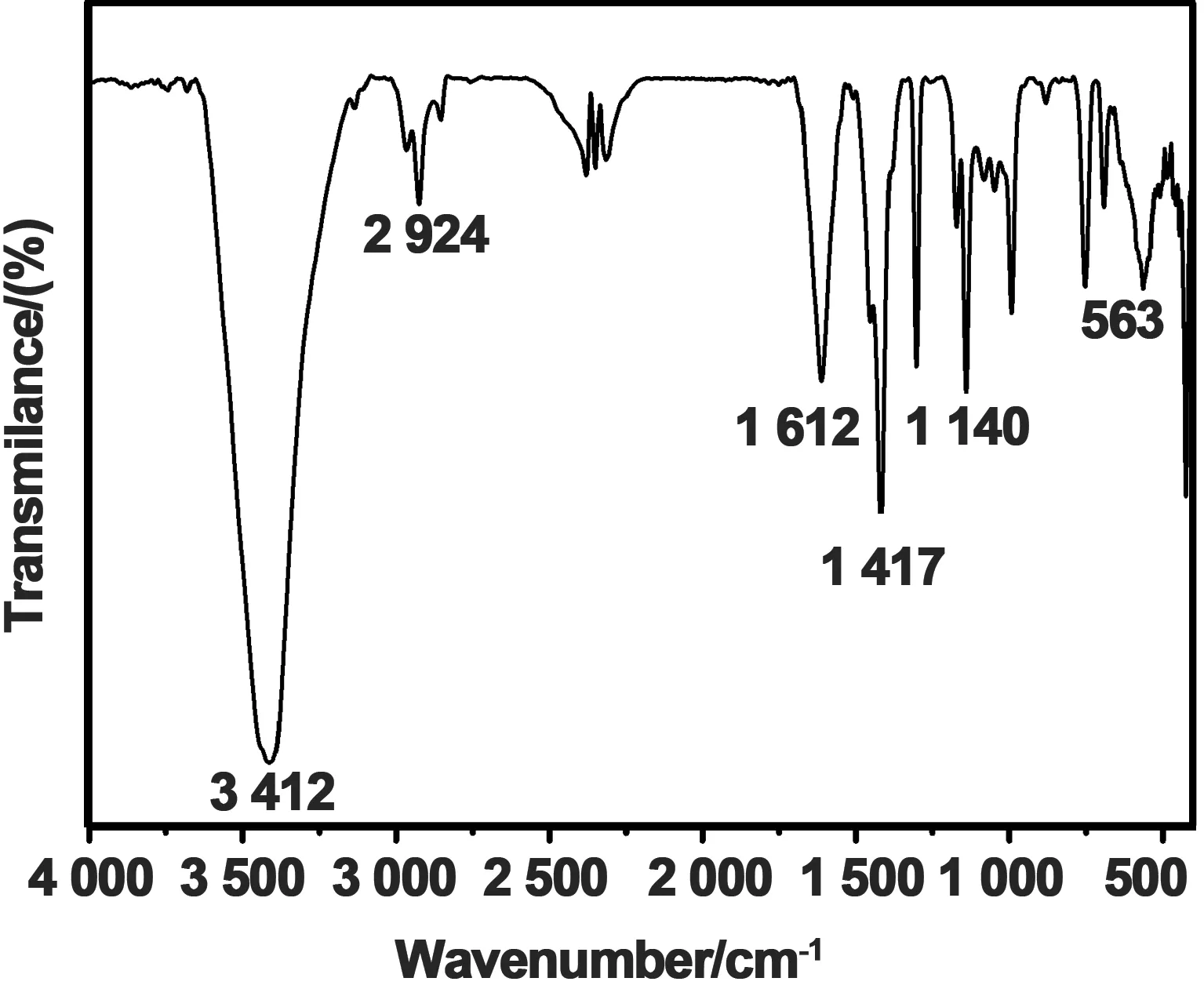
图4 ZIF-67的红外光谱图
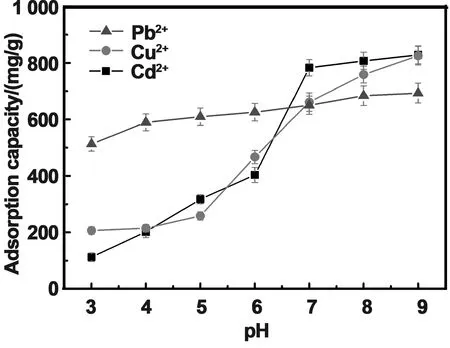
图6 pH对重金属离子吸附性能的影响
2.5.2 吸附时间对重金属离子的吸附影响
吸附时间是衡量吸附效率的主要因素之一,吸附时间对重金属离子浓度的影响的实验条件为:吸附剂的量为5 mg,离子浓度为250 mg/L,吸附时间分别为10,20,30,45,60,90,120,180,240,300,360,480,600和720 min。在吸附时间为180 min时,ZIF-67对Pb2+的吸附量为779.7 mg·g-1,对Cu2+的吸附量为733.8 mg·g-1,对Cd2+的吸附量为564.0 mg·g-1。从Fig.7可以看出:在吸附时间为120 min,Pb2+、Cd2+及Cu2+离子吸附量及达到平衡吸附量的百分率分别为673.9 mg·g-1和86.4%、522.2 mg·g-1和92.6% 及734.2 mg·g-1和100.0%,反映出所制备的ZIF-67对3种离子具有较高的吸附速率。当吸附时间在180 min之前,ZIF-67对Pb2+、Cd2+的吸附量在快速增加。
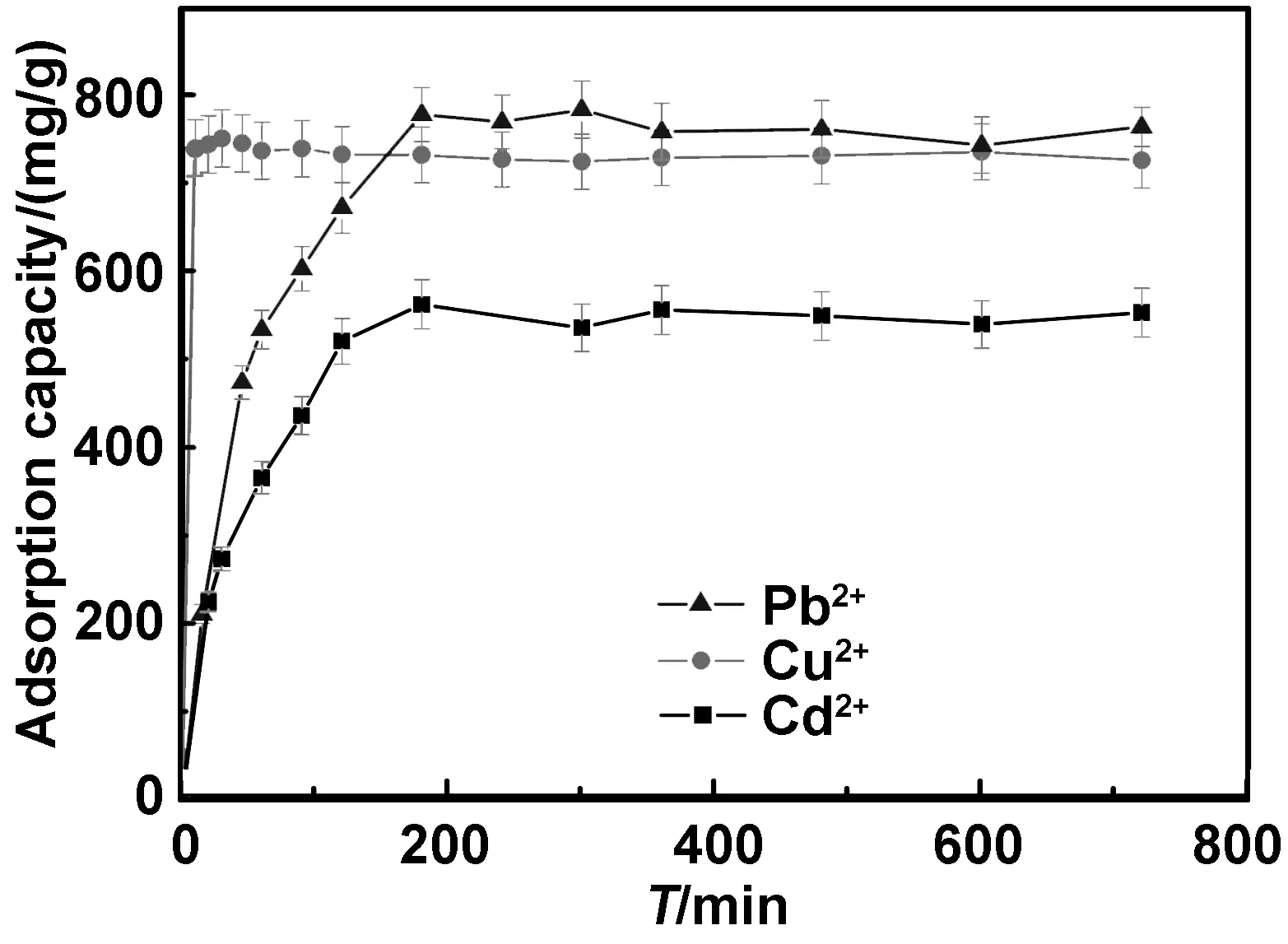
图7 吸附时间对重金属离子吸附性能的影响
2.5.3 初始浓度对重金属离子的吸附影响
为了研究吸附剂最低吸附离子的浓度,我们研究了初始浓度对重金属离子吸附性能的影响。实验条件:吸附剂的量为5 mg,吸附时间为15 h,重金属离子浓度分别为25,50,100,150,200,250和300 mg/L的重金属溶液。从图8可以看出,Pb2+、Cd2+及Cu2+离子的最低吸附浓度25 mg/L下的吸附量分别为:93.8、13.0及32.1 mg/g,显示ZIF-67对Pb2+离子在较低的离子浓度下仍然具有较大的吸附量。当重金属离子浓度达到250 mg·L-1时,ZIF-67对其吸附量趋于稳定。此时,ZIF-67对Cu2+的吸附量为236.1 mg/g,对Pb2+的吸附量为729.2 mg/g,对Cd2+的吸附量为425.5 mg/g。
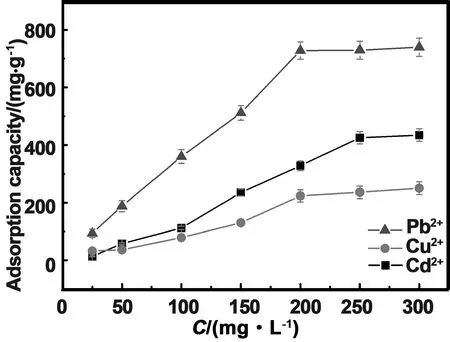
图8 初始浓度对重金属离子吸附性能的影响
2.5.4 吸附性能比较
表1为文献中报道的不同吸附剂对不同重金属离子吸附性能的比较。由表1可知,本工作合成的ZIF-67材料对重金属离子具有优异的吸附效果。
表1不同吸附剂对不同重金属离子吸附容量的比较
Table1Comparisonoftheadsorptioncapacity(mg/g)ofdifferentheavymetalionswithotheradsorbents
3 结 论
用甲醇作为溶剂在较短时间(8h)室温条件下制备了ZIF-67材料,XRD、电镜、红外光谱及XPS结果表明所制备的材料为中心离子为Co2+离子,有机配体为2-甲基咪唑的晶体材料,中心离子与2-甲基咪唑的配位结构中仍然保留了-NH-基团。吸附实验表明:pH值对吸附量具有显著影响,其中铅离子对pH响应性最低,我们推测铅、镉及铜与ZIF-67之间的作用力为静电作用力和配位键,其中铅离子与ZIF-67之间主要以配位键为主要作用力。ZIF-67对Pb2+、Cd2+和Cu2+具有较快的吸附速率,对铅离子的具有最低吸附浓度。制备的ZIF-67材料将有望应用于移除水体中的重金属离子。

