环状拓扑聚合物在药物载体领域的应用
贾娟英,卞 清,孙 魄,申克静
(安徽工业大学 工程研究院现代分析测试中心,安徽 马鞍山 243032)
0 引 言
在生物医学范畴内,针对人体循环系统复杂化、病灶部位多样化、多种药物协同释放特异化等特点,针对不同患者、不同疾病、不同药物,往往需要特定的给药系统用于高效的药物释放和针对性的疾病治疗[1-2]。因此,如何运用药物载体将药物准确输送到病灶部位,并定时定量释放药物,成为生物医学研究的一项重要课题[3-4]。两亲性嵌段共聚物自组装胶束是目前研究最多的药物载体之一[5]。然而胶束给药系统在血液循环中的稳定性仍然面临巨大的挑战,因为载药胶束必须表现出足够的稳定性,才能在极端稀释、盐、pH等急剧变化、及与血液中的生物分子的相互作用下存留下来,这对于减少靶外相关副作用和促进体内长效循环至关重要[6]。
影响聚合物胶束稳定性的因素有很多,如聚合物的组成,封装药物的特性、环境因素等,聚合物的组成作为其固有性质通常起决定性的作用[7-8]。除了聚合物组成外,聚合物的高级拓扑结构,如环形、星型、超支化等结构对纳米材料的自组装行为和性能有着重要影响[9]。随着环状聚合物材料的不断发展,不断有研究表明环状聚合物自组装体的稳定性远高于同类线性聚合物自组装体,这为环状聚合物在提高药物载体稳定性领域的应用提供了可能,环状聚合物或将成为代替传统两亲性胶束药物载体的新材料。
环状聚合物是一类特殊的拓扑结构聚合物。与相同分子量的线性聚合物相比,环状聚合物由于缺少聚合物链末端而具有许多特殊的物理化学性质,无论是在其本征结构下还是在其溶液状态下,均可表现出不同于线型聚合物的特殊物理化学性能,如较快的结晶速率,较小的旋转半径,较高的折光系数,较高的临界溶解温度和玻璃化转变温度,及较低的本征粘度和水力学体积等[10-12]。
环状聚合物从分类上可以分为单环聚合物和多环拓扑聚合物。合成单环聚合物的方法主要有两种:扩环法[13]和闭环法[14]。扩环法是利用向活性环中插入小型环状单体,使得分子量不断增加而得到环状聚合物;闭环法是通过线型聚合物末端官能团反应成环制备环状聚合物。环状聚合物优于线型聚合物的特殊性质激发了科学家对更复杂环状拓扑结构的研究兴趣,通过结合可控活性聚合与点击化学技术,各种具备精致完美结构的环状聚合物被制备出来,如蝌蚪形,水母形,太阳形,8字形等[15-16]。环状聚合物独特的结构和物理性质已经被广泛应用于化学方法学、生物学、超分子自组装等领域。近年来环聚合物的合成已经取得了重大研究进展,但对其生物特性和潜在的生物医学应用的探索却相对滞后,目前环状聚合物的生物特性和生物医学应用主要集中在生物降解[17]、荧光[18]、超分子自组装[19]、药物载体[20]、基因向量[21]等领域(图1)。本文综述了近年来环形聚合物及其衍生物在药物载体方面的研究进展,并对这一快速发展领域的未来发展进行展望。
1 环状拓扑聚合物的合成
1.1 单环聚合物的合成
在环状拓扑结构聚合物中,单环聚合物是研究最多也是最简单的一类聚合物。单环聚合物合成方法分为两种[22-24]:一种是官能化线性前驱体通过偶联反应生成环状物,称为闭环法;另一种是通过单体插入活化的环状链生成产物,称为扩环法。
闭环反应通常是在极低浓度下,通过使用催化剂在一定时间内促进单分子偶联反应形成环状产物。闭环法根据分子形态的不同又可细分为分子间闭环反应与分子内闭环反应。分子间闭环主要是由含有相同末端基的分子链段与不同分子链段间的偶联关环反应,为了规避多分子间的副反应,闭环反应中反应物精确的化学计量对获得高纯度产物至关重要,因此常控制反应在极稀浓度、等摩尔官能团条件下进行[25-26]。江明等[27]利用蒽与葫芦脲之间的主客体相互作用,合成了两端为蒽的线性聚乙二醇共聚物,该共聚物与葫芦脲在极稀的条件下可进行超分子自组装。由于亲疏水作用,聚乙二醇末端的蒽进入葫芦脲的空腔之中,形成环状超分子聚合物前驱体,在紫外光的照射下(365 nm),蒽形成二聚体,得到稳定的超分子环状聚合物。
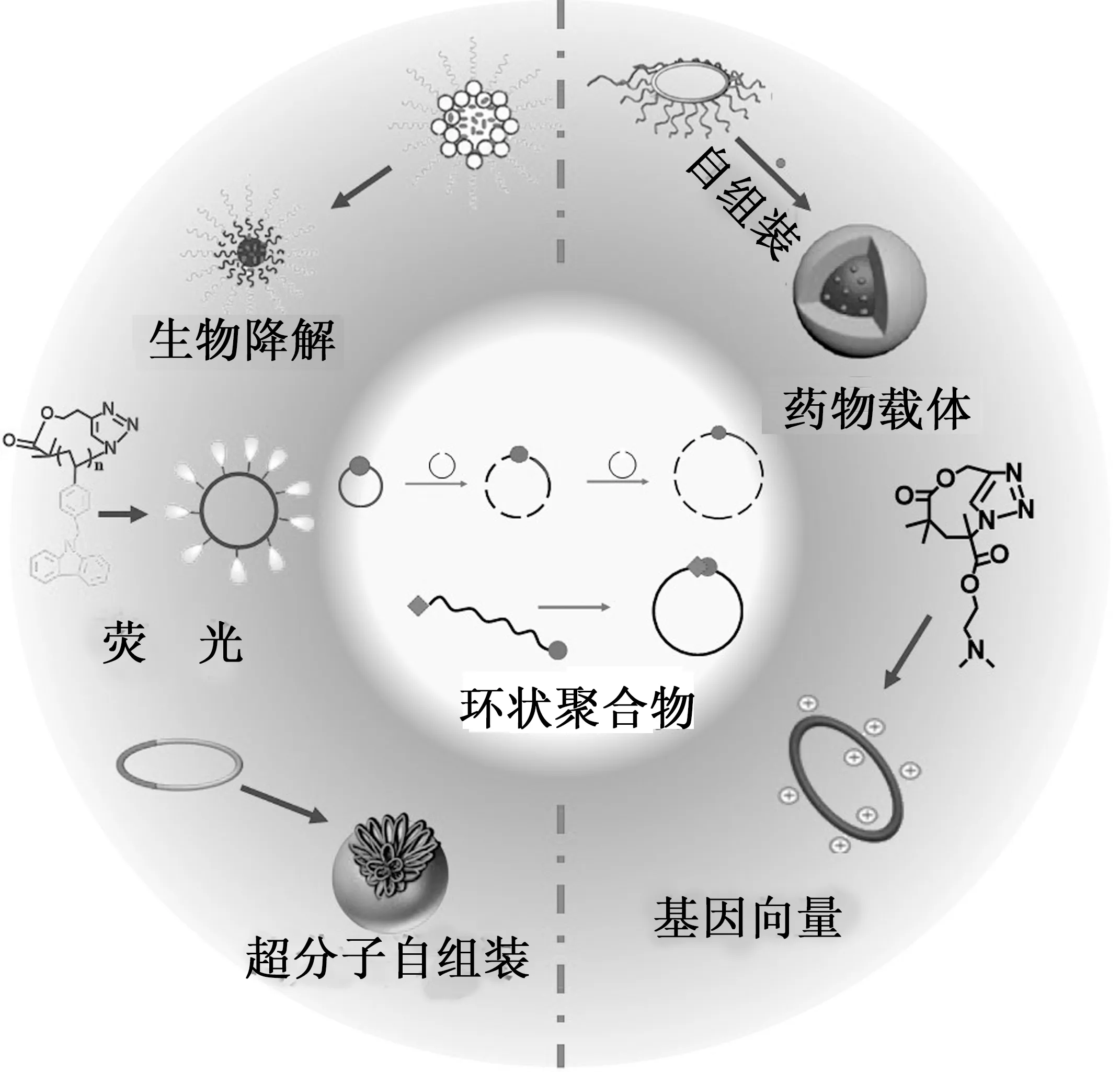
图1 环状聚合物的生物性能和生物医学应用分类示意图[17-21]
Grubbs等[29]首次报道了使用钌基易位聚合催化剂催化1,5-环辛二烯单体聚合合成环状聚丁二烯高聚物,这一工作成为最早合成超高分子量环状聚合物的重要方法。此外Grubbs课题组还合成了一种环状钌基复合催化剂,用于制备基于顺环辛烯单体的环状聚合物[30]和超高分子量的环刷形聚合物[28],研究证明,催化剂活性越高,单体在短时间内的转化率也就越高,因此,使用高活性催化剂通过环扩张易位聚合法可成功制备高分子量环状聚烯烃[31-33]。但是扩环聚合获得的聚合物成分较为复杂,因此提纯分离工作繁琐,且分子量分布较宽,不易获得单分散环状聚合物,另外小分子环状引发剂一般需要在前期多步合成,且环状小分子引发剂种类较少,因此限制了扩环聚合法的应用。

图2 蒽与葫芦脲形成超分子环状聚合物示意图[27]
1.2 多环聚合物的合成
除单环聚合物外,人们对复杂结构的多环拓扑聚合物(如蝌蚪形、数字8形、θ形、环状梳形聚合物等)的研究越来越感兴趣。这些多环拓扑聚合物多通过原子转移自由基聚合(ATRP)、开环聚合(ROP)和点击化学反应制得[34-36]。
Liu[37]等通过叠氮化反应和ATRP反应制备具有8个末端叠氮的八臂星型线性聚苯乙烯,在点击化学反应条件下,将双官能偶联剂—炔丙基醚加入到星形—线形聚合物的极稀溶液中,制备含有多面体低聚倍半硅氧烷(POSS)核的四叶草星型-环状聚苯乙烯聚合物,如图3所示。
环刷形聚合物是一类新型环状拓扑结构聚合物,zhu xiulin[38]等通过ATRP、点击化学和Suzuki偶联反应相结合,合成聚(苯乙烯(4-甲氧基苯基))环刷形聚合物,该方法为研究环刷形聚合物及其他复杂环状拓扑聚合物提供了新的合成思路。
2 环状拓扑聚合物在药物载体领域应用
水溶性聚合物的长效循环时间是药物成功递送到肿瘤细胞的关键。聚合物在体内的循环时间取决于聚合物分子量和聚合物结构。线性聚合物通过聚合物链的端到端运动穿过纳米孔,由于线性聚合物只需要一个聚合物端基进入纳米孔就可以转运,所以线性聚合物比星形聚合物更容易穿过纳米孔;环型聚合物由于缺少链端,所以需要两个链段同时进入纳米孔中才能转运。因此,环状聚合物在体内的分子行为将有别于相同分子量的线性聚合物。Szoka[39]运用ATRP和点击化学合成了四对具有相同分子量且分子量分布较窄的环状和线性聚丙烯酸接枝聚乙二醇聚合物(PAA-PEG),环状聚合物形成的载药胶束在与线性类似物相比,具有更长的体内循环时间和更高的肿瘤部位堆积。该研究证明了相同分子量时环状聚合物拓扑结构显著增加了循环时间和肿瘤吸收,因此,环状聚合物有望成为代替传统两亲性药物载体的替代结构[20,39]。
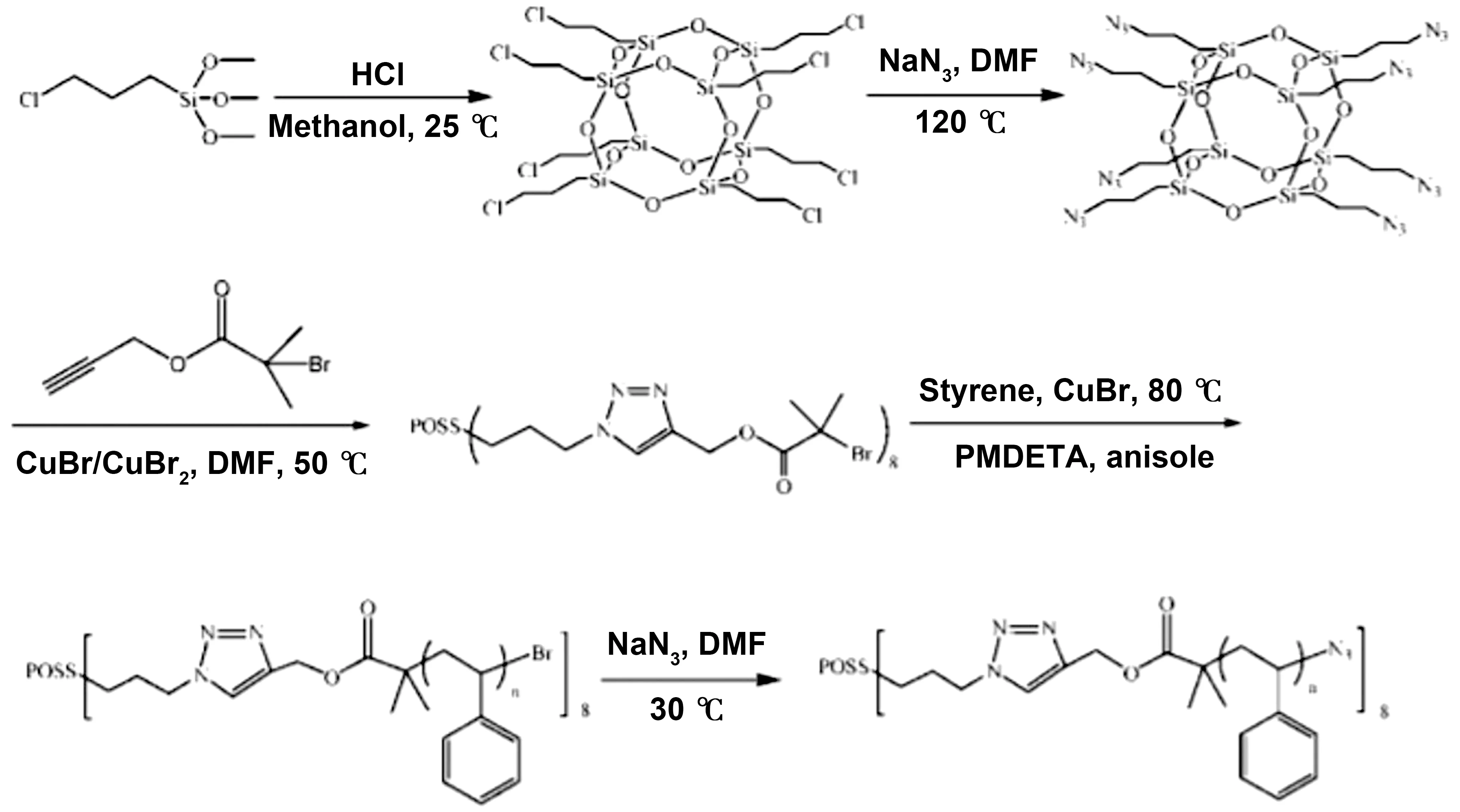
图3 八臂星型线性聚苯乙烯的合成示意图[37]

图4 环刷形拓扑聚合物合成示意图[38]
与线性聚合物相似,环状聚合物的分子量(Mw)和分子量分布(MWD)对其潜在的生物医学应用也有重要影响,如细胞毒性、装载药物的运载效率、肿瘤穿透能力等。Liu[40]等人通过氯单体的开环聚合直接引发具有单羟基功能的环状聚异丙基丙烯酰胺(PNIPAM)前驱体,合成了一种由线性聚己内酯(PCL)疏水链和温敏性PNIPAM大分子环构成的两亲性温敏线性和“蝌蚪状”环状二元嵌段共聚物。与线性二元嵌段共聚物((l-PNIPAM)-b-PCL)相比,温敏性环状二元嵌段共聚物((c-PNIPAM)-b-PCL)自组装胶束具备更低的低临界相转变温度。具有相似分子量和分子量分布的(c-PNIPAM)-b-PCL(Mn=1.24 kDa,PDI=1.10)比(l-PNIPAM)-b-PCL(Mn=1.28 kDa,PDI=1.12)具有更高的药物负载量且药物释放得更快。体外细胞毒性实验表明(c-PNIPAM)-b-PCL聚合物浓度高达1.0 g/L时对细胞仍没有毒性,而聚合物胶束在相同浓度下会造成60%的细胞死亡。
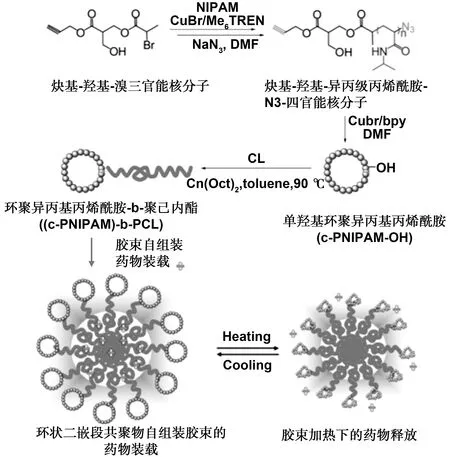
图5 环二嵌段共聚物(c-PNIPAAm)-b-PCL的合成及其自组装体的药物装载与释放示意图[40]
Pun[41]课题组最近报道了葵花形聚合物的设计和合成。首先,他们将环状大分子引发剂作为内核,然后通过原子转移自由基聚合方法(ATRP)聚合亲水性“花瓣”。通过控制聚合反应时间,制备低分子量分布(PDI为1.2~1.3)和粒子尺寸可控的纳米聚集体结构,如图6所示。在此基础上,将常用的癌症靶向配体—叶酸,键合至花瓣末端,并将一种药物模型—荧光素键合在环状内核上,以此证明太阳花形聚合物的可功能化。研究发现,叶酸-葵花形聚合物-荧光素(FA-SF-荧光素)在两种细胞系(FR+KB、FR-A549)中的摄取量均与其剂量有关,并且在FR+KB细胞系中的摄取量较高,这说明在FR+KB细胞系中由叶酸受体介导的内吞作用是叶酸靶向花形聚合物的主要摄取机制。有趣的是,在梳形聚合物(FA-梳形聚合物-荧光素)存在的条件下,其与自由叶酸竞争,即使在聚合物浓度很低的条件下,梳形聚合物在KB细胞系中的摄取也只产生小幅下降,这可能说明该类聚合物比花形聚合物的非特异性摄取水平更高。
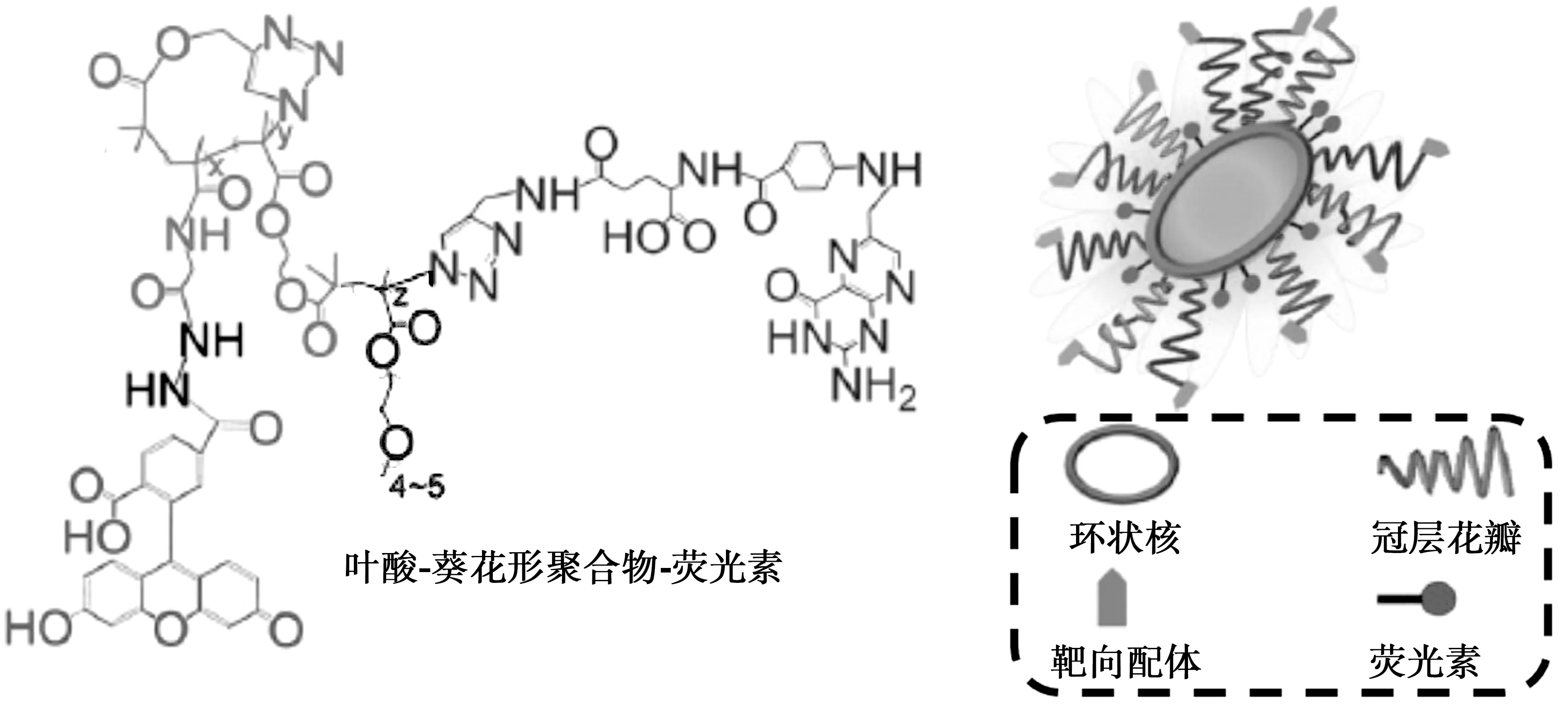
图6 键合了靶向配体和药物的葵花形聚合物分子结构及其示意图[41]
涂晓燕等[42]通过ATRP和点击化学制备了由疏水的环状聚2-羟乙基甲基丙烯酸酯(PHEMA)和温敏性聚合物聚异丙基丙烯酰胺P(NIPAAm)组成的环状刷形聚合物—聚(2-羟乙基甲基丙烯酸酯-g-聚(N-异丙基丙烯酰胺-st-N-羟乙基丙烯酰胺))(cb-P(HEMA-g-P(NIPAAm-st-HEAAm))),还同时还制备了作为对照的组成相同的瓶刷形聚合物(bb-P(HEMA-g-P(NIPAAm-st-HEAAm)))。通过优化两种单体的比例,可将共聚物的LCST值调节至稍高于37 ℃同时低于40 ℃,实现了肿瘤热引发的聚合物载体去稳定化,达到定位药物释放的目的。考察了环状刷形聚合物和瓶刷形聚合物的稳定性、相转变行为、体外释药和细胞毒性等性能。与瓶刷形共聚物相比,环状刷形共聚物形成的单分子纳米粒子具有更好的稳定性;体外释药结果表明,40 ℃时药物快速从环状刷形聚合物自组装纳米粒子中释放出来,说明由高热引发的结构去稳定化和聚合物聚集明显地促进了药物释放。体外细胞毒性实验表明,载药环状刷形聚合物对HeLa细胞表现出比瓶刷形聚合物更高的体外细胞毒性。
为了提高环形聚合物刷的药物负载能力,涂晓燕等[43]通过在环状大分子引发剂聚PHEMA内核上接枝生物相容性较好的疏水聚己内酯(PCL)壳层和亲水聚寡聚(乙二醇甲基丙烯酸酯)(POEGMA)冠层,制备了一种新型核-壳-冠(CSC)结构的两亲性环状刷形共聚物P(HEMA-g-PCL-POEGMA)。主要考察了亲水链段POEGMA为不同链长时,聚合物自组装胶束的稳定性和粒径变化情况,P(HEMA-g-PCL-POEGMA)载药后,载药率提高至4.60%,说明制备的两亲性环状刷形共聚物具有提高抗癌药物负载的能力。

图7 温度敏感型环状刷形共聚物的合成及其自组装载药胶束的相转变示意图[42]
对于单分子胶束而言,环刷形聚合物比瓶刷形聚合物展示出了更为优越的分子稳定性,因此对于药物释放系统来说,环刷形聚合物展现出了更好的应用潜力[43-44]。受到环刷形聚合物结构可提高单分子胶束稳定性这一现象的启发,两亲性两嵌段共聚物的分子内环化成为制备两面型聚合物一种全新的策略。基于此,Liu[20]等通过ATRP、链内点击环化技术(intra-chain click cyclization)、及开环聚合技术(ROP)相结合的方法将疏水的寡聚已内酯单元(HEMA-g-OCL)与亲水的寡聚乙二醇单元(OEGMA)均接枝在了环状内核上,成功地构建了一个两面型的聚合物分子—Cyclic P(OEGMA)-b-P(HEMA-g-OCL),并对其自组装行为及载药性能进行研究。该聚合物能自组装成环状胶束,有趣的是,合成的两面环刷形两亲性嵌段共聚物的体外细胞毒性比瓶刷形类似物更强,这说明这样一个两面环刷形两亲性嵌段共聚物是一种新型的药物控释平台,为构建两面型纳米粒子提供了一个新的思路。

图8 环刷形两亲性二嵌段共聚物自组装过程[20]
受环状拓扑位阻的启发,Wang Yunfei[45]等设计了一种具有环状亲水分子和线性疏水段的两亲性嵌段共聚物,并研究了环状拓扑结构对自组装胶束稳定性的影响。由于其良好的可聚合性,聚甲基丙烯酸寡聚乙二醇酯(POEGMA)被选为亲水性链段,聚己内酯被选为疏水链段;然后合成蝌蚪状的两亲性嵌段共聚物环状聚甲基丙烯酸寡聚乙二醇酯嵌段聚己内酯 (c-POEGMA)-b-PCL(C)和线性聚甲基丙烯酸寡聚乙二醇酯嵌段聚己内酯(l-POEGMA)-b-PCL(L)聚合物,并进一步比较了自组装胶束在临界胶束浓度下的稳定性,胶束大小,体外载药量和药物释放特性,以及体外细胞毒性等。结果表明自组装的环状胶束比线型类似物具有更好的稳定性,CMC胶束尺寸较小,体外释药速度较慢,对HeLa和A549细胞的体外细胞毒性较低。因此,这项工作表明,由于拓扑增强的空间位阻和包装行为,环状亲水分子可以为自组装的胶束提供额外的稳定性,这为制造聚合物胶束提供了一种替代方法,以增强药物递送应用的稳定性。
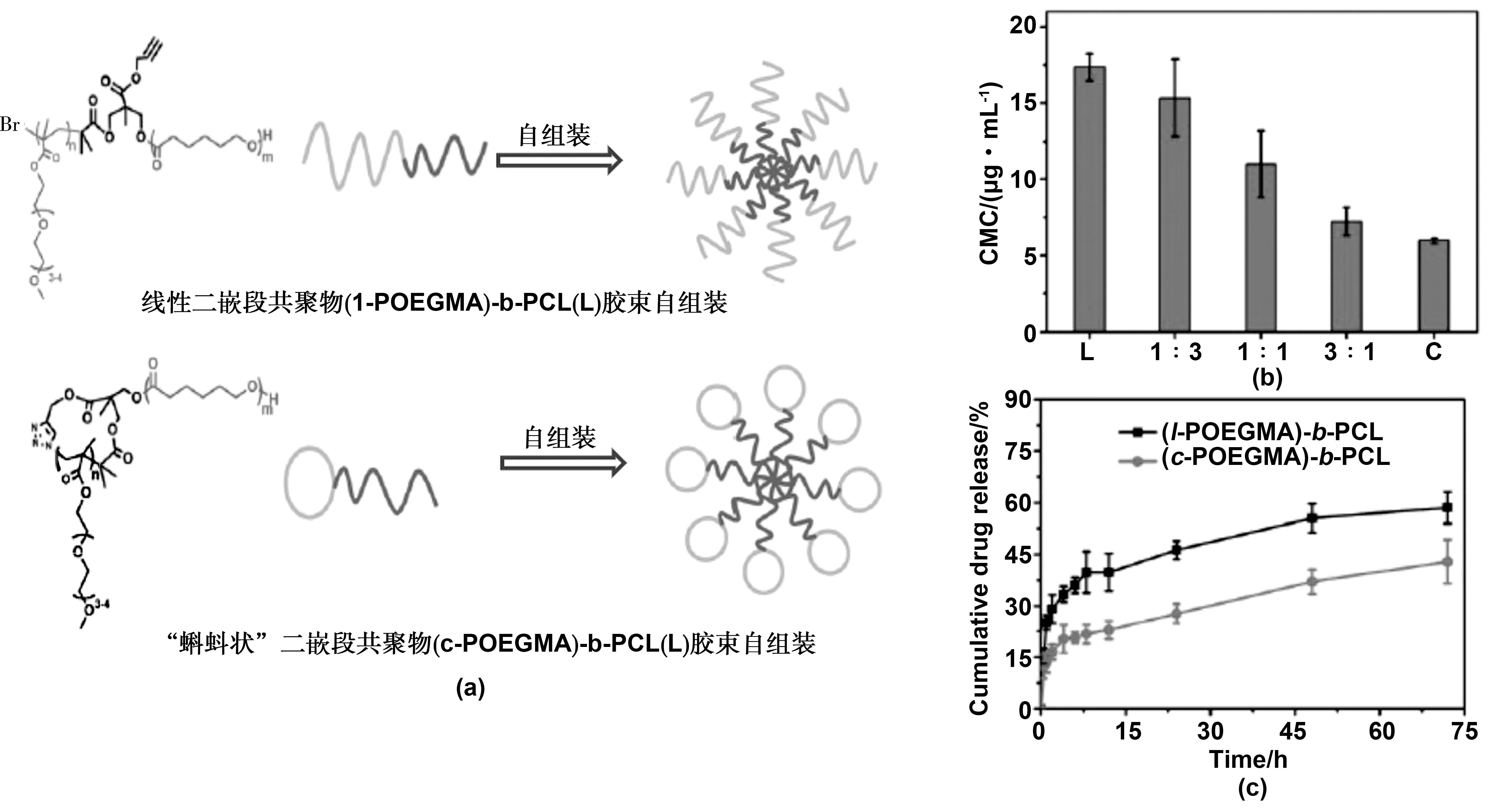
图9 (a)两亲性嵌段共聚物(l-POEGMA)-b-PCL和(c-POEGMA)-b-PCL的分子结构及自组装过程;(b)胶束的临界胶束浓度;(c)两种胶束的体外药物释放情况[45]。
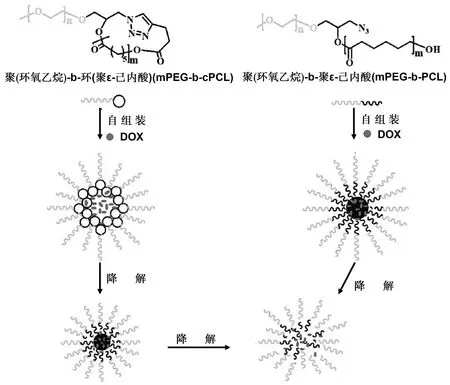
图10 “蝌蚪形”环状、线形嵌段共聚物结构、自组装性能和降解性能示意图[17]。
聚合物拓扑结构对其性能有着重要的影响,拓扑及其衍生结构被证明在药物传递应用方面优于传统的线性类似物。然而,对疏水环组成的两亲性蝌蚪状共聚物的研究并不多见。Guiying Kang[17]等利用ROP技术与点击化学技术合成了蝌蚪状的两亲性嵌段共聚物—聚(环氧乙烷)-接枝-环(聚ε-己内酯)(mPEG-b-cPCL),并制备了一种高稳定性、慢降解速率、高药物装载能力的胶束粒子。本研究揭示了疏水分子对自组装胶束性能的拓扑效应,并开发了一种通过引入环状疏水分子链段来增强胶束稳定性的补充选择。
3 结 语
近年来,在高分子成环反应方面出现了许多新的方法,还有很多有值得一试的新的思路,这些都极大的拓宽了合成环状大分子的道路。但是,从总体上讲,由于大分子成环在热力学和动力学上均较难进行,大多数此类合成还是在极低的浓度下进行的。这极大的限制了环状聚合物在实际应用领域的发展,因此,环状聚合物的合成仍有很大的发展空间,值得人们去继续探索。虽然目前一系列的环状聚合物被不断合成出来,但它们的结构-性能-功能之间的关系及其潜在的应用前景还有待进一步研究。目前,本文综述的一些研究已经初步展示出环状聚合物在生物医学领域具有独特的性能和潜在的医学应用,但一些复杂的机理和药物释放机制还不甚明确,因此,我们有理由相信,刺激响应性环状聚合物的制备将是一个活跃的研究领域,它将在生物医学领域创造出性能更为优越的新型材料。

