血清铁调素-25水平与2型糖尿病肾病中肾功能不良进展的相关性研究*
刘岳鹏
(徐州市中心医院中心实验室,江苏徐州 221000)
糖尿病肾病是糖尿病微血管并发症之一,一旦发生往往不可逆转,最终在较短时间内进入终末期肾病,是成人慢性肾衰竭原因中最重要的单一因素[1],病情进展到后期肾功能严重受损时表现为血清肌酐显著增加[2],患者需要肾替代疗法(肾透析或者肾移植)。通过阐明糖尿病肾病发生发展的危险因素,早期发现糖尿病肾病,进而采取综合措施干预,可以延缓糖尿病肾病的进展,提高患者的生活质量[3]。其中某些与肾脏病变密切相关的,能够反映糖尿病肾病病情进展的因子可作为预测因子为治疗评价提供依据[4]。
铁调素是维持机体铁稳态的调节因子,铁调素-25是其主要活性成分,其作用是下调血清铁水平、负性调节铁吸收、调节铁循环再利用以及铁释放等生理过程。铁调素由肝脏合成产生以后释放进入血液循环,最后经由肾脏排泄,因此,随着肾脏病变的进展,铁调素在慢性肾脏病患者体内形成不同程度蓄积,进而引起铁代谢障碍和/或机体促红细胞生成素(EPO)的低反应性,最终引起或加重患者贫血[5],而贫血又通过多种可能的途径造成糖尿病肾病的不良结局,所以血清铁调素-25可能参与糖尿病肾病的进展,并可作为糖尿病肾病进展的预测因子。
本研究采用巢式病例对照研究设计,目的在于确定铁调素-25是否与2型糖尿病肾病不良进展之间有相关性,为后续将其发展为一个预测2型糖尿病肾病不良进展的因子奠定基础。
1 资料与方法
1.1一般资料 本研究数据来源于徐州市中心医院建立的“糖尿病肾病队列”,该队列收集了2010年以来在徐州市中心医院住院的所有诊断为2型糖尿病肾病的患者,入院同时留取血液和尿液存储在-80 ℃备用。从该队列中选择符合纳入标准的患者进行数据分析。纳入标准:2型糖尿病肾病患者;患者来源于徐州及周边地区;诊断为2型糖尿病型肾病;年龄≥18岁。排除标准:接受过肾移植;终末期肾病;出现糖尿病急性并发症及合并妊娠、痛风或肿瘤;出现急性肺部感染。本研究经本院伦理委员批准,患者均签署书面知情同意书。共220例2型糖尿病患者的资料纳入分析(个别项目多于或少于220例),患者入院时间为2015年4月至2019年6月。以肾小球滤过率(GFR)中位数[51.8 mL/(min·1.73 m2)]为界,将患者划分为GFR低和高水平两组,每组例数是84例,数据部分缺失导致GFR高低分组的总例数少于纳入研究人群的总例数。
1.2仪器与试剂 铁调素-25ELISA试剂盒(德国DRG公司)、EPO ELISA试剂盒(美国Fitzgerald公司)、全自动生化分析仪ADVIA 2400(德国西门子)、糖化血红蛋白分析仪DCAVantange(德国西门子)。
1.3方法 血清铁调素-25水平和红细胞生成素水平采用ELISA法进行测定。GFR通过CKD-EPI公式计算。性别、年龄、体质量指数(BMI)、糖尿病患病时间通过患者自述获得或自患者病历获得。其余数据通过检验科生化分析仪器测量获得。临床指标的判定:高血压判定标准为收缩压≥140 mm Hg或舒张压≥90 mm Hg;高血脂的判定标准为空腹三酰甘油水平≥150 mg/dL(1.7 mmol/L)。血清肌酐加倍定义为截至收集资料的日期为止,患者最后一次血清肌酐测量值为初次测量值的两倍以上;开始肾替代疗法定义为截至收集资料的日期为止,患者接受任何形式的透析疗法;糖尿病肾病不良进展定义为患者开始肾替代疗法或者血清肌酐加倍。
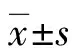
2 结 果
2.1患者临床资料分析 患者年龄中位数为67.1岁,男性占51.80%(114/220);BMI的中位数为29.6 kg/m2;糖尿病患病时间中位数为10年;血清肌酐较患者初次测量值加倍的例数为5例,占2.6%(5/190);开始肾替代疗法的例数为32例,占14.3%(32/224);慢性肾病不良进展例数为37例,占16.7%(37/221)。以GFR中位数为界划分为GFR低和高两组,两组比较,年龄、清蛋白水平、EPO水平、尿蛋白水平、开始肾替代疗法的例数和慢性肾病不良进展差异均有统计学意义(P<0.05)。见表1。
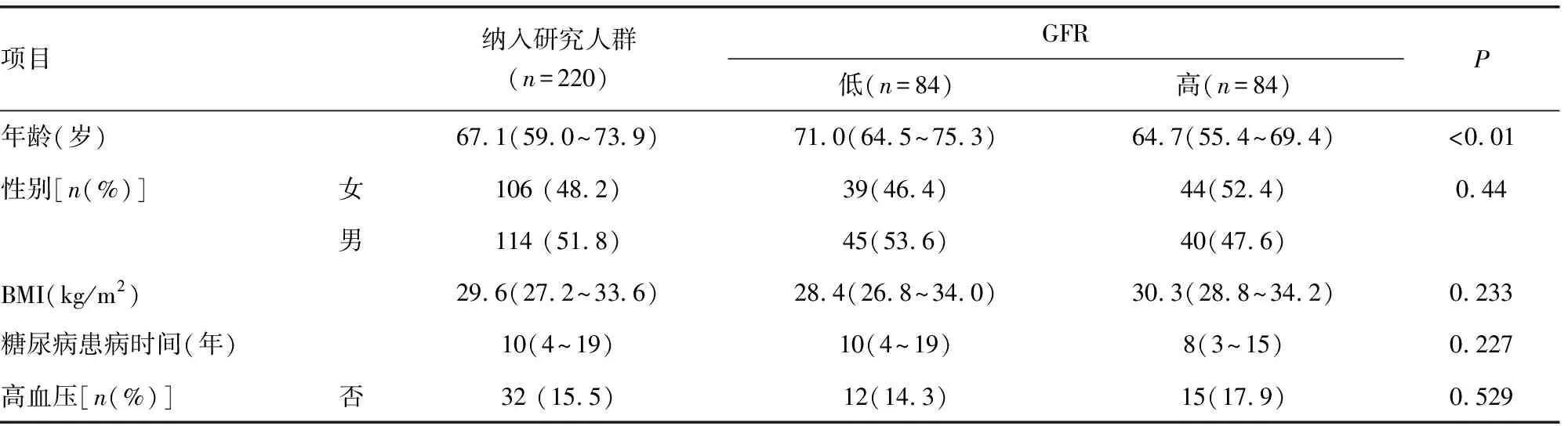
表1 分析过程中涉及的患者一般情况、实验室检查和结局变量描述
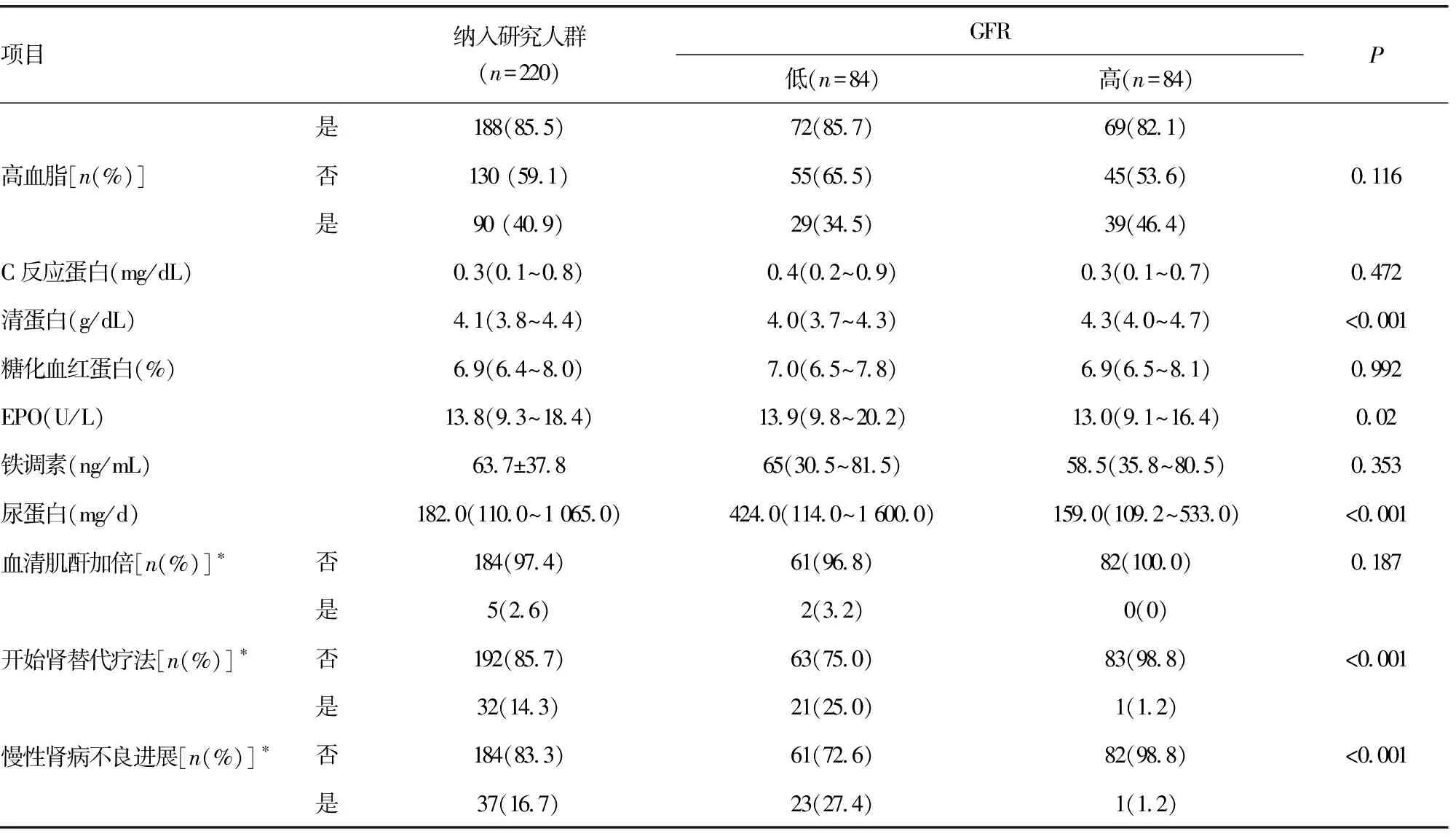
续表1 分析过程中涉及的患者一般情况、实验室检查和结局变量描述

2.2多元Cox回归分析血清铁调素-25与2型糖尿病肾病不良预后之间的相关性 通过多元Cox回归的调整模型调整其他可以影响糖尿病肾病不良预后发生率的因素后,期望揭示血清铁调素-25与糖尿病肾病不良预后之间的相关性并确定其水平。在2型糖尿病肾病患者中,血清铁调素-25不是糖尿病肾病不良结局的相关因素(P>0.05)。铁调素-25若为10 ng/mL,原始模型中HR=1.17,95%CI:1.09~1.27,P=0.000 1;调整模型Ⅰ中HR=1.18,95%CI:0.97~1.45,P=0.097 8。结果变量为肾病不良进展;暴露因素为铁调(10 ng/mL), 调整模型Ⅰ调整了年龄、性别、BMI、糖尿病患病时间、高血压、高血脂、糖化血红蛋白、清蛋白、C反应蛋白、红细胞生成素、铁蛋白和尿蛋白。
2.3GFR、血清铁调素-25与2型糖尿病肾病不良进展的相关性 为了进一步阐述GFR在血清铁调素-25与2型糖尿病肾病不良进展之间相关性中的作用,在GFR高、低两个亚组中考察血清铁调素-25在其中预测糖尿病肾病不良进展中的作用,结果显示在GFR低水平组,调整混杂因素后的多因素Cox回归模型显示,血清铁调素-25与糖尿病肾病不良进展之间呈正相关(HR=2.56,95%CI:1.50~4.40,P=0.000 6),表明的临床意义为血清铁调素-25每增加10 ng/mL,糖尿病肾病不良进展的概率增加1.56倍;而在GFR高水平组,血清铁调素-25与2型糖尿病肾病不良进展之间呈负相关(HR=0.00, 95%CI:0.00~0.21,P=0.016 4),见表3。

表2 GFR是血清铁调素-25与糖尿病肾病不良进展
注:结果变量为肾病不良进展;暴露因素为10 ng/mL铁调素-25; 调整模型调整了年龄、性别、BMI、糖尿病患病时间、高血压、高血脂、糖化血红蛋白、清蛋白、C反应蛋白红细胞生成素和铁蛋白、尿蛋白。
3 讨 论
血清铁调素是体内铁代谢调节的重要激素,被证明与自身免疫性疾病、某些肿瘤和慢性肾病等疾病的进程都有相关性[6]。在糖尿病相关领域中,血清铁调素被证明在2型糖尿病患者中呈低水平表达,而在1型糖尿病患者中表达与健康人无区别[7];此外,其也被证明与糖尿病致慢性肾病的不良进展之间有正相关性[8],以上证据提示血清铁调素-25有潜力发展为临床上预测糖尿病肾病不良进展的指标,为早期干预糖尿病肾病起到提示作用。基于以下两个主要的原因,通过本研究再次确认血清铁调素-25水平与糖尿病肾病不良进展的相关性。第一个原因是之前的研究[8]将1型和2型糖尿病的数据放在一起进行分析,导致结果可能产生偏倚,因为1型和2型糖尿病的发病原因不同,病理生理过程也有较大的区别,与2型糖尿病肾病患者相比,1型糖尿病肾病患者年龄小,BMI偏低,患病的时间较长等;第二个原因是先前研究中研究对象是白种人,其结论是否同样适用于中国人群有待于进一步印证。
在未调整GFR的情况下,多元Cox回归分析的结果显示血清铁调素-25水平与2型糖尿病肾病不良进展之间不存在相关关系,表明铁调素-25不是一个有潜力的2型糖尿病肾病不良进展的预测因子。与相关研究[8]的结论相矛盾,原因推测与前述试验偏倚有关。然而,以GFR作为分层因素的亚组分析的结果(在GFR低的2型糖尿病人群中,血清铁调素-25水平与2型糖尿病肾病不良进展之间存在正相关关系,而在GFR高的人群中,以上关系呈负相关关系),提示GFR对铁调素-25与2型糖尿病肾病不良进展之间的相关关系有重要的影响,相关研究要考察到GFR的影响。2型糖尿病患者在疾病初期GFR高于同年龄非糖尿病的肥胖对照者,这种疾病早期的肾小球高滤过率推测是糖尿病肾病发病的机制之一[9],随着病情的进展,GFR呈进行性下降。根据慢性肾病的GFR分期标准,51.8 mL/(min·1.73 m2)的患者处于G3a期。所以,血清铁调素-25的水平增加提示2型糖尿病肾病不良进展的结论适用于G3a期到G4期(本研究排除了终末期肾病)的慢性肾病患者人群,而在G1~G2期的患者人群中,血清铁调素-25的水平增加提示2型糖尿病肾病不良进展发生可能性低。
另外,以GFR高低分成的两组2型糖尿病肾病患者,在某些数据上也体现出统计学差异,包括年龄、清蛋白水平、EPO水平、尿蛋白水平、开始肾替代疗法的例数和慢性肾病不良进展。由于GFR是反映肾脏功能的重要指标。低GFR代表肾脏损伤重,功能差,造成高水平的尿蛋白、低水平的血清清蛋白,需要进行肾替代疗法。而EPO水平在GFR低的患者中却较高的原因可能是这类患者往往伴有一定程度的贫血,而贫血造成的缺氧状态可能刺激了EPO的升高[1]。在非糖尿病性的慢性肾病患者中的研究也证实GFR一定程度的下降会伴随EPO水平的升高[10]。
本研究可能存在一定的偏倚,特别是将GFR作为分层因素分析的情况下可能存在“限定共享效应”[11]所导致的偏倚。因为GFR下降是慢性肾病中多种原因都可以导致的一种结果,而在GFR低的人群中观察就是在“限定共享效应”的情况下进行。其他偏倚包括患者失访造成数据缺失等。
4 结 论
在整体的2型糖尿病肾病患者中,血清铁调素-25水平与慢性肾病的不良进展之间无相关性,然而在GFR低的2型糖尿病肾病患者中,血清铁调素-25水平升高可能预示肾病不良进展。

