超支化聚合物对羊毛织物的改性研究
杨文丽,王 强,袁久刚,王 平,余圆圆,章金芳
(1.生态纺织教育部重点实验室(江南大学),江苏 无锡 214122; 2.新天龙集团有限公司, 浙江 上虞 312300)
羊毛是一种天然蛋白质纤维,具有蓬松柔软,弹性好等性能,深受广大消费者喜爱[1],但羊毛制品在洗涤过程中易发生严重的毡缩现象[2],影响其服用性能。目前,应用最为广泛的氯化法防毡缩整理对羊毛织物强力损伤大,且产生的可吸附性有机卤化物(AOX)影响人体健康,污染环境[3]。近年来,绿色环保的生物酶法防毡缩加工一直被科研工作者所关注。Kaur等[4]发现酸性菠萝蛋白酶可以在氯化钠存在条件下改善羊毛织物的毡缩性能;张淑梅等[5]将蛋白酶和生物酶活化剂联合使用,使羊毛毡缩性能得到改善。黄玉兰等[6]将蛋白酶处理后的羊毛织物接枝壳聚糖,可提高羊毛织物的防毡缩和抗菌性能。酶法处理羊毛织物能够获得良好的防毡缩性能,但仍存在处理后织物强力损伤大,处理不均匀等问题。
端氨基超支化聚合物(HBP—NH2)含有丰富的氨基,分子之间无缠绕,是一种具有良好水溶性且无固定形状的三维结构树状大分子[7],常用于改善织物性能或赋予新的功能。张峰等[8]将HBP—NH2接枝到高碘酸钠处理的棉织物上,可改善其染色性能。刘艳等[9]发现HBP—NH2改性桑蚕丝织物可提高酸性染料的染色性能,并赋予织物一定抗菌功能。李婷等[10]首先用HBP—NH2制备TiO2纳米线,然后采用浸—轧—烘工艺将TiO2纳米线整理到棉织物上,改善了织物的抗紫外和自清洁性能。新型交联剂三羟甲基磷(THP)常用于固定化酶制备。如Cochrane等[11]采用THP将醇脱氢酶固定到壳聚糖薄膜;Zhang等[12]用THP将大肠杆菌产腈水解酶固定到细胞上。本文探究利用新型交联剂THP通过双向曼尼希交联反应将HBP—NH2共价接枝于羊毛织物,以改善羊毛织物的防毡缩和抗菌等性能。
1 实验部分
1.1 材料和仪器
材料:羊毛织物(105 g/cm2,无锡协新毛纺织股份有限公司),HBP—NH2(实验室自制),弱酸性普拉红B(C.I. Weak Acid Pink B,浙江龙盛化工有限公司),四羟甲基氯化磷(THPC,阿拉丁化学试剂有限公司),氢氧化钾(分析纯,国药集团化学试剂有限公司),营养琼脂、营养肉汤(均为生化试剂,上海中科昆虫生物技术开发有限公司)。
仪器:YH-A速试红外线高温染样机(靖江市远虹印染机械有限公司),Nicolet IS 10傅里叶变换红外光谱仪(美国赛默飞世尔科技中国有限公司),Datacolor 650电脑测配色仪(美国Datacolor公司),MJ-160B-Ⅱ霉菌培养箱(上海跃进医疗器械厂),UV-2802S紫外分光光度计(上海尤尼柯仪器有限公司)。
1.2 实验方法
三羟甲基磷(THP)的制备:取等物质的量四羟甲基氯化磷(THPC)与KOH,分别溶于去离子水,剧烈搅拌下将KOH溶液滴加到THPC溶液中,滴加完毕则反应结束。整个反应在室温下进行。
超支化聚合物(HBP—NH2)整理羊毛织物:羊毛织物放入3 g/L的HBP—NH2溶液中,温度60 ℃,时间1 h,两浸两轧,控制轧余率为80%,水洗晾干后将超支化聚合物处理的织物放入THP溶液中反应15 min,充分水洗,烘干待用。
1.3 测试方法
1.3.1 磷含量测定
参照ISO 3946—1982《淀粉和淀粉制品中总磷的测定 分光光度法》和ISO 2962—1984《乳和乳制品中总磷的测定 分子吸收光谱法》测定羊毛织物上的磷含量。
1.3.2 傅里叶红外光谱
将羊毛纤维剪碎,KBr 压片,采用傅里叶红外光谱仪进行测试,扫描32次,分辨率4 cm-1。
1.3.3 染色性能测试
染色工艺:织物浸入染液→染色(弱酸性普拉红B为1%(owf),pH值4.5,浴比1∶50,温度70 ℃,时间60 min)→充分水洗,50 ℃烘干。
采用测色仪测量织物表面颜色深度,测试条件为10°视角,D65光源,试样折叠4层。分别记录K/S值、L*、a*和b*值。
1.3.4 抗菌性能测试
参照 GB/T 20944.3—2008《纺织品 织物抗菌性能的评价》中附录D和附录A,以振荡法和平皿培养法测定羊毛织物的抗菌性能,所选菌种为大肠杆菌。抑菌率计算公式为:
抑菌率=(1-B/A)×100%
式中A、B分别为整理前、后织物上的菌落数。
2 结果与讨论
2.1 THP处理羊毛织物
羊毛织物和THP处理织物用酸消化,消化液用钼酸铵显色,按照文献[13]方法测试磷含量,结果为:经THP处理织物出现蓝色显色反应,且对应吸光度磷含量为(2.488±1.081) mg/g,未处理羊毛未检出磷。表明THP中的羟甲基与羊毛织物上的氨基发生曼尼希反应,生成P—CH2—N键。
2.2 红外光谱(FT-IR)分析
图1为未处理、THP处理和THP/HBP—NH2处理羊毛织物红外光谱图。

图1 不同工艺条件下的羊毛织物红外光谱图

2.3 HBP—NH2改性羊毛氨基含量测试
HBP—NH2分子中含有丰富的氨基基团,极易溶于水,在不同的pH值条件下,氨基会与氢离子以不同形式结合[15]。因此,可采用酸碱滴定法测试HBP—NH2处理后羊毛织物表面的氨基含量。
THP/ HBP—NH2处理羊毛织物氨基含量为0.980 mmol/g,比HBP—NH2单独处理的氨基含量(0.495 mmol/g)多,说明THP作为桥梁,能够同时与羊毛织物上的氨基和HBP—NH2中的氨基发生双向曼尼希交联反应,从而将HBP—NH2接枝到羊毛织物上。这与图1在1 460 cm-1处出现新峰的分析结果一致。
2.4 HBP—NH2处理织物防毡缩性能和断裂强力
分别采用3 g/L的HBP—NH2和3 g/L的HBP—NH2加0.316 mol/L的THP对羊毛织物进行处理,与未改性羊毛织物进行对比。织物防毡缩性能和断裂强力测试结果如图2所示。
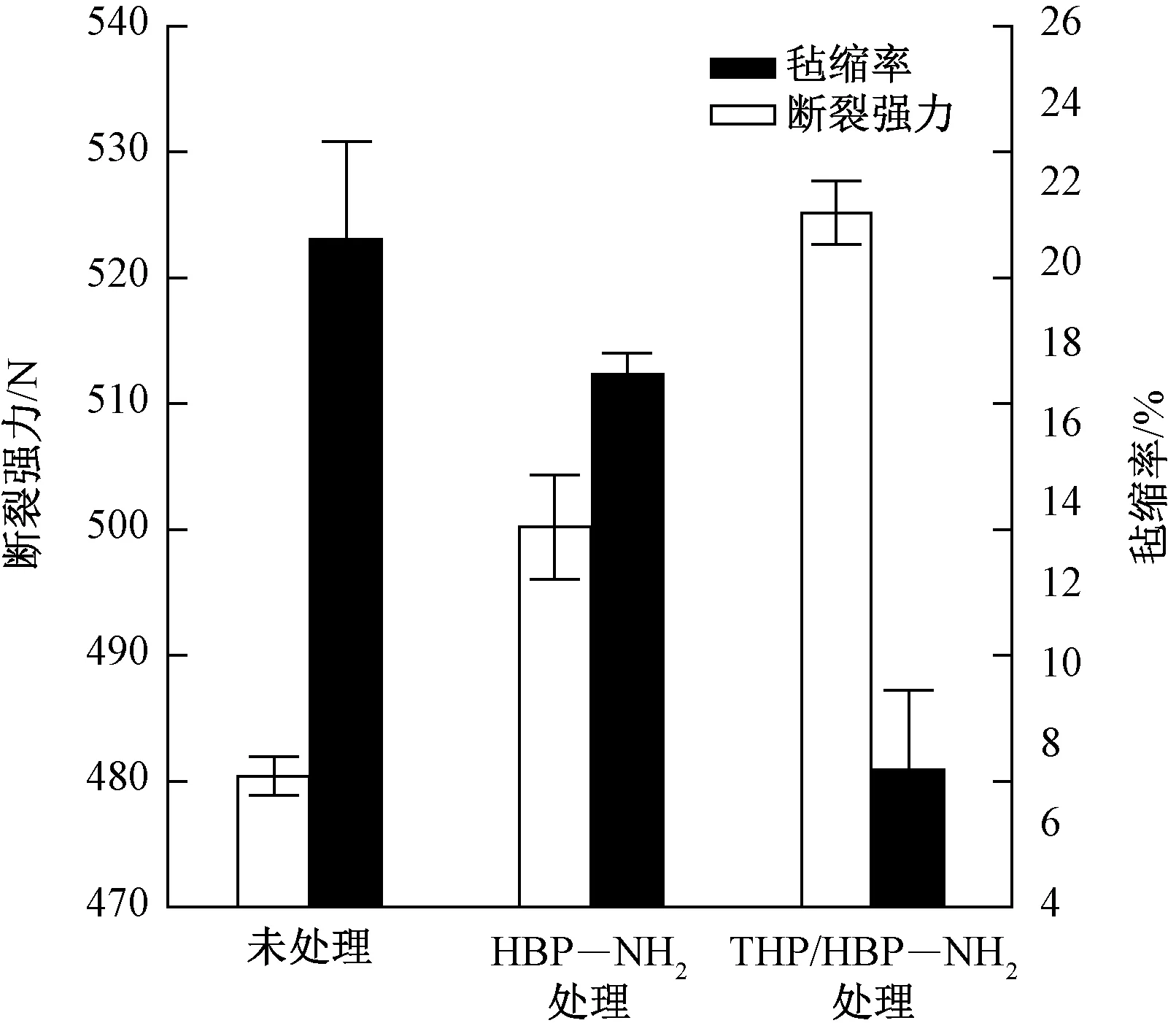
图2 处理工艺对羊毛毡缩率及断裂强力的影响
从图2可以看出,未处理织物毡缩率为20.69%;仅HBP—NH2处理织物毡缩率无明显降低,可见,单独使用HBP—NH2处理织物防毡缩效果有限。THP和HBP—NH2共同处理,织物毡缩率降为7.43%,可以满足机洗标准。这是因为HBP—NH2与纤维大分子产生氢键作用,在羊毛鳞片层表面形成一层薄膜,阻止相邻纤维间的相互咬合,减少纤维间的定向摩擦[6]。单独使用HBP—NH2处理,其只是吸附在纤维表面,耐水洗性能差;而加入THP,除了吸附作用,HBP—NH2能够通过THP作为桥梁,与纤维大分子产生分子间作用,耐水洗性能好。由于HBP—NH2能与纤维大分子形成化学键和氢键,故HBP—NH2处理织物的断裂强力优于未处理织物。
2.5 HBP—NH2改性织物染色性能
羊毛织物染色时,染料先通过鳞片层间隙渗入到CMC(细胞间质)中,再向纤维内部扩散,完成上染[1]。本文对改性羊毛织物在70 ℃下进行低温染色,染色织物K/S值及其他色度指标如表1所示。

表1 不同工艺条件下羊毛织物低温染色性能
从表1可以看出,未处理织物的K/S值低,染料渗透性能差,因为低温条件下,疏水性鳞片层阻碍染料大分子向纤维内部扩散,影响织物的染色性能和渗透性[1];经HBP—NH2处理后羊毛织物K/S值明显高于未处理织物,这是因为,氨基的引入使得羊毛润湿性能增强,溶胀程度增大,有利于染料扩散进入纤维内部,提高织物表面色深和渗透性能;对比HBP—NH2和THP/HBP—NH2处理发现,加THP处理织物的K/S值略低于未加THP处理的织物;因为酸性条件下,THP会部分水解,使发生共价结合的HBP—NH2从纤维上脱落下来,与染浴中的染料结合,导致上染到纤维的染料减少[9];另外,THP处理后织物会变得更加紧密,不利于染料大分子向纤维内部渗透,故渗透性有所下降。
2.6 织物抗菌性能评价
以大肠杆菌为测试菌种,考察HBP—NH2改性羊毛织物的抗菌性能,测试结果如表2所示。

表2 不同工艺改性羊毛织物抗菌性能
从表2可知,经HBP—NH2处理的羊毛织物比未经处理羊毛织物抑菌率高,吸附HBP—NH2的抑菌率为81.35%,而THP/HBP—NH2改性织物的抑菌率92.37%,且都出现明显的抑菌圈,说明HBP—NH2处理后的织物具有良好的抗菌性能。在静电作用下,带正电的氨基会与呈负电性的菌体产生强烈的吸附作用,直接穿透菌体细胞壁,与细胞膜结合并破坏细胞膜,使细胞内物质释放,抑制生长甚至导致其死亡[16]。与HBP—NH2处理的羊毛织物相比,THP/HBP—NH2改性羊毛织物的抑菌率明显提高,表明增加织物表面的氨基含量能够提高羊毛织物的抗菌性能。
3 结 论
①三羟甲基磷(THP)能与羊毛分子中的氨基发生曼尼希反应,并可将端氨基超支化聚合物(HBP—NH2)接枝到羊毛织物上,提高织物表面的氨基含量。
②仅HBP—NH2处理的羊毛织物毡缩率与未处理织物相比有一定程度的下降,但未达到防毡缩的目的;THP/HBP—NH2改性织物的毡缩率下降到7.43%,达到机可洗要求。
③与未处理织物相比,HBP—NH2改性羊毛织物低温染色性能良好,且织物具有较好抗菌性能,抑菌率为92.37%。

