改性沸石制备及其同步去除农田排水氮磷研究
王梦娴,周有荣,李英凯,房云清,秦弋丰,李旭东*
农业面源污染已经成为水环境污染的重要来源[1]。我国第一次污染源调查报告显示,农业源产生的氮、磷已分别占地表水体氮、磷污染负荷的57%和67%[2]。农田排水作为农业面源污染的主要形式之一,具有水质水量时空变化较大、瞬时性强、碳氮比不协调等特点[3],因此不适宜采用传统污水处理技术对其进行处理。现今国内外一般采用植被缓冲带、稳定塘、生态沟渠、生态浮床、人工湿地、前置库、丁型潜坝、反硝化生物反应器[4]等措施对农田排水中面源污染物进行拦截和去除。如朱金格等[5]在太湖水源地陆域保护区构建生态沟-湿地系统对涵盖施肥期的农田尾水进行了拦截净化,出流最低TN、NH+4-N分别可达地表Ⅴ类水和Ⅳ类水标准,出流TP稳定达到地表Ⅲ类水标准。但现有处理技术普遍占地面积大,对水量较大的应急情况处理效果差,建成多年后才可稳定运行,且易受环境条件的影响,难以应对施肥初期灌溉或降雨引起的高负荷污染农田排水。
针对上述情况,本研究提出一种通过投加改性沸石粉末并自然沉降的方式处理农田排水。沸石是以硅铝酸盐为主的一类矿物的总称,因其特殊的骨架结构及自身静电作用,而具有良好的吸附性能、阳离子交换性能及热稳定性。但天然沸石(Naturezeolite,NZ)铝氧四面体结构的负电性,决定了其几乎不能去除水中磷酸根、硝酸根等阴离子污染物,而通过改性能够实现沸石对氮磷的同步去除[6-7]。通过改变沸石吸附剂的表面电荷、阳离子类型及活性基团,可使沸石材料对目标污染物的吸附活性得到明显改善[8]。结合吸附质特性引入靶向性吸附活性基团,例如酸碱改性[9-10]、表面活性剂改性[11-12]、金属改性[13]等,提高沸石表面活性位点,增加其对目标污染物的选择吸附性能,是近年来沸石改性研究的热点。目前,国内外通过改性沸石(Modified zeolite,MZ)进行氮磷去除的研究多集中于生活污水和工业废水[14-16],针对于农田排水的改性沸石高效去除氮磷的方法尚不完善,污染物去除机理尚未完全明确。
本文针对农田排水中氮、磷等污染物,研究改性沸石的最佳制备条件及其污染物去除效能,通过性质表征、吸附动力学和热力学研究不同改性沸石的吸附特性和吸附机理,探究改性沸石快速高效去除农田排水中氮、磷的效果及可行性。
1 材料与方法
1.1 试验材料
大量文献表明,施肥后1~2周为农田氮磷径流流失关键期,农田排水中主要污染物平均浓度接近《城镇污水处理厂污染物排放标准》(GB 18918—2002)中规定的一级A标准[17-19],故本试验用水参考该标准进行人工配制。采用NH4Cl模拟NH+4-N成分,质量浓度约为5 mg·L-1;KH2PO4模拟TP成分,质量浓度约为0.5 mg·L-1;KNO3模拟NO-3-N成分,质量浓度约为10 mg·L-1。
试验所用沸石产自浙江省缙云县,类型为斜发沸石,粒径为3~5 cm,阳离子交换量(Cation exchange capacity,CEC)为1.65 mmol·g-1。经去离子水洗净后烘干,研磨至粒径≤75μm后进行改性。试验所用改性剂为:NaCl,99.9%,萨恩化学技术(上海)有限公司;LaCl3·7H2O,99.9%,国药集团化学试剂有限公司;溴代十六烷基吡啶(Cetylpyridinium Bromide,CPB),98%,上海麦克林生化科技有限公司。
1.2 沸石改性
(1)NaCl改性沸石(MZ-Na)的制备:将NZ按照固液比1∶20置于不同浓度(0.1、0.2、0.3、0.4、0.5、0.6 mol·L-1)的NaCl溶液中,于恒温摇床在25 ℃、200 r·min-1条件下振荡2 h,用去离子水清洗至AgNO3试剂检测不到Cl-,干燥至恒质量后进行NH+4-N吸附试验。确定最佳NaCl浓度后,再置于不同固液比(1∶10、1∶20、1∶30、1∶40、1∶50)中进行同上步骤改性,确定最佳固液比。
(2)LaCl3改性沸石(MZ-La)的制备:将NZ按照固液比 1∶20置于不同浓度(0.000 5、0.001、0.003、0.005、0.010、0.015、0.020、0.025、0.030 mol·L-1)的LaCl3溶液中,后续处理及固液比试验操作同NaCl改性,吸附采用TP溶液。
(3)CPB改性沸石(MZ-CPB)的制备:将NZ按照固液比 1∶20置于不同浓度(0.005、0.01、0.02、0.04、0.06、0.08、0.10、0.12、0.14 mol·L-1)的CPB溶液中,并于恒温摇床在40℃、200 r·min-1条件下搅拌24 h,后续处理及固液比试验操作同NaCl改性,吸附采用NO-3-N溶液。
1.3 改性沸石吸附特性试验
1.3.1 吸附动力学
通过单一污染物静态吸附试验确定:NZ吸附NH+4-N最佳投加量为5 g·L-1;MZ-Na吸附NH+4-N最佳投加量为3 g·L-1;MZ-La吸附TP最佳投加量为7 g·L-1;MZ-CPB吸附NO-3-N最佳投加量为15 g·L-1。
称取0.7 g MZ-La加入到100 mL模拟农田排水溶液中,称取1.5 g MZ-CPB加入到100 mL模拟农田排水溶液中,于25 ℃、200 r·min-1振荡不同时间(1、5、10、20、30、40、50、90、120、180、240、360 min)后测定上清液中相应污染物浓度,并用准一级、准二级动力学模型对所得数据进行拟合。
1.3.2 吸附等温线
称取0.7 g MZ-La分别加入到100 mL初始浓度为 1、5、10、20、30、40、50、60 mg·L-1的磷溶液中,于25、35、45 ℃下200 r·min-1振荡30 min后测定上清液中磷浓度。称取1.5 g MZ-CPB分别加入到100 mL初始浓度为 2、5、10、15、20、30、40、50 mg·L-1的 NO-3-N溶液中,于25、35、45 ℃下200 r·min-1振荡30 min后测定上清液中NO-3-N浓度,并用Langmuir、Freundlich吸附等温模型对所得数据进行拟合。
1.4 农田排水处理试验
取模拟农田排水溶液100 mL置于250 mL锥形瓶中,加入一定量的沸石(改性沸石的功能特性按沸石最佳投加量进行投加),于恒温摇床上以200 r·min-1的速率振荡一定时间后沉淀,取上清液进行分析测定。通过测定吸附前后溶液中NH+4-N、NO-3-N和TP浓度,按下式计算吸附量与去除率:
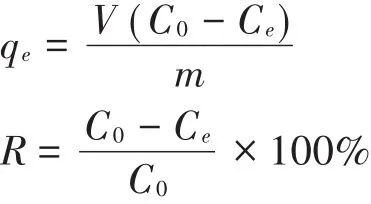
式中:qe为平衡吸附量,mg·g-1;R为吸附质去除率,%;C0和Ce分别为起始状态和平衡状态时的吸附质浓度,mg·L-1;V为溶液体积,mL;m为吸附剂质量,g。
1.5 分析方法
NH+4-N采用纳氏试剂分光光度法测定(浓度成分均以N计);TP采用钼酸铵分光光度法测定(浓度成分均以P计);NO-3-N采用紫外分光光度法测定(浓度成分均以N计)[20]。材料的比表面积分析采用Autosorb-IQ3进行BET分析;Zeta电位分析采用双功能/omni纳米粒度Zeta电位仪进行测定;表面形貌特征采用LaB6扫描电子显微镜观察,之后采用扫描电镜能谱仪对材料微区进行EDS元素分析。
2 结果与讨论
2.1 改性沸石最佳制备条件
NaCl浓度、固液比对MZ-Na去除NH+4-N的影响如图1a和图1b所示。随着NaCl浓度升高,NH+4-N去除率由79.80%增加至89.84%,这是由于Na+通过离子交换作用置换出NZ中半径较大的Mg2+、Ca2+等金属离子,从而形成钠型沸石,其具有良好的离子交换性能。继续升高NaCl浓度,NH+4-N去除率基本保持不变,因此最佳NaCl浓度为0.2 mol·L-1。固液比对去除率影响不大,因此选用较大固液比1∶10作为MZ-Na的制备条件。
LaCl3浓度、固液比对MZ-La去除TP的影响如图1c和图1d所示。LaCl3浓度为0.01 mol·L-1时,MZ-La对TP去除率达到98.98%,这是由于La3+以La(OH)3、La2O3为主要存在状态有效负载于沸石上,并通过络合作用实现对TP的吸附,因此最佳LaCl3浓度为0.01 mol·L-1。固液比对去除率影响不大,因此选用较大固液比1:10作为MZ-La的制备条件。
CPB浓度、固液比对MZ-CPB去除NO-3-N的影响如图1e和图1f所示。当CPB浓度小于0.02 mol·L-1时,去除率随CPB浓度升高而增加,这是由于CPB负载比例大于50%沸石CEC时,表面正电荷数量会逐渐增加,进而增强对阴离子污染物的吸附,在最佳CPB浓度下,CPB双层负载于沸石表面,使其表面带正电荷;但进一步增加CPB浓度去除率会降低,主要原因在于过高的负载比例会造成疏水性增加,使得吸附量下降,因此最佳CPB浓度为0.02 mol·L-1。固液比1∶20时NO-3-N去除率达最大值83.06%,继续降低固液比,去除率保持不变,所以选用固液比1∶20作为MZ-CPB的制备条件。
2.2 改性沸石性质表征
2.2.1 比表面积分析(BET)及Zeta电位分析
对NZ、MZ-Na、MZ-La和MZ-CPB进行比表面积及孔径分析,结果如表1所示。NZ经NaCl改性后,比表面积由 7.535 m2·g-1增加至 25.507 m2·g-1,平均孔径由1.428 nm增加至17.057 nm,Na+通过离子交换作用置换出NZ中半径较大的Mg2+、Ca2+等金属离子,引起介孔及大孔数量的增加,沸石孔道的拓宽更利于Na+从孔中出入,与溶液中的NH+4进行交换,比表面积的增加也使MZ-Na的阳离子交换性能显著提高。MZ-La的比表面积、孔容和平均孔径也有一定程度增加,因为改性阶段去除了NZ孔道内的水分和无机杂质,使得沸石孔道拓宽、孔径增大,比表面积的改变也增强了MZ-La对NH+4-N的吸附性能,使离子交换反应更易进行,因此MZ-La对NH+4-N和TP都有较好的去除效果。MZ-CPB比表面积有所减小,是因为阳离子表面活性剂分子较大,结合到沸石表面后,其表面形成类似胶束覆盖物,造成沸石表面孔隙堵塞,从而比表面积减小。同时,CPB改性后,Zeta电位由天然沸石的-42.31 mV变为35.38 mV,说明CPB负载改变了沸石表面电性,正电性也实现了对阴离子污染物的有效吸附。
2.2.2 扫描电镜能谱分析(SEM-EDS)

图1 改性剂浓度及固液比对改性沸石去除率的影响Figure 1 Effect of concentration of modifier and solid-liquid ratio on removal rateof modified zeolite

表1 NZ和改性沸石的比表面积、孔容、孔径及Zeta电位Table 1 Surface area,pore vlume,pore radius and Zeta potential of natural zeolite and modified zeolit
对NZ、MZ-Na、MZ-La和MZ-CPB进行扫描电镜分析,结果如图2所示。在×10 000的放大倍数下观察,NZ表面较光滑,通道杂质多,缺乏连续性;MZ-Na沸石形状不规则,有棱角,可看到明显的脉络结构;MZ-La与MZ-CPB形貌特征发生较大的变化,沸石表面覆盖有一层物质,可能是LaCl3或CPB以某种形式负载在沸石表面。
NZ和各改性沸石能谱分析结果如表2所示。MZ-Na中Na含量上升,K、Ca和Mg含量下降,证实了MZ-Na吸附NH+4-N能力的增加,这是由于Na+置换出NZ中半径较大的K+、Ca2+和Mg2+,增大了其离子交换容量。MZ-La中La含量由0增加至2.50%,说明La成功负载到MZ-La上,La的成功负载使沸石表面带有正电基团La-OH+2,与带负电的PO34-产生静电引力,产生含磷络合物,从而增强TP吸附性能。但是LaCl3改性后,Si/Al比减小,沸石骨架中铝氧四面体的增加使其携带负电荷增加,所以MZ-La电性较NZ无明显变化,与Zeta电位测定结果一致。LaCl3分子结构较大,无法进入沸石孔腔内部,所以不影响沸石内部孔穴吸附NH+4-N的能力,从而实现MZ-La对NH+4-N和TP的同时吸附。MZ-CPB中Br含量由0增加至0.81%,原因是CPB阳离子基团负载于沸石表面,形成定向排列的吸附层,从而作为平衡离子的Br-含量增加。在吸附过程中,一部分阴离子污染物会与Br-发生阴离子交换作用与静电吸引作用,从而大幅提高了其对阴离子污染物的吸附性能。

图2 NZ和改性沸石的SEM图Figure 2 SEMimages of natural zeolite and modified zeolite
2.3 改性沸石的功能特性
NZ及改性沸石去除模拟农田排水中NH+4-N、NO-3-N和TP的效果如图3所示。MZ-Na可将NH+4-N由4.82 mg·L-1降至0.22 mg·L-1,改性后NH+4-N去除率为95.40%,比NZ提高15.86%,但对NO-3-N和TP吸附效果不佳。MZ-La可将TP浓度由0.50 mg·L-1降至0.005 mg·L-1,改性后TP去除率为98.85%,比NZ提高了97.76%;且MZ-La对NH+4-N也有较强的吸附作用,去除率为95.52%,但MZ-La对NO-3-N基本无吸附作用。MZ-CPB提高了对NO-3-N的吸附作用,将NO-3-N由10.07 mg·L-1降至2.08 mg·L-1,改性后NO-3-N去除率为79.35%,比NZ提高了79.15%;MZ-CPB对TP的去除率也达到了70.61%,当CPB浓度较低时,沸石表面形成单层负载,阴离子污染物的吸附位点位于负载在沸石上的CPB亲水性正电头端,当CPB浓度较大时,疏水性尾端与溶液中CPB的疏水性尾端通过范德华力结合使沸石表面带正电,为水体中阴离子污染物提供吸附活性位点[21];但经过CPB改性后,NH+4-N去除能力有所降低,原因为疏水碳链结合的有机相会使部分负电荷吸附活性位点被覆盖。但CPB由于分子太大而无法进入沸石内部空腔,而通常沸石外部表面积只占沸石总表面积的1%,外部阳离子交换量占沸石总阳离子交换量的10%[22],所以,CPB改性对沸石阳离子交换性能影响不大。
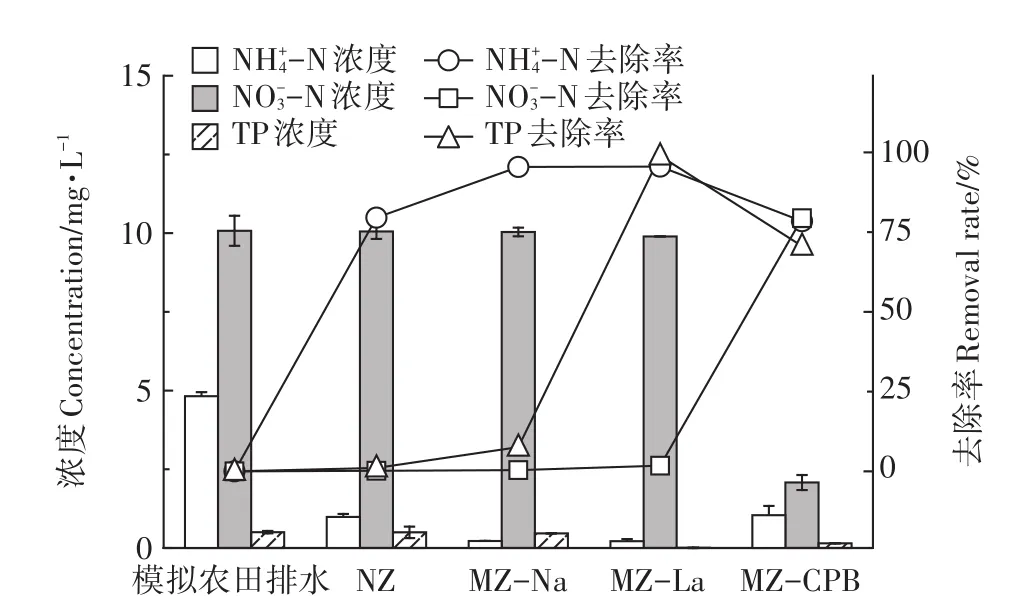
图3 改性沸石氮磷去除效果Figure 3 Removal of NH+4-N,NO-3-Nand TPby modified zeolite

表2 NZ和改性沸石的元素组成(%)Table 2 Elemental composition of natural zeolite and modified zeolite(%)
综上所述,若要同时去除农田排水中的NH+4-N、NO-3-N和TP,需选用MZ-La和MZ-CPB作为组合吸附材料使用。
2.4 改性沸石吸附特性
鉴于MZ-Na仅对NH+4-N吸附功能有提高,但对TP和NO-3-N吸附效果不佳,因此改性沸石的吸附动力学和热力学主要针对MZ-La和MZ-CPB进行研究。

图4 反应时间对MZ-La(a)、MZ-CPB(b)去除NH+4-N、NO-3-N和TP的影响Figure 4 Effect of reaction time on NH+4-N,NO-3-Nand TPadsorption of MZ-La(a),MZ-CPB(b)
2.4.1 吸附动力学
反应时间对MZ-La去除NH+4-N、NO-3-N和TP的影响如图4a所示。在0~10 min内,MZ-La对NH+4-N和TP的去除率上升得很快,原因在于阳离子交换和络合作用均为快速反应,且反应初期污染物浓度较高,MZ-La上的吸附位点较多,所以吸附速度较快。10 min后,去除率增加缓慢并趋于平稳,MZ-La逐渐到达吸附平衡。反应时间对MZ-CPB去除NH+4-N、NO-3-N和TP的影响如图4b所示。在吸附反应开始的前20 min,MZ-CPB去除NO-3-N和TP的速度随时间快速增加,20 min后,吸附反应逐渐达到平衡状态。但MZ-CPB去除NH+4-N的速率上升较慢,50 min后方可达到平衡状态。
两种改性沸石吸附氮磷的动力学模型拟合结果如表3所示,由表3可知,准二级动力学模型能够更好地描述MZ-La和MZ-CPB吸附NH+4-N、NO-3-N和TP的过程,说明MZ-La和MZ-CPB的吸附过程受化学吸附机理控制,吸附速率由吸附剂表面未被占据的吸附位点数目决定。

表3 MZ-La与MZ-CPB吸附NH+4-N、NO-3-N和TP的动力学模型拟合结果Table 3 Fitting results of adsorption kinetic models of NH+4-N,NO-3-Nand TPon MZ-La and MZ-CPB
2.4.2 吸附等温线
不同温度下,MZ-La吸附TP和MZ-CPB吸附NO-3-N的Langmuir和Freundlich等温吸附模型拟合曲线如图5、图6所示。结果表明,MZ-La的吸附容量随TP平衡浓度的增加而增加;同时,随着反应温度的升高,吸附TP的量呈上升趋势,说明升温有利于吸附平衡正向移动,吸附过程为吸热反应。MZ-CPB的吸附容量随NO-3-N平衡浓度的增加而增加,但吸附量随着反应温度的升高而降低,说明较低温度有利于MZ-CPB的吸附。

图5 MZ-La吸附TP的Langmuir(a)和Freundlich(b)等温吸附模型非线性拟合曲线Figure 5 Fitting curves of Langmuir adsorption isotherm(a)and Freundlich adsorption isotherm(b)of TPonto MZ-La
MZ-La对TP的Langmuir、Freundlich吸附等温模型拟合结果见表4。由表4可知,MZ-La对TP的吸附与Freundlich吸附等温模型拟合度较高(R2>0.99),其理论最大吸附容量为5.716 mg·g-1。Freundlich吸附等温模型中的参数1/n反映了吸附剂与污染物之间的结合能力,MZ-La的1/n为0.3~0.5,说明吸附过程容易进行。MZ-CPB对NO-3-N的Langmuir、Freundlich吸附等温模型拟合结果见表5。由表5可知,MZ-CPB对NO-3-N的吸附与Langmuir吸附等温模型拟合度较高(R2>0.97),其理论最大吸附容量为2.881 mg·g-1,且其平衡参数RL介于0~1间,说明吸附过程为优惠吸附[23]。
2.5 改性沸石对农田排水处理效果的研究

图6 MZ-CPB吸附NO-3-N的Langmuir(a)和Freundlich(b)等温吸附模型非线性拟合曲线Figure 6 Fitting curves of Langmuir adsorption isotherm(a)and Freundlich adsorption isotherm(b)of NO-3-N onto MZ-CPB
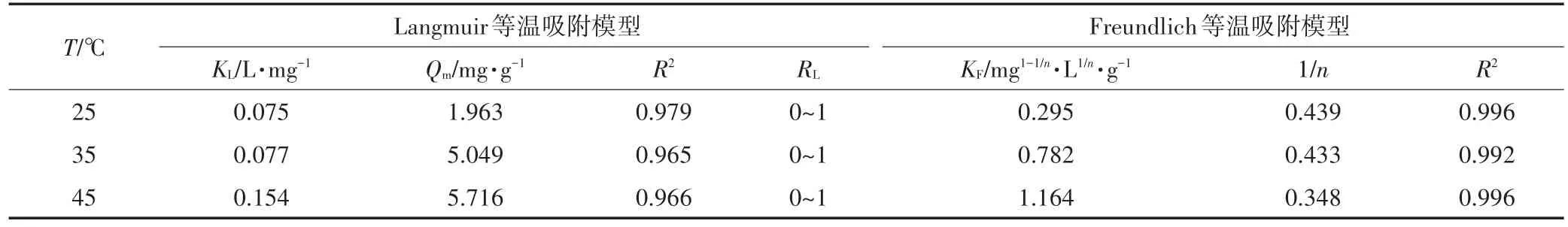
表4 MZ-La吸附TP的等温吸附模型拟合结果Table 4 Fitting results of adsorption isotherms of TPon MZ-La
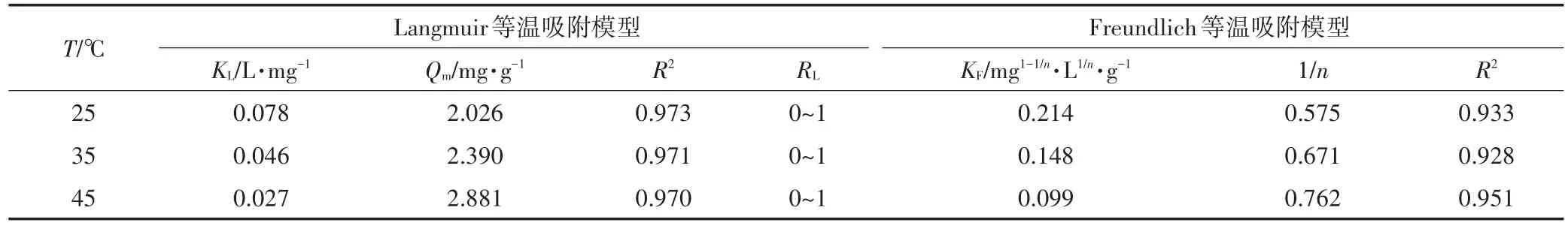
表5 MZ-CPB吸附NO-3-N的等温吸附模型拟合结果Table 5 Fitting results of adsorption isotherms of NO-3-Non MZ-CPB
前期试验表明,任何单一改性沸石均难实现同时去除NH+4-N、NO-3-N和TP。所以选用MZ-CPB与MZLa组合投加并沉降的方式处理模拟农田排水。由图3可知,MZ-CPB具有较好的NO-3-N去除能力,通过单一污染物静态吸附试验确定其最佳投加量为15 g·L-1,在此基础上配以不同投加量的MZ-La进行模拟农田排水氮磷去除试验,同时根据图4确定试验反应时间为20 min,待沸石沉降(约7 min)后测定水中各污染物浓度,结果如图7所示。由图7可知,对NH+4-N而言,投加15 g·L-1MZ-CPB与9 g·L-1MZ-La时效果最好,出水NH+4-N 浓度为 0.19 mg·L-1,去除率为97.24%;对NO-3-N和TP而言,投加15 g·L-1MZ-CPB与8 g·L-1MZ-La时效果较好,出水NO-3-N浓度为2.18 mg·L-1,去除率为78.21%,出水TP浓度为0.015 mg·L-1,去除率为97.12%。综合考虑3种目标污染物,建议组合吸附剂投加量为15 g·L-1MZ-CPB与8 g·L-1MZ-La,在此投加量下,出水NH+4-N浓度和TP浓度分别为0.23 mg·L-1和0.015 mg·L-1,可满足地表水环境质量Ⅱ类水标准(GB 3838—2002),去除率分别为95.38%和97.12%;出水NO-3-N浓度为2.18 mg·L-1,去除率为78.21%。实际使用时,可根据污染物浓度及处理要求调整用量。同时,将吸附饱和的组合改性沸石放入0.1 mol·L-1的NaOH溶液中,在40℃条件下振荡3 h,静置沉淀后用去离子水清洗,烘干后测定其对NH+4-N、NO-3-N和TP的去除效率,结果表明组合改性沸石再生后NH+4-N吸附能力恢复率为89.30%;NO-3-N吸附能力恢复率为88.72%;TP吸附能力恢复率为90.33%。

图7 改性沸石组合投加量对模拟农田排水去除率的影响Figure 7 Influence of mixed adsorbent dosage on simulated farmland drainage onto modified zeolite
3 结论
(1)采用 0.01 mol·L-1的LaCl3溶液按照固液比1∶10对NZ进行改性,制成的MZ-La可同步吸附NH+4-N(95.52%)和TP(98.85%);采用0.02 mol·L-1的CPB溶液按照固液比1∶20对NZ进行改性,制成的MZ-CPB可同步吸附NH+4-N(78.39%)、TP(70.61%)和NO-3-N(79.35%)。MZ-La和MZ-CPB可作为农田排水氮磷去除的材料。
(2)改性后LaCl3、CPB会以某种形式负载在于MZ-La与MZ-CPB沸石表面,MZ-La中La元素含量增加了2.5%,MZ-CPB中Br元素含量增加了0.81%。MZ-La和MZ-CPB分别在10 min和20 min内即可达到吸附平衡,其吸附过程均符合准二级动力学模型。MZ-La对TP的吸附符合Freundlich吸附等温模型(R2>0.99),理论最大吸附容量为 5.716 mg·g-1。MZ-CPB对NO-3-N的吸附符合Langmuir吸附等温模型(R2>0.97),理论最大吸附容量为2.881 mg·g-1。
(3)组合投加15 g·L-1MZ-CPB与8 g·L-1MZ-La处理模拟农田排水,反应20 min,沉淀7 min后,出水NH+4-N、NO-3-N和TP浓度分别为0.23、2.18 mg·L-1和0.015 mg·L-1,去 除 率 分 别 为 95.38%、78.21% 和97.12%,效果良好。表明组合改性沸石可作为农田排水氮磷同步应急处理材料。

