CT引导下术前自体血定位在胸腔镜肺小结节切除术中的应用
许建新 许志扬 关军 林建生
随着高分辨率CT检查的普及,肺部结节检出率明显增多。针对肺磨玻璃结节的外科处理已逐步成为胸外科临床工作的重要组成部分。但是,由于肺磨玻璃结节体积较小、缺乏实性成分等因素,胸腔镜手术中常常出现肺结节辨认困难,无法定位病灶,给手术带来不少挑战和困难。目前国内报道较多的术前有创定位方法是CT引导下Hook-wire定位以及微弹簧圈定位[1]。我科曾应用弹簧圈术前定位取了不错的效果[2]。随着多年的摸索,于2018年1月~2019年6月,我科采用术前CT引导下自体血定位肺小结节,对25例25处孤立性肺小结节行胸腔镜切除术,效果良好,报道如下。
资料与方法
一、 一般资料
本组25例,男14例,女11例。年龄45~76(56.3±12.8)岁。病灶直径7~22(10.27±8.01) mm,距离脏层胸膜深度6~28 (15.24±4.83)mm,位于左上叶7例,左下叶4例,右上叶9例,右下叶5例。
对于肺结节穿刺定位的适应症并无统一标准,现主要是依据结节类型与距胸膜距离综合判断,本研究入选标准:①实性结节,直径≤1 cm,距离脏层胸膜≥1cm;②纯磨玻璃结节;③混合型磨玻璃结节,距离胸膜≥1 cm;④病灶无胸膜牵拉征,未累及胸膜;排除标准:(1)直径大于30mm;(2)距离脏层胸膜距离大于30 mm;(3)排除肺血管性病变或病灶靠近肺大血管;(4)严重心肺功能不全或有出血倾向患者;所有患者定位及手术前均已知情同意。
二、 方法
依据术前影像学检查选择合适的体位,并行胸部CT薄层扫描精确测量结节与胸壁、壁层胸膜的距离,确定穿刺部位、进针层面、进针路径。穿刺前抽取病人自体血5 mL备用。常规消毒、铺巾,利多卡因局部麻醉后,在放射科技术人员的配合指导下,用CareFusion公司生产的20G穿刺针行经皮行肺穿刺,针尖走形路径根据适时CT三维指导调整,最后定位于小结节周边约1cm的正常肺实质内,将自体血注入于病灶旁,并逐步回退针头,将自体血输注于路径过程中肺实质内(见图1、2)。完成后再次行CT确认定位效果以及有无气胸、血胸等并发症。定位完成后患者返回病房,于次日接受胸腔镜手术。
胸腔镜手术采用双腔气管插管全麻,单肺通气。于第7肋腋中线、第3或第4肋腋前线、第8或9肋间肩胛下角线分别作胸腔镜孔、主操作口、辅助操作孔。置入胸腔镜探查,可见定位处肺脏层胸膜表面不同程度淤血征,呈暗红色(见图3),与周围肺组织界限尚清楚。若因结节距离较深、着色较浅或与周围界限不清时,根据术前定位时,自体血位于结节的上或下层面手指触诊,使用直线切割缝合器行病变部位楔形切除,取出标本,根据自体血输注路径仔细触摸寻找病变,确认后,术中送快速冰冻病理切片,根据结果决定是否进一步行肺叶切除术及淋巴结清扫术。
结 果
本组25例25处孤立性肺小结节均经自体血注入成功定位,定位成功率100%,本组中发生无症状气胸1例,未进一步处理。未见血胸、栓塞、咯血等严重并发症。所有患者无中转开胸。定位操作时间15~35(20.5±8.1) min,定位不理想3例,均为肺组织塌陷后定位处暗红色着色与周围肺组织界限不甚清楚,辨认稍困难,结合术前CT以及体表标志等仍可定位。
胸腔镜楔形切除术均获成功。楔形切除时间10~25(18.6±4.7) min。25例肺小结节术后病理:非典型腺瘤样增生3例,原位癌6例,微浸润腺癌8例,腺癌5例,炎症1例,纤维化结节伴炭末沉积1例,结核1例。
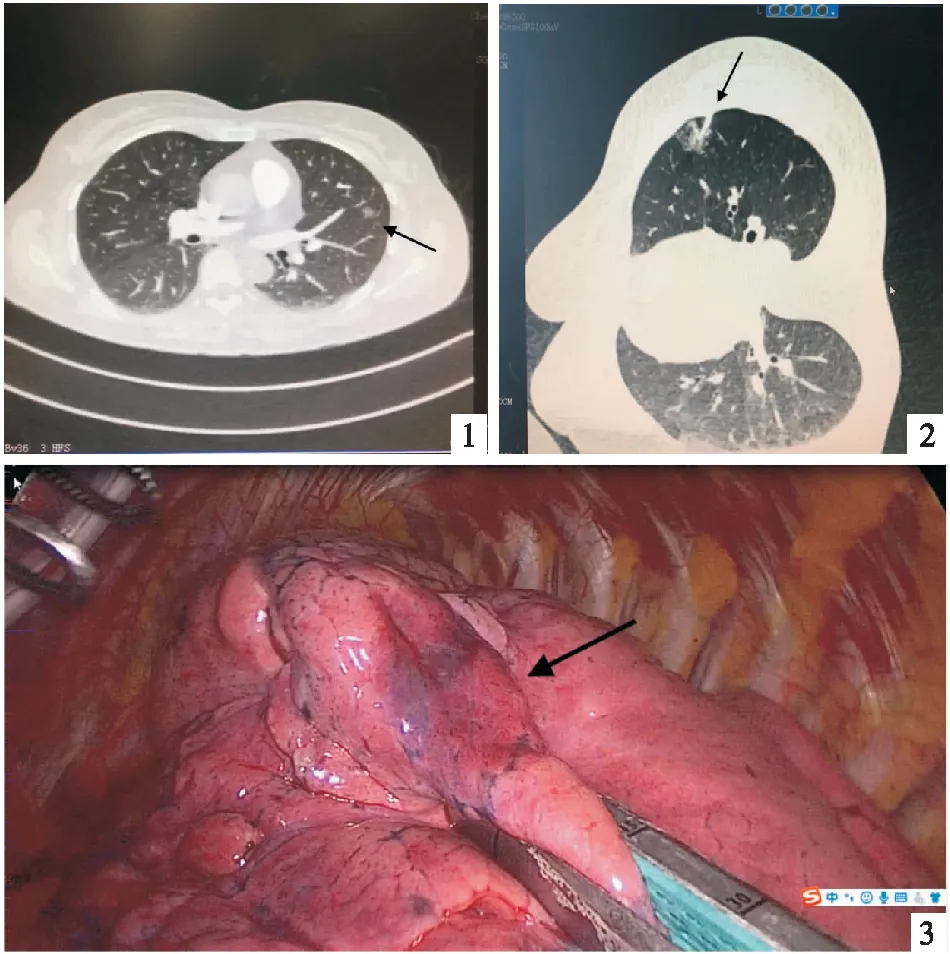
图1 病灶位于左上肺 图2 穿刺针注入自体血 图3 定位点成暗红色
讨 论
在高分辨CT 肺癌筛查的大背景下,肺磨玻璃结节检出率处于上升趋势。肺微小结节由于体积小,实型成分少,导致胸腔镜手术中触诊困难。Tamura等[3]研究结果显示,当结节直径<15mm且距离胸膜>10mm,术中结节识别失败率达100%;当结节贴近胸膜或者结节直径>15 mm 且距离胸膜<5 mm时,术中结节识别率高达85.3%。所以寻找出理想的定位方法一直是胸外科的热点以及难点。这种理想的方法不仅体现在准确性、可辨识性、牢固性,也要兼顾安全、便捷、花费少等方面。
对于肺内微小结节的定位方法大致可分为无创的术中定位方法和有创的术前定位方法两大类。主要有术中解剖标志物定位、Hook-wire以及微弹簧圈定位、染料定位、放射对比剂与核素定位、术中超声定位、触觉压力感应定位、3D打印导板辅助定位等[1]。经皮肺穿刺注入亚甲蓝等染料存在弥散问题,可能致术中无法辨识病灶位置。放射性核素定位方法快速高效,但对设备要求高,价格昂贵,且仅限于表浅的病灶,腔镜下超声属于无创方法,但其分辨率低、易受肺内气体影响,对于亚厘米结节诊断率低[4]。Hook-wire定位的并发症主要为气胸及定位针脱落移位,气胸的发生率较高[5](7.5%~49.1%)。且对于基层医院来说,没有专门为手术准备的CT机,需要放射科、手术室、介入科等多科室配合,实际可操作性差。微弹簧圈定位,定位后不必立即手术,不需要限制患者活动,但同样有气胸、弹簧圈游走、断针残留、脱落等问题。
目前随着胸外科对小结节处理的经验增多,主刀医师触诊经验的丰富,对于一般结节手指触诊的准确率越来越高,而位置深在的病例目前可使用较为成熟的肺段切除解决问题,对术前定位的依赖性降低了。能否应用最简单最经济的方法来定位小结节,是胸外科医师一直思考的方向。McConnell等[6]研究中采用了自体血加上亚甲蓝混合注入为17例患儿行术前定位,方法安全有效。本组研究中采用了注入自体血定位术前小结节25例,起到了良好的效果,也总结了较多的临床经验:(1)化繁为简,这种定位方法是有创的术前定位方法中最简单的,最便捷的,可以为术者提供明确的定位点,同样非常直观;(2)类似于单纯的穿刺术,对定位实施医师的要求低,不需要任何的高值耗材,仅仅是患者的5 mL自体血注入即可完成准确的术前定位,定位成本非常低。相对于Hook-wire以及弹簧圈定位,可明显降低患者经济负担;(3)自体血便于取材,含有丰富的纤维蛋白原,可有效地自凝,纤维蛋白形成保护膜可覆盖肺组织创面或裂口,促使瘘口愈合。同时没有异物刺激等不良反应等,具有明显优势[7]。熊伟[8]等胸腔内灌注自体血联合粗管负压吸引治疗难治性气胸,不良反应少,复发率低。本组中仅发生1例无症状性气胸,个人认为和自体血的材料优势直接相关;(4)穿刺针的粗细是影响并发症发生率的重要因素,穿刺针越粗,并发症发生率越高[9]。本组中采用的是20号针头,完全能满足自体血的顺利注入,而没有必要采用更粗的穿刺针。这样可以最大限度的减少气胸的发生率。有报道称医用胶定位会引起剧烈的胸痛不适,以及胶水注入引起的刺激性咳嗽和特殊气味[10],我们采用的自体血定位,本组研究中并未观察到此种现象;(5)亚甲蓝作为最常用的定位染料,染色后要求3 h以内手术,不然会出现扩散的情况。我们于手术前一天注入自体血定位后,短时间内不易被吸收,但若间隔时间过长,则可能出现定位点发散,使定位点变得稍模糊;(6)相对于置入Hook-wire或者微弹簧圈,自体血定位体位更自由,无需特殊制动,手术安排更从容,避免了在介入科、CT室以及手术室之间的繁琐的协调工作。我们曾遇到1例病人,术前做好自体血定位后,下半夜意外出现发热,后不得不取消手术。若术前置入的是Hook-wire或者微弹簧圈,则会非常被动。
CT引导下自体血定位有其独特的优势,但随着应用例数不断增加后,也发现一些不足之处。最大的劣势在于对可能存在矽肺或者粉尘接触病史的男性患者,术前自体血定位有可能注入到碳末沉积的肺表面,导致识别困难。本组中出现的定位不理想3例情况均属于此种类型,但我们仍可通过壁层胸膜上的穿刺点或者脏层胸膜上的染色深浅观察到。而对于大部分无吸烟史的女性患者来说,肺组织质地好,均匀,无碳末沉积,有非常直观、明显的效果;相对于我科之前应用的弹簧圈定位技术[2],弹簧圈拖尾盘曲于肺脏层胸膜表面一个点,自体血定位则为一小面积血肿,相对来说定位不够精准,但其实并不影响切除;对于位置过深的结节,所有的定位技术均存在不足之处,自体血定位也有同样的问题,但随着目前精准肺段切除手术的应用、肺血管、支气管三维重建技术的普及[11]以及触诊经验的丰富,对深部结节实施精准定位,显得不那么必要。
目前,任何一种肺内小结节的定位方法均不完美。CT引导下注入自体血定位肺内小结节,操作方便,简单有效,经济实用,可有效降低定位成本,副作用以及并发症少,可提高胸腔镜肺楔形切除术的成功率,为临床提供有力支持。

