眼科手术导航的OCT图像畸变矫正
陈 聪,杨 帆,范立成,沈超逸
(苏州大学 机电工程学院,江苏 苏州 215000)
1 引 言
白内障是世界上导致人眼失明的主要眼科疾病,全世界因白内障致盲的患者约占6%[1-2]。目前,人工手术存在撕囊困难,超声乳化能量过高等问题。随着生物医学成像技术及激光技术的发展[3],由光学相干断层扫描成像导航的飞秒激光辅助白内障手术已经渐渐取代了人工白内障手术[4-9],其具有手术时间短,精度高,细胞损伤低等优点。
光学相干断层扫描(Optical Coherence Tomography,OCT)是20世纪90年代由D.Huang 等提出的一种新的成像方法,具有成像速度快,分辨率高的特点,能够实现整个眼前节成像,被广泛应用于眼科疾病诊断[10-11]。而将其应用到眼科手术导航中需要确定其成像位置。目前,国际上已有的数种完善的飞秒激光辅助白内障手术系统均使用OCT为手术进行导航,获取指定手术位置的相关信息。但是人眼做为一个光学系统本身具有屈光能力,角膜等组织会带来光程上的变化,OCT重构眼组织结构必然会产生实际位置误差,这在临床手术中会产生极大影响。所以有必要提出相关方法,矫正图像重建时由于组织折射带来的实际成像位置偏差。国内外有许多学者对此展开了研究,D.Borja等在谱域光学相干层析成像系统中使用几何光学分析方法[12],对成像组织内部进行光学追迹,但仅仅矫正了晶状体的误差; YU-CHERNG CHANG[13]等提出使用光学距离直接乘以相应折射率的方法直接计算厚度信息。
针对眼科手术中需要快速获取指定手术区域的深度信息,本文提出了一种将OCT应用到飞秒激光白内障手术导航的方法,其具体为OCT扫描位置的定位和OCT图像信息的矫正。本文基于扫频OCT及光学CCD相机搭建的实验平台,结合数字图像处理,对扫描坐标系和相机坐标系进行坐标匹配,完成OCT扫描定位,最终达到指定位置扫描的目标。然后基于光学基本斯涅尔定律和费马原理,结合图像处理相关算法对OCT图像进行矫正,建立了矫正的相关数学模型。
2 OCT图像导航方法
2.1 OCT扫描定位
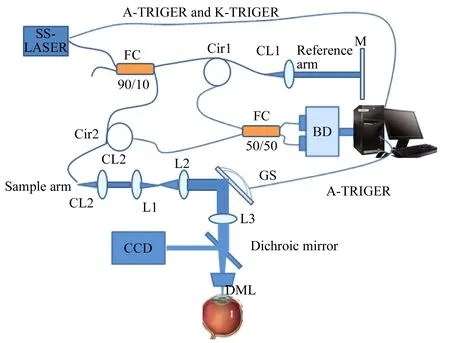
图1 本文系统结构示意图
本文通过二向色镜组合扫频光相干断层成像系统(SS-OCT)和光学CCD相机,系统结构如图1所示(SS-LASER:扫频光源;FC:光纤耦合器;Cir:光纤环形器;M:反射镜;CL:光纤准直器;BD:平衡光电探测器;GS:振镜;L:聚焦透镜;DML:负压吸引环),扫频光源(HSL-20,Santec,Japan)发出的光经90/10光纤耦合器分光,90%的光经光纤环形器1(Cir1)后进入参考臂模块,10%的光经光纤环形器2(Cir2)后进入样品臂模块。参考臂由平面反射镜将光返回并由Cir1传入50/50光纤耦合器,样品臂光经透镜组L1,L2扩束后由XY振镜(GVSM002/M,Thorlabs,USA)改变光的二维空间位置,由L3聚焦入射到样品,由样品不同深度层面形成各自的后向散射并原路返回由Cir2传入50/50光纤环形器,形成的干涉信号由双通道平衡探测器(PDB470C 400 MHz,Thorlabs,USA)接收,探测器内含两个互相匹配的光电二极管和超低噪声的高速互阻放大器,能够将信号相减处理有效消除工模噪声。接收到的信号经光电转换后由12位双通道高速数据采集卡(APX5200A,Santec,JAPAN)以500 MHz的采样率记录。系统最大轴向扫描速度50 kHz,轴向分辨率12.55 μ m,在空气中最大成像深度15.5 mm。CCD实时检测样品实际情况,负压吸引环固定样品。
本文利用红外显示光板确定激光的实际扫描位置来定位OCT扫描路径。吸环为透明物体,它所在的实际坐标系即被观测样品所在坐标系。本文通过获取相机的图像像素坐标系、吸环坐标系以及OCT扫描坐标系之间的几何关系,实现样品的定位测量,具体步骤如下:
(1)吸环坐标系获取
使用光源照明吸环,由于吸环灰度值明显区分于周围物体,通过设定阈值范围的方法,即可实现吸环提取如图2右所示。由于左边还存在部分非吸环物质,在对其做最小内切圆后,使用HALCON区域中心提取算子area_center,即可得出被观测样品的中心位置(x0,y0)(图2右)。
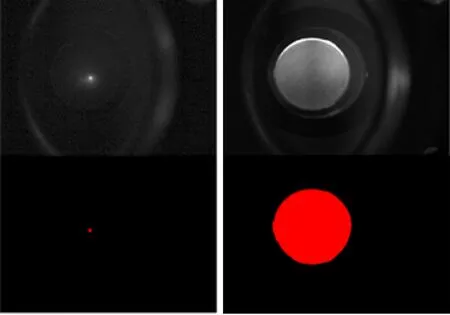
图2 光斑初始位置(左)和样品坐标中心(右)
(2)OCT扫描坐标提取
OCT扫描位置由振镜决定,首先给出振镜X轴、Y轴电压为0 V,将红外探测光板置于吸环下方。图2左可清晰看见光板上OCT扫描原点为一亮点,提取其中心像素坐标即为原点位置为(x1,y1)(图2左)。
(3)坐标系配准
如图3所示,根据坐标系转换公式得:

图3 光斑初始坐标系和样品中心坐标系
为验证本定位扫描方法对于引导OCT扫描指定位置的精确性,本文在完成前述定位扫描的基础上,进行了样品指定位置成像,对半径为3 mm的亚克力半球为样品以水平,垂直方向不同位置进行扫描,通过OCT的图像上最高点A和最低点B和A-SCAN图(图4)上相应的峰值点获取深度方向信息,将其与样品相应位置计算得到的理论深度值进行比较。得到的结果如图5所示。理论深度值和测量值的误差在50 μm以内,可以说明标定的误差极小,测量误差由被测样品的加工精度和实验数据的多次测量取平均值保证。
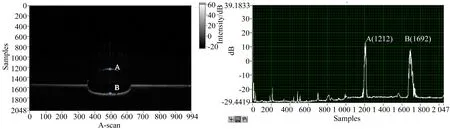
图4 OCT图像和相应的A-SCAN图

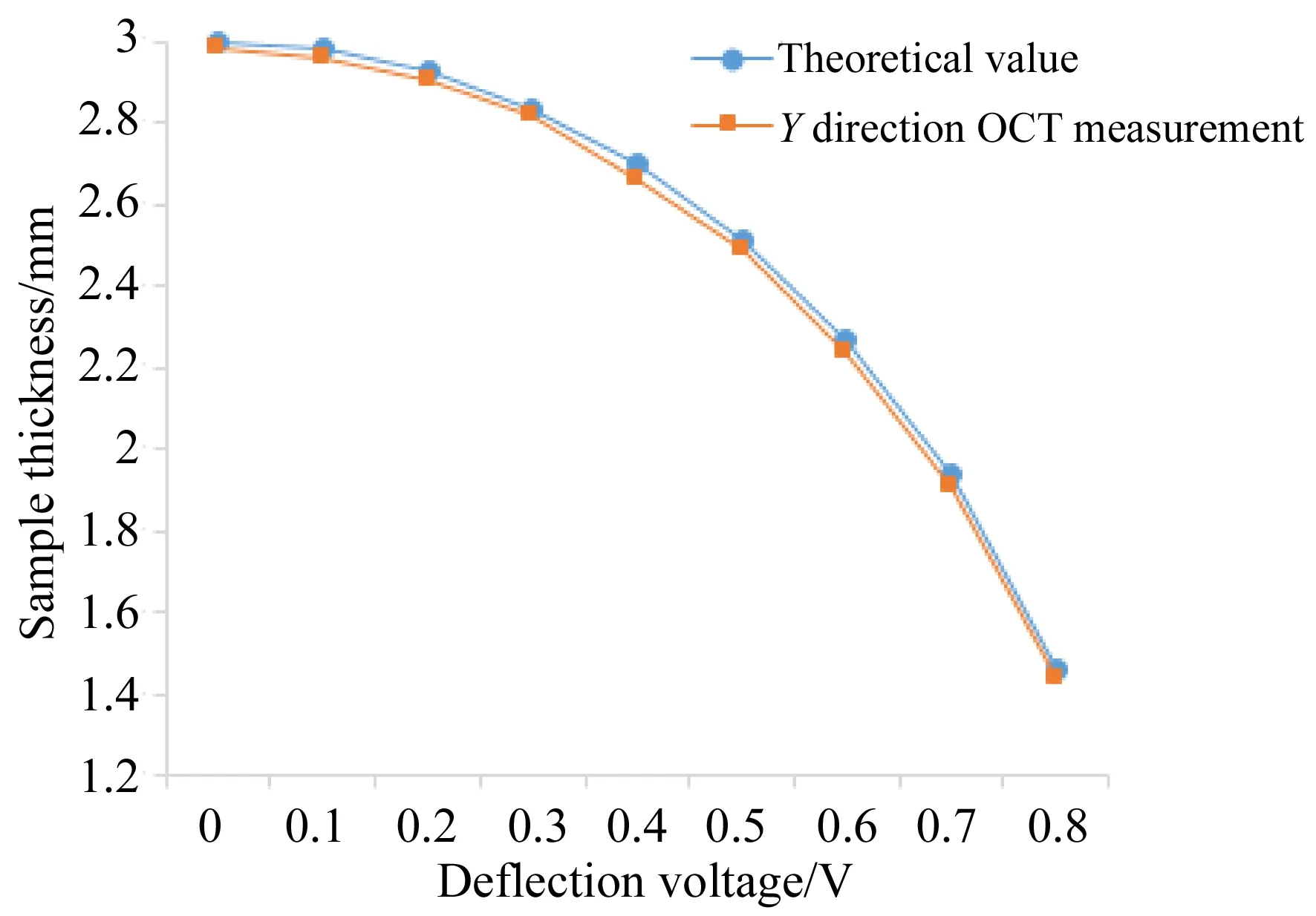
图5 X,Y方向理论深度值和测量值对比
2.2 OCT图像矫正理论分析
如图6为OCT重建图像时的光路传播。假设OCT光束经聚焦透镜后以垂直于水平面方向射入被测样品,(n0,n1,n2)分别表示不同的介质折射率。当(n0,n1,n2)三者相等且分隔界面为水平面时,光线由点(a,b)出射,继续以垂直于水平面方向经过点(a1,b1)和(x1,y1)。这种情况下,重建所得二维图像即为样品实际内部图像,仅需将整体深度除以介质折射率即可获得样品内部实际信息。
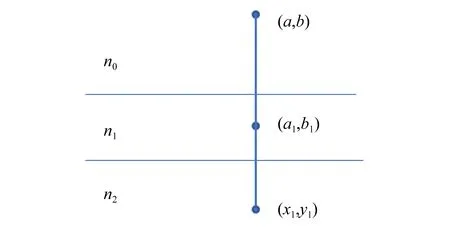
图6 理论OCT重建光线示意图
OCT在对样品成像时不考虑光线折射、分隔界面几何形状以及光透过不同样品时实际光程变化,但在实际应用中,各样品内部不同深度往往折射率各不相同,且不同介质间的分隔层面几何形状各式各样。如图7所示为实际情况下OCT重建光线示意图,设点(x0,y0)为OCT成像位置,点(x1,y1)为实际位置,即矫正后图像所在位置。
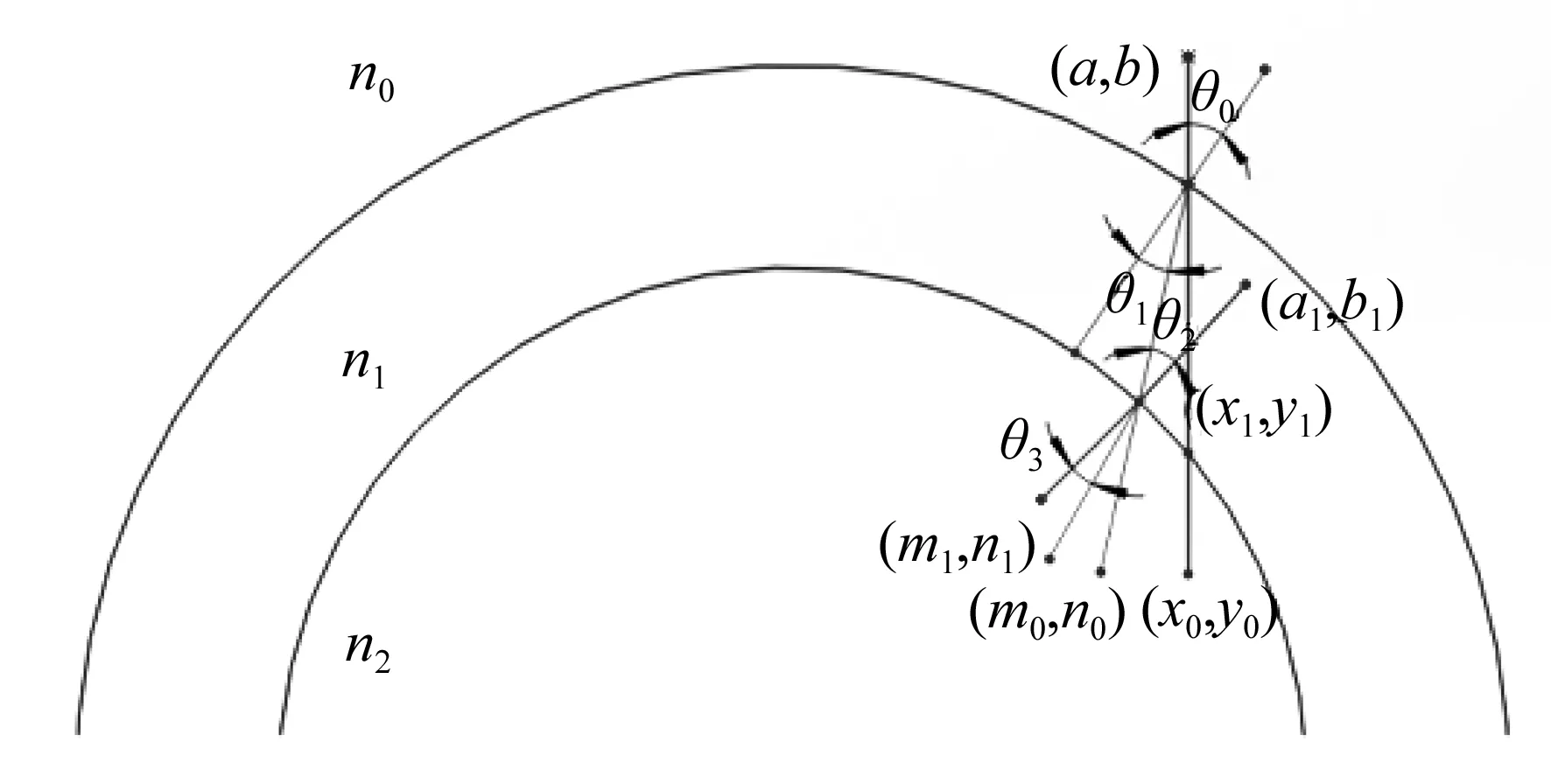
图7 实际OCT重建光线示意图
根据折射定律和费马原理得到角膜下表面矫正公式如式(1)所示:
(1)
即可求得矫正后的点(x1,y1)的坐标。
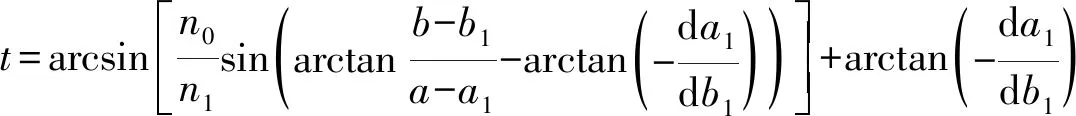
(2)
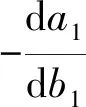
囊膜矫正公式如式(3)所示:
(3)
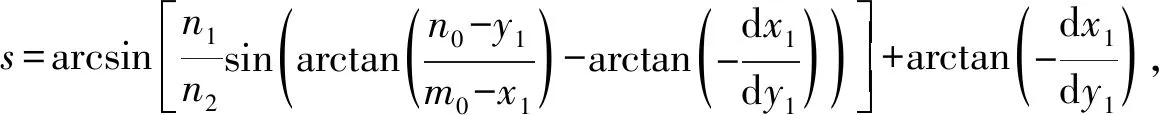
(4)
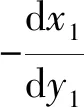
3 实验验证
3.1 实验1
使用玻璃管(图8(a))进行实验验证,经游标卡尺测量得到其厚度为1.02 mm(图8(b)),对样品使用OCT采取图像(图8(c)),使用水平集方法[14]提取样品轮廓(图8(d)),图像矫正后如图8(e)所示。矫正前玻璃管厚度为1.43 mm,矫正后玻璃管厚度为1.03 mm,基本符合实际情况;玻璃管内壁由畸形的弧形矫正为半圆形,矫正后的图像基本符合玻璃管成像截面形状,故矫正有效。
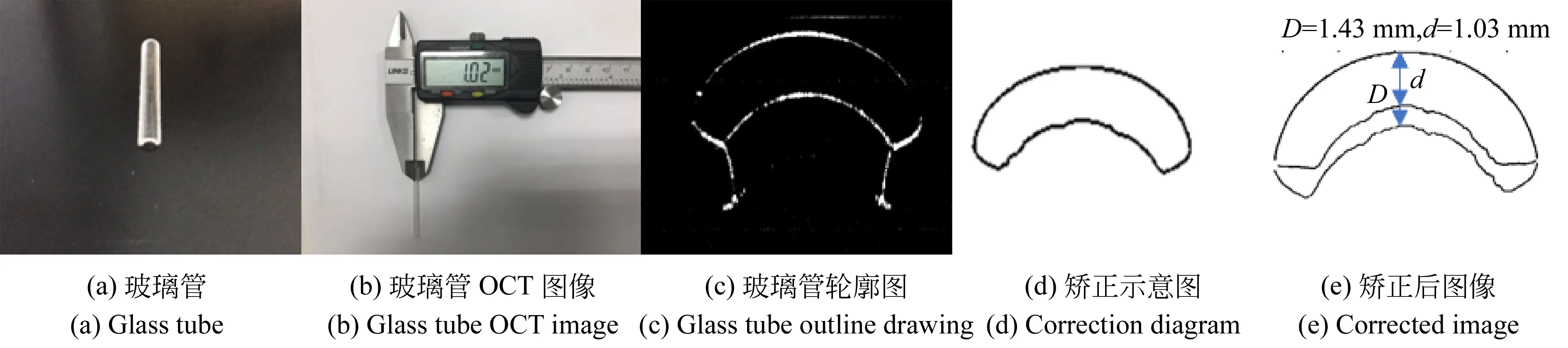
图8 对玻璃管进行实验验证
3.2 实验2
对特定位置使用采取到的猪眼角膜图像和OCT图像(图9),通过像素点位置相互关系测定其虹膜间距,如表1所示。
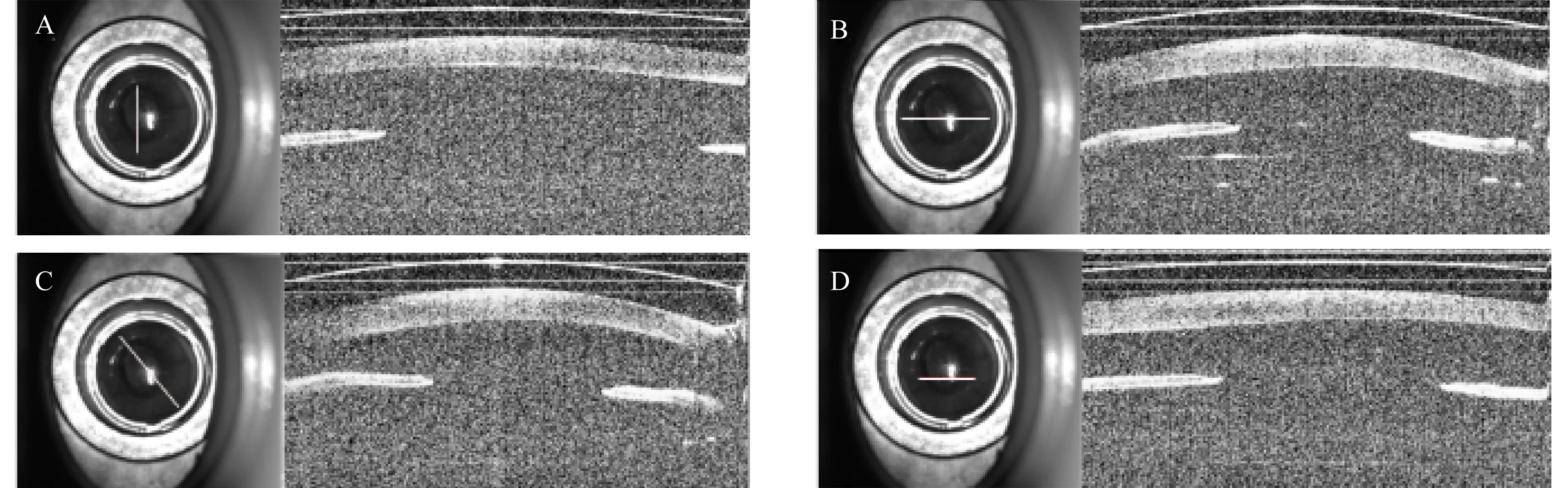
图9 特定扫描轨迹OCT图像
表1OCT与CCD图像虹膜间距实验数据对比表
Tab.1 Comparison of experimental data of OCT and CCD image iris spacing (mm)
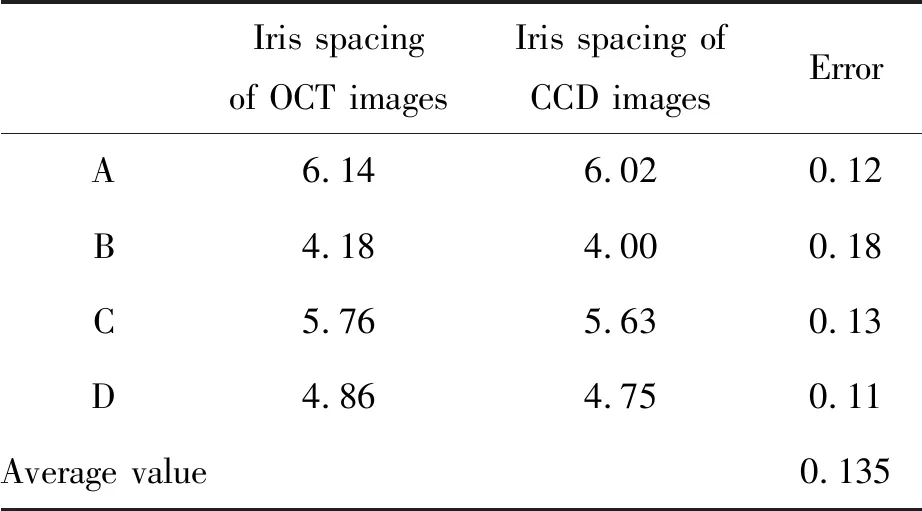
Iris spacing of OCT imagesIris spacing of CCD imagesErrorA6.146.020.12B4.184.000.18C5.765.630.13D4.864.750.11Average value0.135
OCT横向扫描误差约在135 μm左右,横向误差较小,在手术接受范围内,可以忽略不计,故无需矫正。
4 结 论
本文通过OCT系统和CCD相机,结合数字图像处理相关知识,对OCT图像导航系统在飞秒激光辅助白内障手术中所需要的标定进行方法研究,成功将扫描坐标系和样品坐标系进行坐标匹配,完成指定位置的图像扫描(深度误差约为50 μm),并通过光学相关定理对OCT图像进行重构误差矫正,经由实验验证可以准确矫正OCT图像的误差,达到飞秒激光辅助白内障手术的精度要求。为在飞秒激光辅助白内障手术中应用OCT图像导航打下坚实的基础。

