代谢工程改造大肠杆菌合成反式-4-羟基-L-脯氨酸
李 强,韩亚昆,蒋 帅,张 悦,吴鹤云,徐庆阳,谢希贤
(天津科技大学生物工程学院,代谢控制发酵技术国家地方联合工程实验室,天津 300457)
反式-4-羟基-L-脯氨酸是一种稀有亚氨基酸[1],主要以多肽形式存在于动物的胶原蛋白中[2]。反式-4-羟基-L-脯氨酸具有延缓衰老功效以及抗肿瘤、抗高血压作用[3-4],也被用于合成碳青霉烯类抗生和消炎药等药物[5-6],因在医药保健、材料化工、食品营养和护肤美容等行业都具有广泛应用[7]。近年来,随着反式-4-羟基-L-脯氨酸在医药和美容领域应用的显著增加,其市场需求量逐年增加,这对反式-4-羟基-L-脯氨酸的工业生产提出了更高的要求。
反式-4-羟基-L-脯氨酸的生产方法主要包括蛋白质水解法、化学合成法和微生物发酵法[8]。蛋白质水解法和化学合成法工艺复杂、原料成本高,而微生物发酵法具有周期短、易控制、产率高和污染小等优点,是大规模工业化生产反式-4-羟基-L-脯氨酸的理想方法。20世纪60年代开始,国内外很多科学家就开始对反式-4-羟基-L-脯氨酸生物合成开展研究,主要集中在L-脯氨酸-4-羟基化酶筛选和反式-4-羟基-L-脯氨酸产生菌构建方面。Baldwin等[9]首次从Streptomyces grixaviridru P8648分离得到L-脯氨酸-4-羟化酶,并确定了该酶的底物特异性。Shibasaki等[10]从指孢囊菌RH1中鉴定了L-脯氨酸-4-羟基化酶的基因,随后将该基因克隆转入大肠杆菌W1485,该重组菌在添加前体物L-脯氨酸的条件下发酵100 h,反式-4-羟基-L-脯氨酸产量达到41 g/L,生产强度达到0.41 g/(Lg h)。后,Shibasaki等[11]进一步将密码子优化后的指孢囊菌的L-脯氨酸-4-羟基化酶基因引入L-脯氨酸生产菌中,以葡萄糖为底物发酵99 h,反式-4-羟基-L-脯氨酸产量达到25 g/L,生产强度达到 0.25 g/(Lg h),为直接发酵法生产反式-4-羟基-L-脯氨酸奠定了基础。为构建发酵性能更好的反式-4-羟基-L-脯氨酸的生产菌株,Falcioni等[12]尝试在谷氨酸棒状杆菌来源的L-脯氨酸生产菌引入密码子优化后的指孢囊菌 L-脯氨酸-4-羟基化酶基因,发酵23 h,反式-4-羟基-L-脯氨酸产量达到7.1 g/L,生产强度达到0.31 g/(Lg h)。林凡[13]在Escherichia coli BL21(DE3)导入含密码子优化后的指孢囊菌的L-脯氨酸-4-羟基化酶基因,发酵64 h,反式-4-羟基-L-脯氨酸产量达到41.5 g/L,生产强度达到 0.65 g/(Lg h),这也是目前报道发酵水平最高的菌株。这些工程菌的构建和改进推动了反式-4-羟基-L-脯氨酸的微生物发酵法生产。

图 1 大肠杆菌反式-4-羟基-L-脯氨酸合成代谢路径Fig. 1 Biosynthetic pathway of trans-4-hydroxy-L-proline in E. coli
如前所述,虽然已有一些反式-4-羟基-L-脯氨酸工程菌的构建研究,但现有菌株的生产效率仍然偏低,这也导致了反式-4-羟基-L-脯氨酸的生产成本偏高。另外,由于这些菌株通过质粒克隆的方式引入L-脯氨酸-4-羟基化酶基因,一方面增加了菌体的负担,另一方面会出现因质粒丢失导致发酵不稳定,这些也限制了菌种在规模化生产中的应用。针对这些问题,本研究从Micromonospora sp. CNB394筛选到一个高活性的L-脯氨酸-4-羟基化酶,并采用系统代谢工程技术通过阻断L-脯氨酸的降解、解除L-脯氨酸反馈抑制、强化L-脯氨酸合成途径,以及引入羟化反应途径,构建高效率的反式-4-羟基-L-脯氨酸工程菌(图1)。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与质粒
本研究所使用和构建的菌株、质粒见表1。

表 1 实验所用菌株和质粒Table 1 Strains and plasmids used in this study
1.1.2 试剂
Primer STAR HS DNA聚合酶 大连宝生物科技有限公司;2h Rapid Taq Mix、ClonExpress®II One Step Cloning Kit 南京诺唯赞生物科技有限公司;质粒快速提取试剂盒、DNA凝胶纯化回收试剂盒 美国Omega 公司;引物及基因均由苏州金唯智科技有限公司合成。
1.2 仪器与设备
5 L发酵罐 上海保兴生物设备有限公司;S-433D氨基酸分析仪 北京捷盛依科科技有限公司;SBA-40C生物传感仪 山东省科学院生物研究所。
1.3 方法
1.3.1 工程菌构建
菌株构建过程中,利用规律成簇的间隔短回文重复-associated protein 9(clustered regularly interspaced short palindromic repeats-associated protein 9,CRISPRC a s 9)基因编辑方法进行基因的敲除和整合[14]。CRISPR-Cas9系统包括pGRB和pREDCas9两个质粒,其 中p R E D C a s 9 携 带g R N A 表 达 质 粒p G R B 的消 除 系 统、λ 噬 菌 体 的R e d 重 组 系 统[15]及C a s 9 蛋白表达系统[16],含奇霉抗性(工作质量浓度 100 mg/L),32 ℃培养。pGRB以pUC18为骨架,包括启动子J23100、gRNA-Cas9结合区域序列和终止子序列,含氨苄青霉抗性(工作质量浓度100 mg/L),37 ℃培养。构建质粒pGRB的目的是转录相应gRNA,从而与Cas9蛋白形成复合体,并通过碱基配对和PAM识别目的基因靶位点,实现目的DNA双链断裂。
1.3.1.1 gRNA质粒和重组DNA片段构建
为构建gRNA质粒,先设计合成两条完全反向互补的单链DNA,然后通过退火形成双链DNA,该双链DNA中间序列是靶位点的特定gRNA间隔序列,两端序列与pGRB具有同源序列。利用ClonExpress®II One Step Cloning Kit,双链DNA与线性化pGRB通过同源重组形成gRNA表达质粒。利用引物设计软件primer5,以待敲除基因或待整合位点的上下游序列为模板,设计上下游同源臂引物(扩增长度约400~500)。以待整合基因为模板,设计整合基因的扩增引物,聚合酶链式反应(polymerase chain reaction,PCR)扩增上下游同源臂和目的基因片段后,再经过重叠PCR制备重组片段。
1.3.1.2 DNA片段重组
首先,将pREDCas9质粒通过化学转化的方式导入E. coli W3110感受态细胞中[17]。通过菌落PCR筛选正确的阳性重组子,菌株接种于LB培养基32 ℃过夜培养,然后按1%的接种量转移到100 mL 2h YT培养基中(1.6%蛋白胨、1%酵母浸粉、0.5% NaCl)。32 ℃培养至细胞OD600nm达到0.1~0.2后,添加0.1 mmol/L异丙基-β-D-硫代半乳糖苷诱导重组酶表达。继续培养至细胞OD600nm达到0.4~0.5,收集菌体制备电转感受态细胞[18]。将200 ng重组DNA片段和100 ng gRNA质粒加入感受态细胞,并转移至0.1 cm电转杯中,在1 850 kV条件下进行电转化[19]。 电转化后的细胞加入1 mL SOC培养基中32 ℃复苏2 h,然后取100~200 μL涂布到含氨苄和奇霉抗性的LB平板上。32 ℃过夜培养,挑取单菌落进行菌落PCR验证,筛选阳性重组菌株。将阳性菌株在含有0.2%阿拉伯糖的LB培养基中培养,诱导pREDCas9中质粒消除系统切割pGRB。最后将菌株在42 ℃培养过夜,消除温敏性质粒pREDCas9,获得无质粒的工程菌株。
1.3.2 摇瓶发酵
1.3.3 发酵罐分批补料发酵
发酵罐的培养基与摇瓶发酵培养基相同。利用无菌水将茄形瓶斜面菌种制成菌悬液,接入总装液量为3 L的5 L发酵罐中。通过pH值电极控制自动流加氨水(体积分数25%)维持pH 7.0左右;发酵过程温度恒定在37 ℃;通过调节搅拌桨转速和通风量控制溶氧在25%~35%之间。培养至细胞OD值达到12~16时,以15%接种量接入新鲜的发酵培养基。发酵过程中控制pH 7.0左右,温度维持在37 ℃,溶氧维持在25%~35%之间。当培养基中的葡萄糖消耗完之后,以一定的速率流加80%的葡萄糖溶液,维持发酵培养基中的葡萄糖质量浓度在5 g/L以下[22]。
1.3.4 发酵过程中检测与分析
大肠杆菌生物量利用紫外分光光度计在600 nm波长处的OD值检测;发酵液中葡萄糖含量由SBA-40C生物传感仪检测;发酵液中谷氨酸、L-脯氨酸以及反式-4-羟基-L-脯氨酸的含量采用S-433D氨基酸分析仪检测;氨基酸含量采用茚三酮柱后衍生法利用S-433D氨基酸分析仪测定[23]。色柱分析条件:色柱LCA K06/Na,进量50 μL,检测波长570 nm和440 nm,流动相流速 0.45 mL/min,反应器温度130℃。其中,L-脯氨酸和反式-4-羟基-L-脯氨酸反应后产物可在440 nm波长处被检测到,其他氨基酸反应后产物可在570 nm波长处被检测到。
1.4 数据统计学分析
发酵数据代表3 组平行发酵数据的f s。利用t检验双尾分布对两组发酵参数进行单向方差分析。P<0.05,差异显著;P<0.01,差异极显著。
2 结果与分析
2.1 木糖诱导基因表达系统建立
在代谢工程研究中,对相关的内源基因和异源基因进行过表达是常用的改造策略。T7启动子是大肠杆菌中报道最强的启动子,但是大肠杆菌自身没有T7 RNA聚合酶,因首先需要在大肠杆菌中引入来源于T7噬菌体的RNA聚合酶[24]。另外,T7启动子表达基因过强时,有时会影响菌体的生长,因需要控制T7 RNA聚合酶的表达时间及表达量。本研究首先利用CRISPR-Cas9基因编辑方法,以大肠杆菌W3110为出发菌,在lacZ位点整合了木糖启动子控制的T7 RNA聚合酶基因,可实现在木糖诱导的条件下启动T7 RNA聚合酶的表达[21]。随后对dgsA(编码糖代谢转录抑制因子)启动子-10区进行点突变,解除了葡萄糖对木糖启动子转录的阻遏作用[25]。最后对xlyA(木糖异构酶)进行基因敲除,阻断木糖的代谢途径,减少木糖因分解代谢导致的损失[26]。通过以上基因操作,构建的菌株HYP01可在木糖诱导的情况下实现相关基因的过表达。
2.2 强化L-脯氨酸合成途径
2.2.1 L-脯氨酸操纵子过表达对L-脯氨酸合成的影响
γ-谷氨酸激酶为L-脯氨酸合成的限速酶,受到L-脯氨酸的反馈抑制。根据报道[27],将编码γ-谷氨酸激酶基因proB中319位G替换成A,编码蛋白的第107位氨基酸天冬酰胺替换为L-脯氨酸,可解除L-脯氨酸的反馈抑制。启动子是代谢工程中调节基因表达的重要元件[28],其中T7启动子(PT7)和trc启动子(Ptrc)是大肠杆菌中应用最广泛的两种强启动子[29],但两者转录强度不同。本研究首先敲除了菌株HYP01 L-脯氨酸脱氢酶基因putA,阻断前体物L-脯氨酸的降解途径,构建菌株HYP02(表1)。
为验证PT7和Ptrc对L-脯氨酸操纵子的表达效果,在菌株HYP02的假基因位点yghX处整合proB*A,分别由PT7和Ptrc启动转录,分别构建了菌株HYP03和HYP04。摇瓶发酵结果如图2所示,HYP03的L-脯氨酸产量达到5.5 g/L,HYP04的L-脯氨酸产量达到11.8 g/L,是HYP03 L-脯氨酸产量的2.14 倍。图2表明,采用Ptrc控制L-脯氨酸操纵子的过表达,效果更好。

图 2 不同启动子控制L-脯氨酸操纵子过量表达的发酵参数比较Fig. 2 Comparison of fermentation parameters for overexpression of proline operon controlled by different promoters
氨基酸分析结果还显示,HYP03和HYP04的发酵液中都有少量L-谷氨酸积累(图2),说明L-谷氨酸到L-脯氨酸的代谢通量仍需要加强。由于L-脯氨酸操纵子在Ptrc控制下效果更好,本研究在菌株HYP04的假基因位点trpR处整合第2个拷贝的Ptrc-proB*A,构建了菌株HYP05。摇瓶发酵结果如图3所示,HYP05的L-脯氨酸产量达到13.2 g/L,相比菌株HYP04(12.1 g/L)提高了9.1%,L-谷氨酸质量浓度为0.4 g/L,比HYP04降低了77.8%,说明L-脯氨酸操纵子基因双拷贝进一步增强了 L-脯氨酸的合成通量。

图 3 双拷贝proB*A对L-脯氨酸产量的影响Fig. 3 Effect of double proB*A copy on proline production
2.2.2 增加胞内NADPH供应对L-脯氨酸合成的影响
NADPH是细胞内重要的还原力,对于多种氨基酸的合成代谢都具有重要的作用[30],氨基酸的生物合成往往因NADPH的供应不足而受到限制。如图1所示,合成1 mol的L-脯氨酸需要3 mol NADPH,NADPH的供应也是L-脯氨酸合成的限制性因。大肠杆菌的基因pntAB编码吡啶核苷酸转氢酶PntAB,可以催化NADP(H)与NAD(H)之间氢负离子可逆转移,增强PntAB的表达被证明能够有效提高大肠杆菌胞内NADPH的供应[31]。由于PntAB是膜蛋白,表达量过大有时也会对菌体生长造成负面影响。本研究在HYP05的假基因yeeP位点处整合了自身启动子控制的pntAB基因,构建了菌株HYP06。摇瓶发酵结果如图4所示,HYP06的L-脯氨酸产量达到15.3 g/L,相比HYP05(13.1 g/L)提高了16.8%,说明增加NADPH的供应显著提高L-脯氨酸的积累。

图 4 增强NADPH供应对L-脯氨酸产量的影响Fig. 4 Effect of enhancing NADHP supply on proline production
2.3 高活性L-脯氨酸-4-羟基化酶的筛选
大肠杆菌中不存在L-脯氨酸-4-羟基化酶基因,反式-4-羟基-L-脯氨酸合成途径的重构需要引入外源的 L-脯氨酸-4-羟基化酶基因,因高活性的L-脯氨酸-4-羟基化酶是反式-4-羟基-L-脯氨酸工程菌构建的关键。根据指孢囊菌RH1的L-脯氨酸-4-羟基化酶的氨基酸序列(GenBank:BAA20094.1),在NCBI数据库通过BLAST比对,挑选了与L-脯氨酸-4-羟基化酶具有保守催化结构域的4 个基因(分别命名为p4H1、p4H2、p4H3和p4H4),分别来源于Micromonospora sp. CNB394、Nocardia sp. BMG111209、Kutzneria albida DSM 43870、Streptomyces sp. SA15。将密码子优化后的p4h、p4H1、p4H2、p4H3和p4H4连接到pTrc99a,导入菌株HYP06中,构建了菌株HYP07、HYP08、HYP09、HYP10和HYP11。摇瓶发酵结果如图5所示,HYP07、HYP08、HYP09和HYP10发酵液中反式-4-羟基-L-脯氨酸质量浓度分别为8.6、9.5、7.6 g/L和2.3 g/L,表明p4H1、p4H2、p4H3具有L-脯氨酸-4-羟基化酶的活性。来源于Micromonospora sp. CNB394的p4H1活性最高,与菌株HYP07相比,HYP08的反式-4-羟基-L-脯氨酸产量提高了10.5%。

图 5 含L-脯氨酸-4-羟基化酶的菌株发酵参数比较Fig. 5 Comparison of fermentation parameters for recombinant strains with different L-proline-4-hydroxylases
2.4 L-脯氨酸-4-羟基化酶过表达对反式-4-羟基-L-脯氨酸合成的影响
为验证p4H1在基因组上的表达活性,将p4H1整合于菌株HYP06的假基因位点tehB处,分别由PT7和Ptrc启动转录,构建了菌株HYP12和HYP13。摇瓶发酵结果如图6所示,HYP12的反式-4-羟基-L-脯氨酸产量达到4.9 g/L,比菌株HYP13(3.2 g/L)高53.1%;说明p4H1在PT7控制下的表达效果更好。

图 6 不同启动子控制p4H1过量表达的发酵参数比较Fig. 6 Comparison of fermentation parameters for overexpression of p4H1 controlled by different promoters
从图6可知,HYP12和HYP13的发酵液中均有前体物L-脯氨酸残留,说明L-脯氨酸-4-羟基化酶的表达量不足。为进一步提高反式-4-羟基-L-脯氨酸的产量,在HYP12假基因ycjV处整合第2个拷贝的PT7-p4H1,构建了菌株HYP14。如图7所示,HYP14的反式-4-羟基-L-脯氨酸产量达到11.7 g/L,相比HYP12(5.0 g/L)提高了 1.34 倍,L-脯氨酸质量浓度降低到3.5 g/L。随后在HYP14的假基因yjiP位点进行整合了第3个拷贝的PT7-p4H1,构建了菌株HYP15。反式-4-羟基-L-脯氨酸产量达到13.6 g/L,相比HYP14提高了16.2%,L-脯氨酸质量浓度降低到1.5 g/L。
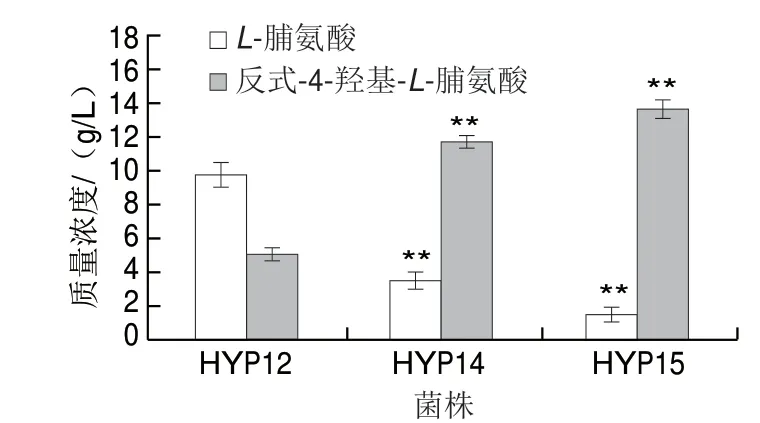
图 7 p4H1拷贝数对发酵参数的影响Fig. 7 Effect of p4H1 copy number on fermentation parameters
2.5 工程菌发酵罐分批补料发酵
为评估菌株HYP15的生产性能,在5 L发酵罐中进行分批补料发酵实验。如图8所示,随着发酵时间延长,细胞生物量逐步增加,最终OD600nm达到了70。12~36 h,反式-4-羟基-L-脯氨酸保持了较高的合成速率,40 h的产量达到48.6 g/L,糖酸转化率(最终合成反式-4-羟基-L-脯氨酸总量与上发酵消耗总糖量之比)和生产强度分别达到了21.6%和1.22 g/(Lg h)。发酵液中可检测到的副产物有L-脯氨酸和乙酸,质量浓度分别为2.3 g/L和0.9 g/L。
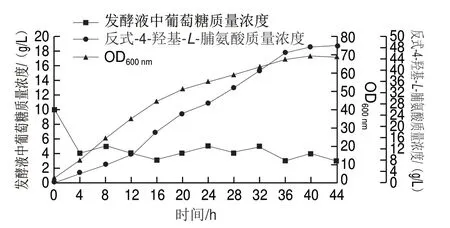
图 8 工程菌HYP15在5 L发酵罐分批补料发酵曲线Fig. 8 Fed-batch fermentation profiles of the engineered strain HYP15 in a 5-L bioreactor
3 结 论
本研究构建了1 株无质粒、从头高效合成反式-4-羟基-L-脯氨酸的大肠杆菌基因工程菌。工程菌的构建过程包括:1)通过引入木糖启动子控制的T7 RNA聚合酶基因,在大肠杆菌W3110中建立木糖诱导的基因表达系统;2)通过删除L-脯氨酸脱氢酶基因putA,阻断L-脯氨酸的降解途径;3)通过L-脯氨酸操纵子和吡啶核苷酸转氢酶基因整合,增强了L-脯氨酸的合成代谢;4)筛选到高活性的L-脯氨酸-4-羟基化酶基因p4H1;5)通过L-脯氨酸-4-羟基化酶基因整合,强化反式-4-羟基-L-脯氨酸的合成代谢。以葡萄糖为碳源进行分批补料发酵40 h,工程菌HYP15的反式-4-羟基-L-脯氨酸产量达到48.6 g/L,糖酸转化率和生产强度分别达到了21.6%和1.22 g/(Lg h)。
与现有报道的反式-4-羟基-L-脯氨酸生产菌相比,该工程菌,具有以下优势:1)菌株基因型明确,遗传稳定性好;2)不含质粒表达载体,避免抗生的使用;3)发酵周期短,生产强度高。工程菌具有良好的工业化前景,为反式-4-羟基-L-脯氨酸发酵法生产提供了理论支持。

